| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Mecanisme moleculare protectoare care permit respiratia aeroba
Multe reactii biochimice esentiale pentru metabolismul aerob al celulei necesita transferul a 4 e- la molecula de O2 pentru a forma H2O (dupa reactia: O2 + 4e- + 4 H+ = 2H2O). De cele mai multe ori transferul are loc simultan, fara formarea altor intermediari ai reducerii.
Deoarece O2 este un oxidant puternic si acceptor de mare afinitate al e-, el poate avea rolul de acceptor de e- nu numai la capatul catenei respiratorii membranare, ci si in alte reactii de oxidare a substratului, catalizate de enzimele solubile in citoplasma. Aceste reactii pot fi fiziologice, producatoare sau neproducatoare de energie sau sunt nefiziologice si in anumite conditii sunt letale, deoarece O2 molecular este redus secvential, univalent, formand intermediari reactivi cu diferite grade de toxicitate. Reducerea O2 cu un singur e- produce radicalul superoxid (.O2-), care la pH fiziologic se reduce inca odata univalent si formeaza H2O2 (produsul reducerii bivalente) (fig. 56).
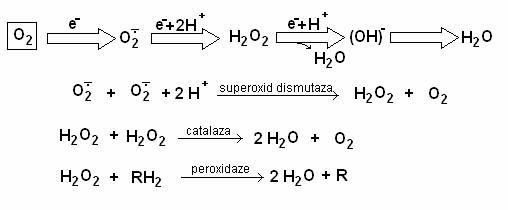
Fig. 56. Reducerea completa a unei molecule de O2 la apa, necesita 4 electroni. In acest proces se formeaza compusi intermediari (radicalul anionic superoxid (O-2) peroxidul de O (H2O2) si radicalul hidroxil (OH-). Ionul O-2 este eliminat de superoxid dismutaze (SOD), iar H2O2 este indepartata de catalaze si peroxidaze.
In consecinta, celula bacteriana este supusa permanent unui stress oxidativ, care, functional se poate defini ca ca un exces de oxidanti* in mediul celular, deoarece in anumite conditii, rata producerii intermediarilor reducerii partiale a O2 depaseste capacitatea celulei de a-i elimina.
Oxidantii sunt molecule care pot sa se reduca prin oxidarea altor molecule.
NO . (oxidul nitric) se formeaza prin actiunea nitric-oxid-sintazei (NOS), care oxideaza L-arg la citrulina si NO.. Microorganismele sunt expuse actiunii NO. endogen rezultat prin reactia de denitrificare(reducerea respiratorie a nitratilor) la multe bacterii si fungi.
Reactia O2- cu NO formeaza un oxidant puternic - peroxinitritul ONOO-. Reactia este de 3 ori mai puternica decat inactivarea O2- sub actiunea SOD. Peroxinitritul se formeaza cu o rata optima la concentratii echivalente de NO si O2-.
Intermediarii reducerii O2 reactioneaza cu toate tipurile de macromolecule si produc leziuni ale moleculelor de ADN, ARN, proteine, iar prin peroxidarea lipidelor apar leziuni membranare.
Toate organismele si-au dezvoltat mecanisme protectoare pentru a atenua efectele oxidantilor. Mecanismele de aparare a celulei fata de stressul oxidativ sunt de doua categorii: preventive si reparatorii.
Mecanismele preventive actioneaza prompt si previn aparitia leziunilor oxidative, prin distrugerea derivatilor reactivi ai O2 sau limiteaza durata actiunii unor reactii, ca de exemplu, peroxidarea lipidelor.
Peroxidul de H (H2O2) rezulta prin transferul a doi e-, la o molecula de O2, catalizat de NADH-oxidaza, dupa reactia:
![]()
H2O2 are o toxicitate moderata. Oxideaza componentele membranare si enzimele, lezeaza ADN si produce mutatii, inhiba procesele de transport membanar. H2O2 este indepartata, cel mai adesea sub actiunea catalazei, prin conversia la H2O si O2, sau a peroxidazelor, care o reduc la H2O, dupa reactia:
![]()
O molecula de H2O2 se reduce, iar alta se oxideaza.
Catalaza este o enzima neinductibila, cel mai adesea, un homotetramer cu un protohem/subunitate. Este produsa abundent de bacteriile aerobe si de cele facultativ aerobe. Cele microaerofile produc cantitati mici de catalaza. Enzima nu este produsa de bacteriile strict anaerobe si nici de cele anaerobe aerotolerante. Unele bacterii lactice sintetizeaza totusi o catalaza adevarata, daca in mediu se gaseste hemina, deoarece ele nu sintetizeaza grupul prostetic hem al catalazei.
Peroxidazele sunt flavoproteine fara metale grele si catalizeaza dehidrogenarea unui substrat (AH2), in prezenta H2O2. Cea mai importanta este NADH-peroxidaza:
![]()
Glutationul este substratul glutation-peroxidazei (GP) care indeparteaza H2O2 si peroxizii lipidici care rezulta din atacul radicalilor liberi asupra lipidelor. GP este reciclata pe calea glutation-reductazei, pentru a indeparta alta molecula de H2O2. Glutationul elimina, de asemenea, .OH si peroxizii lipidici care rezulta din atacul radicalilor liberi asupra lipidelor.
Ionul O2- (superoxid) se formeaza in cantitati mici in timpul procesului respirator normal. Are reactivitate moderata, capabil sa actioneze ca oxidant sau ca reducator in sistemele biologice. Este relativ stabil, ceea ce ii permite sa difuzeze la distante relativ mari inainte de a-si exercita efectele toxice. O2. generat extracelular poate dobandi acces la tintele intracelulare pe calea canalelor pentru anioni. La pH acid (in focarul inflamator sau in interiorul fagosomului), O2- se protoneaza si formeaza HO2. cu sarcina neutra si de aceea trece mai usor prin membrane si reactioneaza cu sine insusi, formand H2O2.
O2- produce distrugerea oxidativa a lipidelor si a altor componente ale celulei. Are durata de actiune cea mai lunga dintre toti intermediarii reducerii O2 si actiunea sa se poate produce succesiv, asupra mai multor molecule. O2- este eliminat sub actiunea superoxid-dismutazelor (SOD). SOD se combina cu 2 molecule de O2-, dupa reactia:
![]()
Ionul superoxid este eliminat rapid si nu se acumuleaza in celula. Anihilarea .O2- este o strategie esentiala de aparare, deoarece nu numai ca limiteaza actiunea sa directa, dar previne reducerea Fe mediata de .O2- si generarea .OH.
Sunt 3 forme de SOD in natura: eucariotele, unii fungi si putine bacterii produc in special CuZnSOD, homodimere, cu 2 subunitati identice legate necovalent, fiecare cu cate un atom de Cu si Zn. Bacteriile anaerobe obligate produc in special FeSOD(dimeri), iar cele aerobe produc predominant MnSOD(dimeri si tetrameri). Unele bacterii produc ambele tipuri de SOD. Unele bacterii patogene(M. tuberculosis) secreta FeSOD in mediul extracelular, ca o cale de rezistenta la atacul oxidant. La bacteriile facultativ-anaerobe (E. coli), SOD este periplasmica si nivelul activitatii ei creste dupa expunerea la O2. Nocardia asteroides are activitate SOD asociata cu peretele celular, care poate fi secretata in mediul extracelular si contine cantitati echimolare de Fe, Mn si Zn.
Singurele organisme care nu poseda enzime protectoare sunt bacteriile anaerobe stricte. De aceea, O2 exercita efecte toxice letale asupra lor.
Radicalul hidroxil liber (OH.) se formeaza prin reducerea trivalenta a O2 in vitro, prin reactia H2O2 cu .O2-. Aceasta reactie este amplificata de un catalizator metalic (Fe3+). Se formeaza si ca rezultat al actiunii radiatiei ionizante.
OH. este cel mai reactiv dintre intermediarii reducerii O2 , fiind cel mai puternic agent oxidant. Efectele sale oxidante se manifesta asupra tuturor categoriilor de molecule organice (proteine, ADN, lipide). Este probabil, unul dintre agentii moleculari care omoara celulele dupa iradiere x sau gama.
Datorita reactivitatii foarte inalte, difuzia .OH este limitata inainte de a intalni substraturile oxidabile. Mecanismul actiunii sale consta in initierea cascadei radicalilor liberi. Oxidarea acizilor grasi nesaturati intr-o membrana lipidica poate produce radicalul peroxil (HO2), care reactioneaza cu alte molecule lipidice invecinate, generand alti radicali lipidici. Se initiaza reactia in lant a radicalilor liberi, care se propaga la situsuri indepartate de situsul primar al reactiei.
Oxigenul singlet (1O2) este o forma moleculara cu energie superioara si se formeaza cand cei doi e- pereche dobandesc spini antiparaleli, fie ca se afla pe acelasi orbital, fie pe orbite diferite. In aceasta forma, O2 nu primeste un electron suplimentar, ci numai energie suplimentara, care schimba spinul unuia dintre electroni.
1O2 este un poluant atmosferic. Poate fi produs fie spontan, fie prin sisteme enzimatice. Cea mai comuna cale chimica a producerii sale este reactia O2 cu lumina vizibila. Procesul implica prezenta unei molecule a unei substante colorate care absoarbe lumina.
1O2 se genereaza prin actiunea lactoperoxidazei si mieloperoxidazei, prezente in lapte, saliva si in fagocite. In fagocite, 1O2 are rolul de a omori agentul fagocitat. In prezenta 1O2 se produc reactii de oxidare, al caror rezultat este distrugerea oxidativa a componentelor celulare vitale, ca de exemplu, fosfolipidele membranei celulare.
Mecanismele reparatorii actioneaza tardiv si repara leziunile cauzate de molecule reactive care nu au fost anihilate de sistemele de aparare preventiva. Fiecare conditie de stress induce sinteza unui set de proteine, unic pentru categoria agentului inductor al stressului. Unele proteine induse de stressul oxidativ sunt comune si pentru alte tipuri de stress (stressul hipertermic, infometarea etc.).
Stressul oxidativ altereaza numeroase cai metabolice. Gradul de alterare este dependent de capacitatea de raspuns al celulei la stress. Eliminarea timpurie a stresului oxidativ, prin mecanismele preventive este esentiala pentru supravietuirea celulei.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 1446
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2024 . All rights reserved