| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
UNIVERSITATEA DIN PITESTI
FACULTATEA DE STIINTE
SECTIA CHIMIE-FIZICA
ACTIVITATI DE INVATARE BAZATE
PE EXPERIMENTE DE
LABORATOR. EXEMPLIFICARI
Este o metoda fundamentala de predarea-invatarea stiintelor naturii.
Experimentul de laborator este metoda euristica de organizare si realizare a activitatilor practice pentru deducerea informatiilor teoretice, concretizarea, verificarea, aprofundarea si consolidarea cunostintelor si deprinderilor psiho-motorii in perspectiva pregatirii elevilor pentru integrarea socio-profesionala.
Experimentul este o observare provocata. A experimenta inseamna a-i pune pe elevi in situatia de a concepe si practica ei insisi un anumit gen de operatii cu scopul de a observa, a studia, a dovedi, a verifica, a masura rezultatele. E o provocare intentionata a unui fenomen in conditii determinate, in scopul observarii comportamentului, al cercetarii raporturilor de cauzalitate, al descoperirii legitatilor care-l guverneaza, al verificarii unor ipoteze.
Chimia fiind o stiinta experimentala care isi bazeaza procesul teoretic si isi gaseste aplicativitatea practica in lucrarile de laborator, are la baza experimentul atat ca metoda de investigatie stiintifica cat si ca metoda de invatare. Conceptul in corelatie cu principiile didactice moderne, experimentul de laborator urmeaza treptele ierarhice ale invatarii, conducand elevul de la observarea unor fenomene chimice pe baza demonstratiei, la observarea fenomenelor prin activitatea proprie (faza formarii operatiilor concrete), apoi la verificarea si aplicarea in practica a acestora (faza operatiilor formale) cand se cristalizeaza structura formala a intelectului si in continuare, la interpretarea fenomenelor observate care corespunde cu faza cea mai inalta din treptele ierarhice ale dezvoltarii (faza operatiilor sintetice).
Astfel, in predarea-invatarea "conceptului de acid" in diferite etape se percurg toate aceste faze. In scoala generala se efectueaza o serie de experiente care pun in evidenta faptul ca in solutie apoasa acizii pun in libertate ioni H+ conform teoriei lui Arrhenius (inrosesc turnesolul, descompun piatra de var, reactioneaza cu metale, etc.). se realizeaza astfel faza operatiilor concrete.
In liceu se explica caracterul acid al unor substante, prin cedarea protonilor conform teoriei lui Br nsted (acizii pot fi ioni sau molecule). Se stabileste ca fiecarui acid tare ii corespunde o baza conjugala slaba - faza operatiilor formate.
Intr-o urmatoare etapa se stabileste experimente si se demonstreaza teoretic caracterul acid al unor compusi organici datorat efectelor care apar in molecule.
Experimentele chimice se folosesc de obicei, integrate, in numar mai mare sau mai mic, in diferite etape ale lectiilor. Multitudinea sferelor de informatii din domeniul chimiei, reprezentate prin notiuni, concepte, fenomene si legi solicita o gama diversificata a experimentelor. Deci, experimentele de laborator pot fi organizate diferentiat, formularea sarcinilor concrete pentru efectuarea unui experiment ridicand probleme care implica: scopuri ale invatarii, accesibilitatea la invatare, continutul invatarii, locul in procesul invatarii, corelarea cu alte strategii didactice de invatare.
CRITERII DE CLASIFICARE A EXPERIMENTELOR DE LABORATOR
Clasificarea experimentelor de laborator este strict legata de varietatea de sarcini si se poate face dupa mai multe criterii:
a) Criteriul locului in ierarhia invatarii:
Dupa acest criteriu, experimentele de laborator pot fi:
I. reproductive (demonstratia se reproduce dupa un program dinainte stabilit indicandu-se si ceea ce trebuie sa se observe si la ce concluzie se ajunge).
II. productiv - creative si de cercetare (au loc in context problrmatizat in care se afirma capacitati operationale la nivel superior).
Experiente:
- Intr-o eprubeta se introduce o solutie de permanganat de potasiu care se alcalinizeaza cu carbonat de sodiu. In acest amestec se barboteaza etena (preparata in prealabil). Se observa decolorarea solutiei si aparitiei unui precipitat brun de dioxid de mangan.
In solutia de permanganat se barboteaza acetilena (preparata in prealabil). Se observa decolorarea solutiei si aparitia unui precipitat brun de dioxid de mangan. Ecuatiile reactiilor chimice efectuate sunt:
3H2C = CH2 + 2KMnO4 + 4H2O HO - H2C ¾ CH2 - OH + 2KOH + 2MnO2
3HC º CH + 8KMnO4 + 4H2O 3HOOC ¾ COOH + 8KOH + 8MnO2
Prin efectuarea acestor experiente se ilusreaza faptul ca atat alchenele cat si alchinele pot suferi reactii de oxidare, agentul oxidant fiind permanganatul.
Marea majoritate a experientelor care se efectueaza in scoala au o functie reproductiva si pot fi integrate in orice moment in lectie.
In
aceasta categorie pot fi incluse experimentele in urma carora se poate deduce o
regula, o lege, cat si experimentele cu caracter de cercetare.
CREAREA UNEI MOTIVATII
Un numar mare de reactii chimice sunt utilizate in industria chimica pentru obtinerea unor produse utile.
Pentru a controla procesul chimic care are loc este necesara o analiza profunda a factorilor de care este influentat. Viteza cu care se produce o reactie chimica este determinanta pentru utilizarea acesteia in industrie. De aici necesitatea de a fi stabiliti factorii care influenteaza viteza reactiilor chimiei.
FORMULAREA PROBLEMEI
Observatiile experimentale arata ca transformarea unor reactanti in produsi corespunzatori de reactie necesita un anumit timp. Marimea care caracterizeaza desfasurarea unui proces ce se petrece in timp este definita ca viteza. In reactiile chimice variaza atat concentratiile reactantilor cat si ale produsilor.
Prin experimentul pe care il vom prezenta, urmarim sa stabilim dependenta vitezei de reactie si concentratie. Prin experimentul propus se urmareste sa se stabileasca aceasta dependenta.
ENUNTAREA IPOTEZEI
Experimental s-a constatat ca viteza de reactie depinde de concentratie. Deci se presupune ca exista o relatie, ce poate fi concretizata printr-o expresie matematica intre viteze de reactie si concentratie. Prin experimentul propus se urmareste sa se stabileasca aceasta dependenta.
ELABORAREA UNOR SISTEME EXPERIMENTALE
Pentru a pune in evidenta desfasurarea unor reactii chimice in timp este necesar sa masuram concentratia unui reactant sau a unui produs in diferite momente. Reactia chimica trebuie sa se desfasoare suficient de lent pentru a putea stabili valoarea unor concentratii in anumite momente. Deci pentru masuratorile de viteza ale reactiilor chimice nu se vor utiliza reactii de neutralizare sau reactii cu formare de precipitant, deoarece acestea au loc practic instantaneu, ci se vor folosi reactii redox sau reactii cu degajarea unui gaz, care permit stabilirea concentratiei reactantilor sau produsilor in diferite momente ale procesului chimic. Astfel se poate examina sistemul iodura I- - apa oxigenata H2O2.
In reactia redox care are loc se formeaza I2. Prezenta acestuia poate fi pusa in evidenta cu ajutorul amidonului.
2KI + H2O2 +2HCl 2KCl + I2 + 2H2O.
DESFASURAREA EXPERIMENTULUI
Se pregatesc doua seturi de experiente. In primul set de experiente se lucreaza la concentratii diferite in iodura de potasiu, iar in al doilea set se variaza concentratia in apa oxigenata.
ORGANIZAREA OBSERVATIILOR
In urma efectuarii experientelor se noteaza timpul pana la aparitia culorii albastre (aceeasi pentru toate probele).
DISCUTAREA PROCEDEELOR UTILIZATE
Se stie ca viteza reprezinta
variatia concentratiei in unitatea de timp v=Dc/Dt.
S-a luat in
considerare faptul ca iodul care rezulta in urma reactiei chimice se identifica
cu amidon, producandu-se o coloratie albastra a acestuia de o anumita
intensitate (considerata etalon) in momentul cand concentratia iodului atinge o
anumita valoare. Acestei valori ii corespunde in toate experientele aceeasi
variatie c a reactantului (in primul
set de experiente KI si in al doilea H2O2).
Se poate alege, in mod arbitrar, marimea c ca unitatea de masura a variatiei concentratiei (Dc=1).
In aceste conditii viteza de reactie este numeric egala cu valoarea reciproca a intervalului de timp scurs din momentul amestecarii reactantilor si pana in momentul cand apare coloratia albastra. Asadar pentru calculul vitezei de reactie se poate utiliza relatia v=1/Dt.
Deci, se calculeaza viteza de reactie pentru cele doua seturi de experiente.
Cu datele obtinute se traseaza graficul dependentei vitezei in functie de concentratia solutiilor de apa oxigenata utilizata.
Dupa cum era de asteptat, viteza de reactie creste atat cu cresterea concentratiei in iodura, cat si cu cresterea concentratiei in apa oxigenata.
ASIMILAREA UNOR NOTIUNI NOI
![]()
Din analiza unui numar
mare de experimente s-a ajuns la concluzia ca viteza de reactie nu este
frecvent dependenta linear de concentratie. De obicei, aceasta dependenta ia
forma unei functii exponentiale. Deci, in legea de viteza, concentratiile
reactantilor trebuie sa apara la anumite puteri, acestea definindu-se ca ordine de reactie. Pentru sistemul
studiat I- - H2O2, legea de viteza putand fi
reprezentata astfel:
unde k - este
PRELUCRAREA DATELOR
Utilizand datele experimentale se pot calcula valorile ordinelor de reactie.
FORMULAREA CONCLUZIILOR
Se considera o reactie de tipul: aA + bB Produsi, in care a si b sunt coeficientii stoichimetrici ai reactantilor A si B, viteza de reactie se exprima prin relatia:
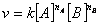
care reprezinta legea de viteza; nA si nB sunt ordinele partiale de reactie.
VERIFICAREA REZULTATELOR
Se examineaza dependenta vitezei de concentratie pentru o serie de sisteme chimice cu utilizari practice si se face o clasificare a reactiilor chimice in functie de ordinul de reactie.
APLICAREA IN PRACTICA
|
este dependenta numai de numarul de nuclee 14C prezentate. Care este ordinul de reactie? Scrieti ecuatia ce reprezinta legea de viteza.
Se pot prezenta o serie de probleme prin care sa se stabileasca valoarea vitezei de reactie a unui proces odata cu modificarea concentratiei unui reactant, cunoscandu-se legea de viteza.
In structura capacitatii umane intra trei categorii de componente:
- anticipative (pregatitoare ale experimentului);
- efective (de realizare a experimentului);
- evaluative (de analiza a rezultatelor experimentale).
Aceste categorii de comportamente impun trei etape distincte, obligatorii fiecarui experiment:
- etapa pregatitoare (consta in introducerea elevului in problemele experimentului, stabilirea motivatiei teoretice, a conditiilor materiale, formularea unor ipoteze, stabilirea ordinii operatiilor de efectuat), realizata prin parcurgerea punctelor 1, 2, 3, 4 - in experimentul prezentat;
- etapa de efectuare (consta in realizarea experimentului, observarea directa a fenomenului si interpretarea acestor observatii) - punctul 5;
- etapa de evaluare (consta in formulartea concluziilor pe baza interpretarii observatiilor si a le confrunta cu ipotezele); se va parcurge prin efectuarea indicatiilor de la punctele 6, 7, 8, 9, 10, 11, 12.
b) Criteriul participativ al elevilor
Dupa acest criteriu, experimentele de laborator pot fi:
I - experiment demonstrativ efectuat de profesor sau de o grupa de elevi;
II - experiment frontal realizat de toti elevii, in acelasi timp individuali sau pe grupe.
I Experiment demonstrativ
Pentru ca experimentul demonstrativ sa-si atinga scopul trebuie sa parcurga o serie de etape.
Prin intermediul reactiei cuprului cu acidul azotic vom marca aceste etape.
MOTIVATIA DEMONSTRATIEI
Se stie ca metalele situate in seria activitatii electrochimice, dupa hidrogen, nu il pot dizlocui din acizi. Ele vor reactiona numai cu acizii cu actiuni oxidanta. In urma acestei reactii rezulta sare si oxid de nemetal in stare de oxidare inferioara.
Astfel, prin reactia cuprului cu acidul azotic ar trebui sa se formeze azotatul de cupru si monoxidul de azot. Daca se introduce un span de cupru intr-o solutie de acid azotic se observa degajarea unui gaz de culoare brun-roscata (NO2). Prin experienta pe care o voi prezenta se va demonstra totusi formarea NO.
ORIENTAREA ATENTIEI SPRE CEEA CE ESTE ESENTIAL
Pe parcursul experientei se va urmari culoarea gazului care se degaja si schimbarea acestuia in contact cu oxigenul din aer.
EFECTUAREA DEMONSTRATIEI
Intr-o eprubeta cu tub lateral se introduce un span de cupru. Tubul lateral se conecteaza cu un alt tub care permite ca gazul degajat in urma reactiei chimice sa poata fi colectat sub apa. Cu pipeta introdusa in dopul de la gura eprubetei se introduc cateva picaturi de acid azotic. Dupa umplerea eprubetei cu gazul incolor se ridica acestea si se observa schimbarea rapida a culorii gazului din eprubeta. Aceasta devine rosu-brun, specifica hipoazotidei.
ENUMERAREA OBSERVATIILOR
In eprubeta ce a continut spanul se observa aparitia unei solutii de culoare albastra specifica ionilor Cu2+. Gazul care s-a strans sub apa este incolor, specific NO. Dupa ridicarea eprubetei cu gaz acesta devine rosu-brun datorita formarii NO2.
INTERPRETAREA OBSERVATIILOR
Acidul azotic este un agent oxidant puternic si cuprul este reducator. Are loc reactia redox:
3Cu + 8HNO3 3Cu(NO3)2 + 2NO + 4HO
In urmatoarea etapa NO este oxidat de oxigenul din aer:
NO + 1/2O2 NO2
CONCLUZIONAREA OBSERVATIILOR
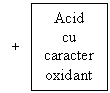
In urma efectuarii acestei experiente si reactiei cuprului cu acidul sulfuric se poate prezenta o schema generala:
H2

|
H2O |
II. Experimentul frontal
Experiente de acest tip pot fi efectuate de catre elevi individual sau pe grupe. Prin efectuarea acestora i se ofera elevului posibilitatea de a participa in mod direct: la perceperea fenomenelor, la cunoasterea proprietatilor substantelor putand sa sesizeze utilizarile acestora in practica.
Proprietatile chimice ale acidului clorhidric pot constitui tema unui experiment frontal. Indicatiile de lucru pot fi prezentate intr-o fisasau se poate lucra cu ajutorul manualului.
Experienta 1
Actiunea acidului clorhidric asupra indicatorilor.
Experienta 2
Actiunea HCl asupra metalelor.
Experienta 3
Actiunea HCl asupra acizilor metalici.
Experienta 4
Actiunea HCl asupra bazelor.
Experienta 5
Actiunea HCl asupra sarurilor.
Experienta 6
Reactia HCl cu amoniac.
Profesorul generalizeaza proprietatile chimice ale acidului clorhidric prezentand urmatoarea schema:
MCln+H2
M2On MCln+H2O
M(OH)n MCln+H2O
MmAn MCln+HmA
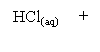
c) Criteriul capacitatii umane
Acesta include notiunea de capacitate de investigare experimentala, adica metoda experimentului stiintific in cunoasterea realitatii. In functie de sfera acestor capacitati, experimentele pot fi:
I - experimentele pentru deprinderi motorii;
II - experimente pentru deprinderi intelectuale.
Aceasta clasificare nu poate delimita strict sfera experientelor ce se desfasoara in laboratorul de chimie. Este importanta precizarea faptului ca nu exista expeienta care sa fie destinata in exclusivitate insusirii deprinderilor motorii in afara deprinderilor intelectuale, iar fiecare activitate experimentala este conceputa sub forma unei anumite strategii de invatare.
I. Experimente pentru deprinderi motorii
Inca din primii ani de studiu al chimiei elevii sunt pusi in situatia de a lucra cu aparatura de uz general, confectionata din sticle (eprubete, pahare Berzelius, pahare Erlenmeyer, palnii etc.) si cu ustensilele de laborator (cleste pentru eprubete, spatule, linguri de ars etc.), sa manipuleze sursele de incalzire.
Prin efectuarea experientelor prevazute in programa scolara elevii reusesc sa-si formeze deprinderile motorii necesare.
In liceu elevii claselor cu profil de chimie iau contact cu unele elemente de analiza cantitativa si anume cu analiza volumetrica.
Analiza volumetrica permite determinarea
continutului unui anumit component al
substantei de analizat, prin masurarea exacta a volumului de reactiv, de concentratie cunoscuta, care reactioneaza cantitativ cu componentul cautat.
Deoarece analiza volumetrica urmareste determinarea substantelor in amestec prin masurarea exacta a volumelor de solutii utilizate, o problema importanta este aceea a aparaturii necesare. Vasele utilizate in analiza volumetrica sunt:
baloane cotate care se folosesc pentru pregatirea solutiilor de concentratii cunoscute;
cilindrii gradati utilizati in masurarea aproximativa a volumelor de solutie;
pipete pentru masurarea cantitatilor mici de solutie;
biurete, vase cu care se masoara volumul de solutie in timpul titrarii.
Pentru a utiliza aceste ustensile de laborator este necesara formarea unor deprinderi motorii mai deosebite.
Elevii vor fi pusi in situatia de a efectua operatia de titrare - aceasta necesitand o tehnica deosebita. Dar in afara de a-si forma deprinderi motorii de efectuare a acestei operatii, elevii trebuie sa-si formeze deprinderi intelectuale de a alege reactivii necesari pentru dozare, de a prelucra date obtinute in urma operatiei de titrare.
II. Experimente pentru formarea si dezvoltarea deprinderi intelectuale
Experiente pentru invatarea de notiuni si concepte
Prin seturi de experiente prezentate intr-o fisa de lucru, sau utilizand indicatiile din manual sau dintr-un caiet de lucrari practice, elevii pot stabili, de exemplu: "metodele de obtinere si proprietatile unui nemetal (clorul, sulful, etc.), proprietatile chimice ale unui metal (magneziu, fierul, etc.), proprietatile chimice ale unui acid sau ale unei baze etc.
Experiente pentru stabilirea si verificarea unor reguli
In scopul stabilirii egalitatii dintre echivalentii de acid si baza ( nH O = nHO ), deci a verificarii regulii CaVa = CbVb se poate realiza titrarea acid-baza in scopul determinarii concentratiei unei baze sau acid.
Experiente pentru rezolvarea unor probleme
Pentru a intari convingerea elevilor ca reactiile chimice in desfasurarea lor respecta legi general valabile este util ca inaintea prezentarii unei probleme sa se efectueze experienta sau experientele care sunt obiectul acelei probleme (daca este posibil).
Astfel, pentru a studia reactia de bromurare a benzenului se poate efectua o activitate experimentala si rezolva o problema.
Experienta:
Intr-o eprubeta curata se introduc 2-3 ml benzen. Se adauga 2-3 g pilitura de fier si 5ml solutie de brom in tetraclorura de carbon. Se incalzeste amestecul de reactie de 60-70 C pe baie de aburi. Se observa degajarea de acid bromhidric si decolorarea solutiei de brom.
Pornind de la aceasta experienta se poate formula o problema de tipul:
La bromarea benzenului rezulta un amestec de mono- si dibrobenzen. Daca procentul de brom din amestecul de produsi bromurati este de 40%, care va fi compozitia in procente a amestecului.
In unele cazuri elevii sunt solicitati sa rezolve probleme ce au la baza rezultatele unor experiente efectuate anterior sau pe baza unor date din literatura de specialitate. Astfel se poate propune o problema ce are la baza masurarea pH-ului cu ajutorul unui pH-metru.
-100 ml solutie de acid clorhidric diluat se titreaza cu o solutie de NaOH-0,1N. Se urmareste variatia pH-ului in timpul titrarii. Rezultatele sunt inregistrate in tabel.
|
VHO-(ml) | ||||||||
|
pH |
|
VHO-(ml) | |||||||
|
pH |
Se cere:
a) trasati curba pH=f(V);
b) din grafic stabiliti punctul de echivalenta;
c) care este normalitatea solutiei de acid clorhidric?
d) ce indicator se va utiliza: metilorage, albastru de bromtimol sau fenolftaleina?
Elevii pot fi solicitati sa formuleze probleme pe baza unor experiente efectuate. Astfel se pot executa cateva experiente:
Reactia metalelor cu acizii.
Reactii acido-bazice.
Apoi elevii vor prezenta enuntul unor probleme care au la baza experientele executate.
d) Criteriul locului in lectia de chimie
Dupa locul pe care il ocupa in lectie, experimentele de laborator se pot clasifica in:
I - experimente pentru stimularea interesului fata de noile informatii (se efectueaza in momentul de introducere in lectie):
II - experiente pentru invatarea noilor informatii, aprofundarea sau extinderea lor (in lectia propriu-zisa);
III - experimente pentru fixarea cunostintelor (se introduc pe parcursul lectiei in momentele de feed-back sau in lectii de recapitulare);
IV - experimente pentru evaluare (locul lor este valabil putand fi utilizate la inceputul invatarii, pe parcursul ei sau la sfarsitul procesului de invatare).
LECTIA DE LABORATOR
Lectia de lucrari de laborator este destinata muncii independente a elevilor, pentru fixarea cunostintelor, pentru formarea priceperilor si deprinderilor practice.
Lucrarile de laborator sunt cele mai importante lectii de chimie, deoarece valoarea lor instructiv-educativa nu poate fi suplinita de nici o alta activitate in procesul cunoasterii.
In cadrul lectiilor de laborator sarcinile didactice sunt specifice, ca de altfel si locul particular (laboratorul) in care se desfasoara activitatea propusa.
Pentru a-si atinge scopul este necesar ca lucrarile de laborator sa fie bine organizate. Scopul lucrarilor de laborator fiind fixarea temeinica a cunostintelor, lucrarile se aleg in asa fel inct sa se refere la problemele esentiale din programa analitica. Se va avea in vedere ca exista o strnsa legatura intre cunostintele predate si experientele ce se vor efectua. Experientele alese vor fi simple si sugestive, pentru a concretiza rapid cunostintele teoretice ce urmeaza a fi fixate. Timpul pentru efectuarea lucrarilor trebuie just dozat, astfel incat sa nu existe timpi morti, dar nici sa nu fie necesar un ritm rapid de executie, care ar avea drept consecinta neintelegerea fenomenelor reproduse. Pentru a evita aceast, profesorul anunta tematica lucrarilor, normeaza timpul necesar pentru executarea fiecarei experiente in parte.
Lectia de laborator se poate desfasura fie frontal, toti elevii executnd in acelasi timp (pe grupe sau individual) acelasi experiment, fie pe grupe, care executa in acelasti timp experimente diferite. Organizarea experientelor dupa metoda frontala prezinta pentru profesor o serie de avantaje si anume:
Stimuleaza elevii in efectuarea corecta a experimentului, toti urmarind aceleasi rezultate;
Usureaza conducerea lectiei, controlul elevilor, discutarea rezultatelor obtinute si formularea concluziilor.
Lucrarile de laborator vor fi organizate, pe cat posibil, pentru a se executa individual. In cazul cand spatiul si dotarea laboratorului nu permit aceasta, unele lucrari se pot face pe grupe de 2-3 elevi, stabilind, in acest caz in grupe, ordinea de experimentare, pentru a oferi posibilitati egale de lucru tuturor elevilor. Uneori, pentru a putea ilustra toate proprietatile de baza ale unei substante sau ale unui grup de substante, se poate recurge si la experiente cu caracter demostrativ, care vor fi executate de catre unii elevi.
Structura unei lectii de laborator cuprinde urmatoarele etape principale:
a) o parte introductiva, care cuprinde anuntarea temei si organizarea activitatii
b) o parte fundamentala - desfasurarea lucrarilor propriu-zise
c) discutii de incheiere - descprinderea unor concluzii
d) tema pentru acasa.
a) La inceputul lectiei se anunta tema, se arata scopul ei si se da planul lucrarilor ce se vor executa.
Pregatirea elevilor pentru lectia de laborator se ralizeaza prin:
repartizarea elevilor la locul unde urmeaza sa execute lucrarea;
distribuirea unor materiale care nu se gasesc pe mesele de lucru;
instruirea elevilor cu privire la tehnica de lucru; aceasta se face diferentiat, in functie de clasa cu care se lucreaza, de nivelul de pregatire al elevilor, de gradul de dificultate al experimentelor propuse.
Profesorul da anumite instructiuni asupra modului cum se vor face observatiile si cum se vor nota rezultatele, schitand tabelul pentru intocmirea referatului.
Pentru buna desfasurare a lucrarilor, profesorul reaminteste regulile de baza in ceea ce preveste conduita elevilor in laborator si, in mod special, face observatii pentru prevenirea accidentelor.
b) Desfasurarea lucrarilor practice se face pe baza planului stabilit. In aceasta parte a lectiei, profesorul trebuie sa se convinga daca elevii au inteles cu adevarat problemele care se pun si tehnica de lucru, pe baza raspunsurilor primite de la elevi si a felului in care ei lucreaza.
Profesorul va observa modul de lucru al fiecarui elev si ii va obisnui cu observarea corecta a experientelor. Deoarece elevii sunt inclinati ca in descrierea reactiilor pe care le efectueaza sa trecaa direct la concluzii, fara mentionarea fenomenelor care se petrec intermediar (de exemplu, schimbarea culorii inainte de topirea unei substante, aparitia bulelor de gaz pe suprafata metalelor inainte de degajarea propriu-zisa a gazului, in reactia acestora cu acizii, aparitia de precipitat etc.), acestia vor fi indrumati sa faca distinctie intre observatii si interpretarea lor.
Inlocuirea observatiilor prin concluzii contravine unui experiment de calitate. De aceea profesorul conduce observatia si orienteaza discutiile, pentru formularea concluziilor juste ce se desprind din lucrari.
In cazul in care un experiment nu reuseste, acesta va fi reluat in cadrul aceleiasi lectii sau, cel mai tarziu, in lectia urmatoare, lamurindu-se exact cauzele nereusitei. In felul acest se evita neincrederea elevilor cu privire la caracterul obiectiv al fenomenului urmarit, sau la priceperea profesorului.
Dupa executarea fiecarui experiment, elevii isi noteaza in caiete cele observate, inclusiv ecuatiile reactiilor chimice care au avut loc. Pentru a se asigura caracteristicile acestora, un elev le va scrie pe tabla. Cu ajutorul planului de pe tabla, care se completeaza treptat, pe masura ce se executa experientele, cat si in baza datelor notate de elevi, se intocmeste referatul lucrarii respective.
Referatele au mare valoare formativa, deprinzand elevii cu o munca ordonata si sistemica. Acestea trebuie sa cuprinda descrierea experimentului, observatiile elevilor, ecuatiile reactiilor chimice si concluziile si, daca este cazul, schemele instalatiilor folosite. In functie de lucrarea executata, referatul mai poate sa contina raspunsurile la unele intrebari, puse in partea intorductiva a lucrarii, precum si domeniile de aplicare a experimentului.
c) Discutia de incheiere urmareste sa scoata in evidenta importanta teoretica si practica a lucrarilor de laborator si trage concluziile asupra modului cum s-au desfasurat ele. Tot aici, profgesorul verifica schita referatelor elevilor, face observatii pe marginea acestora, noteaza unii elevi, in functie de modul in care au lucrat si de rezultatele obtinute.
Ultimele minute ale unei lectiide laborator sunt rezervate pentru strangerea materialelor si punerea in ordine a locului de munca.
d) Tema pentru acasa reprezinta intocmirea referatului, care cuprinde concluziile experientelor efectuate.
Pentru a ilustra modul cum se organizeaza si se desfasoara o lectie de lucrari de laborator, se dau mai jos trei modele de planuri ale acestui tip de lectie.
|
a) PLAN DE LECTIE DE LABORATOR |
|
|
Data: | |
|
Clasa: |
a VIII-a |
|
Obiectul: |
Chimie |
|
Subiectul lectiei: |
Proprietatile acizilor si bazelor |
Scopul lectiei: |
Consolidarea cunostintelor despre acizi si
baze. Formarea |
|
Tipul lectiei: |
Lucrare de laborator |
Obiective operationale: Pentru a se realiza legatura dintre partea teoretica predata si ceea ce se executa practic, elevii trebuie sa cunoasca:
- Ce sunt acizii? Exemple.
- Ce sunt bazele? Exemple.
- Cum se poate recunoaste un acid si o baza cu ajutorul hartiei indicator.
- Diverse reactii care reflecta proprietatile specifice acizilor si bazelor.
Metode de invatamant folosite: lucrare de laborator frontala, conversatei, demonstartie, experiment.
Mijloace didactice: trudse individuale, stativ cu eprubete, reactivii necesari (se specifica substantele).
DESFASURAREA LECTIEI
Moment organizatoric: 5 minute
notarea absentelor si organizarea activitatii;
repartizarea elevilor la mesele de lucru (materialele si reactivii se distribuie de preferinta inainte de inceperea orei);
se face recomandarea ca nimeni sa nu se atinga de materiale pana in momentul experimentarii;
pe masa sa se gaseasca numai caietul de notite;
in cazul cand spatiul si dotarea laboratorului nu permit executarea tuturor experientelor individual, se grupeaza cate 2 elevi la o trusa. Se anunta ce experiente va efectua fiecare:
elevul nr. 1, experientele: 1-3-5;
elevul nr. 2, experientele: 2-4-6.
Anuntarea temei si organizarea activitatii: 5 minute
Astazi se va face o lucrare de laborator pentru a recapitula cunostintele despre acizi si baze. Tema lucrarii este:"Proprietatile bazelor si acizilor".
Experientele efectuate se vor trece in caiet sub forma unui referat. Se reaminteste structura referatului, schematizandu-l pe tabla.
|
Experiente efectuate |
Observatii asupra desfasurarii experientelor |
Ecuatiile reactiilor chimice care au avut loc |
Concluzii |
Coloana 1 si 3 se completeaza in clasa, pe masura efectuarii lucrarilor; acasa elevii vor completa coloanele 2 si 4, aratand pe scurt conditiile in care se petrece fiecare reactie si concluziile.
Desfasurarea lucrarilor: 30 minute
Planul lucrarilor ce se vor efectua de elevi:
Nr. 1. Actiunea acidului clorhidric asupra indicatorilor.
Nr. 2. Actiunea hidroxidului de sodiu asupra indicatorilor.
Nr. 3. Reactia dintre acidul sulfuric si oxidul de cupru.
Nr. 4. Reactia dintre hidroxidul de calciu si bioxidul de carbon.
Nr. 5. Reactia dintre hidroxidul de sodiu si sulfatul de cupru.
Nr. 6. Reactia dintre acidul sulfuric si clorura de sodiu.
Nr. 7. Reactia de neutralizare a hidroxidului de sodiu cu acidul clorhidric.
(ultima experienta se efectueaza demonstrativ de catre un elev).
Prin metoda conversatiei se reamintesc cunostintele teoretice care stau la baza lucrarilor ce se vor efectua, pe masura ce ele se desfasoara, pentru a realiza legatura dintre teorie si practica si pentru a indruma activitatea elevilor.
- Ce sunt acizii? Exemple.
- Ce sunt bazele? Exemple.
- Cum se poate recunoaste un acid si o baza cu ajutorul indicatorului? Dar o baza?
Se efectueaza experienta 1 si 2, pentru a identifica cele doua substante care se gasesc in solutie in eprubetele A si B.
Concluzie:
Schimbarea culorii indicatorilor turnesol fenolftaleina
Sub actiunea acizilor rosu incolor
Sub actiunea bazelor albastru rosu-carmin
- Cu ce substante pot reactiona acizii? (metale, oxizi bazici, saruri)
Se efectueaza experienta nr. 3. Se scrie ecuatia reactiei care a avut loc.
Cum se recunoaste formarea sulfatului de cupru? (Solutie albastra)
- Bazele cum reactioneaza cu oxizii? (Numai cu oxizii acizi)
Se executa experienta nr. 4. Se scrie ecuatia reactiei care a avut loc.
Ce substanta a rezultat si cum ati recunoscut-o?
Concluzie: acizii si bazele reactioneaza cu unii oxizi rezultand o sare si apa.
- Cu ce substante mai pot reactiona bazele? (Cu sarurile, dar numai bazele alcaline)
Se efectueaza experienta nr. 5. (Metoda de obtinere a bazelor insolubile). Se scrie ecuatia reactiei chimice care a avut loc.
- Cum se prezinta hidroxidul de cupru?
- Acizii pot reactiona cu sarurile? (numai anumiti acizi, cu anumite saruri)
Se efectueaza experienta nr.6. Se scrie ecuatia reactiei chimice care a avut loc.
Ce substanta a rezultat si cum se poate pune in evidenta?
Concluzie: acizii si bazele pot reactiona in anumite conditii cu sarurile, obtinandu-se alt acid sau alta baza si o sare.
- Dar bazele si acizii reactioneaza intre ei? Ce rezulta din reactie? Se scrie ecuatia reactiei.
- Cum se numeste acest fel de de reactie chimica? (Se precizeaza ca reactia de neutralizare are loc numai cand se pune o anumita cantitate de acid si de baza, pentru a rezulta o sare si apa, adica o solutie cu caracter nici bazic, nici acid, ci neutru.)
Un elev executa experienta nr. 7, neutralizand cu o solutie diluata de acid clorhidric o solutie diluata de hidroxid de sodiu, in prezenta de turnesol, pana la obtinerea culorii violet.
Discutia de incheiere: 5 minute
Deoarece s-au tras concluzii partiale, se fac aprecieri numai asupra modului cum s-au desfasurat lucrarile, asupra cunostintelor teoretice constatate, asupra disciplinei din timpul orei.
Se recomanda si se controleaza ca elevii sa lase ordine la locul unde au lucrat.
Tema pentru acasa: 5 minute
Scrierea referatului pe caietul de teme. Se da un exemplu de modul cum se vor completa coloanele 2, 3, 4 pentru experienta nr. 3.
- Prin incalzire se obtine sulfatul de cupru de culoare albastra.
- acizii reactioneaza cu oxizii bazici, rezultand o sare si apa.
|
b) PLAN DE LECTIE DE LABORATOR |
|
|
Data: | |
|
Clasa: |
a VIII-a |
|
Obiectul: |
Chimie |
|
Subiectul lectiei: |
Proprietatile chimice ale metalelor |
Scopul lectiei: |
Consolidarea cunostintelor despre metale.
Formarea |
|
Tipul lectiei: |
Lucrare de laborator |
Obiective operationale:
Arderea metalelor.
Combinarea metalelor cu sulful si halogenii.
Actiunea metalelor asupra acizilor si sarurilor.
Metode de invatamant folosite: lucrare de laborator frontala: conversatia, demonstartia, experimentul.
Mijloace didactice: trudse individuale de sticlarie si ustensilele, reactivii necesari.
DESFASURAREA LECTIEI
Moment organizatoric: 5 minute
notarea absentelor si organizarea activitatii;
repartizarea elevilor la locurile unde vor efectua lucrarea;
distribuirea materialelor si a reactivilor necesari cu recomandarea ca nimeni sa nu se atinga de ele pana in momentul inceperii experimentarii.
Anuntarea temei si organizarea activitatii: 5 minute
Astazi se executa lucrarea de laborator care se intituleaza "Proprietatile chimice ale acizilor". Executareaexperientelor se face individual sau se grupeaza cate doi elevi in subgrupa de lucru.
Desfasurarea lucrarilor 30 minute
|
Experimentul |
Observatii |
Ecuatiile reactiilor |
Concluzii |
|
Arderea metalelor in aer (Mg, Cu) |
- Magneziul arde cu .. - Cuprul arde cu ... |
..O2 Cu + .. |
Reactivitatea metale-lor se poate deduce dupa intensitatea lu-minoasa a scanteilor |
|
Combinarea metalelor cu sulful (Fe) |
- Amestecul se aprinde si arde .... |
|
Metal +. |
|
Combinarea metalelor cu halogenii (Na; Cl2) |
- Sodiul arde in ... si formeaza un .. |
Metal + clor |
|
|
Actiunea metalelor asupra apei: |
- Sodiul reactioneaza . cu apa - Magneziul.... - Cuprul ... |
Na+H2O .+ H2O Cu + H2O |
Reactivitatea metale-lor fata de apa este ... si depinde de ... Metalele..nu reac-tioneaza cu apa |
|
Actiunea metalelor asupra acizilor Zn, HCl, Cu, Fe, H2SO4, Cu |
- Zincul si fierul scot . din .. Nu...Cu...dar reactioneaza cu .. |
Zn + HCl Cu + Hcl Zn + H2SO4 Cu + HnO3 |
Fierul si zincul .. din acizi. Cuprul reactioneaza numai cu . fara sa |
|
Actiunea metalelor asupra sarurilor Zn, Pb(NO3)2 Fe, CuSO4 |
Sarma de cupru ... solutia s-a colorat in ... Cuiul de fier ... |
Zn + Pb(NO3)2 Fe + CuSO4 |
Unele metale scot din.. altele .... Metal1 +Sare2 Metal2 +Sare1 |
Discutia de incheiere: 7 minute
Se fac aprecieri numai asupra modului cum s-au desfasurat experientele, se trag concluzii partiale si se recomanda elevilor sa faca curat la locul de munca.
Tema pentru acasa: 5 minute
Se anunta necesitatea scrierii complete a referatului de laborator in caietul de teme.
|
Valeriu Sunel, Ioana Ciocoiu, Tiberiu Rudica, Elena Bicu |
- Metodica predarii chimiei, Editura Marathon, |
|
|
Ortansa Petroveanu, Olga Petrescu, Rodica Constantinescu |
- Metodica predarii chimiei in liceu, Editura Didactica si Pedagogica, Bucuresti, 1982 |
|
|
S. Fatu, |
- Invatarea eficienta a conceptelor fundamentale de chimie, Editura Corint, Bucuresti, 1997 |
|
|
S. Fatu |
- Metodica predarii chimiei in liceu, Editura Corint, Bucuresti, 1997 |
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 8697
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2024 . All rights reserved