| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
APA IN SISTEMELE BIOLOGICE
Apa este componetul principal al oricarui sistem biologic. Organismele vii reprezinta sisteme apoase inal compartimentate.
"Apa este originea si matricea vietii" ( Albert Szent).
In evolutia sa ontogenetica peocentul din corpul uman descreste continuu de la 97% la embrionul de doua luni la 67 - 74% pentru nou nascut si 58-67% in cazul organismului adult.
Datorita diferentierii celulare cu fiecare noua zi de viata si datorita aparitiei tesuturilor dense, are loc o descrestere a continutului de apa.
Apa este o molecula triatomica, formata din doi atomi de hidrogen si un atom de oxigen. Este o molecula plana caracterizata prin distanta de 0,958Å dintre atomii de hidrogen si atomul de oxigen in planul XoY, cat si de unghiul de 105 pe care il formeaza axele celor doi atomi de hidrogen fata de atomul de oxigen.
Cei 10 electroni ai moleculei de apa sunt distribuiti astfel: doi electroni ai oxigenului pe primul strat - se gasesc in permanenta in apropierea nucleului; 8 electroni de valenta graviteaza pe niste orbite eliptice alungite.
Doua perechi de electroni se afla pe orbite axate pe directiile O - H. Acestia sunt electroni ce formeaza legaturi covalente.
Alte doua perechi de electroni graviteaza pe doua orbitew situate perpendicular pe planul nucleului (electroni neparticipanti) molecula de apa are structura tetraedica - nucleul de oxigen este in centru.
Molecula de apa poate forma legaturi coordinative, punti de O2 cu alte molecule. Fiecare molecula de apa se poate lega coordinativ cu alte patru molecule formand structuri spatiale (ex: gheata).
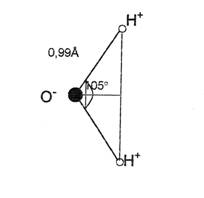
Figura nr. 1 - Structura moleculara a apei / desenata
Legatura dintre atomul de oxigen si atomii de hidrogen in molecula de apa este o legatura covalenta cu caracter partial ionic (40%) care confera oxigenului o incarcare electrica negativa si hidrogenului o incarcare electrica pozitiva. Comportarea electrica a moleculei de apa este in acest caz dipol.
Intre moleculele de apa vecine se formeaza legaturi de hidrogen , fiecare molecula putand forma doua legaturi de hidrogen.
Datorita configuratiei dipolare a moleculei de api se creaza in jurul sau un camp electrostatic intens ceea ce permite legarea cu alte molecule de apa vecine prin legaturi de hidrogen. Ruperea legaturilor intermoleculare se face cu un consum de energie proportionala cu intensitatea legaturilor intermoleculare.
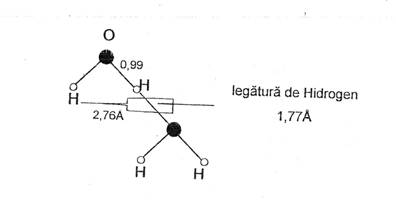
Figura nr. 2 - Legatura de hidrogen - desenat
Modele de structura a ghetii si apei lichide
Apa se gaseste in natura in cele trei stari de agregare: solida, lichida si gazoasa. Fiecare din cele trei stari prezinta particularitati de structurare datorita caracterului dipolar a moleculei de apa si a legaturilor de hidrogen pe care aceasta molecula le poate realiza.
Starea gazoasa
Cu ajutorul difractiei cu raze X pe cristale de gheata s-a demonstrat ca moleculele de apa sunt dispuse in structura spatiala tetraedrica.
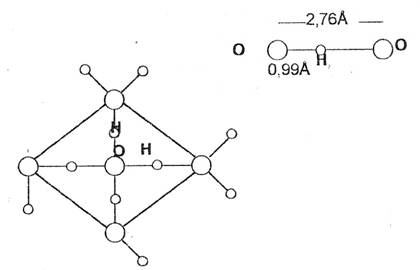
Figura nr.3 - Structura tetraedrica a apei solide -desenat
Aceasta structura este destul de goala, avand o densitate calculata de aproximativ 0,9g/cm3.
Un cristal de gheata este format din mai multi tetraedri dispusi spatial care confera stabilitate dar si o structura suficient de goala.
Prin topirea ghetii forma tetraedrica se modifica, pentru modificarea configuratiei fiind necesara caldura latenta de topire. Distrugerea configuratiei de cristal se face ca unele spatii din acest cristal sa fie ocupate de alte molecule de apa ceea ce explica cresterea densitatii apei spre 4C cand densitatea este maxima de 1g/cm3. odata cu cresterea temperaturii peste 4C apare o agitatie termica suficient de mare ce determina micsorarea densitatii moleculelor de apa peste aceasta temperatura.
Pentru ca o molecula de apa sa inghete ea trebuie sa cedeze mediului 1,44kcal stiut fiindca energia legaturilor de hidrogen pentru gheasa este de 10kcal/mol. Din acest bilant energetic se poate deduce ca aproximativ 15% din legaturile de hidrogen se rup atunci cand gheata se topeste. Concluzia dedusa de aici este ca apa contine inca 85% legaturi de hidrogen dupa dezghetare deci configuratie spatiala de gheata.
Pauling propune o forma de "cusca" caracteristica pentru apa pura. In aceasta configuratie o molecula de apa libera este inconjurata de 20 de molecule de apa legata prin legaturi de hidrogen. Aceasta structura poarta numele de clatrat, fiind specifica pentru apa la 4C.
In interiorul celulei avem:
apa de hidratare pe macromolecule
apa legata cu rol specific de structuralizare a macromoleculelor cat si de structuralizarea a apei de catre aceste macromolecule in diversele lor configuratii spatiale.
Apa legata are proprietati specifice fata de apa normala.
Datorita fortelor electrostatice generate de legatura de hidrogen cat si de cuplareaa dintre moleculele de apa in apropierea unor macromolecule care isi modifica structura prin modificarea functiei sale speciale.
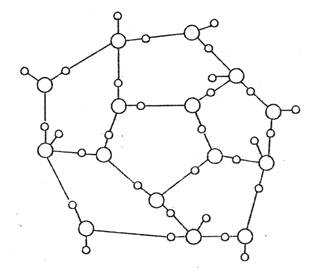
Figura nr. 4 - Structura de clatrat -dsenat
Straturile macromoleculare pot fi in numar limitat datorita fortelor de interactiune dintre ele.
Primul strat fata de macromolecula este mai legat, cu o mobilitate scazuta iar stratul II si III fiind cu forte de legatura mai scazute.
Nu trebuie confundata in totalitate apa legata de apa de hidratare.
Apa citoplasmatica:
rezista la hidratare;
nu ingheata chiar la - 20 C;
nu are proprietatile obisnuite de solvent la cristaloizi;
nu este transferata prin membrane in schimbul osmotic dintre celule si mediul extern;
formare de cristali hidrati - moleculele hidrofobe, in momentul dizolvarii in apa, creaza o cavitate, devenite molecule interstitiale in structura de clatrat (cazul gazelor hidrocarburice - metan - sau al unor anestezice);
formare de retele de apa in apropierea macromoleculelor prin structurarea apei pe aceste macromolecule (exemplu: colagenul cu molecule de apa in forma de retea);
Apa ca mediu dispersant, dizolvant si ionizat
Molecuele polare de apa determina in jur un camp electric intens ceea ce implica ca apa sa fie un foarte bun solvent.Apa este mediu dispersant al particulelor coloidale in care se desfasoara procesele biofizice si biochimice ale metabolismului celular.
Apa rupe coeziunea macroscopica a substantelor dizolvate.
Dispersia substantelor dizolvate prin interactiune dintre dizolvant si dizolvat se numeste solvare in cazul dizolvantului si hidratate in cazul apei.
Substantele macromoleculare organice si macromoleculare nedisociabile disperseaza in apa datorita existentei in molecula lor a legaturilor hidrofobe.
Solubilitatea lor depinde de numarul de legaturi hidrofobe raportate la greutatea moleculara a substantelor (glucoza, uree).
Datorita ε = 80 (constanta dielectrica a apei) electrolitii indusi in apa disociaza.
Prezenta acizilor (donori de protoni) sau bazele in apa (acceptori de protoni) modifica pH - ul solutiei care variaza intre 14 si 0.
Apa in sisteme biologice
Organismul viu se prezinta ca un sistem de apa brodat cu proteine , lipide, glucide si alte molecule si macromolecule. In mediul apos, o apa cu un mare grad de structuralizare, au loc toate reactiile importante.
Toate membranele sunt tapetate cu straturi foarte subtiri de apa fixate foarte bine de acestea si formeaza o structura semicristalina.
Se presupune ca o mare importanta in rezolvarea multor probleme medicale este cea a structurii apei din interiorul tesuturilor.
Procentajul reprezentat de apa este legat de activitatea metabolica.
Dentina, cu cel mai redus metabolism din corp, contine doar 10% apa.
In cazul uni tesut malign are loc cresterea ponderei apei datorita tranzitiei de la metabolismul aetob la cela anaerob. Prin metode de rezonanta magnetica nucleara se poate determina procentul protonilor ( implicit al apei) dintr -un tesut. O crestere peste un anumit nivel indica o tumoare sau edem.
Apa este matricea vietii. Constituie solventul universal atat in mediul interstitiar cat si in cel intracelular. Este mediul de transport al substantelor de la un organ la altul. Este mediul de aliminare al produsilor de dezasimilatie, de dispersie. Este necesara in reactia de hidroliza. Este tampon pentru variatiile de temperatura. Degajarea de temperatura prin evaporare si rol de termostat prin caldura specifica mare. In organismele vii apa se gaseste in procente diferite in functie de specie si gradul de dezvoltare ontogenetica. La organismele superioare exista apei se poate clasa astfel dupa locul in care se afla in raport cu celula. Apa intracelulara: 70% din total. Apa extracelulara 30% - interstitial 20% si apa circulanta (vasculara) - 7%. Dupa distributia in tesuturi apa tisulara si extratisulara este reprezentata de umorile apoase, silicoase, lichid cefalorahidian si sange. Dupa interactia cu macromolecule biologice apa poate fi libera sau legata (structurata). Dupa provenienta in organism apa poate fi exogena sau endogena.
Cantitatea de apa in tesuturi depinde de coeficientul lipocitic; raportul dintre cantitate de colesterol hidrofil si cantitatea de acizi grasi hidrofobi. Cu cat un organ sau tesut este sediul unor procese metabolice intense cu atat continutul de apa este mai mare.
Deoarece anabolismul scade cu varsta se constata si o scadere a procentului de apa cu varsta: nou - nascut → 76 - 80%; femei 60 - 80 ani → 56 - 60%.
O distributie a apei:
Par - 4%
Dentina - 10 - 9%
Schelet si sesut adipos - 30%
Cartilaj - 50%
Substanta alba - 70%
Substanta cenusie - 85%
Ficat - 75%
Muschi - 76%
Cord 77%
Plaman - 81 %
Plasma - 93%
Tesut embrionar - 97%
Modificarile structurii apei in prezenta solvitilor
Solvitul micsoreaza gradul de ordonare a moleculei de apa, similar cu cresterea temperaturii. Apa se dispune concentric in jurul ionilor formand primul si al 2 lea strat de hidratare. Moleculele hidrofobe creeaza cavitati in apa si devin molecule interstitiare.
Proprietati fizice particulare ale apei si implicatiile lor in biologie
Caldura specifica a apei (4,2 J/kgK) foarte mare fata de oricare substanta solida sau lichida.
Conductibilitatea termica (0,59 sec-1cm-1k-1 la 20C) mai mare ca altele lichide permite un "amortizor si transport termic" in vederea evacuarii caldurii in jurul membranelor sau altor structuri care nu poate fi evacuata prin circulatie de lichide.
Densitatea
Cresterea spre 4C a densitatii apei permite supravietuirea in apa cu gheata, la suprafata a pestilor. Constanta dielectrica explica capacitatea mare de ionizare a substantei dizolvate. Punctele de topire la 0C si fierbere la 100C permit un interval mare in care proprietatile apei se schimba foarte putin. Coeficientul de difuziune ce reprezinta cantitatea de substanta ce difuzeaza printr-o suprafata de 1cm2/sec permite difuziunea libera a substantei existente in lichidele biologice. Coeficientul de viscozitate mic permite o deplasare a straturilor apei in mod liber aproape fara frecare si consum de energie. Coeficientul de tensiune superficiala scade cu cresterea temperaturii datorita agitatiei termice si ruperii legaturii de hidrogen.
Rolul si proprietatile fizice ale apei in termoreglare
Omul = homeoterm (tcorp = constanta) - in ciuda variatiilor de temperatura ale mediului sau ale proceselor biologice cu caracter energetic. Pentru a mentine constanta temperatura este necesara existenta unui sistem de termoreglare. Aportul apei in termoreglare trebuie studiat in conditiile:
in zona de confort termic (t = 25C)
la temperatura inferioara neutralitatii termice
la temperatura superioara neutralitatii termice
in conditii extreme de cald si rece
La temperatura mai joasa de confortul termic este necesar aportul de calorii → termogeneza, iar la temperaturi mai ridicate este necesar o pierdere de caldura → termoliza.
Caldura specifica ridicata a apei explicata prin caracterul puternic asociat al hemoglobinei de hidrogen, organismele vii pot primi cantitati mari de caldura din afara sau din interior fara a-si ridica temperatura proprie.
Un adult are 65% apa in 70 kg de corp. Deci un aport de 45000 de calorii ridica un 1C o masa de apa de 45kg. Sistemul metabolic produce pe zi 2500kcal. Apa termostateaza ridicarea temperaturii prin:
conductibilitate termica care indeparteaza hipertermiile locale;
caldura latenta de evaporare care permite prin evaporare pulmonara si cutanata o pierdere importanta de caldura de catre corp.
Rolul evaporarii pulmonare in termoreglare
Un adult elimina prin plaman 300 - 400 g apa la 24 de ore. Hiperemia mediului ambiant antreneaza o polipnee termica capabila sa creasca eliminarea pulmonara a apei.
Evaporarea cutanata se face prin doua mecanisme:
a. perspiratie insensibila - este difuziunea invizibila a vaporilor de apa sau a lichidului intracelular prin straturile cornoase ale epidermei. Prin acest mecanism se pierd 600 - 800 cm3H2O/zi
b. sudatie - este eliminarea prin piele a unui lichid de excretie(sudatia exocrina - adevarata). Prin acest mecanism se elimina pe zi intre 1L si 1,5L in climat temperat. La temperaturi ridicate se ajunge pana la 20 - 25L/zi. Eficacitatea sudatiei este legata de viteza de evaporare care depinde de suprafata pielii udate, de tensiunea de vapori la temperatura considerata.
Apa in reactiile biochimice
Apa participa la hidroliza enzimatica; reactii de oxidoreducere; biosinteza prin deshidratare, biosinteza proteinelor.
Apa grea
In 1932 Urez observa ca rezidurile bacurilor de electroliza au greutate mai mare decat apa obisnuita. Atunci a descoperit apa grea care se obtine prin electroliza la tensiuni mari.
Proprietati fizice:
are greutatea maxima la 11,6C fata de 4C apa normala;
punctul de topire este la 3,802C;
punctul de fierbere este la 101,42C in conditii normale de presiune;
coeficientul de viscozitate este de 12,6 milipoise:
apa de poate marca cu apa grea pentru studiul metabolismului, metoda se foloseste in spectografia de masa sau retractie;
Actiunea apei grele in organism este de a incetini metabolismul; inhiba diviziunea celulara; aboleste partial capacitatea de conducere a influxului nervos; inhiba transportul activ si contractia musculara.
Aceste modificari se explica prin structuralizarea modificata a apei grele; realizarea in celula a unor complexe apa - proteina mai stabile. La inlocuirea apei cu apa grea se genereaza modificari profunde in functia miocardului, forta de contractie scade iar timpul de latenta creste.
Apa celulara si intracelulara
Fortele care mentin apa intracelulara (osmotice) actionand prin membrane. Apa intracelulara reprezinta 55% din greutatea organismului. Apa extracelulara este reprezentata de fluidul interstitial si fluidele circulante. In interiorul celulei exista apa de hidratare pe macromolecule si apa legata cu rol specific de structuralizare a macromoleculelor cat si fenomen invers.
Apa celulara are o serie de proprietati diferite de apa obisnuita atat din cauza dimensiunilor domeniior cu aspecte chimice distincte pe care le ocupa in celula precum si faptului ca solvitii au momente electrice de dipol puternice ce contribuie la organizarea clusterilor.
Apa celulara are o serie de caracteristici precum.
rezistenta neobisnuita la liofilizare
nu ingheata nici la - 20 grade celsius
nu are proprietiti normale de sovatare ale cristaloizilor
nu poate fi transferata osmotic prin memebrana celulara
Datorita fortelor electrostatice generate de legatura de hidrogen cat si de cuplarea dintre moleculele de apa in apropierea unor macromolecule putem vorbi de straturi monomoleculare de apa in apropierea macromoleculelor, straturi care isi modifica structura prin modificarea structurii macromoleculelor. Straturile monomoleculelor pot fi limitate datorita fortei de interactiune dintre ele.
Primul strat fata de macromolecula este mai legat avand o mobilitate scazuta fata de stratul 2 si 3 care au forta de legatura mai mica.
Proprietatile apei citoplasmatice:
rezista la deshidratare;
nu ingheata;
nu are proprietati obisnuite de solvent pentru cristaloizi;
nu este transferata prin membrana in schimbul osmotic dintre celule si mediul extern.
Aceste proprietati caracterizeaza apa legata = apa fixata, necongelabila, nesolvanta, intransferabila, osmotic. In tesuturile animale aproximativ 5 - 10% din apa tisulara este apa legata.
Pentru determinarea structuralizarii apei este rezonanta magnetica nucleara si tomografia de rezonanta magnetica nucleara care da imaginea structuralizata apei corelata cu modificarile functionale sau patologice ale diverselor structuri.
Compatibilitatea apei in organism
Apa intracelulara reprezentand locul reactiilor metabolice. Apa extracelulara constituie mediul inconjurator fiecarei celule; este continut fluidul circulant si interstitial.
Pentru evidentierea diferitelor compartimente pot fi utilizate metode de dilutie, colorare sau izotopi radioactivi. Concentratia substantei test variaza intre compartimente in functie de timp printr-o lege multiexponentiala.
Metoda analizei compartimentale este generala atat pentru determinarea compartimentarii apei cat si pentru studiul medicamentelor.
Proprietatile biofizice ale apei
Caldura speciffica a apei (4,2 J/kgK) foarte mare fata de oricare substanta solida sau lichida permite o stabiliyare a temperaturii in diversele procese biologice (ex. caldura produsa in travaliul muscular sau in procesele energetice aparute in metabolism)
Conductibilitatea termica (0,59 sec-1cm-1k-1 la 20C) mai mare ca altele lichide este un "amortizor si transport termic" in vederea evacuarii caldurii in jurul membranelor sau altor structuri care nu poate fi evacuata prin circulatie de lichide.
Caldura latenta de vaporizare (2,43 J/kg la 37C) este mult mai amre ca la alte lichide fiind un factor determinant si favorizant in homeotermie
Densitatea: cresterea la 4C a densitatii permite supravietuirea in apa cu gheata la suprafata a pestilor.
Constanta dielectrica ε = 78,5 la 25C explica capacitatea mare de ionizare a substantelor dizolvate in apa
Punctele de topire 0C si fierbere la 100C permit o plaja mare in care proprietatile apei se schimba putin
Coeficientul de difuziune (2.4.10-4 cm2/s) reprezinta cantitatea de substanta care difuzeaza printr-o substanta de 1cm2 intr-o secunda. Permite difuziunea libera a substantelor existente in lichidele biologice
Coeficientul de viscozitate este mic ceea ce permite o deplasare a straturilor apei in mod liber fara o frecare si consum de energie intre ele
Coeficientul de tensiune superficiala 75,6.10-3 N/m la 0C scade cu cresterea temperaturii, prin ruperea legaturilor de hidrogen si agitatia termica.
Datorita proprietatilor fizice si chimice exceptionale, apa poate indeplini in organism o serie de functii:
solvent universal
reactant in reactiile de electroliza
agent de dispersie
produs final al reactiilor de oxidare si condensare
vehicol de transport pentru oxigen, nutrienti si hormoni in fluidele circulante ( de exemplu: sangele, limfa)
lichi de flotatie pentru anumite celule libere ( leucocite, eritrocite, etc)
instrument de aliminare a toxinelor ( transpiratia, urina,etc.)
tampon termic datorita marii sale calduri specifice
protector mecanic al structurilor sensibile ( sistemul nervos central, fatul)
Prin faptul ca viata este atat de conditionata de apa, acest lichid, atat de comun, are proprietati cu totul si cu totul remarcabile.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 3448
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2024 . All rights reserved