| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
1) Un gaz ocupa la presiunea de 4 atm un volum de 60 m3. Care va fi volumul ocupat de acest gaz la presiunea de 12 atm, temperatura ramanand aceeasi?
Rezolvare:
p1V1 = p2V2 =>
![]()
2) Un gaz este introdus la temperatura de 0C si presiunea de 150 atm intr-un cilindru care are capacitatea de 40 l. Din acest cilindru se scot 1000 l gaz masurat in conditii normale. Ce presiune va indica manometrul?
Rezolvare:
Aducem gazul din cilindru la conditii normale:
p1V1 = p2V2 =>
![]()
Scoatem 1000 l de gaz: 6000 - 1000 = 5000 l gaz ramas.
Introducem gazul in cilindru si-l comprimam:
p3V3 = p4V4 =>
![]()
3) Intr-un cilindru cu capacitatea de 30 l se afla un gaz la presiunea de 60 atm si temperatura de 0C. Mai introducem in acest cilindru o noua cantitate de gaz care masoara in conditii normale un volum de 1200 l. Ce presiune va indica manometrul?
Rezolvare:
Aducem gazul la conditii normale:
p1V1 = p2V2 =>
![]()
Introducem 1200 l gaz:
1800 + 1200 = 3000 l gaz (conditii normale)
p3V3 = p4V4 =>
![]()
4) Un gaz se gaseste la temperatura de 0C. Cu cate grade trebuie incalzit gazul pentru ca volumul sau sa creasca de doua ori?
Rezolvare:
V = ![]() (1 + αt)
(1 + αt)
V = ![]() =>
=> ![]()
![]() (1 + αt) =>
(1 + αt) => ![]()
![]() => t = 273C
=> t = 273C
5) La 30C un gaz ocupa un volum de 800 cm3. Care va fi volumul aceluiasi gaz la 100C, presiunea ramanand aceeasi?
Rezolvare:
![]() =>
=> ![]()
T1 = 273 + 30 = 303 K; T2 = 100 + 273 = 373 K
![]()
6) Intr-un recipient inchis ermetic se afla 10 l de gaz cu temperatura de 27C si la presiunea de 2 atm. Care va fi presiunea gazului din recipient, daca temperatura scade la 0C?
Rezolvare:
![]()
![]() =>
=> ![]()
T1 = 273 + 27 = 300 K; T2 = 273 K
![]()
7) Un gaz se gaseste la temperatura de 0C. Cu cate grade trebuie incalzit gazul pentru ca presiunea sa creasca de 5 ori?
Rezolvare:
p = ![]() (1 + βt) p = 5
(1 + βt) p = 5![]() =>
=>
![]() =
= ![]() (1 + βt)
(1 + βt)
4 = βt => ![]()
t = 4 ∙ 273 = 1092C
8) Un gaz este incalzit la volum constant de la 25C la 100C. De cate ori va creste presiunea lui?
Rezolvare:
![]() =>
=> ![]()
T1 = 25 + 273 = 298 K; T2 = 100 + 273 = 373 K
![]()
9) Un gaz ocupa la 10C si 720 mmHg un volum de 950 cm3. Care va fi volumul ocupat de acelasi gaz in conditii normale?
Rezolvare:
![]() =>
=> ![]()
![]()
![]()
10) O cantitate de 1,35 g dintr-un gaz cu M = 44 g/mol ocupa la 25C un volum de 0,5 l. La ce presiune se afla gazul?
Rezolvare:
pV = nRT
![]() =>
=> ![]()
![]()
11) Sa se calculeze masa moleculara a unui gaz daca la temperatura de 40C si presiunea 5 atm, 17 l din acesta cantareste 92,73 g.
Rezolvare:
![]() =>
=> ![]()
![]() g/mol
g/mol
12) Care este densitatea CO2 la 27C si 3 atm ?
Rezolvare:
![]()
![]() =>
=> ![]()
13) Un amestec de H2 si N2 contine 2 moli N2. Se cere masa H2 si numarul de moli daca amestecul ocupa 20 l la 20C si 3,2 atm.
Rezolvare:
pV = nRT => ![]()
n = 2,66 moli amestec
![]()
![]()
14) La presiunea de 10 atm un amestec gazos are concentratia in procente volumetrice: 30% CO, 60% N2 si 10% CO2. Determinati presiunile partiale ale gazelor din amestec.
Rezolvare:
![]()
![]()
![]()
15) Presiunile partiale ale gazelor unui amestec gazos format din NO si NO2 sunt egale cu 272 mmHg si respectiv 528 mmHg. Calculati continutul volumetric al gazelor din amestec.
Rezolvare:
![]()
![]() =>
=> ![]() => 34% NO
=> 34% NO
![]() =>
=> ![]() => 66% NO2
=> 66% NO2
16) Se amesteca 5 l CO2 cu presiunea de 1,2 atm cu 4 l O2 cu presiunea de 1 atm si 3 l N2 cu presiunea de 2 atm. Volumul total fiind de 8 l sa se determine presiunea amestecului de gaze.
Rezolvare:
![]() =>
=>
![]()
![]()
17) Un vas cu volumul de 22,4 l contine 2 moli H2 si 1 mol N2 la 273 K. Sa se determine presiunile partiale ale gazelor.
Rezolvare:
![]()
![]()
![]()
![]()
![]()
pV = nRT => ![]()
![]()
![]()
![]()
18) Un amestec de CH4 si N2 cu masa totala de 60 g si compozitia 70% masice CH4 ocupa volumul de 1 litru la o presiune data si temperatura de 130C. Sa se calculeze presiunea totala a amestecului de gaze si presiunile partiale ale celor doua gaze din amestec, considerand ca acest amestec se comporta ca un amestec de gaze perfecte.
Rezolvare:
![]() =>
=>
![]()
T = 273 + 130 = 403 K
![]()
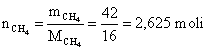
![]()
![]()
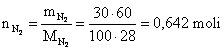
![]()
![]()
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 1570
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2024 . All rights reserved