| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Henderson-Hasselbalch
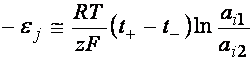
Exista cazuri in care se cere in mod expres ca proba sa nu fie impurificata cu anionii Cl- (acestia ar putea interfera in determinare) iar se utilizeaza in loc de KCl, KNO3 si se realizeaza o punte dubla (jonctiune dubla). In Laboratorul de Analiza Instrumentala exista acest tip de electrod la determinarea I- si la titrarea de precipitare (Cl- si I-).
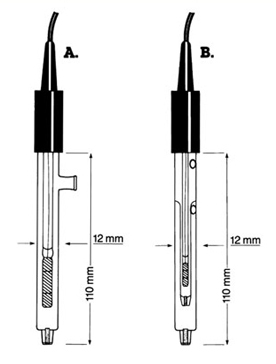
Electrozi de referinta cu jonctiune dubla
Reprezentarea schematica a unei celule electrochimice
1. Celule electrochimice cu jonctiune lichida jonctiuneA ||
- Cand electrodul de referinta este un electrod de speta a II,-a, Hg;Hg2Cl2|Cl-:
M ½ M z+ || KCl ½ Hg2Cl2 ; Hg sau daca avem electrod de referinta Ag; AgCl ½ Cl-
Ag; AgCl ½ Cl- || KCl ½AgCl; Ag
(ind) (ref)
- Cand electrodul indicator este un electrod de speta I, M / Mz+ iar cel de referinta este ENH (SHE)
Þ Pt; H2 ½ H+ Cl- || KCl || Mz+ ½M acesta celula contine 3 faze lichide si 2 jonctiuni
Pentru determinarea potentialului electrodului de calomel:
Pt; H2 ½ H+ Cl- || KCl || Hg2Cl2; Hg
Pentru determinarea potentialului electrodului de Ag; AgCl:
Pt; H2 ½ H+ Cl- ½½KCl ½½AgCl2; Ag
2. Celule electrochimice fara jonctiune lichida
Pt; H2 ½ H+ Cl-| AgCl;Ag
Electrozi metal-complex M|Mz+; A-b, Ag|Ag+;CN-
Mz+ + A-b Û MA-(b-z)
Electrozi de speta a III a
Zn|ZnC2O4, Ca C2O4 |Ca2+
Ag|AgS,CuS|Cu2+
Electrozi cu membrana Electrodul de sticla
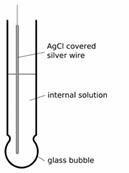


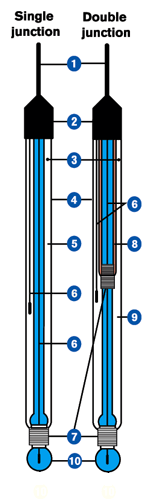 Electrod
de sticla cu electrod de
Electrod
de sticla cu electrod de
referinta Hg;Hg2Cl2/Cl
Electrod de sticla cu electrod
de referinta fir Ag;AgCl/Cl-
Electrod de sticla combinat
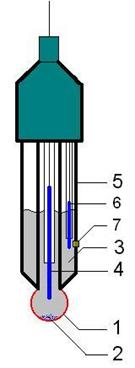
dar poate fi si electrod de calomel.
![]()
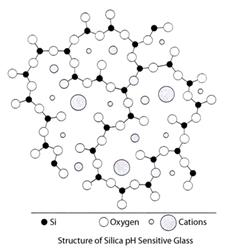
![]()
em ee ei
em e +s RT/zFln (aH+)e aH+)i, s£
e st e - s 0,059 log aH+)i, e st - constanta
em e st - s 0,059 pHe
(membrana)
Ag;AgCl êHCl, sol. pH necunoscut.êê sol. pH cunoscut || KCl êAgCl;Ag
Reprezentarea schematica -celula electrochimica pentru determinarea pH-ului cu electrod de sticla
E = em er,e ej
E = er,i em ej er,e eas potentialul de asimetrie
E = e st - s 0,059 pHe + ej er,e eas e st - s 0,059 pHe
potentialul de asimetrie eas
Ag;AgCl êHCl, sol. pH =7êê sol. pH =7 || KCl êAgCl;Ag
E=¹
Aplicatii analitice
Directe
Determinarea potentiometrica a pH-ului cu electrod de sticla
Solutii tampon standard de pH:
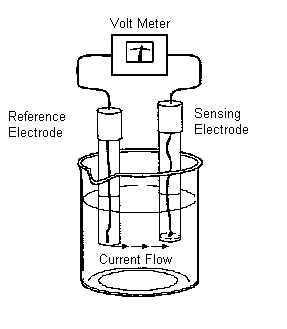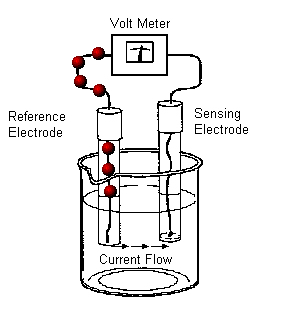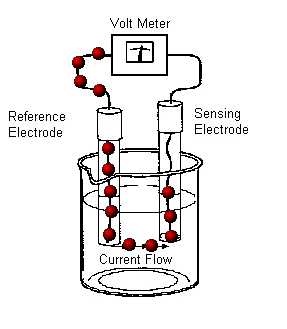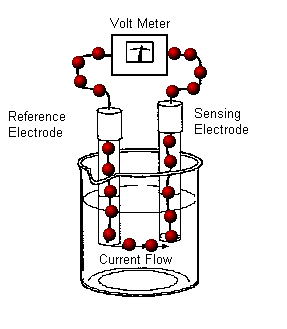

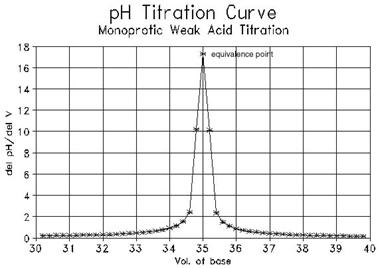
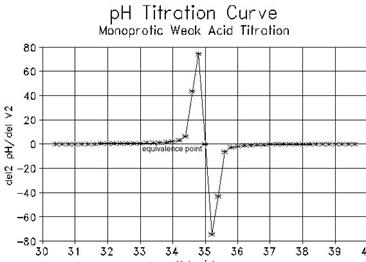
Indirecte -titrari potentionetrice de neutralizare
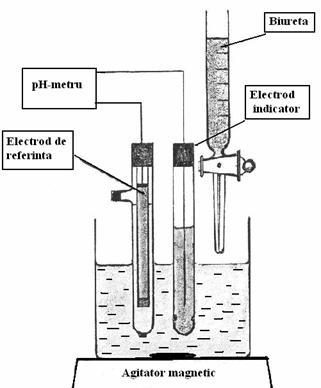
Instalatie experimentala pentru titrari potentiometrice
Exercitiu
Electrodul de chinhidrona
Q +2H+ +2e- Û H2Q
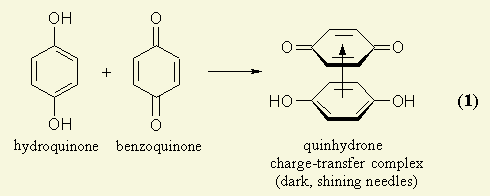
Q;H2Q|H+
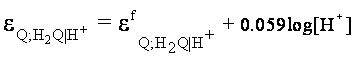
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 2160
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2024 . All rights reserved