| CATEGORII DOCUMENTE |
| Alimentatie nutritie | Asistenta sociala | Cosmetica frumusete | Logopedie | Retete culinare | Sport |
![]()
Introducere - Istoric
Clasificarea tumorilor peniene
Leziunile benigne
Leziuni non - cutanate
Leziuni benigne cutanate
Leziuni cutanate premaligne
Cornul cutanat
Balanita keratozica
Leukoplakia
Leziuni dermatologice cu etiologie virala
Condiloame acuminante
Sarcomul Kaposi
Tumora Buschke-Lwenstein
Carcinomul scuamocelular
Carcinomul in situ
Boala Bowen
Papulomatoza Bowenoida
Eritroplazia Queyrat
Carcinomul invaziv
Preventia
Istoria naturala
Modul de prezentare
Semnele
Simptomele
Diagnosticul
Examinarea
Biopsierea
Examene de laborator
Radiologie
Evaluarea tumorii primare
Evaluarea lanturilor ganglionare
Stadializare
Tratamentul
Tratamentul tumorii primare
Tratamentul topic 5-fluorouracil (5-FU)
Terapia laser
Radioterapia
Radioterapia externa
Brahiterapia
Tratamentul chirurgical
Biopsia - exereza
Circumcizia
Tratamentul chirurgical micrografic - Mohs
Amputatia partiala de penis
Amputatia glandului si postectomia cu grefa
de piele pe capetele corpilor cavernosi
Amputatia totala de penis
Operatii de exereza larga
Reconstructia peniana dupa amputatia
peniana si emasculatie
Tehnici chirurgicale
Amputatia partiala a penisului
Amputatia totala de penis
Tratamentul lanturilor ganglionare
Proceduri modificate
Biopsia limfonodulului santinela (SLNB),
limfodisectia extinsa dincolo de nodulul
santinela, biopsia ganglionara
Citologie aspirativa cu ac fin (FNAC)
Harta limfatica intraoperatorie (IOLM)
Limfodisectia superficiala si disectia inghino-
femurala completa modificata
Limfadenectomia inghino-femurala si ilio-
obturatorie radicala
Tratamentul lanturilor ganglionare
Tehnici chirurgicale
Consideratii anatomice
Biopsia ganglionului santinela
Limfodisectia inghinala modificata
Limfodisectia radicala ilioinghinala
Radioterapia regiunii inghinale
Chimioterahimioterapia
Protocolul de urmarire
(conform ghidurilor EAU)
Tumori maligne non-scuamoase
Carcinomul cu celule bazale
Melanomul
Sarcoamele
Boala Paget
Carcinom adenoscuamos superficial
Boli maligne limforeticulare
Metastaze
Bibliografie
Introducere - Istoric
Una din cele mai vechi referinte in ceea ce priveste conduita terapeutica in cancerul de penis dateaza din primul secol dupa Hristos, Celsus raportand amputarea si cauterizarea consecutiva a bontului penian. Boala era relativ comuna si a fost mentionata in scrieri egiptene, persane, ebraice si indiene.
In 1761, celebrul anatomist Morgagni, care a fost prezent la o penectomie partiala realizata de Valsalva, a descris procedura. Prima descriere detaliata, a unei operatii ce viza tratamentul radical al unui carcinom de penis, ii este atribuita lui Thiersch in 1875.
Sir William MacCormack, pe un lot de 5 pacienti in 1886, a facut penectomii totale, sectionand scrotul cu incizii inghinale bilaterale similare cu cele ale lui Thiersch.
In 1898, Curtis recomanda indepartarea ganglionilor inghinali in bloc si amputarea penisului de la simfiza pubiana.
In 1912, Gibson pleda pentru rezectia in bloc a penisului si a ganglionilor inghinali bilateral.
Din 1924, Barringer si Dean recomandau doar amputatia partiala a penisului la 1,5 cm proximal de leziune, urmata de radioterapie inghinala.
In 1931, Young a raportat rezultatele sale in urma unor penectomii partiale cu disectii ganglionare unilaterale ca tratament al carcinomului scuamos, tehnica practicata din 1907.
Rolul disectiei nodulilor limfatici in cancerul penian a crescut odata cu descrierea anatomica a ganglionilor regiunii inghinale realizata de Daseler in 1948. Cinci ani mai tarziu, Baronofsky descria disectia ganglionilor ilioinghinali, inclusiv aducerea muschiului croitor pentru a acoperi vasele femurale.
Cabanas in 1977 a descris nodulul santinela in lantul nodal inghinal care era primul implicat in metastaze.
Astazi, leziunea primara poate fi abordata prin excizie locala, criochirurgie, radioterapie, terapie laser, amputatie partiala si amputatie totala. Pentru lanturile ganglionare tehnicile chirurgicale de disectie inghino-femurala si ilio-obturatorie sunt consistent imbunatatite.
In perioada 1975-2004 au fost operati in Centrul nostru 156 de pacienti cu cancer penian.
Excizia tumorii a fost practicata la 12 pacienti, amputatia partiala la 105 cazuri, amputatie totala - 25 , emasculatie - 10 cazuri, 4 cazuri de amputatie a glandului cu grefa de piele pe capetele corpilor cavernosi; 47 de limfodisectii inghino-femurale dintre acestea la 20 de pacienti s-a practicat si limfodisectie ilio-obturatorie.
Clasificarea tumorilor peniene (Tabelul nr.1)
|
Leziuni benigne |
Leziuni non - cutanate Leziuni benigne cutanate |
|
Leziuni cutanate premaligne |
Cornul cutanat Balanita Keratozica Balanita xerotica obliterantaLeukoplakia Leziuni dermatologice cu etiologie virala Condiloame acuminante Sarcomul Kaposi Tumora Buschke-Lwenstein |
|
Carcinomul scuamocelular | |
|
Alte carcinoame primitive peniene |
|
|
Tumori mezenchimale |
|
|
Tumori melanocitice |
|
|
Tumori hematopoietice |
|
|
Tumori secundare / metastaze |
Leziunile benigne
Leziuni non - cutanate
Tumorile benigne peniene cuprind chistele de incluzie congenitale si dobandite, chiste de retentie, siringoame si neuriloame.
Chistele de incluzie congenitale apar la nivelul rafeului peno-scrotal.
Chistele de incluzie dobandite sunt mai frecvente dupa circumcizie sau traumatisme.
Chistele de retentie provin din glandele sebacee localizate in zona mucoasa a preputului si din tegumentul penisului.
Chistele de retentie pot aparea in zona parameatala ca urmare a obstructiei glandelor uretrale.
Siringoamele - tumori benigne ale glandelor sudoripare pot deveni mari si simptomatice.
Neurinoamele au fost descrise la nivelul frenului si preputului.
Tumorile benigne ale tesuturilor de sustinere includ angioame, neurinoame, lipoame si mioame.
Angioamele sunt, de obicei, superficiale si apar mai frecvent la nivelul frenului si coroanei glandului ca papule sau macule punctiforme rosietice.
Neurinoamele se prezinta ca papule ferme, albicioase, la nivelul frenului si santului coronar.
Formatiunile peniene si deformarile sau pseudo-tumorile pot aparea dupa autoinjectare sau implantarea de corpi straini. Testosteronul uleios ca si alte uleiuri obisnuite au fost aplicate sau injectate in penis, producand un proces lipo-granulomatos distructiv care poate mima tumora.
Granulomul piogenic poate aparea in locul autoinjectarilor in cadrul terapiei impotentei.
Boala Peyronie atipica sau la debut se poate prezenta ca formatiuni localizate la baza penisului.
Ocazional, flebitele si limfangitele pot produce cordoane sau noduli penieni subcutanati.
Cand diagnosticul este nesigur, orice leziune benigna trebuie tratata prin excizie locala si analiza histopatologica, in vederea excluderii malignitatii.
Leziuni benigne cutanate
Papulele peniene albicioase, papiloamele si papulele coronale sunt, de obicei, leziuni intalnite la nivelul glandului. Apar la aproximativ 15% din barbatii cu varsta postpubertala si mai frecvent la cei necircumcisi.
Se prezinta ca leziuni lineare, curbe sau neregulate in siruri formate din excrescente conice sau globulare, culoarea variind de la albicios galben la rosu si sunt localizate de-a lungul santului coronar.
Sunt considerate angiofibroame acrale; cand sunt de dimensiuni mai mari pot fi confundate cu condiloamele acuminate. Tratamentul nu este necesar de obicei, dar pot fi rezolvate prin fulguratie cu laser CO . Aceste leziuni nu au fost asociate cu malignizarea.
Eritroplazia Zoon este caracterizata printr-o placa stralucitoare eritematoasa sau eroziune care la biopsie demonstreaza straturi celulare normale, dar si un infiltrat dens de plasmocite. De obicei afecteaza glandul, dar si preputul. Tratamentul se face prin circumcizie, dar studiile au aratat si eficienta tratamentului cu laser CO . Totalitatea rash-urilor si ulceratiilor datorate iritatiilor, alergiilor sau infectiilor trebuie incluse in diagnosticul diferential al leziunilor cutanate.
Leziuni cutanate premaligne
Anumite leziuni peniene histologic benigne au fost desemnate ca avand potential malign sau in stransa legatura cu dezvoltarea carcinomului scuamos.
In studiile mari, 42% dintre pacientii cu carcinom scuamo-celular au avut leziuni peniene pre-existente. De altfel, incidenta dezvoltarii acestor leziuni de carcinom scuamo-celular nu este cunoscuta.
Cornul cutanat
Cornul
cutanat penian este o leziune rara. Se dezvolta de obicei pe o
leziune cutanata pre-existenta de tip
Examenul microscopic arata hiperkeratoza, diskeratoza si acantoza. Tratamentul consta in excizie chirurgicala cu o margine de tesut normal in jurul leziunii. Aceste leziuni pot reaparea si pot fi maligne la o noua biopsie chiar daca histologia initiala a fost benigna.
Deoarece aceasta tumora poate evolua spre carcinom, este esentiala evaluarea histologica atenta a bazei si urmarirea atenta a locului de excizie.
Balanita keratozica
Aceste leziuni neobisnuite se prezinta ca excrescente hiperkeratozice, la nivelul glandului si pot avea caracteristici microscopice de carcinom verucos. Au tendinta la recadere si pot reprezenta o forma precoce a acestei tumori. Tratamentul presupune excizie, ablatie cu laser si crioterapie. Leziunile necesita tratament agresiv si supraveghere buna. Fibrosarcomul glandului a fost raportat dupa tratamentul prin crioterapie al balanitei keratozice.
Balanita xerotic obliteranta (BXO) reprezinta o varietate cu localizare genitala a lichenului sclero-atrofic care se prezinta ca pete albicioase la nivelul preputului sau glandului, adesea interesand meatul si uneori fosa naviculara.
Leziunile pot fi multiple si pot avea aspect de mozaic.
Meatul apare albicios, indurat, edematos. Pot aparea eroziuni glandulare, fisuri si stenoza meatala.
Leziunea este mai des intalnita la barbatii necircumcisi, de varsta medie, dar totusi se poate intalni si la copii. Sunt descrise patru stadii ale bolii:
1. leziunea preputului care devine neretractil (fimoza)
2. leziunea preputului si glandului cu aderente intre ele
3. leziunea ce cuprinde preputul, glandul, meatul si uretra anterioara
4. leziuni asociate cu zone neoplazice - carcinom scuamos sau verucos.
Simptomele includ durere, disconfort local penian, prurit, erectii dureroase si obstructie urinara.
Histologic, se observa epiderm atrofic cu pierderea arhitectonicii normale, omogenizarea colagenului in treimea superioara a dermului, combinate cu zone de infiltrat limfocitar si histiocitar.
Leziunile seamana cu cele de lichen scleroatrofic descoperite in alte zone ale corpului.
Anumite studii asociaza balanita xerotic obliteranta cu carcinomul scuamocelular si cu dezvoltarea carcinomului la un interval mare dupa ce o leziune de balanita xerotic obliteranta a fost tratata.
Rara dar foarte dificil de tratat este afectarea uretrala intinsa ce necesita clasic excizia leziunilor si uretroplastie in doi timpi, dar rezultate bune au fost obtinute prin uretroplastie intr-un timp cu grefa de mucoasa bucala plasata dorsal.
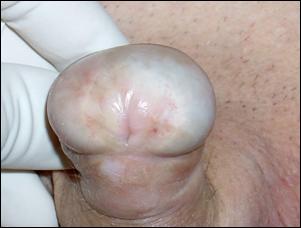
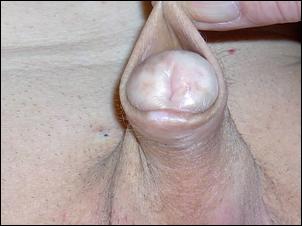
a. b.
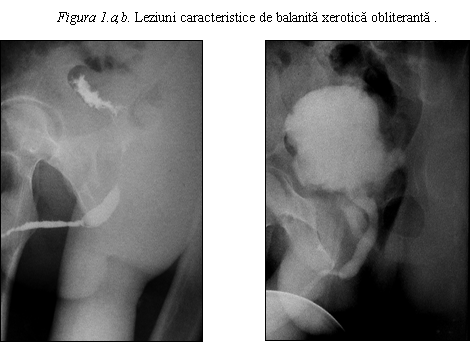
a. b.
Figura 2.a,b. Strictura
intinsa a uretrei anterioare consecutiva BXO.
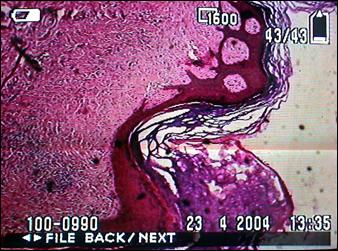
Aspectul anatomo-patologic
Leziuni:
hipercheratoza
atrofie epiteliala
fibroza eozinofila > 4 mm
vacuolizarea celulelor membranei bazale
infiltrat inflamator difuz si focal subepitelial.
Figura 3. Aspect anatomopatologic
Tratamentul consta in aplicarea de unguente topice cu cortizon, cortizon injectabil si excizie chirurgicala. Stenoza de meat este o complicatie frecventa care necesita dilatatii repetate, injectii cu cortizon sau chiar meatoplastie.
Este esentiala urmarirea atenta cu efectuarea de biopsii daca apar modificari.
Leukoplakia
Leziunile se prezinta ca placi albicioase unice sau multiple care afecteaza adesea meatul.
Histologic se observa hiperkeratoza, parakeratoza si hipertrofie cu edem dermal si infiltrat limfocitar. Examinarea microscopica atenta este necesara pentru excluderea malignitatii.
Tratamentul implica eliminarea iritatiei cronice si circumcizia. Excizia chirurgicala si iradierea au fost folosite in tratamentul leukoplakiei. Leziunea a fost asociata cu carcinom scuamocelular in situ si cancer verucos penian.
Din cauza relatiei stranse cu carcinomul, urmarirea atenta a locului exciziei, cu biopsii periodice ale leziunilor incomplet excizate, este necesara pentru detectarea precoce a modificarilor maligne.
Leziuni dermatologice cu etiologie virala
Studiile sugereaza implicarea virala in anumite leziuni peniene. Condiloamele acuminate si boala Bowen par a fi legate de infectia cu papilomavirusuri umane (HPV).
Herpes virusul uman 8 (HHV), cunoscut ca asociat sarcomului Kaposi, este implicat puternic ca agent etiologic in SIDA.
Condiloame acuminante
Condiloamele acuminate sunt excrescente mari, papilomatoase, in general considerate benigne.
Cunoscute ca nevi genitali sau venerieni, au predilectie pentru zonele umede, glabre ale corpului si pe ariile cutaneo-mucoase din zonele perineale si genitale.
Leziunile sunt moi, friabile si pot fi unice, pediculate sau cu aspect conopidiform cu baza larga de implantare. Leziunile sunt rare inainte de pubertate si cand apar pot sugera abuzul sexual.
La barbat, condiloamele apar frecvent la nivelul glandului, corpului penisului si preput. Meatul trebuie atent inspectat. Leziunile reapar in locuri noi dar si in cele tratate anterior. La aproximativ 5% din pacienti exista afectare uretrala care se poate extinde la uretra prostatica. Rar, afectarea severa uretrala poate necesita uretroplastie.
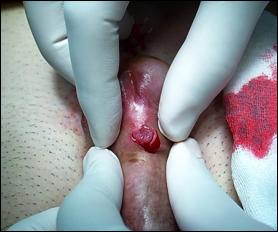
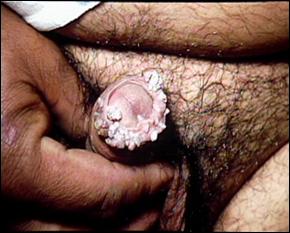
a. b. Figura 4. Condiloame acuminante. a) peniene; b) uretrale.
Afectarea vezicala, rar citata, este greu de tratat eficient. La examenul microscopic se observa un strat extern de tesut keratinizat sustinut de stroma conjunctiva. Stratul epitelial este format din siruri bine ordonate de celule scuamoase. De obicei este prezent un infiltrat dermal limfocitar. Tratamentul acestor leziuni cu podofilina poate induce modificari histologice sugestive de carcinom. Asadar, orice tratament topic cu podofilina trebuie sa fie precedat de biopsii din leziunile mari ce par a fi condiloame acuminate.
Interesul pentru condiloamele acuminate a crescut foarte mult, stimulat de intelegerea relatiei dintre infectia cu HPV si respectiv anumite neoplasme.
Termenii - candiloame genitale, nevi venerieni, nevi genitali, infectie genitala cu HPV - se refera in intregime la o boala cu transmitere sexuala cauzata de HPV.
Desi infectia cu HPV nu este o boala cu transmitere sexuala ce trebuie raportata, numarul infectiilor noi este estimat la 500.000-1.000.000 cazuri/an. Prevalenta nu este cunoscuta.
Infectia cu HPV este recunoscuta ca principalul agent etiologic in displazia cervicala si in cancerul cervical.
Un numar important de parteneri ai femeilor cu condiloame cervicale prezinta leziuni neidentificabile prin inspectia obisnuita si nu sunt constienti ca sunt infectati sau ca au potential de infectare.
La examinarea microscopica, koilocitul este patognomonic pentru infectia cu HPV, reprezentand o celula ce prezinta nucleu atipic inconjurat de o cavitate.
Tehnicile de hibridizare a ADN-ului au fost folosite pentru identificarea si clasificarea infectiilor cu HPV si au putut fi identificate astfel 40 de subtipuri.
Tipurile virale 6, 11 si 42-44 sunt asociate cu condiloame mari si grad scazut de displazie.
Tipurile 16, 18, 31, 33, 35 si 39 sunt asociate cu potential mare de malignizare.
Studiile recente sugereaza ca proteinele virale de transformare tumorala ale virusurilor 16 si 18, mai ales proteinele E6 si E7, pot activa genele supresoare tumorale cu producerea pRb si p53 si pot fi agentii cauzali ai anumitor tipuri de cancer penian.
E6 se leaga cu proteina p53 ducand la degradarea rapida a acesteia rezultand instabilitate cromozomiala, mutatii ale ADN-ului, si aneuploidie.
E7 se leaga si fosforileaza proteina retinoblastomului pRb, ducand la eliberarea de factor de transcriere E2F care activeaza mitoza.
Infectia HIV poate predispune pacientii afectati de dezvoltarea rapida a carcinomului scuamos prin pre-existenta infectiei HPV. Boala subclinica poate fi detectata prin aplicarea de solutie de acid acetic 5% la nivelul penisului, urmata de inspectiile cu lupa. Leziunile devin albicioase si pot fi observate leziunile plate adesea invizibile la inspectia obisnuita. Leziunile aceto-albicioase nu se datoreaza mereu infectiei cu HPV, iar pentru confirmarea diagnosticului trebuie realizata biopsia.
Inspectia atenta a bazei penisului, scrotului si zonei inghinale sunt esentiale. Trebuie examinat meatul si daca se confirma leziuni, trebuie efectuata uretroscopie.
Tratamentul topic al condiloamelor cu podofilina sau acid tricloracetic este bine stabilit si are succes in cazul leziunilor mici.
Se aplica saptamanal o solutie de podofilina 0,5-1 % pentru o perioada de 2-6 saptamani.
Deoarece tegumentul normal poate fi afectat de podofilina, trebuie urmarit atent un asemenea tratament, cu toate ca protocoalele de autoaplicare au fost utilizate cu succes.
Circumcizia indeparteaza leziunile preputiale, asigura expunere larga pentru tratamentul topic si permite monitorizarea post-tratament.
Fulguratia si excizia pot fi oportune pentru evitarea zonelor mari de macerare, ulcerare si infectie secundara.
Tratamentul chirurgical cu laser a fost utilizat extensiv in tratamentul condiloamelor.
Tratamentul chirurgical utilizand rezectoscopul pediatric poate fi util pentru rezolvarea leziunilor mari intrauretrale.
Pentru rezecarea leziunilor va fi folosita cea mai mica putere de rezectie, iar utilizarea electrocauterului trebuie redusa la minim pentru evitarea dezvoltarii stricturilor uretrale.
Leziunile intrauretrale sunt dificil de tratat. Aplicarea zilnica a cremelor cu 5-Fluorouracil timp de 3 saptamani a fost folosita cu succes pentru tratarea leziunilor uretrale.
Trebuie avut grija sa se aplice crema pe lungimea uretrei si sa se evite aplicarea pe tegumentul scrotal. Utilizarea unei creme pe baza de oxid de zinc sau a unui suport scrotal pot fi ajutatoare.
Asocierea cremelor cu 5-FU la terapia laser, nu creste rata vindecarilor.
Diferite tipuri de interferon au fost utilizate in tratamentul condiloamelor. Un studiu randomizat a demonstrat ca utilizarea intra-lezionala, pe termen scurt, de interferon alfa-2b are efect asupra condiloamelor. Utilizarea altor tipuri de interferon este mai putin clara. Terapia cu interferon este rezervata leziunilor extensive si refractare.
Infectia cu HPV este comuna si asa cum a fost aratat mai sus are potential carcinogenetic.
Condilomatoza a fost asociata cu carcinomul scuamo-celular penian. Transformarea maligna a condiloamelor in carcinom scuamo-celular a fost raportata. Condiloamele acuminate localizate in zonele perianale, scrotale si orale au prezentat de asemenea degenerare maligna.
Incidenta crescuta a neoplaziei intraepiteliale peniene a fost demonstrata la partenerii femeilor cu neoplazie intraepiteliala cervicala.
Infectia HPV a fost implicata in dezvoltarea papulomatozei Bowen. Rolul HPV in transformarea leziunilor condilomatoase catre leziuni maligne, continua sa fie studiat cu atentie.
Sarcomul Kaposi
Sarcomul Kaposi, descris prima data in 1972, reprezinta o tumora a sistemului reticulo-endotelial. Se prezinta ca o leziune cutanata neovasculara, ca o papula proeminenta, dureroasa, sangeranda sau ca leziune ulceroasa cu aspect albastrui. Histologic, tumora are aspect neovascular cu proliferari endoteliale si celule fusiforme.
Sarcomul Kaposi a aparut initial rar in Europa si America de Nord. Se caracteriza printr-o tumora lent progresiva ce afecteaza extremitatile distale la cei varstnici. Apare in special la est-europeni, evrei sau italieni. Sarcomul Kaposi a fost descoperit si la alte populatii: tinerii negri africani si pacientii cu tratament imunosupresiv. Boala este strans asociata cu pacientii ce prezinta SIDA si evolutia clinica fiind mai agresiva la acestia.
Subcategoriile Sarcomului Kaposi:
1). Sarcomul Kaposi clasic ce apare la pacientii fara imunodeficienta, iar evolutia este putin zgomotoasa si rar fatala.
2). Sarcomul Kaposi asociat tratamentului imunosupresor ce apare la pacientii care primesc tratament imunosupresor pentru transplant de organ sau alte indicatii. Adesea regreseaza prin modificarea dozelor imunosupresoarelor.
3). Sarcomul Kaposi african care apare la barbatii tineri si care poate fi silentios sau agresiv in evolutie.
4). Sarcomul Kaposi epidemic sau asociat infectiei HIV care apare la pacientii cu SIDA.
Formele clasice si imunosupresive sunt considerate nonepidemice.
Sarcomul Kaposi nonepidemic limitat la penis trebuie tratat agresiv deoarece este rar asociat cu afectarea difuza a organului. Excizia chirurgicala localizata, sau iradierea externa s-au dovedit eficace. In conditiile extensiei mai mari este indicata amputatia de penis. La pacientii imunosupresati, sarcomul Kaposi regreseaza adesea la intreruperea terapiei imunosupresive; daca nu apare regresia acestora, trebuie efectuata excizie locala sau iradiere.
In tratamentul sistemic al formelor multisistem s-au utilizat interferon si terapie citotoxica.
La pacientii cu SIDA, imunodeficienta secundara predispune gazda la aparitia sarcomului Kaposi cu frecventa de 1/7000 de cazuri.
Primul caz de sarcom Kaposi epidemic asociat infectiei HIV a fost raportat in 1981, iar primul caz cu afectare peniana a fost raportat in 1986. De atunci, sarcomul Kaposi penian a devenit o leziune relativ comuna la pacientii cu SIDA. La primele 1000 de cazuri cu SIDA raportate de CDCP, incidenta sarcomului cu localizare peniana a fost de 44% la homosexuali, de 16% la bisexuali si la utilizatorii de droguri intravenoase si 0% la pacientii hemofilici.
Anumite studii au raportat prezenta sarcomului Kaposi epidemic la pacientii HIV negativ, fapt ce sugereaza ca anumite practici sexuale si un agent cu transmitere sexuala pot fi implicate pentru aceasta forma de boala.
Alte studii indica o relatie stransa intre infectia cu HHV 8 si dezvoltarea sarcomului Kaposi la pacientii cu HIV.
Odata cu larga raspandire a SIDA din 1990, sarcomul Kaposi penian poate fi considerat pe locul doi dintre tumorile peniene, dupa carcinomul scuamocelular.
Desi sarcomul Kaposi poate fi semnul de debut pentru multi dintre pacientii cu SIDA, afectarea precoce a penisului este rara la acestia. Tratamentul este directionat catre paliatie.
Afectarea glandului penian si a corpului spongios poate produce stricturi uretrale, ce necesita uretrostomie proximala. De obicei, aceasta afecteaza mictiunea in pozitie ortostatica. In cazul leziunilor intinse ce afecteaza penisul, se impune amputatia de penis partiala sau totala.
Radioterapia si utilizarea laserului Nd:YAG au fost utilizate pentru usurarea obstructiei uretrei distale.
Tumora Buschke-Lwenstein
(carcinom verucos, condilom acuminat gigant)
Tumora Buschke-Lwenstein a fost descrisa initial de Buschke in 1925 si mai tarziu in USA de Lwenstein (1939).
Ackerman (1948) a descris in cavitatea bucala o tumora similara histologic.
Carcinoame verucoase ale laringelui, vulvei si penisului au fost descrise de Goethals si colaboratorii (1963).
Desi unele carcinoame verucoase non-peniene dau metastaze, metastaze din tumori Buschke-Lwenstein nu au fost descrise. Concret, tumora Buschke-Lwenstein determina invazie locala, produce compresiune si distrugere a tesuturilor adiacente, eroziuni uretrale si fistule.
Dezvoltarea agresiva, combinata cu sangerarea, secretiile si mirosul, determina pacientul sa se prezinte la consult medical.
Incidenta reala a tumorii Buschke-Lwenstein este necunoscuta, dar probabil este mai mare decat cea raportata, deoarece multe cazuri au fost asimilate cu carcinomul scuamocelular penian
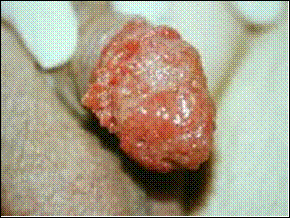 carcinomul
scuamocelular penian cu grad scazut de malignitate. Analiza
retrospectiva a mai multor studii a aratat ca au fost asociate
carcinomului scuamocelular un anumit numar de cancere verucoase sau
condiloame gigante.
carcinomul
scuamocelular penian cu grad scazut de malignitate. Analiza
retrospectiva a mai multor studii a aratat ca au fost asociate
carcinomului scuamocelular un anumit numar de cancere verucoase sau
condiloame gigante.
Tumora Buschke-Lwenstein difera de condiloamele acuminate in sensul ca cele din urma in afara dimensiunii, raman mereu superficiale si nu invadeaza niciodata tesuturile adiacente.
Tumorile Buschke-Lwenstein inlocuiesc, invadeaza si distrug structurile adiacente prin compresiune.
Figura 5. Carcinom verucos.
Pe langa extensia locala, s-a demonstrat ca nu
exista modificari histologice la examenul microscopic si ca
nu metastazeaza.
La examenul microscopic tumora formeaza o masa bogata, cu largi digitatii celulare, adesea cu extensie profunda in tesutul subadiacent. Aceste digitatii sunt formate din celule scuamoase bine diferentiate ce nu prezinta anaplazie celulara si sunt inconjurate specific de o zona densa de infiltrat inflamator acut si cronic.
Ca si condiloamele acuminate, etiologia poate fi virala. In aceste tumori a fost identificat ADN viral al virusurilor HPV 6 si 11.
Metastazele ganglionare ale carcinoamelor verucoase sunt rare, iar prezenta lor reflecta degenerare maligna in leziunea primara. Asemenea modificari au fost citate in carcinoamele verucoase nepeniene. De asemenea, au fost citate cazuri de degenerare maligna in asociere cu carcinomul penian.
Sunt necesare biopsie excizionala si biopsii profunde multiple pentru a deosebi leziunea de cancerul penian.
Tratamentul consta in excizare cu prezervarea cat mai mare a tesutului penian. Leziunile intinse pot necesita amputatie peniana totala. Recaderile sunt comune si urmarirea atenta este esentiala.
Tratamentul topic cu podofilina sau 5-FU nu a dat rezultate, probabil din cauza stratului cornos, gros, caracteristic care este impermeabil la medicatie.
Radioterapia este ineficienta si a fost asociata cu modificari maligne secundare cand este folosita la carcinoame varicoase cu alte localizari.
Bleomicina a fost utilizata ca terapie primara sau adjuvanta pentru carcinoamele verucoase.
A fost raportat tratamentul cu succes al tumorilor Buschke-Lwenstein cu interferon sistemic combinat cu tratament laser Nd:YAG.
Carcinomul scuamocelular
Carcinomul in situ
Carcinomul in situ penian a fost descris pentru prima data de Queyrat in 1911 si este denumit de catre urologi si dermatologi ca fiind eritroplazia Queyrat daca afecteaza glandul penian, preputul sau corpul penian si boala Bowen daca afecteaza restul aparatului genital sau regiunea perineala.
Boala Bowen
Boala Bowen, o afectiune ce are un aspect microscopic similar cu carcinomul in situ dar care are o evolutie benigna, a fost descrisa de Kopf si Bart in 1977.
Boala Bowen se prezinta ca papule multiple pe tegumentul penian sau la nivelul vulvei, aparand de obicei in decada 2-3 de varsta.
Leziunile sunt de obicei pigmentate cu dimensiuni 0,2-3 cm, leziunile mai mici pot fi unite formand leziuni mai mari. Leziunile pigmentate situate pe tegumentul penian si leziunile glandulare au aspect de papule plate.
Diagnosticul este confirmat de biopsie. Histologic, leziunile indeplinesc toate criteriile carcinomului in situ, dar aspectele difera dupa pattern-ul de crestere fiind plate, endofitice sau exofitice. Secvente de ADN specifice HPV16 au fost descoperite in specimenele de boala Bowen si a fost incriminat rolul HPV ca agent cauzal.
Desi aspectul histologic este de carcinom in situ, evolutiv, boala Bowen este invariabil benigna.
Tratamentul presupune electrodesicare, crioterapie, fulguratie laser, unguente cu 5-FU si excizie cu grefa cutanata.
Papulomatoza bowenoida
Se caracterizeaza prin aparitia de papule rotunde rosii-violacee la baza penisului si in regiunea ano-genitala. Apare la pacienti tineri, media de varsta fiind de 28 ani (intre 20-30 de ani).
Din leziuni s-a identificat HPV-16.
Tratamentul consta in:
Topic 5-FU
Vaporizare laser sau fotocoagulare
Electrocauterizare
Crioterapie.
Ca si in cazul celorlalte leziuni, ce prezinta aspect microscopic de CIS penian, se recomanda o urmarire atenta.
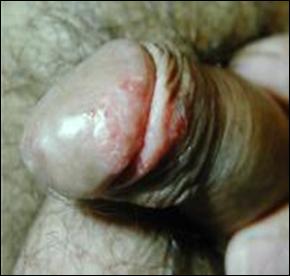
Eritroplazia Queyrat
A fost descrisa de Queyrat in 1911, ca o afectiune cronica a glandului constituita din placarde rosii, foarte putin infiltrante care, in unele, cazuri pot evolua spre epiteliom.
Leziunile sunt localizate exclusiv pe mucoasa genitala externa (gland, sant balano-preputial).
Leziunea prezinta suprafata neteda, nescuamoasa si ne-eroziva, de culoare rosu aprins, cu diametrul de aproximativ 1cm, unica, dar se poate prezenta si sub forma de placarde confluente.
Sunt suple si nedureroase dar foarte persistente (fig.6).
Figura 6. Eritroplazie Queyrat
Microscopic se prezinta sub forma de hiperplazie
epiteliala, cu celule cu grade diferite de modificari; devin ovoide,
dispuse neregulat, tasate, cu pierderea orientarii pe orizontala.
Apar celule atipice, multinucleate; nucleii devenind hipercromatici si de dimensiuni inegale.
Modificarile produse in cazul condilomului acuminat tratat cu podofilina sunt greu de diferentiat de cele ale eritroplaziei Queyrat.
La nivelul dermului se gaseste infiltrat limfocitar si uneori limfoplasmocitar.
Tratamentul consta in:
Topic cu 5-FU
CO2 laser
Microchirurgia prin metoda Mohs.
Carcinomul invaziv
Carcinomul penian are o
incidenta de 0,4% - 0,6% din totalul tumorilor barbatilor
din
Cauzele sunt neclare, dar pot fi legate de cresterea atentiei pentru igiena personala.
Cancerul penian este o boala a pacientului varstnic, cu o crestere brusca a incidentei in decada a 6-a de viata si un varf al acesteia in jurul varstei de 80 de ani. Varsta medie a fost de 58 de ani si respectiv 55 de ani. Desi anumite studii nu au aratat predispozitie rasiala, altele au aratat preponderenta 2:1 pentru negri.
Incidenta carcinomului penian variaza in functie de prezenta sau nu a circumciziei, fimozei, igiena, numarul partenerilor sexuali, infectia cu HPV, expunerea la produsi tabagici si alti factori.
Circumcizia neonatala a fost asociata ca metoda profilactica ce elimina aparitia carcinomului penian, pentru ca se elimina spatiul preputial inchis unde se dezvolta carcinomul penian.
Efectul cronic iritativ al smegmei, produs al actiunii bacteriilor asupra celulelor descuamate ce se afla in sacul preputial, a fost incriminat ca agent etiologic.
O evidenta clara prin care smegma sa fie agent carcinogen, nu a stabilit relatia cu dezvoltarea carcinomului penian, aceasta fiind observata empiric.
Igiena improprie poate duce la acumularea smegmei la nivelul preputiului ce conduce la inflamatie. Asocierea fibrozei conduce la aparitia fimozei care tinde sa intretina procesul.
Fimoza se intalneste la 25-75 % dintre pacientii cu cancer penian, in marea majoritate a studiilor.
Reddy si colab. (1984) au studiat tegumentul penian la 26 de pacienti ce au suferit circumcizie pentru fimoza si au gasit atipie epiteliala la 1/3 din cazuri.
Carcinomul penian este rar la
populatia evreiasca la care circumcizia neonatala este o
manevra obligatorie. Similar, in
In
Datele din mai multe studii demonstreaza ca tumorile peniene sunt rare la indivizii circumcisi neonatal dar mult mai frecvente cand circumcizia este intarziata pana la pubertate. Circumcizia la adulti pare sa ofere mica protectie, sau sa nu ofere protectie pentru dezvoltarea bolii.
Aceste date sugereaza ca perioada determinanta a expunerii la anumiti agenti etiologici a aparut in pubertate si a continuat la adult, facand circumcizia tarzie o metoda profilactica relativ ineficienta pentru cancerul penian.
Infectia cu HPV si expunerea la produsi tabagici par sa fie asociate cu dezvoltarea cancerului penian.
Datele epidemiologice demonstreaza relatia dintre agentii cu transmitere sexuala si cancer, sotiile sau fostele sotii ale pacientilor cu cancer penian au un risc de 3 ori mai mare al cancerului cervical. Investigatiile suplimentare au aratat ca partenerii femeilor cu neoplazie cervicala intraepiteliala au o incidenta mare pentru neoplazie intraepiteliala peniana. Acesti pacienti au fost diagnosticati de asemenea cu incidenta mare de HPV.
Tehnicile biomoleculare (PCR si hibridizarea in situ) au demonstrat rolul etiologic al HPV prin identificarea secventelor ADN specifice ale diferitelor tipuri de HPV la nivelul leziunilor peniene primare (maligne si benigne), dar nu la nivelul tegumentului normal.
Peste 25 de tipuri de HPV afecteaza aparatul genital. Tipurile HPV 6 si 11 sunt cel mai frecvent asociate cu leziuni non-displazice precum nevii genitali dar au fost identificati si in carcinoamele verucoase non-metastatice. Tipurile de HPV 16, 18, 31, 33 sunt asociate cu carcinoame in situ sau invazive. HPV 16 pare sa fie cel mai frecvent detectat in carcinoamele primare si in leziunile metastatice.
Genomul HPV codeaza oncoproteina E6 care se combina cu proteina supresoare tumorala P53 afectadu-se reglarea ciclului celular.
Maden si colab. (1993) a descoperit ca incidenta infectiei HPV direct corelata cu numarul partenerilor sexuali este asociata cu riscul de dezvoltare a cancerului penian.
Desi infectia HPV este un
factor important in dezvoltarea cancerului penian, prezenta acesteia nu
este
Exista studii care demonstreaza o asociere semnificativa intre expunerea la fumul de tigara si dezvoltarea cancerului penian.
Cresterea incidentei cancerului penian la fumatori chiar la pacientii circumcisi a fost raportata de Hellberg si colab. (1987).
Harish si
Desi un istoric de traumatism poate precede dezvoltarea carcinomului penian, se crede ca acesta este mai de graba co-incidental decat cauzal.
Totusi, dezvoltarea carcinomului in cicatricele peniene dupa circumcizie mutilanta a fost descrisa ca forma separata, iar Maden si colab. (1993) au gasit un risc de trei ori mai mare de cancer penian la barbatii cu rash-uri si cicatrice peniana.
Este necesara efectuarea, intr-o analiza extinsa, a unui studiu larg incluzand mai multi factori de risc pentru cancerul penian.
Nu a fost descoperita nici o evidenta clara care sa asocieze cancerul penian cu alti factori precum; profesia, alte boli venerice (gonoree, sifilis, herpes), utilizarea de marijuana sau consumul de alcool.
Hiperplazia scuamoasa
Este reprezentata de o ingrosare acantotica a epiteliului scuamos penian, fara atipii celulare, afectand de regula regiunea glandului, santului coronar si a preputului. Insoteste frecvent variantele papilara si verucoasa ale carcinomului scuamos. Macroscopic mucoasa este de obicei plata, neteda, iar la nivel microscopic se descriu mai multe tipuri, existand leziuni plate, papilare, mixte si pseudo-epiteliomatoase. Frecventa asociere cu carcinomul scuamos, in special variantele bine diferentiate, si continuitatea cu carcinomul invaziv, demonstrata macro- si microscopic, sugereaza ca hiperplazia scuamoasa cu sau fara lichen scleros poate fi considerata o leziune precanceroasa peniana.
Boala Bowen si neoplaziile intraepiteliale inrudite
Carcinomul scuamos in situ penian este reprezentat de doua entitati clinice cunoscute ca boala Bowen (placa eritematoasa, crustoasa, bine circumscrisa) si eritroplazia lui Queyrat (placa eritematoasa, lucioasa, catifelata), ambele entitati dezvoltandu-se pe preput, sant coronar sau gland la indivizii varstnici.
Din punct de vedere morfologic leziunile precanceroase intraepiteliale peniene sunt denumite: ,,displazie usora, moderata si severa", "neoplazie intraepiteliala peniana (PIN) I, II si III" si ,,leziune intraepiteliala scuamoasa (SIL) de grad scazut si grad inalt cu sau fara modificari HPV", preferandu-se ultima terminologie. Leziunile intraepiteliale scuamoase (SIL) pot fi solitare, multifocale sau uneori asociate cu un carcinom scuamos invaziv (5% din cazuri).
Microscopic SIL se caracterizeaza prin prezenta celulelor atipice in treimea inferioara a grosimii epiteliului in leziunile de grad scazut si aproape in intreaga grosime a epiteliului in leziunile de grad inalt.
Koilocitoza poate fi prezenta in special in leziuni asociate cu un carcinom condilomatos. Pattern-ul morfologic al SIL la nivel microscopic este foarte heterogen. Principalele tipuri sunt: cu celule scuamoase, bazaloid si condilomatos, cel pleomorf, pagetoid, cu celule mici si neclasificat intalnindu-se mai rar. In general aspectul microscopic al procesului in situ corespunde pattern-ului carcinomului scuamos invaziv asociat. SIL de grad inalt este similar carcinomului in situ cu alte localizari si trebuie distins de carcinomul urotelial in situ uretral care poate interesa secundar regiunea meatului penian.
Papulomatoza bowenoida
Este un termen propus pentru o boala peniana care prezinta aspecte histologice similare bolii Bowen, dar apare la indivizi tineri (varsta medie este de 30 de ani) ca macule/papule multiple, rosii sau violacee ale tegumentului corpului penian, mai rar pe gland, sant coronar sau preput. Sunt leziuni induse viral (in 80% din cazuri sunt demonstrate tipurile 16 si 18 de HPV, suspectandu-se astfel o transmitere sexuala) si pot regresa spontan.
Carcinomul scuamos penian
Majoritatea tumorilor maligne peniene sunt de natura epiteliala (carcinoame), iar intre acestea ponderea o detine carcinomul scuamos. Multe dintre carcinoamele scuamoase peniene se dezvolta, in ordinea frecventei, pe gland, preput si santul coronar.
Din punctul de vedere al pattern-ului de crestere se descriu mai multe forme:
forma cu extensie superficiala: tumora cu rata de crestere lenta si tendinta centrifuga, interesand exclusiv mucoasa si straturile anatomice superficiale ale glandului, santului coronar si preputului; cel mai frecvent tip histologic asociat cu acest pattern este tipul uzual de carcinom scuamos; o atentie deosebita trebuie acordata evaluarii microscopice a marginilor de rezectie chirurgicala;
forma predominant exofitica, veruciforma: tumora exofitica ce creste lent, avand o configuratie papilara keratotica; de regula este o tumora superficiala, care rareori invadeaza structuri profunde; diferite tipuri histologice se asociaza cu acest pattern de crestere: verucos, condilomatos, papilar si uzual; diagnosticul diferential se face cu leziuni pseudotumorale (xantom verucifom) si tumori benigne (condilom acuminat gigant);
forma predominant endofitica, infiltrativa, ulcerativa, verticala: se prezinta ca o masa tumorala compacta, fungiforma sau ulcerata, cu arii intinse de necroza, invaziva, adesea cu noduli tumorali sateliti ai masei tumorale dominante, localizati profund in corpii spongios si cavernosi; tipurile histologice asociate acestui pattern sunt de regula carcinomul scuamos de tip bazaloid, sarcomatoid, anaplazic, solid si uzual slab diferentiat;
forma multicentrica: se caracterizeaza prin prezenta mai multor focare carcinomatoase independente separate prin zone de tesut normal/benign; pot fi sincrone sau metacrone, apar in multiple compartimente si pot prezenta la nivel microscopic tipuri histologice similare sau diferite; evolutia este similara formei cu extensie superficiala;
forma mixta: tumora care prezinta concomitent diferite pattern-uri de crestere (cu extensie superficiala, predominant endofitica si multicentrica), la nivel microscopic existand o combinatie de tipuri histologice bine si slab diferentiate.
Microscopic carcinomul scuamos penian prezinta mai multe tipuri histologice:
carcinomul scuamos-tipul uzual: reprezinta aproximativ 70% din tumorile maligne peniene si este similar carcinomului scuamos cu alte localizari; varsta medie a pacientilor este 58 de ani; majoritatea sunt carcinoame scuamoase moderat diferentiate, dar pot exista o serie de subtipuri histologice: pseudohiperplazic, acantolitic (pseudoglandular), cu celule alungite, limfoepitelioma-like, trabecular, pleomorf cu celule gigante, cu celule mici, papilar cu celule mici si cu celule clare; in 2/3 din cazuri se asociaza cu SIL, de grad inalt sau scazut, sau cu hiperplazia scuamoasa, de cele mai multe ori de tip plat; trebuie diferentiat macro- si microscopic, uneori asociind tehnici imunohistochimice, de hiperplazia pseudo-epiteliomatoasa, carcinomul urotelial uretral, melanomul malign si angiosarcomul epitelioid.
carcinomul condilomatos: este o tumora maligna rara, cu rata lenta de crestere, bine sau moderat diferentiata, cu aspect macroscopic conopidiform (pattern veruciform de crestere), dimensiuni mari (peste 5 cm) si asemanari morfologice condilomului acuminat datorita modificarilor celulare de tip koilocitotic; trebuie diferentiat la nivel microscopic de condilomul acuminat gigant, carcinomul verucos si carcinomul papilar; metastazele limfoganglionare pot aparea in formele invazive; prognosticul este intermediar intre tipul uzual de carcinom scuamos si celelalte forme de tumori cu pattern de crestere veruciform (carcinomul verucos, carcinomul papilar).
carcinomul verucos: este o varianta foarte bine diferentiata de carcinom scuamos cu rata lenta de crestere si pattern exofitic papilar (tumora vegetanta, sesila, cu baza larga de implantare); in general tumora are dimensiuni intre 1-3 cm, desi au fost descrise si forme gigante distructive; reprezinta aproximativ 5% din tumorile maligne peniene; varsta medie a pacientilor este de 57 de ani, iar supravietuirea de aproximativ 56 de luni (cea mai lunga supravietuire dintre toate tumorile maligne peniene); formele pure de carcinom scuamos nu evolueaza cu metastaze, iar tratamentul consta in rezectia leziunii (radioterapia induce transformarea anaplazica a tumorii); recurentele pot aparea in 1/3 din cazuri datorita rezectiei chirurgicale incomplete sau datorita existentei formei multicentrice neidentificate in momentul diagnosticului initial; diagnosticul diferential microscopic include condilomul gigant, carcinomul condilomatos si carcinomul papilar.
carcinomul papilar: este o tumora exofitica distructiva, cu rata lenta de crestere, localizata de obicei la nivelul glandului, rareori evoluand cu metastaze limfoganglionare inghinale; microscopic prezinta aspecte de carcinom scuamos bine diferentiat fara caractere condilomatoase si trebuie diferentiat de tipul uzual de carcinom scuamos, carcinomul verucos si hiperplazia pseudoepiteliomatoasa.
carcinomul bazaloid: tumora peniana agresiva, slab diferentiata, profund invaziva, de obicei asociata cu infectia cu HPV; reprezinta 5-10% din tumorile maligne peniene, iar varsta medie in momentul diagnosticului este de 52 de ani; mai mult de 50% dintre pacienti prezinta metastaze limfoganglionare loco-regionale la prezentare; macroscopic este o tumora ulcero-infiltrativa localizata la nivelul glandului, originea sa fiind jonctiunea scuamo-tranzitionala din regiunea meatului; se asociaza frecvent cu hiperplazia atipica cu celule bazale si carcinomul in situ bazaloid sau condilomatos si se caracterizeaza prin invazie perineurala, limfatica si venoasa; rata mortalitatii fiind de 59%.
carcinomul sarcomatoid: tumora rara, agresiva, adesea cu pattern de crestere multicentric si dimensiuni mari (peste 5 cm), localizata frecvent la nivelul glandului; microscopic se caracterizeaza prin celule carcinomatoase alungite, iar coloratiile imunohistochimice sunt necesare pentru a exclude un sarcom.
carcinomul adenoscuamos (mucoepidermoid): este o tumora peniana extrem de rara, probabil avand originea in celule glandulare deplasate in regiunea perimeatala; macroscopic este o tumora de dimensiuni mari si invaziva, iar microscopic se caracterizeaza prin pattern bifazic, scuamos si glandular, componenta glandulara avand caractere muco-secretorii (prezinta rectivitate imunohistochimica pentru CEA); mucoasa glandului penian invecinata tumorii prezinta frecvent aspecte de leziuni intraepiteliale scuamoase (SIL); trebuie distins la nivel microscopic de carcinomul scuamos acantolitic (pseudoglandular) penian, carcinomul adenoscuamos uretral si adenocarcinomul glandelor Littre (localizat ventral in penis si restrans la tesutul periuretral si corpii cavernosi);
tumori scuamoase maligne mixte (25% din carcinoamele scuamoase): tipurile mentionate de carcinom scuamos penian se pot asocia cu alte tipuri de carcinom; cele mai frecvente combinatii intalnite sunt intre carcinomul verucos si carcinomul scuamos uzual slab diferentiat (asa-numitul ,,carcinom hibrid") si intre carcinomul condilomatos si carcinomul bazaloid; in aceste situatii prognosticul depinde de componenta invaziva.
Caracteristicile moleculare ale carcinomului penian sunt destul de putine. HPV este implicat in tumorigeneza unui procent redus de carcinoame peniene, respectiv tipul condilomatos si tipul bazaloid.
Rubin si colab. au demonstrat prezenta ADN-ului viral in 33% din cazurile de carcinom scuamos uzual si carcinom verucos, in 80% din carcinoamele bazaloide si in 100% din carcinoamele condilomatoase. Rezultatele obtinute de alti autori confirma frecventa inalta a ADN-HPV in carcinomul bazaloid si condilomatos si o frecventa scazuta in carcinomul verucos. Prin flow-citometrie au fost demonstrate populatii celulare diploide in carcinoamele verucoase si populatii diploide sau polipoide/aneuploide in celelalte tipuri de carcinom scuamos. Expresia p53 si p21 a fost identificata in 80% si, respectiv, 40% din carcinoamele scuamoase peniene. Multi alti factori moleculari au fost studiati, fara a se obtine insa rezultate satisfacatoare privind carcinogeneza peniana. Diagnosticul microscopic al tumorilor peniene trebuie sa includa :tipul si subtipul tumoral; gradul de diferentiere a tumorii; multicentricitatea; carcinomul in situ asociat; profunzimea invaziei; statusul marginilor de rezectie chirurgicala; invazia vasculara; invazia perineurala.
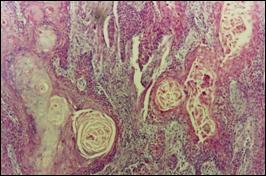 Supravietuirea la 5 si la 10 ani
pentru carcinomul scuamos penian este de 77% si, respectiv, 71%, iar prognosticul depinzand
de urmatorii factori: stadiul patologic (cel mai important factor de
prognostic); tipul microscopic (carcinomul verucos prezinta cel mai bun
prognostic, fiind urmat de carcinomul condilomatos; carcinomul bazaloid si
cel sarcomatoid se caracterizeaza printr-o incidenta inalta
a metastazelor limfoganglionare si o supravietuire scurta); grading-ul microscopic (se coreleaza
foarte bine cu prognosticul); invazia vasculara (este indicator de
prognostic nefavorabil); supraexpresia p53 (evaluata imunohistochimic
coreleaza cu prezenta metastazelor limfo-ganglionare).
Supravietuirea la 5 si la 10 ani
pentru carcinomul scuamos penian este de 77% si, respectiv, 71%, iar prognosticul depinzand
de urmatorii factori: stadiul patologic (cel mai important factor de
prognostic); tipul microscopic (carcinomul verucos prezinta cel mai bun
prognostic, fiind urmat de carcinomul condilomatos; carcinomul bazaloid si
cel sarcomatoid se caracterizeaza printr-o incidenta inalta
a metastazelor limfoganglionare si o supravietuire scurta); grading-ul microscopic (se coreleaza
foarte bine cu prognosticul); invazia vasculara (este indicator de
prognostic nefavorabil); supraexpresia p53 (evaluata imunohistochimic
coreleaza cu prezenta metastazelor limfo-ganglionare).
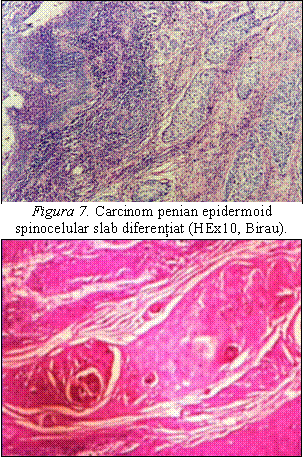
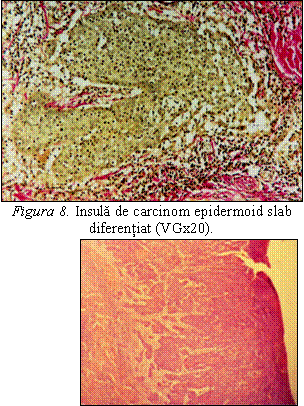
A a.
Figura 9. Carcinom spino-celular
vegetant glandulo-preputial ulcerat, cu arii de invazie
subepiteliala si endoluminala in uretra anterioara
pT3G1.

b.
Carcinom scuamos pT1G2.
Preventia
Circumcizia neonatala efectuata de rutina a fost un subiect controversat. In 1971, Academia Americana de Pediatrie afirma ca: "Nu exista nici o indicatie medicala valida pentru circumcizia neonatala". Acest punct de vedere a fost reiterat in 1975 de un comitet al AAP, iar in 1983 de catre AAP si Colegiul American de Obstetrica si Ginecologie in ghidul de practica perinatala.
In 1988, comitetul a revizuit dupa cum urmeaza: "Circumcizia la nou nascut are beneficii medicale potentiale si avantaje, dar ca si dezavantaje si riscuri. Cand se efectueaza circumcizia, trebuie explicate parintilor beneficiile si riscurile si trebuie obtinut consimtamantul".
Aceste recomandari se bazeaza pe datele ce arata ca incidenta infectiei de tract urinar la baieti poate fi redusa cand se efectueaza circumcizia. Suplimentar informatiile publicate in legatura cu relatia circumcizie - boli cu transmitere sexuala si implicit relatia dintre bolile virale cu transmitere sexuala si cancerul penian sau cervical au inceput sa fie valabile.
Asociatia Americana de Pediatrie a publicat un ghid in care se precizeaza: "Exista beneficii medicale potentiale ale circumciziei la nou nascut, totusi aceste date nu sunt suficiente pentru recomandarea de rutina a circumciziei neonatale. In situatiile in care procedura nu este necesara la copilul sanatos, parintii trebuie sa decida ce este in avantajul copilului".
Orice argument contra circumciziei trebuie sa ia in consideratie ca tumora peniana reprezinta singura tumora pentru care exista o forma simpla si predictibila de profilaxie ce protejeaza organul de risc.

Istoria naturala
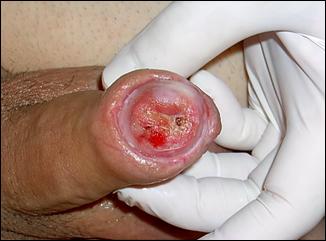
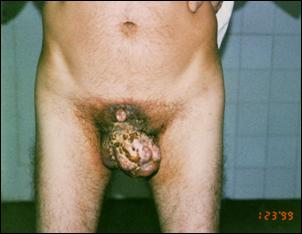
Carcinomul penian debuteaza, de obicei, cu o leziune mica ce se extinde progresiv si afecteaza glandul si corpul penian. Leziunea poate fi papilara si exofitica sau plata si ulcerativa; daca nu se trateaza, autoamputarea peniana poate apare ca rezultat final.
Figura 11. Carcinom scoamocelular (T1).
|
Figura 13. Pacient cu tumora peniana cu infiltrarea tegumentului hipogastric - T4. |
Rata de crestere a leziunilor papilare si ulcerative este similara, dar tumorile plate, ulcerative au o tendinta de metastazare ganglionara precoce si sunt asociate cu un prognostic mai prost la 5 ani.
Leziunile mai mari de 5 cm si cele ce afecteaza peste 75 % din tegumentul penian se asociaza, de asemenea, cu o incidenta crescuta a metastazelor si o scadere a ratei de supravietuire. Totusi, nu a fost gasita o relatie solida intre marimea leziunii, prezenta metastazelor si scaderea supravietuirii.
 Fascia
Buck actioneaza temporar ca o bariera naturala impotriva
extensiei tumorale, protejand corpii cavernosi de invazie. Penetrarea
fasciei Buck si a albugineei permite invazia structurilor vasculare
si astfel apare riscul de diseminare vasculara.
Fascia
Buck actioneaza temporar ca o bariera naturala impotriva
extensiei tumorale, protejand corpii cavernosi de invazie. Penetrarea
fasciei Buck si a albugineei permite invazia structurilor vasculare
si astfel apare riscul de diseminare vasculara.
Afectarea uretrei sau a vezicii urinare este rara.
Figura 14. Adenopatie inghinala voluminoasa.
Metastazele apar in ganglionii regionali femurali si
iliaci care sunt statiile precoce de diseminare ale carcinomului penian.
Limfaticele preputului formeaza o retea care se
anastomozeaza cu limfaticele tegumentare ale corpului penian. Aceste vase
tributare dreneaza in ganglionii inghinali superficiali (ganglionii
externi de fascia lata). Limfaticele glandului se anastomozeaza cu
limfaticele corpilor cavernosi si formeaza o retea la baza
penisului ce dreneaza in ganglionii superficiali. Nodulii superficiali
dreneaza in ganglionii inghinali profunzi.
De aici drenajul se face catre ganglionii pelvini (iliac extern, iliac intern si obturator).
Limfoangiograma peniana, demonstreaza un puternic drenaj de la ganglionii inghinali superficiali catre cei inghinali profunzi si ganglionii pelvieni. Exista multiple interconexiuni la diverse nivele asa incat drenajul limfatic penian se face bilateral catre ambele arii ganglionare inghinale.
Invazia metastatica ganglionara regionala poate duce la cresterea de volum a acestora, la necroza, infectie cronica si deces prin sepsis si hemoragie secundara eroziunii vaselor femurale. Descoperirea clinica a metastazelor la distanta in plamani, ficat, os, creier este nespecifica si s-au identificat in 1 - 10 % din cazuri in majoritatea studiilor. Asemenea metastaze apar de obicei tardiv in evolutia bolii dupa ce leziunea locala a fost tratata. Metastazele la distanta, in absenta invaziei ganglionare regionale, sunt neobisnuite.
Carcinomul penian se caracterizeaza printr-o evolutie lenta determinand decesul majoritatii pacientilor netratati in mai putin de 2 ani.
Nu a fost raportat nici o remisiune spontana a carcinomului penian. Intre 5 - 15 % din pacienti au fost diagnosticati cu un al doilea neoplasm primitiv, iar un studiu a raportat aparitia la 17 % din pacienti a carcinomului secundar.
Modul de prezentare
Semnele
Leziunea peniana
alerteaza de obicei pacientul cu cancer penian. Aspectul variaza de
la induratie moderata, mici excrescente, papula de
dimensiuni mici, pustule,
Fimoza poate ascunde o leziune si poate favoriza dezvoltarea silentioasa a unei tumori.
Uneori poate atrage atentia eroziunea preputului, mirosul neplacut al preputului, sau scurgeri sanguinolente.
 Tumorile
peniene pot aparea in orice zona peniana, dar cel mai frecvent la
nivelul glandului (48 %) si preputului (21%). Aceasta
distributie a leziunilor poate fi datorata expunerii la iritatii
(ex: smegma, HPV) a glandului, santului coronar si
suprafetei preputului.
Tumorile
peniene pot aparea in orice zona peniana, dar cel mai frecvent la
nivelul glandului (48 %) si preputului (21%). Aceasta
distributie a leziunilor poate fi datorata expunerii la iritatii
(ex: smegma, HPV) a glandului, santului coronar si
suprafetei preputului.
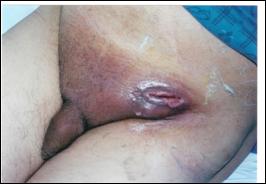
Figura 15.
Formatiune tumorala inghinala ulcerata si
supurata cu tumora peniana ascunsa de fimoza.
Rar pacientul se poate prezenta cu formatiune
tumorala inghinala, ulcerata, supurata, hemoragica,
datorata metastazelor ganglionare pornite dintr-o formatiune
tumorala ascunsa de o fimoza. Semne rare pot fi retentia de
urina sau fistula uretrala mergand pana la afectarea corpilor
cavernosi.
Complicatiile sunt legate de evolutia locala a tumorii prin invadarea uretrei, a corpilor cavernosi si a tegumentelor invecinate. Sangerarea repetata atrage dupa sine anemia.
Metastazele osoase pot da nastere la fracturi pe os patologic, iar cele hepatice la insuficienta hepatica. Blocurile adenopatice pot genera eroziune vasculara femurala urmata de hemoragie cataclismica.
Simptomele
Durerea nu este proportionala cu extensia procesului distructiv local si, de obicei, nu este o modalitate de prezentare. Astenia, scaderea ponderala, maleza generalizata, pot aparea secundar supuratiei cronice. Uneori pot aparea sangerari semnificative din leziunea peniana, din leziunile ganglionare sau din ambele.
Diagnosticul
Pacientii cu cancer penian, mai frecvent decat pacientii cu alte tipuri de cancer, intarzie prezentarea la consultul medical. In studiile mari, intre 15-50 % dintre pacienti intarzie consultul medical mai mult de 1 an de zile. Motivele sunt: lipsa timpului liber, vinovatie, teama, ignoranta si neglijenta personala. Procentul de negare este mare, cu toate ca penisul este observat si poate fi palpat zilnic.
Intarzierea din partea medicului de stabilire a diagnosticului si tratamentului este de asemenea importanta. In anumite cazuri, pacientii au urmat tratamente lungi cu antibiotice si antifungice topice inainte de efectuarea biopsiei.
Desi unele studii arata ca diferenta supravietuirii intre pacientii prezentati precoce si cei prezentati tardiv, este nesemnificativa, alte studii arata scaderea supravietuirii cu cat se intarzie mai mult. Se impune asadar diagnostic si tratament precoce.
Examinarea
La prezentare, majoritatea leziunilor sunt localizate la penis. Leziunea peniana este examinata precizand marimea, localizarea, aderenta si interesarea corpilor cavernosi. Inspectia bazei penisului si a scrotului sunt necesare pentru a exclude extensia in aceste zone.
Tuseul rectal si examinarea bimanuala aduc informatii despre afectarea zonei perineale si prezenta unei eventuale tumori pelvice.
Extrem de importanta este palparea inghinala bilaterala, facuta cu atentie, pentru descoperirea adenopatiilor si caracteristicilor lor (diametru, localizare, numar, mobilitate, relatiile cu structurile adiacente).
Biopsierea
Confirmarea diagnosticului de carcinom penian si precizarea profunzimii invaziei, prezentei invaziei vasculare si a gradului histologic este obligatorie inaintea initierii oricarei terapii.
Biopsia trebuie sa fie o procedura separata de tratamentul chirurgical complet.
Frecvent este necesara incizia dorsala a preputului (dorsal split) pentru a avea o mai buna expunere a leziunii permitand o biopsie corecta.
Nu au fost raportate diseminari dupa biopsiere.
O alternativa este biopsierea cu examinarea sectiunilor la gheata, urmata de amputatie partiala sau totala. Inainte de procedura trebuie obtinut consimtamantul pacientului.
Examene de laborator
La pacientii cu cancer penian testele de laborator sunt frecvent normale. Anemia, leucocitoza, hipoalbuminemia pot aparea la pacientii cu suferinta cronica, malnutritie, supuratie intinsa in zona tumorala primara si zonele metastatice inghinale.
Retentia azotata se dezvolta secundar obstructiei ureterale sau uretrale.
Hipercalcemia, fara detectarea metastazelor osoase a fost asociata cu cancer penian. Intr-un studiu al Memorial Sloan-Kettering Cancer Center, au fost depistati cu hipercalcemie 17 din 81 pacienti adica 20,9%. Hipercalcemia pare sa fie legata de boala. Este adesea asociata cu metastaze ganglionare si poate disparea dupa excizia ganglionilor inghinali implicati.
Tumora si metastazele produc hormon paratiroidian si substante inrudite care activeaza resorbtia osoasa osteoclastica. Tratamentul medical al hipercalcemiei, include hidratare salina pentru refacerea volumului lichidului si pentru favorizarea excretiei sodiului si calciului.
Administrarea de diuretice se face daca se suspecteaza un exces volemic.
Bifosfonatii (ex: Pamidronate, Etidronate) au devenit tratament de prima intentie deoarece si-au demonstrat eficacitatea ca agenti antiresorbtivi si sunt mai siguri ca mitramicina (un agent mai vechi). Pentru hipercalcemiile severe asociate cu manifestari neurologice, se pot combina bifosfonati cu calcitonina si se realizeaza scaderea rapida a nivelelor serice de calciu.
Examene imagistice
Evaluarea tumorii primare
Cavernografia - metoda invaziva ce a fost inlocuita de metode imagistice neinvazive.
Ecografia: - se realizeaza cu transducer de 7,5 Mhz
- aspect invariabil hipoecogen
- nu poate aprecia invazia in tesutul conjunctiv superficial glandular fata
de corpul spongios
- tunica albuginee este identificata cu usurinta
- sensibilitatea detectarii invaziei in corpul cavernos este de 100%.
Evaluarea lanturilor ganglionare
CT / RMN - acuratete similara ca sensibilitate si specificitate de aproximativ 30% in detectarea adenopatiilor, astfel incat CT a fost aleasa ca modalitate imagistica pentru evaluarea ariilor ganglionare inghinale si pelvine ca si pentru excluderea metastazelor la distanta.
Limfangiografia are o utilizare limitata datorita drenajului neregulat si inconstant. ganglionii invadati complet de cancer putand fi exclusi datorita invaziei limfatice complete.
Tomografia are rolul examinarii regiunii inghinale la pacientii obezi sau la cei cu gesturi chirurgicale anterioare in regiunea inghinala, la care examenul clinic poate fi neconcludent.
La pacientii cu metastaze inghinale cunoscute, biopsia CT ghidata din nodulii pelvini mariti, poate aduce informatii importante pentru aprecierea strategiilor chimioterapice neoadjuvante.
In general, metastazele la distanta apar tardiv in evolutia bolii, de obicei la pacientii cu adenopatie inghinala si pelvina cunoscuta. Cele mai frecvente locuri de diseminare sunt: plaman, os si ficat.
In completarea examinarii CT abdominale si pelvine, scintigrafia osoasa si radiografia pulmonara sunt indicate pentru stadierea bolii la pacientii cu suspiciune de metastaze.
Stadializarea
Nu exista un sistem de stadiere universal acceptat. Totusi sistemele UICC, TNM si mai recentul UICC/AJCC-TNM sunt cele mai frecvent utilizate in studiile actuale.
Din punct de vedere istoric,
sistemul
Clasificarea Jackson pentru tumorile peniene
Stadiul I (A) - tumora limitata la gland sau preput
Stadiul II (B) - tumora extinsa la teaca penisului
Stadiul III (C) - tumora cu metastaze inghinale operabile
Stadiul IV (D) - tumori extinse la structuri adiacente; tumori asociate cu adenopatii inghinale
inoperabile sau metastaze.
Sistemul Jackson a fost comun si usor de utilizat dar aduce informatii prognostice minime. Totusi el caracterizeaza pe larg tumorile primare, precum si daca este afectat tegumentul penian fara a include impartirea mai precisa a sistemului TNM. In plus, starea ganglionilor inghinali a fost caracterizata pe larg, ca fiind operabili (stadiul 3) sau inoperabili (stadiul 4).
Valoarea clasificarii TNM consta in stadierea deopotriva a tumorii primare cat si a limfonodulilor regionali.
Stadierea TNM AJCC/UICC din 1997 (fig.17):
Tumora primara (T)
Tx Tumora primara nu a fost evaluata
T0 Fara nici o evidenta a tumorii primare
Tis Carcinom in situ
Ta Carcinom non-invaziv verucos
Tl Tumora invadeaza tesutul conjunctiv subepitelial
T2 Tumora invadeaza corpul spongios sau cavernos
T3 Tumora invadeaza uretra sau prostata
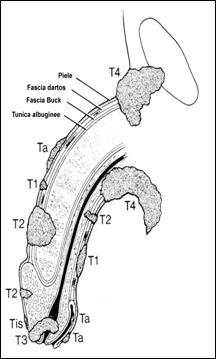 T4 Tumora invadeaza alte structuri adiacente.
T4 Tumora invadeaza alte structuri adiacente.
Limfoganglioni regionali (N)
Nx Ganglionii regionali nu pot fi evaluati
N0 Fara metastaze ganglionare regionale
N1 Metastaze intr-un singur ganglion
inghinal superficial
N2 Metastaze in multipli ganglioni
superficiali sau bilaterali superficiali
N3 Metastaze in ganglionii profunzi inghinali
sau pelvini, unilateral sau bilateral.
Metastaze la distanta (M)
Mx Metastazele la distanta nu au fost evaluate
M0 Fara metastaze la distanta
Ml Metastaze la distanta.
Gruparile de stadiere
Tabelul nr.2. Gruparile
de stadiere (Dupa Fleming ID, Cooper
JS,
|
Tis |
N0 |
M0 |
|
|
Ta |
N0 |
M0 |
|
|
Stadiul I |
Tl |
N0 |
M0 |
|
Stadiul II |
Tl |
N1 |
M0 |
|
T2 |
N0 |
M0 |
|
|
T2 |
Nl |
M0 |
|
|
Stadiul III |
Tl |
N2 |
M0 |
|
T2 |
N2 |
M0 |
|
|
T3 |
N0 |
M0 |
|
|
T3 |
Nl |
M0 |
|
|
T3 |
N2 |
M0 |
|
|
Stadiul IV |
T4 |
Orice N |
M0 |
|
Orice T |
N3 |
M0 |
|
|
Orice T |
Orice N |
M1 |
Versiunea TNM curenta recunoaste de asemenea importanta extensiei invaziei ganglionare ca factor de prognostic al supravietuirii, categorii separate fiind folosite pentru pacientii cu un singur nodul pozitiv (N1) fata de cei cu ganglionii bilaterali (N2) si cu invazie inghinala profunda sau pelvina (ganglioni Cloquet sau ganglioni iliaci) (N3).
Problema cu acest sistem, asa cum a fost aratat de catre Horenblas si colab. (1994), este dificultatea de obtiere a statusul ganglionar inaintea terapiei definitive.
Deci, stadializarea TNM curenta reprezinta un sistem de stadializare patologica in care histologia ganglionara trebuie obtinuta (prin operatie, biopsie, limfadenectomie). Chiar cu aceste trasaturi, extensia ganglionara si aderenta ganglionara nu sunt considerate drept factori determinanti de prognostic.
Deci, valoarea sistemului curent TNM este ca aduce o evaluare de acuratete a tumorii primitive bazata pe stadializarea clinica (examinare, biopsie), dar presupune proceduri invazive pentru evaluarea ganglionara.
Tabelul nr.3. Criteriile de diagnostic pentru stadializarea TNM.
|
Tumora primara (T) Examinare clinica Biopsie incizie-excizie a leziunii cu examinare histologica pentru stadiere, evaluarea structurilor anatomice invadate si prezenta invaziei vasculare |
|
Ganglioni regionali sau juxtaregionali (N) Examinare clinica Tomografie computerizata daca se palpeaza adenopatie inghinala* Disectia ganglionilor superficiali (indicata pentru grad inalt, invazie vasculara sau histologie invaziva) sau citologie aspirativa |
|
Metastaze la distanta (M) Examinare clinica Radiografie pulmonara Determinari biochimice (functie hepatica, calciu) IRM, scintigrafie osoasa |
*TC va fi de asemenea efectuata la pacientii obezi, la cei care au mai suferit tratamente chirurgicale in zona inghinala si la cei la care examninarea fizica nu este concludenta.
Tratamentul tumorilor peniene
Tratamentul tumorilor peniene este complex si cuprinde tratamentul tumorii primare si al lanturilor ganglionare.
Tratamentul tumorii primare
A. Tratamentul topic cu 5-fluorouracil (5-FU)
Fluorourocilul este un analog al uracilului, o baza pirimidinica care se transforma in nucleotidul si dezoxinucleotidul carespunzator, actionand ca antimetabolit. Administrat local pentru tratamentul unor leziuni preneoplazice peniene sau neoplazice provoaca urmatoarea secventa fiziopatologica: inflamatie - eroziune - ulceratie - necroza - vindecare.
Vindecarea poate implica prezenta trecatoare a unui eritem rezidual sau a hiperpigmentarii.
In carcinomul superficial se aplica de 2 ori/zi 3-6 saptamani (uneori pana la 12 saptamani). Se poate administra si in injectii intralezionale, sub forma de solutie apoasa 5%. Nu au fost semnalate efecte toxice sistemice.
Reactiile adverse citate sunt: senzatie de arsura locala, prurit, durere, inflamatie, hiperpigmentare, dermatita de contact, sensibilitate crescuta a pielii la expunerile ultraviolete (vor fi evitate).
B. Terapia laser
Prima ablatie laser in cancerul penian a fost raportata in 1968. In ciuda rezultatelor cosmetice bune si a prezervarii penisului, amputatiile ulterioare au aratat o importanta rata de tumori reziduale si recurente locale.
Este responsabilitatea clinicianului in a selecta pacientii ale caror leziuni au indicatie de terapie laser care sunt:
leziunile premaligne si CIS (boala Bowen, eritroplazia Queyrat)
tumori mici (< 2 cm)
neinvazive (Tis sau T1).
Experienta a aratat ca ablatia laser a tumorilor mai mari de 2 cm sau invazive este posibila tehnic, dar este limitata de o rata mare a recurentei locale.
Tipurile de laser utilizate sunt: Nd:YAG, CO , KTP.
Laserul cu CO are o lungime de unda de 10,600 nm si este puternic absorbit de apa, cu o imprastiere minima. Aceasta permite vaporizarea instantanee a tesutului la locul de impact al razei, cu fierberea apei intracelulare; iar majoritatea energiei incidente este absorbita la o profunzime de mai putin de 0,1mm de tesut.
Laserul Neodymium YAG avand o lungime de unda de 1060 nm, se caracterizeaza printr-o absorbtie minima de catre apa sau pigmenti biologici, precum hemoglobina. Aceasta se traduce printr-o penetrare profunda a tesuturilor 4-6 mm, rezultand necroza de coagulare. Aria locala tratata are un aspect caracteristic - alb si ferm, avand ca substrat denaturarea proteinelor, proces ce se petrece cand temperatura depaseste 600C. Micile vase sangvine sunt coagulate prin procesul de cicatrizare.
Aria tratata nu se inchide, in oarecare masura vindecarea se produce prin reepitelizare secundara.
Malloy si colab. recomanda circumcizia la toti pacientii ce vor urma ablatia laser a tumorilor superficiale ale glandului sau tecii peniene distale.
Penetratia tisulara si energia de fotocoagulare a laserului Neodymium YAG pot fi augmentate prin aplicarea de solutie salina congelata pe suprafata de tratat in timpul expunerii laser. Aceasta raceste suprafata pielii si previne carbonizarea suprafetei si vaporizarea, acestea ducand la o marire semnificativa a penetrantei laserului.
Poate cea mai importanta limitare a laser-terapiei in tratamentul carcinoamelor peniene este reprezentata de lipsa confirmarii histologice a marginilor de rezectie. Aceasta limiteaza metoda la un grup restrans de pacienti ce prezinta tumori mici, superficiale; bine delimitate, iar biopsiile de control post-tratament sunt obligatorii.
Malek a recomandat utilizarea laserului CO in leziunile premaligneale penisului, ce prezinta elemente histopatologice clare de displazie; in timp ce Neodymium YAG este folosit pentru leziunile in situ si carcinoame (T1).
C. Radioterapia
Radioterapia externa
Radioterapia externa in doze de 35-65Gy poate duce la rezultate comparabile cu chirurgia pentru leziunile superficiale si de dimensiuni mici, pentru leziunile infiltrative, voluminoase fiind indicata excizia chirurgicala.
Brahiterapia
In comparatie cu radioterapia externa, brahiterapia pare sa confere un control local mai bun. Brahiterapia se poate practica:
prin mulaj aplicat pe penis de catre pacient, intermitent pe durate de timp calculate pentru a elibera o doza de 60 Gy timp de o saptamana sau cu
fire de iridiu interstial (Ir192) ce elibereaza doze intre 50-70Gy pe o perioada de 5-7 zile, pe parcursul procedurii pacientul purtand sonda uretro-vezicala.
Se recomanda circumcizia pentru expunerea leziunilor inaintea efectuarii sedintelor de radioterapie.
Indicatiile radioterapiei
pacientii tineri cu leziuni mici (2-4 cm), superficiale, exofitice, neinvazive ale glandului sau santului coronar.
pacienti ce refuza tratamentul chirurgical ca terapie initiala.
pacienti cu tumori inoperabile sau cu metastaze ce necesita terapie locala a tumorii primare si in acelasi timp doresc mentinerea penisului.
Dezavantajele metodei constau in:
riscul de progresie tumorala
stenoza de meat uretral
stricturi uretrale - la 40% din cazuri
radionecroza glandului
descuamari epiteliale
edemul acut
scleroza preputiala si fimoza secundara
scleroza glandului
afectarea parenchimului testicular
lipsa confirmarii histopatologice a sterilizarii oncologice a leziunilor.
D. Tratamentul chirurgical
Urmatoarele tipuri de interventii chirurgicale pot fi aplicate in tratamentul tumorilor primare ale penisului:
Biopsia - exereza
Circumcizia
Tratamentul chirurgical micrografic - Mohs
Amputatia peniana partiala
Amputatia glandului si postectomie cu grefa de piele libera despicata pe capetele corpilor cavernosi
Amputatia peniana totala cu uretrostomie perineala
Operatii de exereza larga
Emasculatie
Cistoprostatoveziculectomie cu rezectie de simfiza si ramuri pubiene
Hemipelvectomie
Hemicorporectomie.
Consideratii anatomice
Penisul prezinta:
- o parte fixa - radacina penisului, care se leaga de pelvis
- o parte libera (pendulara) - formata din corpul si glandul penisului.
Corpul penisului are o forma cilindrica, prezinta o fata superioara (dorsala) si o fata inferioara (ventrala).
Glandul este situat distal, prezinta un sant circular in care se gasesc glandele preputiale, iar la varful glandului se gaseste meatul uretral extern.
Structura penisului este formata din:
1. Biopsia - exereza
Inainte de aplicarea oricarei terapii, biopsia este necesara pentru confirmarea histologica si stadializarea prin aprecierea asupra invaziei microscopice. Diferite tehnici pot fi folosite:
citologie umeda
biopsie cu ac fin (CIS)
biopsie incizionala (leziuni ale tecii penisului)
biopsie excizionala (tumori preputiale).
Adesea, incizia dorsala a preputului (dorsal split) este necesara pentru a permite accesul asupra leziunii tumorale. Biopsia incizionala permite cele mai bune informatii asupra profunzimii tumorale si evita sub-stadializarea.
Pentru leziunile ce implica meatul este necesara evaluarea endoscopica a tractului urinar inferior cu biopsii uretrale.
Nu s-au mentionat diseminari tumorale secundare biopsiilor.
2. Circumcizia
Tumorile mici neinvazive localizate la nivelul preputului distal pot fi rezolvate prin circumcizie cu o margine de siguranta de 2 cm. Daca leziunea preputiala nu este excizata larg in tesut sanatos, incidenta recurentei locale este destul de ridicata. Overall si McDougal precizeaza o rata de 32% a recidivei locale la pacientii tratati prin excizie locala si circumcizie. Namayama raporteaza recidiva in 50% din cazuri necesitand amputatie partiala.
Aceste statistici sunt de luat in considerare cand circumcizia este luata in calcul in managementul terapeutic al cancerului preputial si ele atrag atentia asupra necesitatii urmaririi clinice atente a pacientilor cu tumori superficiale de penis. Tot acum trebuie reamintit rolul circumciziei in cadrul tratamentului leziunilor peniene premaligne unde preputul reprezinta o sursa de iritatie si inflamatie cronica, fiind obligatorie la pacientii cu fimoza.
De asemenea, circumcizia este recomandata la pacientii ce urmeaza sa faca tratament radioterapic, fie ca este vorba de iradiere externa ori de brahiterapie.
3. Tratamentul chirurgical micrografic - Mohs
Conceptul de excizie secventiala de straturi subtiri a leziunilor cutanate sub control microscopic (sectiuni congelate), in chirurgia micrografica, vine de la observatia ca procesul canceros se extinde adesea dincolo de leziunea vizibila sau palpabila clinic. Adesea carcinomul scuamos infiltreaza structurile subiacente prin cordoane celulare fine, fenomen ce explica recurenta locala ridicata a tumorilor preputiale superficiale atunci cand marginea de siguranta oncologica este mai mica de 2 cm.
Acest tratament permite mentinerea integritatii anatomice si functionale a penisului fara a face rabat de la principiile oncologice si consta in excizia locala secventiala a tumorii primare, in straturi subtiri si orizontale cu depistarea histologica a elementelor neoplazice reziduale. Examinarea histologica a tesutului excizat fie dupa fixare in formol si includerea la parafina, fie extemporaneu 'la gheata' permite separarea tumorala de tesutul normal cu examinare histologica imediata a marginilor de rezectie.
Rata de curabilitate pentru tumorile cu stadii incipiente este echivalenta cu cea a tehnicilor chirurgicale mai radicale.
Mohs a raportat un procent de 100% curabilitate pentru leziuni mai mici de 1 cm in diametru dar numai 50% rata de curabilitate pentru leziunile mai mari de 3 cm.
In urmarirea la 5 ani, rata de curabilitate este de 74% cu rezultate excelente la pacientii diagnosticati cu tumori in stadii initiale.
Rata de recidiva locala este de 6% fata de 10% dupa amputatia partiala si 18% dupa excizia locala clasica.
Factorii de prognostic pentru acest tip de interventie chirurgicala au fost individualizati astfel: stadializarea si gradingul tumoral, marimea tumorii primare, esecul tratamentului chirurgical sau al radioterapiei anterioare.
Aceasta tehnica ofera o alternativa pacientilor cu CIS la care terapiile conservatoare au esuat si care refuza amputatia partiala.
Complicatiile acestei tehnici sunt stenozele de meat sau modificarile de aspect ale glandului.
Stenoza de meat poate fi tratata prin crearea de lambouri insulare sau prin tehnicile de avansare Y-V. Reconstructia santului coronar imbunatateste aspectul estetic al portiunii distale a penisului. Aceasta tehnica este contraindicata pentru leziunile cu diametrul mare sau in stadiu avansat.
Tabelul nr.4. Ratele recurentei locale in diferitele tipuri de aborduri chirurgicale ale tumorilor peniene superficiale (Tis; T1) (Dupa: Superficial carcinoma of the Penis: Management and Prognosis - Harryhill JF and Carpiniello VF).
|
Modalitate terapeutica |
Rata recurentei (%) |
|
Penectomie partiala |
0-7 |
|
Circumcizie |
32-50 |
|
Ablatie laser |
15-30 |
|
Tratamentul chirurgical micrografic - Mohs |
6 |
|
Radioterapie externa |
30 |
|
Brahiterapie - mulaj - iridiu interstitial |
21 9 |
4. Amputatia partiala de penis
Radicalitatea oncologica prin amputatia partiala este asigurata prin realizarea marginii de siguranta de 2 cm. Dupa izolarea leziunii cu o manusa chirurgicala se va aplica un tourniquet la baza penisului.
Tegumentul se incizeaza circular. Corpii cavernosi sectioneaza pana la uretra. Sunt ligaturate vasele dorsale. Uretra este disecata astfel incat sa se obtina 1 cm distal fata de limita de rezectie a corpilor cavernosi. Nu se face rabat oncologic la disectia uretrei.
Hemostaza se realizeaza la nivelul corpilor cavernosi cu fire separate aproximand marginile fasciei Buck. Se va indeparta tourniquet-ul. Uretra este spatulata pe fata dorsala pentru a preveni stenoza de meat. Se anastomozeaza tegumentul la uretra cu suturi absorbabile 3/0 sau 4/0.
Tegumentul redundant este aproximat dorsal pentru a completa inchiderea plagii. Cateterul utretro-vezical este mentinut pentru minim 24 h.
Cand bontul penian este prea scurt pentru a directiona jetul urinar se poate obtine o lungire suplimentara a bontului prin sectionarea ligamentului suspensor al penisului, sectionarea muschilor ischiocavernosi sau disectia partiala a corpilor cavernosi de ramurile pubiene.
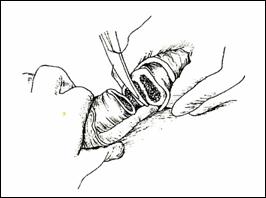
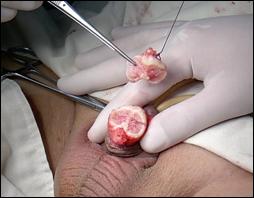
a. b.
Figura 17. Amputatia partiala de penis. a) schema anatomica; b) imagine intraoperatorie.
.

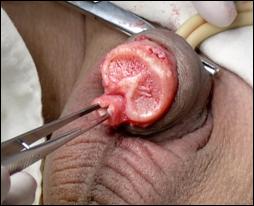
a. b.
Figura
18. a,b. Disectia uretrei
si spatularea acesteia. a)
schema anatomica; b)
aspect intraoperator.
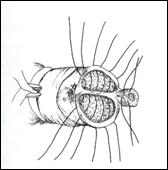


![]() a. b. c.
a. b. c.
Etapele de inchidere a bontului penian. a-c)Scheme anatomice
5. Amputatia glandului si postectomia cu grefa de piele pe capetele corpilor cavernosi
Variantele terapeutice pentru tumorile peniene superficiale Tis, Ta si T1 sunt reprezentate de biopsia-exereza, postectomie, aplicatii topice cu creme citostatice, distructia cu laser si radioterapie.
Biopsia-exereza si postectomia sunt aplicabile tumorilor mici, unice, respectiv limitate la preput. Aplicatiile locale de creme citostatice (5-fluorouracil) sau distructia cu laser pot avea, de asemenea, rezultate favorabile in tumori mici, superficiale, necesitand biopsii multiple si profunde pentru aprecierea invaziei, grading-ul tumoral si o monitorizare stricta a pacientului.
Radioterapia descrisa ca fiind eficienta in unele cazuri, presupune de asemenea, un program de iradiere bine condus si controlat, dezavantajele metodei adaugand riscului de progresie tumorala si consecintele tratamentului - stenoza de meat uretral sau stricturi uretrale - la 40% din cazuri, radionecroza glandului, scleroza glandului si afectarea parenchimului testicular.
Consideram ca toate aceste tratamente "conservatoare" trebuie sa se desfasoare sub controlul unui medic urolog, riscul tratamentului incomplet cu agravarea situatiei locale sau diseminarii ganglionare fiind ridicat.
Experienta Centrului nostru cuprinde cazuri dramatice, de pacienti tineri tratati in servicii dermatologice sau de radioterapie, uneori pe parcursul mai multor ani si ajunsi in stadii in care uneori nici excizia tumorii sau a maselor ganglionare nu mai este posibila.
Amputatia chirurgicala clasica, cu limita de siguranta oncologica de 2 cm este o operatie sigura oncologic, cu procent foarte mic de recidive, dar mutilanta, greu acceptata in special de pacientii tineri.
Amputatia glandului si postectomia cu grefa de piele pe capetele corpilor cavernosi pentru tumori peniene este o metoda ce urmareste imbinarea sigurantei oncologice cu un rezultat estetic si functional foarte bun.
Grefele - definitie Sunt materiale biologice folosite pentru a inlocui pierderi tisulare. Intre momentul prelevarii si cel al plasarii la locul dorit nu beneficiaza de nici o conexiune vasculara cu zona donatoare.
Clasificare:
- dupa suprafata: - insulare
- fragmentare
- intinse.
- dupa grosime: - grefe de piele libera despicata (PLD) [1,2,3]
- subtiri (Tiersch) = din grosimea pielii (0,15-0,25 mm)
- intremediare (Blair) = 1/3-1/2 din grosimea pielii (0,25-0,45 mm)
= epiderm si parte de derm
- grefe de piele toata grosime (PTG) (Padget) = din grosimea pielii
(0,5-0,65 mm) = epiderm + tot dermul (inchiderea se face prin sutura).
Cea mai folosita este PLD. In general, aceasta se recolteaza de pe coapse, fese, trunchi, zone donatoare care se vindeca spontan. Se poate recolta succesiv din aceeasi zona la interval de 6 luni. Se poate aplica pe plagi granulare care se pregatesc prin degranulare sau pe plagi chirurgicale.
In perioada ianuarie 2002 - ianuarie 2005, pentru 4 pacienti cu varste cuprinse intre 36-54 de ani, biopsiati initial in alte servicii urologice sau dermatologice si adresati Centrului nostru cu tumori multiple de gland si preput, s-a practicat amputatia glandului si postectomie.
Protocolul diagnostic a constat in:
examen clinic,
biopsie preoperatorie,
CT abdomino-pelvin,
radiografie pulmonara.
Deoarece aparenta clinica a fost in doua cazuri de tumori infiltrative in gland, s-au prelevat biopsii multiple cu examen histopatologic extemporaneu din albugineea corpilor cavernosi, cu rezultat negativ. Avand in vedere varsta pacientilor si radicalitatea operatiei de exereza, s-a decis grefarea capetelor corpilor cavernosi cu piele libera despicata, recoltata de pe fata interna a bratului in trei cazuri si cu piele toata grosimea de la nivelul abdomenului, cu inchiderea plagii cu sutura intradermica intr-un caz. La doua cazuri cu ganglionii inghinali palpabili, la 6 saptamani postoperator s-a practicat limfodisectie inghino-femurala bilaterala cu rezultat negativ intr-un caz si pozitiv in altul.
Tehnica chirurgicala:
se trec 3-4 fire la nivelul extremitatii preputului cu rol de tractiune si izolare a leziunii;
incizie circulara a pielii tunicii dartos si fasciei Buck sub nivelul glandului;
se diseca complet cu foarfeca si electrocauterul glandul de capetele corpilor cavernosi cu sectionarea uretrei la acest nivel;
se preleveaza multiple biopsii din albugineea corpilor cavernosi;
hemostaza si prepararea patului pentru grefare;
se recolteaza piele libera despicata cu dermatomul de pe fata interna a bratului;
se sutureaza grefa de piele distal la marginea corpului spongios si proximal pana la nivelul tegumentului penian restant;
pansament "tulle gras" usor compresiv.
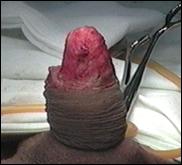
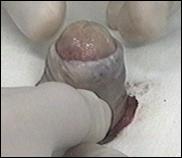

a. b. c.
Figura 20.
a) Pacientul L.P., 38 ani; b,c) aspecte pre si intraperator.

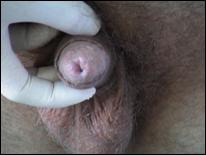

a. b. c.
Aspecte postoperatorii - imediat(a) si la 6 luni (b;c).

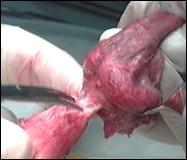
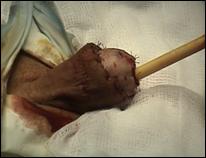
a. b. c.
Figura 22.
Pacientul N.I., 45 ani, grefa
de piele despicata. a) aspect preoperator; b-c) aspecte intraoperatorii.


Figura 23.
a,b) Aspecte la 6 luni
postoperator (+ limfodisectie
inghinofemurala).
a. b.
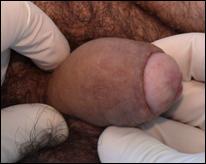


Figura 24.
Pacientul B.G., 54 ani. a) aspect preoperator; b) aspect intraoperator (grefa de piele
toata grosimea); c) aspect la 6 luni postoperator.
a. b. c.
Rezultatul operatiilor a fost favorabil in toate cazurile, cu priza grefei si externarea pacientilor in a 10-a zi postoperator, cu pansamente in ambulator.
In toate cazurile s-a inregistrat o retractie a grefei cu micsorarea suprafetei neoglandului.
Nu s-au inregistrat recidive tumorale locale sau ganglionare inghinale intre 24 si 5 luni postoperator.
Aspectul estetic, de o importanta deosebita in cazul acestui tip de operatie, a fost foarte bun, cu obtinerea unui neogland care este acoperit de tegumentul penian restant ce ia aparenta de preput, greu de deosebit de un penis normal.
Functional, rezultatul este, de asemenea, foarte bun, pierzandu-se doar lungimea corespunzatoare glandului, stimulii psihogeni si cei locali de la nivelul penisului restant asigurand erectia si ejacularea.
Neomeatul rezultat prin sutura grefei de piele la marginile corpului spongios nu are tendinta la stenoza ca in multe cazuri de amputatie peniana clasica.
Un alt avantaj al acestui tip de operatie este reprezentat de posibilitatea depistarii precoce a unei eventuale recidive tumorale.
Aceasta operatie, pe care noi am aplicat-o in cazul unor tumori limitate la gland si preput, poate fi aplicata si in cazul unor tumori infiltrative in corpii cavernosi in cazul in care lungimea bontului penian dupa exereza in limite oncologice, verificate prin examen anatomo-patologic extemporaneu, o permite, cu pastrarea avantajelor sus mentionate.
In concluzie amputatia glandului si postectomia cu grefa de piele pe capetele corpilor cavernosi reprezinta o solutie sigura oncologic si cu rezultat estetic si functional foarte bun pentru tratamentul tumorilor peniene.
6. Amputatia totala de penis
Amputatia totala este indicata in leziunile a caror marime sau localizare contraindica amputarea partiala. Se izoleaza leziunea primara, iar corpii cavernosi sunt disecati proximal de ligamentul suspensor si vasele dorsale care sunt ligaturate.
Sectiunea distala a uretrei si tractiunea ei ventrala ajuta in disectia ei de corpii cavernosi la nivelul regiunii bulbare.
Etapa urmatoare consta in disectia corpilor cavernosi de insertiile lor de la nivelul ramurilor inferioare ale pubelui, dupa care acestia sunt ligaturati cu suturi absorbabile.
La nivelul tegumentului perineal se excizeaza 1 cm de tegument cu aspect eliptic si se creaza un tunel prin tesutul subcutan.
Uretra disecata este transpusa in perineu prin acest tunel, astfel incat sa nu existe angulari pe traseu. Uretra este spatulata si anastomozata la tegumentul perineal.
Incizia primara se inchide cu fire separate dispuse transversal astfel incat se va ridica scrotul anterior indepartandu-se de neomeat.
Se va plasa un tub de dren si un cateter uretro-vezical pentru minim 24 de ore.
Complicatiile rezectei peniene sunt reprezentate de hemoragia din corpii cavernosi atunci cand hemostaza acestora a fost facuta defectuos si sangerarea nu a fost controlata intraoperator prin indepartarea tourniquet-ului de la baza penisului. O alta complicatie ce poate surveni este stenoza de meat uretral.
Tehnicile de reconstructie peniana includ lambouri de la nivelul antebratului, sau mai recent lambouri miocutane de antebrat inervat, combinate cu lambouri din pulpa halucelui pentru reconstructia glandului.
Figura 25. Izolarea
leziunii primare. a) schema anatomica; b) aspect intraoperator.


a. b.
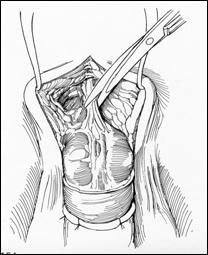
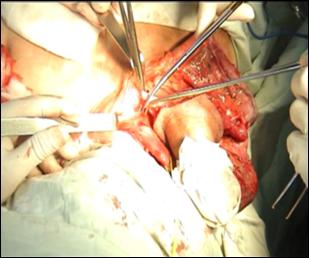
a. b.
Figura 26. Sectionarea ligamentului suspensor si ligatura complexuluidorsal al penisului.
a) schema anatomica; b) imagine intraoperatorie.
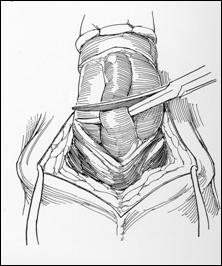

a. b.
Figura 27. Disectia uretrei bulbare de corpii cavernosi. a) schema anatomica; b) aspect intraoperator.
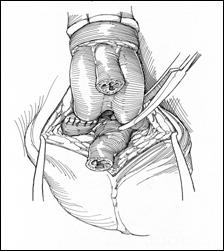

a. b.
Sectionarea radacinii corpilor cavernosi.
a) schema anatomica; b) aspect intraoperator.
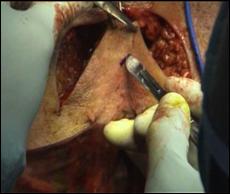
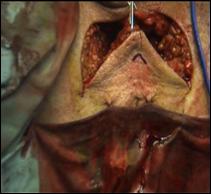
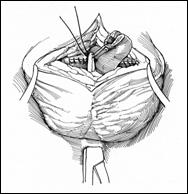
a. b. c.
Figura 29. Uretrostomie perineala. a) schema anatomica; b-c) aspecte intraoperatorii.
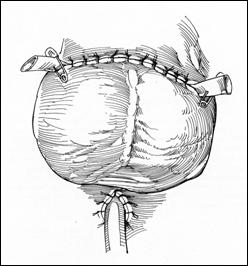

a. b.
Figura 30. Amputatie totala de penis - aspect final. a) schema anatomica; b) aspect intraoperator.
7. Abordul perineal
Se face o incizie perineala in forma de "U" inversat , cu disectia unui lambou de piele si tesut subcutan. Se plaseaza o tractiune pe lamboul de piele si se diseca suprafata muschiului bulbo-spongios de-a lungul intregului perineu.
Se deschide muschiul si se separa de corpul spongios. Se elibereaza acesta si de pe corpii cavernosi. Se taie corpul spongios si uretra; se lasa suficienta lungime pentru a se ajunge la pielea perineala. Se diseca bontul catre diafragma uro-genitala.
Apoi se divide scrotul catre si in jurul bazei penisului. Se taie ligamentul suspensor, se leaga si se sectioneaza complexul dorsal si se diseca corpii la diviziunea lor. Se plaseaza pense pe corpi, se sectioneaza si se inspecteaza bonturile. Se face o incizie circulara sau in "V" in perineu, se ataseaza uretra si se inchide plaga.

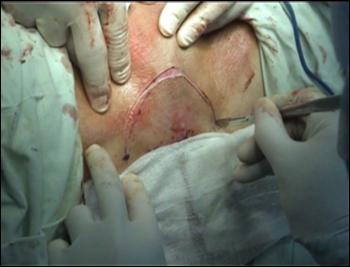
a. b.
Figura 31. Incizie perineala in forma de "U" inversat de-a lungul bulbului uretral.
a) schema anatomica; b) imagine intraoperatorie.
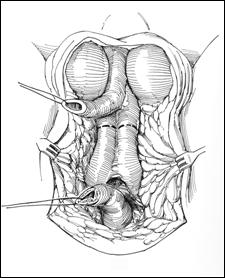

a. b.
Figura 32. Sectionarea uretrei si corpilor cavernosi.
a) schema anatomica. b) imagine intraoperatorie a bontului uretral dupa amputatia peniana totala.

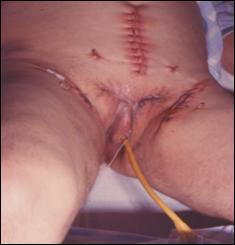
a. b.
Figura 33. a,b. Aspecte postoperatorii amputatie peniana totala,
respectiv emasculatie cu uretrostomie perineala.
8. Operatii de exereza larga
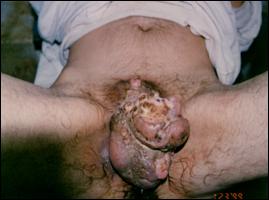
Emasculatia
Cistoprostatoveziculectomia cu rezectie de simfiza, hemipelvectomie.
a.
Cand leziunile cuprind scrotul, tegumentul hipogastric sau
perineal, formand un bloc genito-perineal tumoral se impun operatii de
exereza larga adaptate fiecarui caz in parte ce presupun emasculatie, rezectie de
simfiza sau de ramuri pubiene inferioare, cistoprostatectomie cu
derivatie urinara, limfodisectie ilioobturatorie si
inghinofemurala urmate de interventii de chirurgie plastica
pentru acoperirea zonelor de excizie.
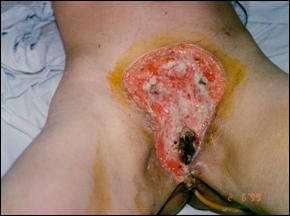

a. b.
Figura 34. a) Tumora peniana voluminoasa ce infiltreaza scrotul si tegumentul hipogastric - aspect preoperator; b) aspect postoperator. Se observa defectul cutanat rezultat in urma emasculatiei si uretrostomia perineala. c) aspect postoperator dupa grefarea zonei de excizie.
Reconstructia peniana dupa amputatia peniana si emasculatie
Pacientii documentati cancer free dupa amputatia partiala de penis pot beneficia de optiunea reconstructiei peniene. Modalitatea de electie pentru reconstructia peniana pare a fi reconstructia cu lambou liber radial de antebrat. S-a dovedit a fi util in reconstructia peniana si lamboul lateral de brat, Acest flap are tegumentul subtire relativ neparos cu vascularizatie individualizata si inervatie cutanata.
Deoarece aceste lambouri prezinta inervatie independenta, ce poate fi mentinuta, se poate reconstrui sensibilitatea erogena.
Corpurile cavernoase proximale ramase servesc drept suport pentru proteza peniana, in timp ce segmentele distale ale corpurilor cavernoase se pot reconstrui cu Gore-Tex ce asigura si substituie tesutul erectil.
Reconstructia peniana dupa amputatia totala de penis reprezinta una dintre cele mai mari provocari ale chirurgiei genito-urinare.
Anatomia si fiziologia tesutului erectil sunt unice si nu pot fi reproductibile prin transferul altor tesuturi.
Conceptele noi in reconstructia microchirurgicala au imbunatatit functionalitatea si aspectul estetic al neofalusului.
Ideal, constructia-reconstructia peniana/falica trebuie sa indeplineasca urmatoarele cerinte:
1) o etapa unica de procedeu microchirurgical.
2) crearea unei uretre competente capabila sa asigure evacuarea normala.
3) reconstructia peniana trebuie sa asigure sensibilitatea tactila si erogena.
4) un penis cu suficient tesut care sa permita un implant prostetic suficient pentru a asigura penetrare vaginala.
5) aspect estetic acceptat de pacient.
Pentru pacientii cu amputatie totala de penis, reconstructia peniana utilizand tehnici microchirurgicale este metoda de electie. Amputatia totala de penis implica substitutie protetica. Protezele peniene de Gore-Tex s-au dovedit a fi cele mai fiabile .
Tratamentul lanturilor ganglionare
Biologia cancerului penian presupune o faza loco-regionala indelungata inainte sa apara diseminarile la distanta.
Prezenta si extensia metastazelor regiunii inghinale sunt cei mai importanti factori de prognostic la pacientii cu cancer penian scuamos.
Acestea afecteaza prognosticul bolii mai mult decat gradul tumorii, dezvoltarea voluminoasa si modelul tumoral morfologic sau microscopic.
In cazul tumorilor peniene spre deosebire de alte tumori genito-urinare cu invazie ganglionara, ce presupun strategii terapeutice sistemice, limfadenectomia singura poate fi curativa si trebuie practicata.
Morbiditatea contra beneficiu. Retinerea in a practica limfadenectomia "automata" la toti pacientii cu cancer penian isi are originea in morbiditatea ridicata pe care procedura o are.
Complicatiile limfadenectomiei sunt:
necroza tegumentara - de la usoara la severa - necesitand grefa cutanata
edem scrotal si al membrelor inferioare mergand pana la limfedemul gigant invalidant
limfocelul
limforeea prelungita
seroamele
infectii ale plagii
flebitele / tromboflebita
tromboza venoasa profunda
trombembolismul pulmonar (TEP).
Complicatiile postoperatorii au fost reduse prin imbunatatirea tratamentului pre- si postoperator, a tehnicii chirurgicale, a colaborarii cu chirurgia plastica pentru acoperirea cu lambou musculo-cutanat si prezervarea dermului, fasciei Scarpa si a venei safene, ca si modificarile limfodisectiei.
Pentru a stabili un management corect al lanturilor ganglionare sunt necesare:
Controlul adecvat al leziunii primare si stabilirea stadiului anatomo-patologic
Examinare inghinala atenta
TC abdomino-pelvin
Rx. toracic.
A). Pacienti fara adenopatii inghino-femurale palpabile - Protocol terapeutic
Tis,Ta,T1 cu ganglioni limfatici inghino-femurali negative
Pacienti cu tumori primare carcinom in situ (Tis), carcinom verucos (To) si cu tumori stadiul T1 grad 1-2, prezinta <10% incidenta de limfonoduli pozitivi si sunt candidati optimi pentru strategie watchful waiting (expectativa armata) ce presupune autopalpare si controale medicale la 3 luni timp de 3 ani. Aparitia unei adenopatii unilaterale la distanta impune limfodisectie inghino-femurala si ulterior pelvina (in functie de rezultatul examenului anatomopatologic) unilaterala + limfodisectie inghinala superficiala controlaterala.
T2, T3 N0 M0 /T1 G3
Leziunile infiltrative si cele cu grad inalt de anaplazie G3 se asociaza in 66% din cazuri cu adenopatii microscopice, deci limfadenectomia profilactica pare justificata, de electie fiind limfodisectia limitata (Catalona).
Reiteram avantajele acestui tip de limfodisectie limitata fata de cea radicala, aceasta fiind cea preferata si in Centrul nostru:
scade morbiditatea
incizie este mai scurta
disectia limitata exclude zonele laterale de artera femurala si caudal de fosa ovala
vena safena este prezervata (cu mentiunea ca in caz de adenopatie voluminoasa - bulky desease - aceasta poate fi sacrificata)
transpozitia muschiului sartorius este evitata.
B) Pacienti cu adenopatii inghino-femurale palpabile - Protocol therapeutic
Tis sau Ta T1 cu adenopatie inghino-femurala palpabila
Se practica antibioterapie 4-6 saptamani dupa indepartarea leziunii primare. In cazul in care adenopatia se remite - pacientul intra in programul de urmarire clinica. In cazul persistentei adenopatiilor se impune limfodisectie inghino-femurala si ulterior pelvina (in functie de rezultatul examenului anatomopatologic) unilaterala si limfodisectie inghinala superficiala controlaterala.
T2-T3, N1-3, M0 - stadiul III
In cazul tumorilor infiltrative cu adenopatii palpabile este indicata de asemenea antibioterapia 4-6 saptamani dupa indepartarea leziunii primare.
Antibioterapia mai de graba scade riscul de infectie al plagii inghinale sau de complicatii septice dupa controlul unei tumori primare infectate, decat sa influenteaze decizia de stadiere chirurgicala.
In continuare protocolul terapeutic presupune:
adenopatia dispare - limfodisectie inghinala superficiala (daca ganglionii sunt negativi la gheata) sau limfodisectie superficiala si profunda limitata (Catalona)
adenopatie unilaterala - limfodisectie ilio-inghinala si inghino-femurala superficiala controlaterala
adenopatie bilaterala persistenta - limfodisectie ilio-inghinala bilaterala.
Adenopatiile persistente dupa tratamentul leziunii primare si dupa 4-6 saptamani de antibiotice sunt cel mai frecvent consecinte ale metastazelor.
De asemenea, adenopatiile ce apar postoperator sunt mult mai probabil cauzate de metastaze decat de un proces inflamator
Studiile au analizat supravietuirea la barbatii la care s-a practicat limfadenectomia precoce in raport cu cea tardiva, supravietuire raportata la examenul anatomo-patologic al nodulilor ganglionari.
Semnificatia prognostica a prezentei si extensiei metastazelor
Criteriile asociate cu supravietuirea pe termen lung dupa rezectia chirurgicala cu tenta curativa a adenopatiei inghinale (80% supravietuire de 5 ani) sunt:
1) metastaze minime (pana la 2 ganglioni)
2) afectare unilaterala
3) fara semne de metastaze extraganglionare si
4) absenta metastazelor in ganglionii pelvini.
Precum s-a aratat, rata de vindecare pentru pacientii la care s-a practicat limfadenectomie inghinala poate ajunge la 80%.
O rata de vindecare de o asemenea amploare prin tratamentul chirurgical al metastazelor ganglionare regionale este similara in experienta urologica cu cancerul testicular, in care limfadenectomia retroperitoneala (RPLND) ofera vindecarea la multi pacienti cu metastaze ganglionare minime.
Stadiul IV - orice T, orice N +, M1 sau T4 (inoperabil)
Adenopatii inoperabile prin fixare, invazie in organele adiacente - Protocol terapeutic
Supravietuirea la acesti pacienti este legata de eradicarea completa a tesutului tumoral. Aceasta sarcina este dificil de indeplinit numai de catre chirurgie, chimioterapie sau radioterapie in monoterapie. Combinatia tratamentului chirurgical si chimioterapie prezinta beneficii in carcinoamele peniene avansate (Pizzocaro, Corral) si, in functie de caz, implica urmatoarele proceduri:
1) Metastaze limfoganglionare fixate
2) >4 cm limfoganglioni inghinali mobili
3) Metastaze limfoganglionare pelvine dovedite imagistic
![]()
 Chemoterapie combinata
Chemoterapie combinata
boala stabilizata
![]()
![]()
![]() Excizabile Non-excizabile
Excizabile Non-excizabile
Rezectie chirurgicala Chirurgie Chimioterapie "de salvare"
agresiva paleativa Radioterapie
Procedurile modificate de stadiere limfoganglinara
La pacientii fara evidente de adenopatie palpabila care sunt selectati pentru a urma proceduri inghinale, in virtutea factorilor de prognostic advers in cadrul tumorii primare, scopul este de a stabili daca metastazele limfoganglionare exista, dar cu morbiditate minima pentru pacient.
O varietate de optiuni terapeutice pentru acest obiectiv au fost raportate:
1). citologia prin aspiratie cu ac fin (fine needle aspiration cytology - FNAC)
2). biopsie ganglionara
3). biopsia limfonodulului santinela
4). limfodisectia extinsa dincolo de nodulul santinela (ESLND)
5). harta limfatica intraoperatorie (IOLM)
6). disectia ganglionilor superficiali si
7). disectia completa modificata.
1. Citologia aspirativa cu ac fin (FNAC)
Experienta cu FNAC este limitata si majoritatea informatiilor deriva din studii singulare (Scappini). Procedura necesita limfoangiografie peniana si/sau o investigatie pentru localizarea nodulilor, urmata de aspiratie sub ghidaj fluoroscopic sau CT scan.
Nodulii multiplii trebuie sa fie analizati separati.
Studiile efectuate si dificultatea tehnica a limfoangiografiei fac aspiratia mai putin practica, ca tehnica de stadiere, pentru pacientii cu limfonoduli nepalpabili. Totusi, aspiratia directa a limfonodulilor inghinali palpabili este usor de realizat si daca este pozitiva, poate aduce informatii folositoare stabilirii tratamentului in continuare.
2. Biopsia ganglionara
Sunt biopsiati ganglionii limfatici superficiali inghino-femurali ce sunt palpabili.
Metoda este usor de realizat tehnic si poate dicta conduita terapeutica ulterioara.
3. Biopsia limfonodulului santinela (SLNB)
Conceptul de SLNB asa cum a fost descris de Cabanas (1977) este sustinut de studiile limfoagiografice peniene detaliate in care sunt demonstrate drenajul limfaticelor peniene intr-un nodul santinela sau intr-un grup de noduli localizati supero-medial de jonctiunea dintre venele safena si femurala in aria venei epigastrice superficiale.
Metastazele in nodulul santinela indica necesitatea unei limfodisectii complete inghinale superficiala si profunda. Acuratetea histologiei nodulului santinela in identificarea metastazelor ganglionare a fost pusa la indoiala de un numar de studii.
4. Limfodisectia extinsa dincolo de nodulul santinela (ESLND)
Deoarece metastazele ganglionare devin palpabile la unii pacienti din aceste studii intr-o perioada de 1 an in care biopsia ganglionilor santinela este negativa, apare un rezultat fals negativ al biopsiei. Autorii indica ipoteza ca biopsiile ganglionare inghinale fals negative sunt rezultatul variatiilor anatomice de pozitie a "nodulului santinela" in campul inghinal.
In concluzie, biopsiile directionate spre o arie anatomica specifica nu sunt precise in identificarea metastazelor microscopice si nu sunt recomandate.
5. Harta limfatica intraoperatorie (IOLM)
IOLM ofera potentialul pentru localizarea precoce a nodulului santinela. Tinta hartii limfatice este stabilirea localizarii limfonodululului santinela in campul limfatic ganglionar inghinal, folosind fie tehnicile obisnuite (substante de contrast albastre VBD), fie radiotrasori.
Tehnicile au fost studiate la pacientii cu melanom malign si carcinoame ale sanului si vaginului ce necesitau evaluarea limfonodulilor regionali.
Tehnica implica injectie intradermica de isosulfan albastru sau technetiu coloidal in jurul leziunii. Substanta de contrast sau trasorul radioactiv este transportata de limfaticele aferente catre un nodul specific. Acest nodul este desemnat nodul santinela. Asa incat, datele preliminare sugereaza ca IOLM permite localizarea precisa a limfonodulilor si astfel stabileste riscul diseminarilor precoce in cancerul penian.
Mai mult, IOLM detecteaza astfel de noduli ori de cate ori apar in campul inghinal. In prezent, aspectele tehnice de IOLM, curbe de invatare si lipsa datelor pe termen lung limiteaza potentialul aplicarii ei pe scara larga comparativ cu alte tehnici de disectie standard.
Datorita procentului mare de rezultate fals negative recomandam limfodisectiile limitate sau complete atat ca metoda de stadializare cat si terapeutica.
6. Limfodisectia superficiala si disectia inghino-femurala modificata
Ambele au fost propuse ca metode de stadiere la pacientii fara adenopatie inghinala palpabila.
Limfodisectia superficiala presupune indepartarea ganglionilor aflati superficial de fascia lata.
Limfadenectomia inghino-femurala completa (indepartarea ganglionilor situati profund de fascia lata aflati in trigonul femural, ca si nodulii pelvini) este practicata doar daca nodulii superficiali sunt pozitivi la examen extemporaneu. Motivatia efectuarii limfodisectiei superficiale este subliniata de studii ce arata lipsa nodulilor pozitivi situati profund de fascia lata chiar daca nodulii superficiali sunt pozitivi. Desi limfaticele corpilor cavernosi si spongiosi se presupune ca pot drena direct in nodulii inghinali profunzi, evidenta clinica sustine ca primul esalon al metastazarii este reprezentat de nodulii superficiali.
Disectia inghinala completa modificata a fost initial propusa de Catalona (1988) si presupune o incizie mica, o disectie inghinala limitata ca intindere si prezervarea venei safene. Aceasta tehnica evita nevoia de a transpune muschiul sartorius pentru a acoperi vasele femurale. Spre deosebire de disectia superficiala, nodulii profunzi din fosa ovala sunt de asemenea excizati. Experienta clinica a confirmat valoarea acestei tehnici, atunci cand este practicata corect, pentru identificarea metastazelor microscopice cu morbiditate minima.
Foarte important este ca limfoangiografia peniana nu a evidentiat un drenaj ganglionar pelvin direct (care sa ocoleasca ganglionii inghinali), asa incat, atat limfodisectia superficiala, cat si disectia inghinala completa modificata ar trebui sa identifice adecvat metastazele microscopice la pacientii cu examinari inghinale clinic negative, fara a fi nevoie de disectie pelvina, daca nodulii inghinali sunt negativi.
Avantajele acestor disectii limitate includ:
1) informatii suplimentare fata de biopsia unui singur ganglion sau unui grup de ganglioni.
2) evitarea posibilitatii de identificare gresita a nodulului santinela prin excizia "tuturor " potentialilor noduli santinela.
3) morbiditate redusa comparativ cu limfadenectomia standard si
4) timp operator redus.
7. Limfadenectomia inghino-femurala si ilio-obturatorie radicala
La pacientii cu adenopatie metastatica rezecabila, valoarea potential terapeutica a limfadenectomiei justifica morbiditatea metodei. Scopul este de a eradica toata tumora vizibila, de a asigura protejarea vaselor expuse si de a asigura vindecarea rapida a plagii (sutura per primam sau acoperire cu lambou musculo-cutanat). Raman totusi cateva probleme.
Limfadenectomia inghinala trebuie sa fie bilaterala si nu unilaterala la pacientii ce prezinta adenopatie unilaterala la prezentarea initiala cu tumora primara.
Incrucisarea anatomica a limfaticelor peniene este bine stabilita si drenajul bilateral este regulat la 43 din 54 de pacienti (79%) la care s-a practicat IOLM la Netherlands Cancer Institute, iar drenajul limfatic al penisului a fost bilateral.
Limfodisectia controlaterala poate fi limitata la zona de deasupra fasciei lata daca nu este gasita prin chirurgie si examen extemporaneu evidenta histologica de noduli superficiali pozitivi.
Suportul clinic pentru procedura bilaterala este gasirea de metastaze controlaterale la >50% din pacientii astfel tratati, chiar cand regiunea ganglionara controlaterala a fost negativa la palpare.
Tehnici chirurgicale
Consideratii anatomice
Ganglionii limfatici inghinali sunt divizati in grupe superficiale si profunde care anatomic sunt separate de fascia profunda a coapsei - fascia lata. Grupul superficial compus din 4-25 ganglioni (medie 8) sunt situati la nivelul fasciei superficiale a coapsei - fascia Camper. Acest grup dreneaza in 2-3 ganglioni inghinali profunzi care sunt situati de-a lungul vaselor femurale. Ganglionul lui Cloquet este cel mai cranial ganglion al acestui grup situat la nivelul canalului femural, medial de vena femurala. Ganglionii iliaci externi dreneaza limfa din: ganglionii inghinali profunzi, ganglionii obturatori si ganglionii hipogastrici. Urmatoarea statie de drenaj este reprezentata de ganglionii iliaci comuni si para-aortici.
Pentru ca safena mare sa intre in vena femurala, ea trebuie sa strabata nu numai fascia profunda (fascia lata si fascia cribriforma) dar si teaca femurala.
Teaca femurala este lunga de aproximativ 4 cm si contine trei compartimente diferite:
compartimentul medial - contine vase limfatice si ganglioni limfatici
compartimentul intermediar - contine vena femurala
compartimentul lateral - contine artera femurala.
Teaca femurala este formata de migrarea straturilor fasciale din peretele abdominal posterior acolo unde vasele de sange ies din abdomen pentru a intra in coapsa. Condensarea fasciei transversalis constituie peretele anterior al tecii femurale, in timp ce peretele posterior este reprezentat de o prelungire a fasciei iliace. Nervul femural nu este localizat in aceasta teaca deoarece el iese din abdomen in fascia subseroasa. El este localizat lateral de canalul femural.
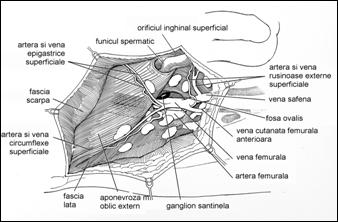
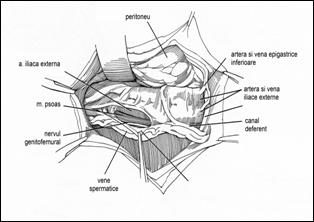
Figura 35. Planse anatomice ce expun regiunea inghino-femurala.
Vascularizatia tegumentului regiunii femurale este asigurata de ramuri din artera femurala comuna:
a. rusinoase superficiale externe
a. iliaca circumflexa superficiala
a. epigastrica superficiala.
Disectia inghinala completa implica ligatura acestor ramuri. Viabilitatea lambourilor tegumentare dupa aceasta limfodisectie depinde de vasele anastomotice din tesutul adipos superficial de fascia Camper. Deoarece drenajul limfatic al penisului se face prin vase situate sub fascia Camper acest strat adipos superficial poate fi pastrat.
Triunghiul femural este marginit de:
superior - ligamentul inghinal
lateral - muschiul croitor
medial - muschiul adductor lung.
Baza (planseul) triunghiului este reprezentata de muschiul pectineal, medial si muschiul iliopsoas lateral. Localizarea crosei safenei este estimata a fi la 2 latimi de deget lateral si inferior de tuberculul pubian.
Limfaticele inghinale sunt clasic descrise ca fiind situate intr-o zona marginita:
superior de ligamentul inghinal
inferior de o linie orizontala ce trece prin punctul de intersectie dintre m. croitor si masa adductorilor
lateral de o linie verticala prin spina iliaca antero-superioara
medial de o linie verticala prin tuberculul pubic.
 In
1948, Daseller a facut o descriptie
anatomica a drenajului limfatic inghinal prin disectii pe un lot de
450 de cadavre. De altfel, Daseller a
aratat prin studiile sale ca aceasta descriere nu cuprinde
toti limfonodulii implicati in diseminarea neoplazica. El a
delimitat aria de disectie ca fiind un patrulater cu urmatoarele
limite:
In
1948, Daseller a facut o descriptie
anatomica a drenajului limfatic inghinal prin disectii pe un lot de
450 de cadavre. De altfel, Daseller a
aratat prin studiile sale ca aceasta descriere nu cuprinde
toti limfonodulii implicati in diseminarea neoplazica. El a
delimitat aria de disectie ca fiind un patrulater cu urmatoarele
limite:
superior de o linie paralela cu ligamentul inghinal la 1cm deasupra acestuia avand lungimea de 12 cm
medial pe tuberculul pubic de o linie verticala lunga de 15 cm
lateral de o linie verticala de 20 cm prin marginea laterala a limitei superioare
inferior de o linie transversala de 10 cm ce leaga extremitatile inferioare ale limitelor laterala si mediala.
Limfodisectia inghinala modificata
Pentru pacientii care, din punct de vedere clinic, nu prezinta ganglioni invadati sau pacientii cu ganglioni minim mariti a fost propusa limfodisectia limitata (Catalona, 1988). Aceasta reprezinta o metoda de compromis intre biopsia ganglionului santinela care uneori este insuficienta (pacientii cu mai mult de un ganglion pozitiv) si limfodisectia inghinala extinsa standard care, uneori, nu este neaparat necesara pentru pacientii cu ganglioni regionali minim invadati si care are o morbiditate ridicata.
Limfodisectia inghinala modificata difera de cea standard prin:
incizia mai scurta
disectia ganglionilor este limitata prin excluderea ganglionilor laterali de artera femurala si inferior de fosa ovala
se prezerva vena safena
se elimina transpozitia muschiului croitor.
Prin aceasta disectie se excizeaza complet ganglionii limfatici inghinali superficiali situati anterior si medial de crosa venei safene precum si ganglionii inghinali profunzi din jurul vaselor femurale, situati profund de fascia lata.
Pacientul este pozitionat intr-o maniera similara celei pentru limfodisectia ilioinghinala radicala.
Tegumentul este incizat pe o distanta de 10 cm la 1,5 cm sub plica inghinala mergand in profunzime pana la nivelul fasciei Scarpa.
Lamboul superior este dezvoltat profund de fascia Scarpa pe o distanta de 8 cm. Un panicul adipos si tesut limfatic va fi dezvoltat avand baza la nivelul penisului. Cordonul spermatic este identificat si reflectat medial. Tot tesutul adipos si areolar situat sub aceasta structura este reflectat caudal ca un pachet ce contine ganglioni limfatici superficiali.
Lamboul inferior va fi dezvoltat sub nivelul inciziei pe o distanta de 6 cm. Vena safena este identificata in centrul campului operator, iesind din acest tesut. Tesutul de excizat va fi disecat dinspre lateral spre medial, prezervand vena safena.
Se ligatureaza atent vasele limfatice din perimetrul disectiei superficiale.
Aceasta manevra este importanta deoarece:
reduce drenajul limfatic postoperator
reduce riscul aparitiei limfocelului postoperator
reduce complicatiile legate de lamboul cutanat.
Ganglionii inghinali profunzi sunt aglomerati in jurul vaselor femurale. Limita superioara este reprezentata de ligamentul inghinal.
Jonctiunea safeno-femurala va fi prezervata.
Limitele disectiei modificate a ganglionilor inghinali profunzi sunt:
superior - ligamentul inghinal, unde este situat ganglionul lui Cloquet
medial - marginea muschiului aductor lung
lateral - artera femurala
caudal - varful trigonului femoral.
Cea mai mare parte a disectiei inghinale profunde se desfasoara medial de vena femurala.
Nu este necesara disectia arterei femurale sau a nervului femural.
Se recomanda ligaturarea tuturor vaselor limfatice intalnite ce constituie adesea cauza drenajului prelungit postoperator.
Piesa operatorie ce contine ganglionii limfatici inghinali profunzi este trimisa pentru examinarea anatomopatologica.
La finalul operatiei se vor utiliza drenaje aspirative inchise pentru drenajul flap-urilor tegumentare cu preventia limfocelului si a seroamelor.
Limfodisectia radicala ilioinghinala
Se face dupa 6 saptamani de la excizia tumorii peniene primare fiind necesara disparitiei componentei inflamatorii a adenopatiei.
Pregatirea preoperatorie consta in: pregatirea colonului, ciorapi elastici si antibioterapie.
Pacientul este pozitionat cu coapsa respectiva usor abdusa si rotata extern. Daca este necesar se va utiliza suport pentru genunchiul flectat.
Se va practica drenaj uretro-vezical, iar scrotul va fi izolat, exclus din campul operator.
S-au descris o serie de diferite tipuri de incizii pentru ganglionii inghinali.
Pentru cazurile ce necesita disectie bilaterala pentru ganglionii inghinali profunzi si superficiali, se va utiliza o incizie oblica sau eliptica sub si paralela cu ligamentul inghinal. Pentru disectia ilio-obturatorie bilaterala se asociaza incizia mediana subombilicala. Aceste incizii sunt utilizate cel mai frecvent pentru ca reduc problemele de necroza tegumentara.
Disectia inghino-femurala este realizata printr-o incizie oblic eliptica centrata de jonctiunea safeno-femurala cu baza la nivelul triunghiului femural. Dimensiunile inciziei sunt determinate de dimensiunile pacientului si ale tesutului adipos precum si de adenopatie. Incizia va fi planificata sa ridice tesut indemn periferic adenopatiei tumorale si simultan sa excizeze tegumentul cu risc major de devitalizare.
Incizia va incepe de la spina iliaca antero-superioara catre tuberculul pubian, paralel cu ligamentul inghinal pe o distanta de 4-6 cm.
Tesutul adipos si areolar va fi disecat de la aponevroza muschiului oblic extern si cordonul spermatic, pana la marginea inferioara a ligamentului inghinal. Unghiul inferior al expunerii inghino-femurale este la nivelul varfului triunghiului femural unde va fi identificata si divizata vena safena mare.
Disectia merge in profunzime sub fascia ce acopera muschiul croitor in lateral si muschiul adductor medial. La varful triunghiului femural vor fi identificate artera femurala si vena femurala, iar disectia va fi continuata superior, de-a lungul vaselor femurale. Vena safena este sectionata la nivelul jonctiunii safeno-femurale, iar disectia este continuata superior pana ce se realizeaza continuitatea cu disectia pelvina la nivelul canalului femural. Vor fi disecate vasele femurale lateral, anterior si medial dar nu vor fi scheletonizate.
Dupa ce triunghiul femural este disecat, muschiul croitor va fi mobilizat din originea sa (SIAS) si va fi transpus fie rotit medial pentru acoperirea vaselor femurale. Originea sa va fi suturata superior la ligamentul inghinal. Canalul femural va fi inchis prin sutura ligamentului Poupart la ligamentul Cooper fara a diminua lumenul venei iliace externe. Inchiderea plagii se face de obicei fara mobilizari tegumentare.
Limfodisectia pelvina se va realiza prin talie hipogastrica. Pentru disectia unilaterala exista trei rute de acces mai frecvent utilizate printr-o incizie unica, oblica:
a) Ligamentul inghinal poate fi incizat vertical deasupra vaselor sau la nivelul spinei iliace antero-superioare.
b) Alt abord consta in incizia fasciei muschiului oblic extern, reflexia craniala a cordonului spermatic incizia planseului canalului inghinal, de la nivelul orificiului inghinal la nivelul tuberculului pubian, cu ligatura vaselor epigastrice inferioare. Aceasta manevra permite acces larg pelvin si retroperitoneal.
c) Abordul preferat consta in incizia musculaturii abdominale anterioare la 4-5 cm deasupra si paralel cu ligamentul inghinal, cu mobilizarea mediala a peritoneului.
Limfodisectia pelvina include: ganglionii iliaci comuni distali, iliaci externi si obturatori.
Piesa de rezectie va fi exteriorizata prin canalul femural. Alternativa o constituie grupele ganglionare separate: pelvin, respectiv inghinale.
Se utilizeaza drenaje aspirative inchise. Se utilizeaza lambouri scrotale, miocutane in cazul defectelor tegumentare mari.
Pentru minimalizarea limfedemelor in perioada postoperatorie precoce se utilizeaza: ciorapi compresivi si pozitia ridicata a membrelor inferioare. Anticoagulantele postoperator sunt obligatorii.
Terapiile combinate utilizand chimioterapie plus chirurgie sau radioterapie au fost utilizate cu rezultate incurajatoare in tratamentul carcinomului cu celule scuamoase cu localizare laringiana si la nivelul anusului. Strategii similare au fost utilizate pentru a diminua problemele estetice si functionale aparute dupa amputatia peniana in cazuri selectionate. S-a raportat tratamentul cu succes a 2 cazuri de carcinom scuamos al penisului utilizand terapii combinate: laser, radioterapie si chimioterapie cu peplomicina.
Un studiu preliminar de tratament cu alfa-interferon combinat cu retinoid-etretinat aplicat unui grup de pacienti cu carcinom scuamos cu diferite localizari (inclusiv peniana) au aratat o activitate moderata impotriva acestor tipuri de tumori sugerand ca terapiile combinate ce includ retinoizi pot avea rol in tratamentul tumorilor peniene in stadiul metastatic.
Modalitatile terapeutice combinate-chirurgie, radioterapie, chimioterapie au fost utilizate cu oarecare succes in conversia tumorilor din stadiul nerezecabil la prima prezentare la stadiul potential rezecabil.
Se aduce coapsa in abductie si rotatie externa si se plaseaza o mica pernita sub genunchi. Se ancoreaza piciorul de gamba contralaterala. Se pune un ciorap elastic pana la genunchi; dupa operatie se extinde pana la nivelul coapsei. Se drapeaza si se expune ombilicul, tuberculul pubic, spina iliaca antero-superioara si coapsa anterioara. Se recomanda insertia unui cateter de silicon cu balon 18 Ch prin bontul penian. Se sutureaza scrotul la coapsa contralaterala. Se marcheaza pe piele tesutul ce va fi excizat cu un instrument de marcat. Se plaseaza o linie la 1 cm sub si paralela cu ligamentul inghinal, incepand de la tuberculul pubic si pana la 12 cm lateral. Se traseaza o linie perpendiculara de 20 cm medial si una de 15 cm lateral si se inchide cadranul.


a. b.
Figura 37. Pozitia pacientului: membrele pelvine in flexie si rotatie externa.
a) schema anatomica; b) imagine preoperatorie.
Se fac lambouri pe pielea deasupra si dedesubtul marginilor marcate, lasandu-le adecvat acoperite de 2-3 cm de fascie Camper impreuna cu propria-i grasime subcutana. Se folosesc carlige de piele, suturi statice si retractoare. Se manuiesc lambourile cu grija si se tin acoperite cu bureti umezi de apa sarata. Se mobilizeaza catre marginile premarcate dar nu mai mult. Daca tumora intereseaza si pielea se excizeaza in bloc.

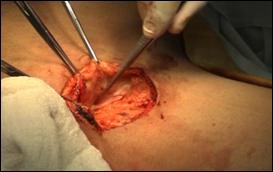
a. b.
Figura 38. Crearea lambourilor cutanate acoperite de fascie Camper.
a) schema anatomica; b) imagine intraoperatorie.
Se incepe de la marginea superioara a inciziei sa se ajunga la aponevroza muschiului oblic extern si se "curata" in jos peste ligamentul inghinal catre fascia lata a coapsei.
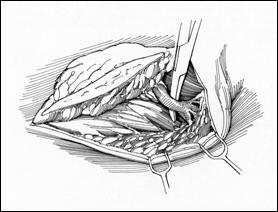 Incizia fasciei lata se face chiar sub
ligamentul inghinal de-a lungul marginii sale laterale, peste muschiul
croitor, disecand tesutul dintre pense si ligaturand-o cu fire
absorbabile fine. Se evita scurgerea de limfa.
Incizia fasciei lata se face chiar sub
ligamentul inghinal de-a lungul marginii sale laterale, peste muschiul
croitor, disecand tesutul dintre pense si ligaturand-o cu fire
absorbabile fine. Se evita scurgerea de limfa.
Se elibereaza marginile laterale si mediale ale masei limfoganglionare prin disectie si ligaturare. Cand se ajunge infero-medial la vena safena mare, se diseca in jurul ei, dar ea se pastreaza pentru a se reduce edemul postoperator al gambei.
a.
 In
cazul in care adenopatia este voluminoasa, prezervarea venei safene nu
trebuie sa reprezinte un obstacol chirurgical, ea fiind sacrificata
ori de cate ori conditiile locale o ce, pentru a respecta radicalitatea
interventiei chirurgicale.
In
cazul in care adenopatia este voluminoasa, prezervarea venei safene nu
trebuie sa reprezinte un obstacol chirurgical, ea fiind sacrificata
ori de cate ori conditiile locale o ce, pentru a respecta radicalitatea
interventiei chirurgicale.
Se mobilizeaza masa prin disectie din lateral inspre medial, peste ramurile nervului femural si apoi peste teaca femurala. Se pastreaza nervii motori, dar se sacrifica nervii cutanati si se diseca acele ramuri ale sistemului vascular femural ce iriga tesutul subcutanat.
Figura 39. a) Izolarea venei safene
mari pe lasou (schema operatorie); b,c)
izolarea venei safene mari la varful triunghiului femural si la
nivelul jonctiunii safeno-femurale.

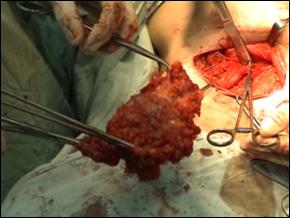
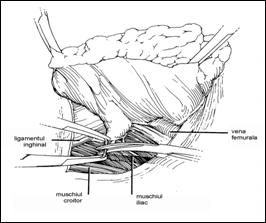
Figura 40. a,b. Se mobilizeaza fascia profunda medial de adductori catre teaca femurala si se excizeaza fascia.
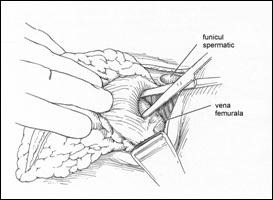
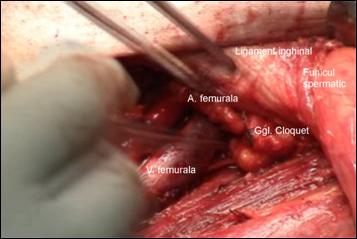
a .
b.
Figura 41. Excizia tesutului limfatic medial de artera femurala.
a) schema anatomica; b) imagine intraoperatorie.
Se scheletizeaza vascularizatia femurala medial si anterior in trigonul femural.
Se evita disectia lateral de artera femurala, sub fosa ovala dar se ligatureaza toate ramurile, in asa fel incat sa se elibereze masa nodala inghinala profunda.
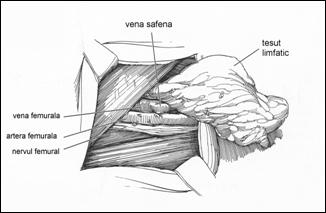
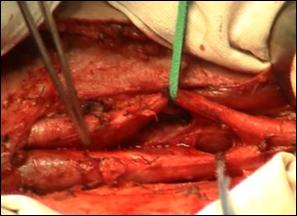
b.
a.
a. b.
Figura 42. a) indepartarea masei ganglionare inghinofemurale profunde - schema anatomica;
b) vasele femurale disecate si izolate pe lasou - aspect intraoperator.
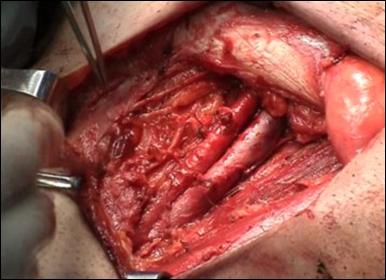
Figura 43. Aspect intraoperator final dupa limfodisectia radicala inghino-femurala

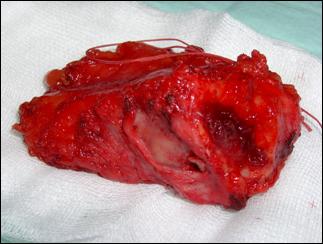
Figura 44. Piese de limfodisectie inghino-femurala profunda.
Limfodisectia ilio-obturatorie

Variantele de abord:
ilio-inghinal
median
(talie hipogastrica).
Se incizeaza si se diseca fascia oblica externa la aproximativ 3 cm deasupra ligamentului inghinal in directia fibrelor sale pentru marirea plagii operatorii. Se deschide muschiul oblic si fascia transversala.
Figura 45. Incizia aponevrozei
oblicului extern - schema
anatomica
Se diseca profund si lateral, expunandu-se peritoneul, care este separat de peretele pelvin lateral. Ureterul va urca cu peritoneul; el marcheaza limita superioara a disectiei unde se incruciseaza cu bifurcatia arterei iliace comune. Se incepe disectia iliaca de sus in jos.
Se identifica nervul genitor-femural lateral de vasele iliace si se diseca fascia chiar medial de el, reflectand-o lateral de pe muschiul psoas. Pentru lantul iliac extern se diseca artera iliaca externa medial, iar apoi se diseca intre artera si muschi. Apoi se trece peste vena iliaca translatand vasele epigastrice inferioare din nou catre limita inferioara a disectiei.
Se excizeaza ganglionii limfatici localizati la bifurcatia iliacei comune. Pentru lantul limfatic obturator, se retrage vena iliaca externa pentru a-i se curata suprafata, expunandu-se muschiul obturator extern. Se desface planul vecin muschiului, expunandu-se venele obturatoare, care se pot rupe usor provocand o sangerare greu de controlat.
Se localizeaza nervul obturator, la emergenta de sub marginea mediala a muschiului psoas, trecand pe sub vasele iliace langa bifurcatia venei iliace comune, se diseca si se tractioneaza medial.
Tesutul limfoganglionar se diseca sub forma de cordon si se trece prin canalul femural, sau se diseca si se trimite la anatomie patologica separat. Se eticheteaza componentele pelvine si inghinale pentru identificare.

a.
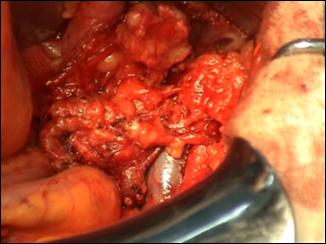
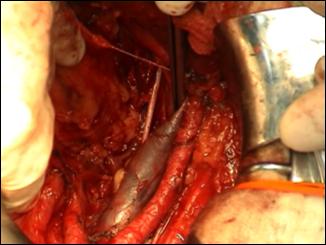
b. c.
Figura 46. Limfodisectie ilio-obturatorie.
a) schema anatomica; b,c) aspecte intraoperatorii (inainte si dupa indepartarea tesutului limfoganglionar din fosa obturatorie si de pe vasele iliace
In cazul limfodisectiei ilio-obturatorii bilaterale, abordul este printr-o incizie abdominala mediana subombilicala. Apoi se fac cele doua incizii inghinale sub si paralel cu ligamentul inghinal pentru disectia inghino-femurala. Artera femurala palpabila va fi la mijlocul liniei de incizie inghinala.
Reconstructia inghinala dupa limfodisectie
Se diseca muschiul croitor la nivelul insertiei pe spina iliaca anterioara. Se plaseaza pe nervul femural si vase.
Se sutureaza la reflectarea ligamentului inghinal, fixandu-l lateral.
Se verifica marginile pielii, in special cea inferioara si se excizeaza toate marginile neviabile.
Daca este necesar, se aplica o grefa de piele.
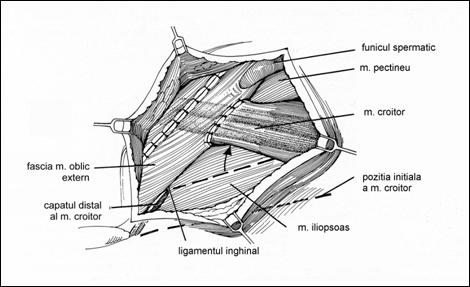
Figura 47 Acoperirea vaselor femurale prin mobilizarea muschiului croitor din originea sa si
transpozitia sa mediala
- schema anatomica.
Se insereaza tuburile de dren prin zonele nedisecate, punandu-le pe ambele parti ale muschiului croitor. Se inchide pielea cu fire subcuticulare absorbabile. Se aplica tampoane dezinfectante, dar nu comprese. Se ridica ciorapul elastic la nivelul coapsei. Se continua cu antibiotice.
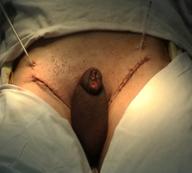

Figura 48. Plasarea tuburilor de dren.
a) schema anatomica; b,c) imagini postoperatorii - se observa plasarea tuburilor de dren.
Schimbarile in tehnica limfodisectiei si inciziile utilizate au limitat complicatiile descrise anterior dupa astfel de proceduri. Dovedirea faptului ca limfaticele tegumentare nu sunt implicate in diseminarea neoplazica si faptul ca limfodisectia este extinsa sub fascia Scarpa au dus la diminuarea leziunilor tegumentare. Transpozitia muschiului Sartorius deasupra vaselor femurale a minimalizat incidenta trombozelor si eroziunilor vasculare.
Majoritatea problemelor de plaga sunt secundare pierderilor tegumentare la nivelul marginilor plagii.
Aceste probleme tegumentare apar deoarece vascularizatia tegumentara a membrelor inferioare se face prin vase cu distributie musculo-cutanata sau fascio-cutanata. Cu disectia cutanata fara a ridica si muschiul sau fascia corespondenta lambourile cutanate restante raman cu circulatia de vecinatate.
Transa superioara reprezinta zona de tranzitie intre teritoriul vascular cuticular al arterelor iliace circumflexe si teritoriile vasculare musculo-cutanate ale coapsei.
Extensia inferioara a disectiei este clar in teritoriu vascular musculo-cutan si daca este agresiva creaza un lambou ce este deasupra posibilitatilor de vascularizatie prin plexul dermal. In majoritatea cazurilor in aceste situatii numai o mica zona superficiala de tegument se necrozeaza astfel incat aceste arii pot fi usor acoperite de grefe tegumentare. In cazurile cu pierderi tegumentare substantiale este necesar transfer tisular. O serie de lambouri locale sunt disponibile pentru transpozitie. Lambourile musculo-cutanate de gracilis sunt usor transpozabile la nivelul defectului inghinal.
In cazuri cu pierderi tegumentare si mai importante se folosesc lambouri de tensor fascia lata, lambouri musculo-cutane din dreptul abdominal ipsi- sau contralateral precum si lambouri omentale.
Radioterapia regiunii inghinale
Performantele radioterapiei primare in tratamentul regiunii inghinale sunt reduse de incertitudinea rezultata din lipsa de acuratete a stadializarii clinice si frecvent, prin lipsa de confirmare histologica a metastazelor ganglionare.
Alta rezerva a tratamentului metastazelor ganglionare inghinale este ca, regiunea inghinala nu tolereaza doze mari, putand rezulta necroze si ulceratii ale pielii.
Adenopatiile inflamatorii reduc eficacitatea radioterapiei si exacerbeaza complicatiile.
Grasimea perilimfatica,
ce adesea inconjoara ganglionii, poate actiona ca o bariera
protectoare impotriva unei radioterapii efective a depozitelor metastatice
ganglionare. Informatiile privind folosirea radioterapiei ca prima
modalitate de tratament in cancerul penian vin in special din Europa si
Rolul adjuvant sau terapeutic al radioterapiei este controversat. Chiar daca metastazele sunt documentate prin biopsie ganglionara, eficacitatea unei radioterapii ulterioare este imposibil de evaluat deoarece biopsia ar fi putut indeparta tot tesutul tumoral
Radioterapia pentru metastazele ganglionare documentate prin examinare histologica a fost comparata cu chirurgia.
O rata de 50% supravietuire la 5 ani a fost observata la grupul celor operati si una de 25% la cei iradiati. Alte studii au relatat ca radioterapia inghinala nu s-a dovedit a fi efectiv terapeutica.
Mai multe centre scandinave au efectuat radioterapie atat tumorii primare, cat si ganglionilor inghinali in toate cazurile de cancer penian; limfadenectomia se practica in continuare daca persista ganglioni palpabili sau apar ulterior.
Murrel si Williams (1965) au gasit ca din 11 pacienti ce au fost iradiati in zona inghinala fara a fi prezentat anterior ganglioni palpabili, 3 au dezvoltat metastaze ganglionare. Aceste procentaje foarte strans apropiate ale incidentei metastazelor subclinice ce se intalnesc prin limfodisectia efectuata atunci cand examinarea clinica este normala, sugereaza ca radioterapia nu influenteaza evolutia bolii. Mai mult, datorita modificarilor tisulare dupa iradierea inghinala, evaluarea clinica a regiunii inghinale este dificila, iar complicatiile limfodisectiei dupa radioterapie pot fi semnificative.
Radioterapia poate fi indicata la pacientii cu ganglioni inghinali ulcerati, fixati, inoperabili. in unele cazuri, iradierea zonei inghinale este bine tolerata, poate rezulta o ameliorare semnificativa si poate amana pentru o perioada prelungita complicatiile locale.
In concluzie, radioterapia regiunii inghinale nu este la fel de eficace terapeutic ca limfodisectia, dar poate fi folositoare pentru ameliorarea bolii (scop paleativ) in situatiile cu ganglioni inoperabili. S-a optat pentru a nu combina radioterapia postoperatorie cu limfadenectomia, dar altii au utilizat combinatia aceasta (Engelstad).
Chimiotera
Datorita relativei raritati a carcinoamelor peniene, experienta folosirii chimioterapiei este limitata. Folosirea topicelor cu 5-FU in leziunile superficiale si precanceroase a fost deja discutata.
5-FU a fost folosit ca perfuzie intravenoasa continua la un numar limitat de pacienti.
Alte trei chimioterapice folosite sunt: Cisplatin, Bleomicin si Methotrexat.
Experienta cu chimioterapia combinata ramane limitata.
Cisplatin ca unic chimioterapic si-a demonstrat eficacitatea in carcinoamele scuamoase ale capului si gatului si in alte localizari, studii separate relateaza folosirea lui in cancerul penian.
Doza utilizata este de 70-120 mg/m2 la fiecare 21 de zile.
In combinatie cu radioterapia, doza de Cisplatin este scazuta (50 mg/m2).
Bleomicina parea a fi foarte eficace in tratamentul cancerului penian si cancerului scrotal.
Methotrexatul a produs raspuns partial la 8 din 13 pacienti (61%) tratati la Memorial Sloan Kettring C. C.
Combinatia Vincristin cu Bleomicin si Methotrexat (VBM) a fost administrata in 12 cure saptamanale la 17 pacienti la Milan National Tumor Institute atat ca program terapeutic neoadjuvant (5 pacienti), cat si postoperator (12 pacienti). Pacientii tratati cu combinatia VBM, ca terapie adjuvanta, aveau boala avansata (risc inalt): 9 prezentau dezvoltare tumorala extraganglionara, 5 aveau invazie ganglionara pelvina si 5 metastaze ganglionare bilaterale. La urmarirea dupa tratament de 18-102 luni, a aparut doar o recidiva. Datele din acest centru au confirmat mai departe valoarea chimioterapiei adjuvante. 82 % din 25 de pacienti cu ganglioni pozitivi care au primit polichimioterapie (VBM) adjuvanta au supravietuit 5 ani, comparativ cu 37 % din 31 de pacienti cu ganglioni pozitivi tratati numai chirurgical.
Combinatia Methotrexat cu Bleomicin si Cisplatin (MBP) a fost administrata la 14 barbati cu cancer scuamos metastatic al tractului genital. La 12 pacienti tumora era localizata la nivelul penisului. La mai multi pacienti s-a administrat intra-arterial Bleomicin si Cisplatin. Rata de raspuns totala a fost de 72 % (14% raspuns complet, 57% raspuns partial), desi durata medie a fost doar de 6 luni.
Corral si col. (1998) raporteaza informatii suplimentare cu acest regim in faza a doua de studiu. Din 21 de pacienti evaluabili cu carcinom scuamos penian, 12 (57%) manifestau un raspuns obiectiv. Asa cum am amintit, durata de raspuns a fost scurta. Supravietuirea medie totala a fost 11 luni, supravietuirea celor ce au raspuns la acest tratament fata de cei ce n-au raspuns fiind aproape semnificativa statistic. Mai important, totusi, la pacientii redeveniti fara boala, numai prin chimioterapie sau chimioterapie urmata de rezectie chirurgicala sau radioterapie (1 caz), media de supravietuire a fost de 34 de luni.
Prin urmare, o abordare multimodala agresiva pentru obtinerea statutului de pacient fara boala poate fi importanta in cancerele peniene avansate.
Southwest O.G. relateaza datele studierii unui regim MBP ce foloseste o doza totala redusa a celor 3 agenti. Haas si col. (1999) administreaza MBP la 45 pacienti cu tumora peniana avansata local sau metastaze, proveniti din 31 de institutii diferite. Au fost 5 raspunsuri complete si 8 raspunsuri partiale printre cei 40 de pacienti evaluati (32,5% rata de raspuns). Toxicitatea a fost foarte ridicata, incluzand 5 decese legate de tratament. Desi regimul MBP poate fi asociat cu raspuns semnificativ, toxicitatea poate fi semnificativa, in special cand se administreaza in afara locurilor specializate.
VBM a fost folosit de asemenea ca neoadjuvant, cu raspuns partial relatat la 3 din 5 pacienti cu metastaze ganglionare extrem de mari (6-11 cm). Acesti 3 pacienti au fost ulterior complet rezecati si au fost fara tumora la intervale variind intre 20-72 de luni. In alt studiu cu terapie neoadjuvanta, 4 pacienti cu tumora stadiul 3 au fost tratati cu o combinatie de cisplatin si 5-FU, apoi rezecati. Doi pacienti au fost gasiti la specimenul limfadenectomie fara tumora reziduala si boala n-a mai aparut pe o perioada variind intre 6 si 40 de luni dupa chirurgie la vreun pacient.
In concluzie, chimioterapia poate induce raspuns in cancerul penian metastatic. Aceste raspunsuri au, in general, un caracter partial si o durata scurta. In viitor, tratamentul optim va folosi, cel mai probabil chimioterapia intr-un abord multidisciplinar ce include chirurgie si probabil radioterapie pentru a obtine statusul disease-free.
Raritatea carcinomului in SUA face
dificila efectuarea trialurilor de faza a II-a si a III-a pentru
chimioterapie eficace. Aceste informatii trebuie sa vina din
trialuri efectuate in America de Sud, Africa sau
1). terapie neoadjuvanta in stadiul 3;
2). terapie adjuvanta cand evaluarea anatomo-patologica a ganglionilor releva metastaze ganglionare extinse sau metastaze ganglionare ce reprezinta factori predictivi pentru scaderea supravietuirii si
3). chimioterapie paleativa la pacientii cu tumori locale inoperabile sau metastaze la distanta.
Tumorile maligne cu originea la nivel glandular, preputial sau penian raman localizate pe o perioada indelungata. Cand apar metastazele, acestea urmeaza un patern clar: primii invadati sunt ganglionii inghinali si ulterior cei pelvini.
O istorie naturala favorabila, permite tratamentul chirurgical al majoritatii pacientilor cu cancere peniene incluzand si pe cei ce prezinta metastaze inghinale.
Protocolul de urmarire a tumorilor peniene
(conform recomandarilor EAU)
Tumora primara - Terapie conservatoare
Examen fizic
primii 2 ani la 2 luni
al 3-lea an la 3 luni
al 4-lea si al 5-lea an la 6 luni.
- Amputatr partiala / totala
Examen fizic
primii 2 ani la 4 luni
al 3-lea an la 6 luni
al 4-lea si al 5-lea an la 12 luni.
Lanturile ganglionare - Supraveghere
Examen fizic
Citologie / biopsie in caz de suspiciune
primii 2 ani la 2 luni
al 3-lea an la 3 luni
al 4-lea si al 5-lea an la 6 luni.
- Limfodisectie (pN0)
Examen fizic
primii 2 ani la 4 luni
al 3-lea an la 6 luni
al 4-lea si al 5-lea an - nu este necesar.
- Limfodisectie (pN+)
Examen fizic /CT /Rx. toracic
primii 2 ani la 2-3 luni
al 3-lea an la 4- 6 luni
la 6-12 luni dupa aceea.
Tumorile maligne non-scuamoase
Melanoamele si carcinoamele cu celule bazale au incidenta scazuta la nivelul penisului, deoarece, probabil, tegumentul acestei zone este mai putin expus razelor solare. Tumorile maligne cu originea in structurile de sustinere ale penisului sunt de asemenea rare si includ combinatii de tumori musculare netede, striate, fibroase, vasculare sau cu originea in tesutul adipos.
Carcinomul cu celule bazale
Mai putin de 15 cazuri raportate au fost bine documentate. Tratamentul consta in excizia locala ce asigura virtual curabilitatea. Nu s-au raportat metastaze sau recurente locale.
O varianta benigna a carcinomului cu celule bazale - leziune precanceroase = fibroepiteliomul lui Pinkus - a fost raportata si are originea la nivelul tecii penisului. Diagnosticul se face prin biopsie excizionala ce este curativa
Melanomul
Mai putin de 1% din cancerul primar de penis este melanotic.
Melanomul se prezinta ca o papula placa sau ulceratie negru-albastrui sau brun-roscata localizata pe gland. Poate aparea frecvent si pe preput. Diagnosticul se face prin examenul histologic al biopsiilor.
Caracteristicile prognostice pentru melanoamele cu alte localizari (profunzimea invaziei si dimensiunile tumorii) nu se aplica leziunilor peniene (prin experienta redusa).
Leziunile metastatice s-au gasit la 60 % dintre cazuri. Metastazele hematogene se realizeaza prin vasele corpilor cavernosi.
Diseminarea limfatica se face prin permeatie la nivelul ganglionilor ilioinghinali. Modalitatea primara de tratament este chirurgical, iar chimio- si radioterapia s-au dovedit a avea caracter adjuvant sau paleativ.
Pentru stadiul 1 (leziune localizata fara metastaze) si stadiul 2 (metastaze la nivelul unei singure regiuni) excizia adecvata a tumorii primare prin amputatie partiala / totala a penisului impreuna cu limfodisectie ilioinghinala bilaterala ofera cele mai mari sanse de vindecare. Prognosticul acestor pacienti este sever existand foarte putini supravietuitori la 5 ani, datorita frecventei metastazelor dincolo de posibilitatile de excizie chirurgicala.
Sarcoamele
Tumorile primare mezenchimale ale penisului sunt foarte rare. Varsta pacientilor: 0-80 ani.
Semnele si simptomele la prezentare sunt: tumora subcutanata, durere peniana, tumefactie peniana, priapism si obstructie urinara.
S-au raportat prezenta sarcoamelor sub aspectul unei placi Peyronie. Incidenta si simptomatologia sarcoamelor si tumorilor benigne ale penisului este similara.
Leziunile maligne s-au descris mai frecvent la nivelul proximal al tecii penisului fata de cele benigne situate la nivel distal.
Cele mai frecvente leziuni sunt cele cu origine vasculara (hemangioepitelioame) urmate ca frecventa de cele cu origine nervoasa, miogenica sau fibroasa.
Sarcoamele raportate au fost: histiocitom fibros, sarcom epiteloid, osteosarcom.
Sarcoamele sunt clasificate ca superficiale cand isi au originea in structurile de sustinere tegumentare si profunde cu originea in structurile de sustinere ale corpilor cavernosi.
Excizia larga in suprafata si amputatia peniana partiala s-au utilizat in cazul tumorilor superficiale si amputatia totala pentru tumorile profunde. Recurentele locale sunt caracteristice sarcoamelor. Pentru a evita recurentele locale se recomanda amputatia totala chiar in cazul leziunilor superficiale.
Metastazele regionale sunt rare si daca adenopatia nu este palpabila nu se recomanda limfodisectie regionala. Metastazele la distanta sunt de asemenea rare, acest fapt justificand tratamentul local agresiv.
Nu se poate aprecia rolul radio - si chimioterapiei.
Sarcomul Kaposi - de obicei o manifestare cutanata a unei afectiuni generalizate limforeticulare - poate produce leziuni genitale, dar actual este asociata mult mai frecvent cu infectia HIV.
Boala Paget
Boala Paget a penisului este foarte rara. Microscopic se prezinta ca o zona bine delimitata eritematoasa, eczematoida ce nu poate fi clinic deosebita de eritroplazia Queyrat sau boala Bowen. Semnele clinice includ: disconfort local, prurit si ocazional secretie serosanghinolenta. Microscopic diagnosticul pozitiv este facut prin evidentierea celulelor mari, clare, rotunde sau ovale, cu nuclei hipocromatici (celule Paget).
Boala Paget este mult mai rara la nivelul penisului decat la nivelul scrotului sau perineului. Tumora creste tipic la nivelul tegumentului corpului penian la pacienti in decadele VI-VII de viata sub forma unor leziuni ulcerate, umede, rosietice.
Diagnosticul diferential clinic si microscopic include papuloza cu celule clare, diskeratoza pagetoida, metaplazia mucinoasa, boala Bowen, carcinomul urotelial uretral sau carcinoamele peniene cu diseminare pagetoida si melanomul malign.
Carcinomul bazocelular penian microscopic este similar celui tegumentar. Tumora poate fi multicentrica, nu metastazeaza si trebuie diferentiata de carcinomul scuamos bazaloid.
Foarte rare cazuri de carcinom cu celule Merkel au fost descrise la nivel penian.
Boala Paget poate fi mesagerul unui carcinom cu localizare profunda (celulele Paget urcand spre suprafata prin ductele epidermului).
La nivelul penisului neoplazia primara poate fi adenocarcinomul glandelor periuretrale sau carcinomul glandular. Boala Paget a penisului s-a descris ca poate aparea dupa radioterapia efectuata pentru carcinom tranzitional vezical.
Excizia completa a tegumentului si tesutului subcutanat reprezinta terapia de electie.
Daca adenopatia inghinala este prezenta se recomanda limfodisectie regionala. Pot aparea recidive la nivelul limitei zonei de excizie.
Carcinom adenoscuamos superficial / de suprafata
Este o tumora rara caracterizata prin prezenta elementelor histologice atat scuamoase cat si glandulare ce sunt independente de glandele uretrale.
Macroscopic se prezinta ca o masa tumorala exofitica mare (5-9 cm), ferma, alb-cenusie, ce implica glandul sau teaca peniana distala. Microscopic glandul contine mucina, prezinta reactie pozitiva pentru antigenul carcinoembrionar.
Tratamentul consta in excizia locala si dispensarizare.
Boli maligne limforeticulare
Bolile maligne lifoganglionare afecteaza rar penisul.
Leucemia poate infiltra corpul penian rezultand priapism. Cand se deceleaza infiltrarea limfomatoasa a penisului, o cercetare atenta a bolii sistemice este imperios necesara.
Daca leziunea peniana este intradevar tumora primara, poate fi utilizat tratamentul chimioterapic sistemic, care reprezinta cea mai eficienta modalitate terapeutica pentru boala locala, pentru metastazele oculte cat si in ceea ce priveste prezervarea formei si functiei.
Radioterapia locala in doza mica a fost de asemenea raportata ca metoda terapeutica de succes.
Metastaze
Leziuni metastatice peniene sunt rare. Doua sute de cazuri sunt mentionate in literatura. Organele cu leziuni neoplazice primare sunt: vezica urinara, prostata, rectul si mult mai rar rinichii si plamanii.
Caile de metastazare sunt:
extensie directa,
diseminare retrograda venoasa sau limfatica,
embolii arteriale.
Diagnosticul diferential: priapism idiopatic, ulceratii veneriene, tuberculoza, maladia Peyronie, tumori primare benigne sau maligne.
Metastazele peniene reprezinta o forma avansata a unei maladii virulente ce se manifesta de obicei rapid dupa diagnosticul si tratamentul leziunii primare.
Supravietuirea dupa prima prezentare este de obicei sub 2 ani.
Tratamentul chirurgical este rar indicat in cazul invaziei corpilor cavernosi proximali. Amputatia peniana indicata numai daca alte metode antalgice esueaza.
Tratamentul antalgic consta in sectiunea nervului dorsal.
Radio - si chimioterapia de regula nu sunt eficiente.
Bibliografie
Abeshouse
BS,
Abeshouse BS: Primary and secondary melanoma of the genitourinary tract. South Med J 1958;51:994-1006.
Abratt
RP,
Abratt RP: The treatment of bilateral ulcerated lymph node metastases from carcinoma of the penis. A case report. Cancer 1984;54:1720-1722.
Ackerman
Ahmed T, Sharloff R, Yagoda A: Sequential trials of methotrexate, cisplatin, bleomycin for penile cancer. J Urol 1984;132:465-468.
Akimoto T, Mitsuhashi N, Takahashi I, et al: Brachytherapy for penile cancer using silicon mold Oncology 1997;54:23-27.
Alani RM, Munger K: Human papillomaviruses and associated malignancies. J Clin Oncol 1998;16:330.
Cabanas R: An approach to the treatment of penile carcinoma. Cancer 1977;39:456-466.
Cabanas RM: Anatomy and biopsy of the sentinel lymph nodes. Urol Clin North Am 1992;19:267-276.
Carpiniello VL, Malloy TR, Sedlacek TV, Zderic SA: Results of carbon dioxide laser therapy and topical 5-fluorouracil treatment for subclinical condyloma found by magnified penile surface scanning. J Urol 1988;140:53-54.
Carpiniello VL, Schoenberg M, Malloy TR: Long-term followup of subclinical human papillomavirus infection treated with the carbon dioxide laser and intraurethral 5-fluorouracil: A treatment protocol. J Urol 1990;143:726-728.
Carpiniello VL, Schoenberg M: Laser treatment of condyloma and other external genital lesions. Semin Urol 1991;9:175-179.
Carpiniello VL, Zderic SA, Malloy TR, Sedlacek TV: Carbon dioxide laser therapy of subclinical condyloma found by magnified penile surface scanning. Urology 1987;29:608-610.
Catalona WJ: Modified inguinal lymphadenectomy for carcinoma of the penis with preservation of saphenous veins: Technique and preliminary results. J Urol 1988;140:306-310.
Catalona WJ: Role of lymphadenectomy in carcinoma of the penis. Urol Clin North Am 1980;7:785-792.
Chan WP, Chaing SS, Huang AH, Lin CN: Penile frenulum neurilemoma: A rare and unusual genitourinary tract tumor. J Urol 1993;144:136-137.
Chang TS,
Coetzee T: Condyloma acuminatum. South Afr J Surg 1977;15:75-80.
Colberg JW, Andriole GL, Catalona WJ: Long-term follow-up of men undergoing modified inguinal lymphadenectomy for carcinoma of the penis. Br J Urol 1997;79:54-57.
Cole LA, Helwig EB: Mucoid cysts of the penile skin. J Urol 1976;115:397-400.
Converse R. - Reconstructive Plastic Surgery, 1977
Copulsky J, Whitehead ED, Orkin LA: Condyloma acuminata in a three-year-old boy. Urology 1975;5:372-373
Cormack GC, Lamberty BG: The blood supply of thigh skin. Plast Reconstr Surg 1985;75:342-354.
Corral DA, Sella A,
Cubilla AL, Barreto J, Caballero C, et al: Pathologic features of epidermoid carcinoma of the penis. A prospective study of 66 cases. Am J Surg Path 1993;17:753-763. 172. Horenblas S, Jansen L, Meinhardt W, et al: Detection of occult metastasis in squamous cell carcinoma of the penis using a dynamic sentinel node procedure. J Urol 2000;163:100-104.
Horenblas S, Kroger R, Gallee MP, et al: Ultrasound in squamous cell carcinoma of the penis: A useful addition to clinical staging? A comparison of ultrasound with histopathology. Urology 1994;43:702-707.
Horenblas S, van Tinteren H, Delemarre JF, et al: Squamous cell carcinoma of the penis: Accuracy of tumor nodes and metastases classification system and role of lymphangiography, computerized tomography scan, and fine needle aspiration cytology. J Urol 1991;146:1279-1283.
Horenblas S, van Tinteren H, Delemarre JF, et al: Squamous cell carcinoma of the penis. III. Treatment of regional lymph nodes. J Urol 1993;149:492-497.
Horenblas S, van Tinteren H: Squamous cell carcinoma of the penis IV: Prognostic factors of survival: Analysis of tumor, nodes and metastasis classification system. J Urol 1994;151:1239-1243.
Hubbell CR, Rabin VR, Mora RG: Cancer of the skin in blacks. V. A review of 175 black patients with squamous cell carcinoma of the penis. J Am Acad Dermatol 1988;18(2 Pt 1):292-298.
Hueser JN, Pugh RP: Erythroplasia of Queyrat treated with topical 5-fluorouracil. J Urol 1969;102:595-597.
Iwasawa A, Kumamoto Y, Fujinaga K: Detection of human papillomavirus deoxyribonucleic acid in penile carcinoma by polymerase chain reaction and in situ hybridization. J Urol 1993;149:59-63.
Jaffe HW, Bregman DJ, Selik RM: Acquired
immunodeficiency syndrome in the
Jaffe HW,
Jurkiewicz Mathes - Krizek Plastic Surgery, 1990
McCarthy May - Littler Plastic Surgery, 1990
Pizzocaro G, Piva L, Bandieramonte G, Tana S: Up-to-date management of carcinoma of the penis. Eur Urology 1997;32:5-15.
Pizzocaro G, Piva L, Nicolai N: Improved management of nodal metastases of squamous cell carcinoma (SCC) of the penis. J Urol 1995;153:246A.
Pizzocaro G, Piva L: Adjuvant and neoadjuvant vincristine, bleomycin, and methotrexate for inguinal metastases from squamous cell carcinoma of the penis. Acta Oncologica 1988;27:823-824
Planz B, Brunner K, Kalem T, et al: Primary leiomyosarcoma of the epididymis and late recurrence on the penis. J Urol 1998;159:508
Plaut A, Kohn-Speyer AC: The carcinogenic action of smegma. Science 1947;105:391-392.
Pochedly C, Mehta A, Feingold E: Priapism with hyperacute stem-cell leukemia. NY State J Med 1974;74:540-541.
Pompeo AC, Mesquita JL, Junior WA, et al: Staged inguinal lymphadenectomy (SIL) for carcinoma of the penis (CP): 13 years prospective study of 50 patients. J Urol 1995;153:246A.
Poynter JH, Levy J: Balanitis xerotica obliterans: Effective treatment with topical and sublesional steroids. Br J Urol 1967;39:420-425.
Pratt RM, Ross RTA: Leiomyosarcoma of the penis. Br J Surg 1969;56:870-872.
Pratt-Thomas HR, Heins HC, Latham E, et al: The carcinogenic effect of human smegma: An experimental study. Cancer 1956;9:671-680.
Prescott RJ,
Pressman D, Rolnick D, Turbow B: Penile horn. Am J Surg 1962;104:640-641.
Puras A, Fortuno R, Gonzalez-Flores B,
Sotolongo A: Staging lymphadenectomy in the treatment of carcinoma of the
penis. Proc Kimbrough Urol Semin 1980;
Puras A, Gonzalez-Flores B, Fortuno R, et al: Treatment of carcinoma of the penis. Proc Kimbrough Urolog Semin 1978;12:143.
Puras-Baez A, Rivera-Herrera J, Miranda G, et al: Role of superficial inguinal lymphadenectomy in carcinoma of the penis. J Urol 1995;153:246A.
Queyrat L: Erythroplasie du gland. Soc Franc Dermatol Syphilol 1911;22:378.
Rasbridge SA, Parry JR: Angiosarcoma of the penis. Br J Urol 1989;63:440-441.
Raynal M, Chassagne D, Baillet F, Pierquin B: Endocuritherapy of penis cancer. Recent Results Cancer Res 1977;60:135-141.
Stein BS: Laser treatment of condylomata acuminata. J Urol 1986;136:593-594.
Stewart AL, Grieve RJ, Banerjee SS: Primary lymphoma of the penis. Eur J Surg Oncol 1985;11:179-181.389. Stone KM: Epidemiologic aspects of genital HPV infection. Clin Obstet Gynecol 1989;32:112-116.
Su CK, Shipley WU: Bowenoid papulosis: A benign lesion of the shaft of the penis misdiagnosed as squamous carcinoma. J Urol 1997;157:1361-1362.
Suchaud JP, Kantor G, Richaud P, et al: Curietherapie des cancers de la verge: Analyse d'une serie de 53 cas. J Urol (Paris) 1989;95:27-31.
Sufrin G, Huben R: Benign and malignant
lesions of the penis. In Gillenwater JY (ed): Adult and Pediatric Urology, 2nd
ed.
Summers JL: Pyogenic granuloma: An unusual complication of papaverine injection therapy for impotence. J Urol 1990;143:1227-1228.
Tannenbaum MH, Becker SW: Papillae of the corona of the glans penis. J Urol 1965;93:391-395.
Taylor GI, Corlett RJ, Boyd JB: The deep
inferior epigastric artery island rectus musculocutaneous flap. Strauch B,
Vasconez LO, Hall-Findlay EJ (eds): In Grabb's Encyclopedia of Flaps, vol 3.
Taylor GI, Corlett RJ, Boyd JB: The versatile deep inferior epigastric (inferior rectus abdominis) flap. Br J Plast Surg 1984;37:330-350.
Theodorescu D, Fair WR, Herr HW, et al: Expectant management of patients with T1-4NoMo penile cancer. J Urol 1995;153:247A.
Theodorescu D, Russo P, Zhang ZF, et al: Outcomes of initial surveillance of invasive squamous cell carcinoma of the penis and negative nodes. J Urol 1996;155:1626-1631.
Thomas JA, Small CS: Carcinoma of the penis in southern Indian. J Urol 1968;100:520-526.
Ubben K, Kryzek R, Ostrow R: Human papilloma virus DNA detected in two verrucous carcinomas. J Invest Dermatol 1979;22:195-210.
Uehling DT: Staging laparotomy for carcinoma of penis. J Urol 1973;110:213-215.
Union Internationale Contre le Cancer
(UICC): TNM Atlas: Illustrated Guide to the TNM/pTNM Classification of
Malignant Tumours, 3rd ed.
Vaeth JM, Green JP, Lowry RO: Radiation therapy of carcinoma of the penis. Am J Roentgenol Rad Ther Nucl Med 1970;108:130-135.
Vapnek JM, Hricak H, Carroll PR: Recent advances in imaging studies for staging of penile and urethral carcinoma. Urol Clin North Am 1992;19:257-266.
Whitmore WF: Tumors of the penis,
urethra, scrotum, and testes. In Campbell MF, Harrison HH (eds): Urology, 3rd
ed.
Wiener JS, Walther PJ: The association of oncogenic human papillomaviruses with urologic malignancy. Surg Oncol Clin North Am 1995;4:257-276.
Wishnow KI,
Yamashita T, Ogawa A: Ultrasound in penile cancer. Urol Radiol 1989;11:174-187.
Yeole BB, Jussawalla DJ: Descriptive
epidemiology of the cancers of male genital organs in greater

Vizualizari: 10497
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2024 . All rights reserved