| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Echilibre binare lichid-solid cu eutectic, ecuatiile Schrder-van Laar
Se cunosc numeroase sisteme care in faza lichida sunt miscibile dar sunt total nemiscibile in faza solida, ca de exemplu: oxiclorura de fosfor-piridina, clorura de iod-acid acetic, acid propionic-apa, cianamida-apa, acid acetic-apa, foramida-piridina, etc. Echilibrul izobar este descris de schema:
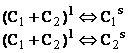
(8.45)
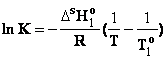
Se stabileste pentru fiecare forma analitica a
curbei de coexistenta dintre faza lichida si solidul corespunzator. Prin
aplicarea legii de distributie Nernst se obtin curbele de cristalizare ale lui
Schrder-van Laar. Daca sistemul este considerat ideal, avem:
(8.46) (8.47)
![]()
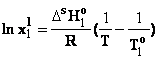
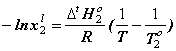
unde T este temperatura de solidificare a unei
solutii cu o compozitie data, iar To1 este temperatura de
solidificare a componentului C1 pur, iar DsHo1este
entalpia de topire. Pe baza datelor de mai sus se obtine ecuatia Schrder-van
Laar in raport cu componentul C1 din primul echilibru si respectiv cu componentul C2 din cel de-al
doilea echilibru prin rationamente analoge:
(8.48) (8.49)
In cazul sistemelor reale in ecuatiile de mai sus intervin coeficientii de
activitate termodinamica. Punctul eutectic se caracterizeaza printr-o anumita compozitie si temperatura pentru un sistem dat. Pozitia eutecticului este practic foarte putin influentata de presiune. S-a demonstrat ca la cresterea presiunii eutecticul se deplaseaza spre compozitii mai sarace in componentul 2.
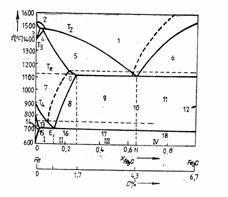
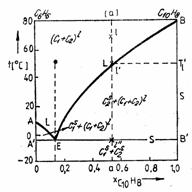
Figura 8.28 Diagrama de faza a sistemului Figura 8.29 Diagrama de faza a sistemului
benzen- naftalina (Fe-Fe3C) si (Fe-C)
Echilibrele lichid-solid apar in solutiile solide, in seria cristalelor mixte, pe un domeniu larg de compozitii, in functie de natura sistemului. Astfel pot apare mai multe zone lacunare de miscibilitate. Aspectul diagramelor lacunare este divers. Zonele de coexistenta ale lichidului bicomponent cu Cs1 sau cu Cs2 difera de la un sistem la altul. Se pot astfel studia amestecuri de azotati de potasiu si titan, silicati de magneziu si mangan, amestecuri de metale etc. Un exemplu mult studiat il constituie fontele, otelurile, aliajele in general.
Transformarile structurale ale constituientilor, in urma incalzirii sau racirii lente a aliajelor, se pot urmari pe diagramele de echilibru ca cea din figura 8.29. Prin linie continua este redata diagrama fier-cementita, iar punctat este redata diagrama fier-grafit. Aliajele cu grafit corespund echilibrului stabil, iar cele cu cementita corespund unei stari metastabile. Constituentii structurali ai otelurilor si ai fontelor albe (1,7-6,67%C) sunt pusi in evidenta pe diagrama Fe-Fe3C, iar cei ai fontelor cenusii fac parte din sistemul stabil, fier-grafit.
Echilibre de faza lichid-solid se pot evidentia si in cazul compusilor de aditie, care difera de situatia cristalelor mixte. Compusii de aditie sunt caracterizati printr-o structura reticulara proprie, care difera de cea a compusilor puri. Curba de echilibru reprezentata intr-o diagrama T=T(x), prezinta un maxim care corespunde compozitiei acestei combinatii. Compusii de aditie apartin unor clase diferite de corpuri, in functie de natura chimica a compusilor care ii genereaza.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 3003
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved