| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Echilibrul lichid-vapori al amestecului de doua lichide nemiscibile
Daca moleculele substantelor prezente intr-un amestec sunt diferite, interactiunile dintre ele slabesc, fiind predominante cele dintre moleculele de acelasi fel. In acest caz lichidele devin nemiscibile si curbele de condensare si fierbere vor avea forma celei prezentata in fig. 5.6. a amestecului clor-benzen-apa.
In punctul E vaporii sunt saturati in ambii componenti. Scaderea temperaturii duce la condensarea simultana si totala a ambilor componenti.
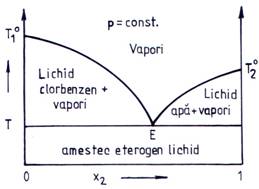
Fig. 5.6. Diagrama izobara a temperaturilor de fierbere si
condensare a amestecului clor-benzen-apa
Intr-un amestec de doua lichide nemiscibile, presiunea totala de vapori p este egala cu suma presiunilor de vapori ale componentilor puri la temperatura data.
![]() (5.105)
(5.105)
Amestecul alcatuit din doua lichide nemiscibile fierbe atunci cand presiunea de vapori totala egaleaza presiunea atmosferica. Datorita conditiei (5.105), temperatura de fierbere a amestecului este mai mica decat a celor doi componenti in parte. Acest fapt sta la baza antrenarii cu vapori. Procedeul este utilizat la distilarea unor lichide greu volatile (temperatura de fierbere ridicata) si nemiscibile cu apa sau alt lichid, care se descompun la temperatura proprie de fierbere astfel ca nu pot fi purificate prin distilarea obisnuita (in vid). Este cazul uleiurilor, substantelor aromatizante si esentelor din industria alimentara. Procedeul consta prin adaugarea la amestec a unui lichid nemiscibil cu cel in cauza, fierberea acestora si apoi prin condensare se separa in doua faze lichide.
Presupunand ca vaporii se comporta ideal, compozitia acestora se poate calcula din relatiile:
![]() (5.106)
(5.106)
![]() (5.107)
(5.107)
Proportia componentilor in distilatul obtinut la antrenare va fi aceeasi ca in vaporii din care provine. Pe baza relatiilor (5.106) si (5.107) se poate scrie:
![]() (5.108)
(5.108)
unde: n2, n1 = numarul de moli al celor doi componenti;
m2, m1 = masele celor doi componenti;
M2, M1 = masele moleculare ale celor doi componenti.
Din relatia (5.108) rezulta raportul de antrenare al maselor celor doi componenti in distilat:
![]() (5.109)
(5.109)
Se observa din relatia (5.109) ca raportul maselor celor doi componenti pentru un anumit raport al presiunilor de vapori este proportional cu raportul maselor moleculare.
Cu cat masa moleculara M1 a lichidului de antrenare este mai mica, cu atat mai mare va fi cantitatea m2 de produs antrenat. Din acest punct de vedere apa este un antrenant ideal.
Antrenarea cu vapori de apa se utilizeaza si la determinarea masei moleculare a lichidului greu volatil (M2). Din relatia (5.109) rezulta M2:
![]() (5.110)
(5.110)
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 2289
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2026 . All rights reserved