| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
RESURSE NATURALE SI PROTECTIA MEDIULUI
TEHNICIAN CHIMIST DE LABORATOR
TEMA DE PROIECT:
CUPRINS
ARGUMENTULpag. 4
CAPITOLUL 1. FENOLII
1.1. Prezentarea generala a fenolilor
1.2. Proprietatilile fenolilor
1.2.1. Proprietatiile fizice ale fenolilor
1.2.2. Proprietatiile chimice ale fenolilor
CAPITOLUL 2. OBTINEREA FENOLULUI
2.1. Prin topirea sarurilor acizilor sulfonici aromatici cu hidroxid
de sodiu
Prin substitutia nucleofila
Prin oxidarea alchilbenzenilor
Prin procedeul cumenului
Se obtine industrial din produsele rezultate la cocsificarea
carbunelui
CAPITOLUL 3. ANALIZA FENOLULUI
3.1. Metode de analiza
3.2. Determinari pentru fenol
CAPITOLUL 4. UTILIZARILE FENOLULUI
CAPITOLUL 5. SECURITATEA SI SANATATEA IN MUNCA PREVENIREA SI STINGEREA INCEDIILOR
CAPITOLUL 6. PROBLEME DE POLUARE PROTECTIA
MEDIULUI
CAPITOLUL 7. CONCLUZII
BIBLIOGRAFIE
ANEXE
ARGUMENTUL
Proiectul cu tema "Obtinerea fenolului si utilizarile sale" a fost elaborat in scopul
sustinerii examenului de certificare profesionala in invatamant liceal, nivel 3, profilul "Resurse naturale si protectia mediului", specializarea "Tehnician chimist de laborator".
Proiectul cuprinde 8 capitole, care au mai multe subcapitole
In primul capitol am prezentat generalitatile despre fenoli, proprietatile fizice si chimice ale acestora. Fenolul este un compus organic derivat din benzen prin inlocuirea unui atom de hidrogen cu o grupare hidroxil, avand numeroase utilizari in industrie.
In capitolul al doilea am indicat metodele de obtinere a fenolului. Acesta se poate obtine prin
Capitolul al treilea descrie analiza fenolului : metode de analiza si determinarile de laborator pentru stabilirea calitatii acestuia.
In capitolul al patrulea al proiectului sunt indicate utilizarile fenolului. Acesta este utilizat in diferite domenii cum ar fi: industria colorantilor, la fabricarea materialelor plastice, a medicamentelor, s.a.
In capitolul al cincilea si al saselea sunt prezentate masurile de SSM si respectiv, problemele de poluare si protectia mediului, la fabricarea si prelucrarea fenolului.
Capitolul 7 prezinta concluziile si in continuare am indicat bibliografia pe care am consultat-o pentru elaborarea proiectului.

CAPITOLUL 1.
FENOLII
1.1. Prezentarea generala a fenolilor
Fenolii sunt compusi hidroxilici in care gruparea functionala (-OH) este legata la un atom de carbon al unui nucleu benzenic (in stare de hibridizare sp2). Au formula generala :
Ar - OH
In fenoli, nucleul aromatic atrage electronii neparticipanti ai atomului de oxigen din grupa hidroxil (-OH), intarind legatura carbon-oxigen.
Consecinte:
Ø atomul de oxigen din grupa hidroxil (-OH) devine mai puternic legat de nucleu si grupa hidroxil nu poate fi inlocuita
Ø scade densitatea electronica a oxigenului si atomul de hidrogen este mai slab legat de el, hidrogenul este mai usor cedat ca proton (H+) explicand aciditatea mai mare a fenolilor fata de alcooli
Ø creste densitatea electronica la nucleu, ceea ce face ca fenolii sa dea
mai usor reactii de substitutie decat benzenul.
Denumirea fenolilor depinde de pozitia si tipul substituentilor in nucleu. Sunt utilizate nomenclatura rationala si sistematica. Astfel prezenta unei grupe hidroxil (-OH) in nucleul benzenic formeaza un alcool aromatic, care dupa nomenclatura traditionala se numeste fenol, iar dupa cea sistematica hidroxibenzen.
Formula fenoliilor este: C6H5-OH
Dupa numarul gruparilor hidroxil din molecula, fenolii se pot clasifica in:
a) Fenoli monohidroxilici
b) Fenoli polihidroxilici
Fenolii monohidroxilici au o singura grupare hidroxil (-OH) in molecula lor. Cel mai simplu fenol monohidroxilic este hidroxibenzenul C6H5-OH numit in mod obisnuit fenol iar omologul lui este hidroxitoluenul (CH3)C6H5-OH crezolul, la care se deosebeste trei izomeri dupa pozitia relativa a substituentilor la nucleul aromatic si nume: orto-crezol, mete-crezol, para-crezol.
Exemple de fenolii monohidroxilici:
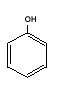
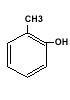
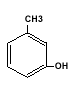
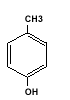
Fenolii polihidroxilici contin in molecula lor mai multe grupari hidroxil. Fenolii di si trihidroxilici derivand de la benzen, sunt substante solide, frumos cristalizate cu urmatoarele denumiri si puncte de topire:
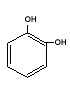
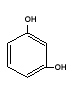
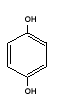
Metilfenolii sunt denumiti crezoli, iar dimetifenolii xilenoli. Uneori, fenolii sunt denumiti ca hidroxi-compusi, de exemplu:
oh oh cooh
oh
o-Crezol 2,6-Dimetifenol Acid p-hidroxibenzoic (2,6-Xilenol)
1.2. Propritatile fenolilor
Fenolii au atat proprietati fizice cat si chimice.
1.2.1. Proprietatile fizice ale fenolilor
Fenolii sunt substante solide, cristalizate, cu miros caracteristic patrunzator. Sunt putin solubili in apa, usor solubili in alcool, benzen etc.
Fenolul pur se prezinta sub forma de cristale incolore care in timp se oxideaza si se coloreaza in rosu. Fenolul este toxic si caustic (produce arsuri pe piele). Naftolii sunt inodori, greu solubili in apa. Sunt substante toxice si corozive.
Fenolii sunt substante solide la temperatura obisnuita. Sunt substante cristaline si incolore. Fenolii au caracter slab acid, ceea ce a condus la denumirea de acid feric pentru fenol. Au un miros patrunzator si neplacut. Fenolii sunt usor solubili in apa si solubili in dizolvanti organici.
Fenol - fisa tehnica
denumirie: Fenol
formula chimica: C6H6O sau C6H5OH
aspect: cristale albe, prin oxidare galbui portocalii
masa molara: 94,11 gmol−1
stare de agregare: solid
densitate: 1,06 gcm−3
punct de topire 40,9 C
punct de fierbere: 181,9 C
presiune vapori 0,2 hPa (20 C)
solubilitate buna in apa
Toxic -
Caustic


1.2.2. Proprietatile chimice ale fenolilor
Fenolii pot sa reactioneze in mai multe moduri si cu diferite substante.
a) Reactia fenolilor cu metalele
C6H5-OH + Na → C6H5-ONa + H2
Fenoxid de sodiu
b) Reactia fenolilor cu bazele
C6H5-OH + NaOH→ C6H5-ONa + H2O
Fenoxid de sodiu
c) Reactia fenolilor cu derivati halogenati (reactia de substitutie la nucleul aromatic)
|
|
+
CH3-Cl
|
|
|
d) Reactia de hidrogenare
C6H5-OH + 3H2
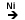 C6H11OH
C6H11OH
Ciclohexanol
e) Identificarea fenolilor (FeCl3)
C6H5-OH + FeCl3 → C6H5-OFeCl2 + HCl
f) Reactia cu HCl gazos
C6H5-OH + HCl → C6H5-Cl + H2O
Clorobenzen
g) Reactia de esterificare cu un alcool
C6H5-OH + HO-C2H5 → C6H5-O-C2H5 + H20
Alcool etilic Eter difenilic
h) Reactia de ardere a fenolului (fenolul aprins arde punand in libertate negru de fum)
C6H5-OH +O2 → 6C +3H2O
In concluzie fenolii pot da:
a) reactii determinate de nucleul benzenic(reactii asemanatoare cu benzenul)
OH OH
C6H5 - OH + Cl2 AlCl Cl + + HCl
Cl
OH OH
NO2
C6H5 - OH + HONO2 + + HOH
NO2
OH OH
CH3
C6H5 - OH + CH3 - Cl + + HOH
CH3
OH OH
S03H
C6H5 - OH + HOSO3H + + HOH
SO3H
b) reactii determinate de prezenta grupei hidroxil
- reactia cu NaOH
C6H5 - OH + NaOH C6H5 - ONa + ½ H2
- reactia de eterificare
C6H5 - ONa +R - X C6H5 - O - R + NaX
O proprietate importanta a fenolului este interactiunea cu aldehida formica si formarea rasinilor fenolformaldehidice:
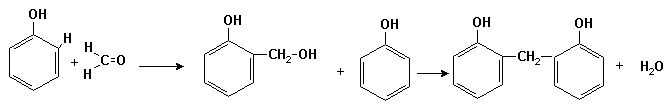
Acest proces prezinta o reactie de polimerizare-policondensare, care decurge mai adinc cu formarea unor polimeri - fenolformaldehidici.
c) Pentru fenol este caracteristica reactia de culoare cu clorura de Fe(III) - formarea unui compus de culoare violeta. Aceasta reactie se utilizeaza ca reactie de identificare a fenolului.
reactia fenolilor cu clorura ferica
fenol ---- coloratie violet
crezolii ------ coloratie albastra
hidrochinona ------ coloratie albastra
-naftolul ----- coloratie violet intensa
- naftolul ----- coloratie verde
CAPITOLUL 2.
OBTINEREA FENOLILOR
Fenolii se pot obtine prin mai multe procedee:
Prin topirea sarurilor acizilor sulfonici aromatici cu hidroxid de sodiu
(la 2500-3000C)
C6H5-S03Na + NaOH →C6H5-OH + Na2SO3 + H20
Benzen sulfonat Sulfat de
de sodiu sodiu
SO3Na ONa
(Topire alcalina)
Fenoxidul de sodiu rezultat este tratat cu un acid mai puternic decat fenolul (pentru a-l deplasa pe acesta din combinatii), acidul sulfuros. Rezulta pe langa fenol, bisulfit de sodiu care este folosit la transformarea acidului benzensulfonic in sare de sodiu si eliberarea de acid sulfuros care este refolosit.
O Na OH
(Descompunere)
Prin substitutia nucleofila a clorbenzenului cu grupa hidroxil folosind alcalii puternice si temperatura ridicata (intrucat clorbenzenul are o reactivitate scazuta).
Prin oxidarea alchilbenzenilor.
Industrial se aplica oxidarea cumenului (izopropilbenzenului) la hidroperoxid de cumen (cu aer la 120oC si 4 atm.) si descompunerea hidroperoxidului in acetona si fenol in prezenta acidului sulfuric (0,02-0,1%).
Prin procedeul cumenului
Oxidarea izopropilbenzenului
O - O - H
CH2 CH3 - CH - CH3 CH3 - C - CH3
C6H6 + + O2
CH - CH3
OH
H SO + CH3 - C - CH3
O
Se obtine industrial din produsele rezultate la cocsificarea carbunelui
Din gudronul de carbune prin distilare fractionata se obtin mai multe fractiuni care se titreaza cu hidroxid de sodiu.
C6H5-Cl + NaOH → C6H5-OH + NaCl
conditii: NaOH c=30%, 350C, 250 atm
Fenolul a fost izolat in 1837 din gudroanele rezultate la distilarea carbunilor, de catre Runge Astazi se mai obtine din gudroane, dar, in cantitati mari si prin sinteza. Este un produs incolor, solid, cristalizat sub forma de ace, cu miros specific. In contact cu aerul devine rosiatic datorita oxidarii.
Este toxic, in contact cu pielea produce arsuri. Se foloseste in cantitati mari la obtinerea fenoplastelor (prin condensare cu aldehida formica), a policaprolactamei a unor coloranti si medicamente (acid acetil salicilic).
Crezolii (orto, meta si para -metilfenolii) se separa tot din gudroane.
Actiunea bactericida creste la alchilfenoli cu cresterea lungimii catenei atingand un maxim pentru C5 dupa care scade din nou cu cresterea numarului de atomi de carbon din catena.
a-Naftolul si b-naftolul se gasesc, de asemenea, in gudroanele rezultate la carbonizarea carbunilor. Sunt foarte putin solubili in apa dar se dizolva in alcool si eter etilic. Se obtin si prin sinteza:
a-Naftolul prin hidroliza in mediu de acid sulfuric a a naftilaminei:
NH2 OH
b-Naftolul prin topirea alcalina a acidului b-naftalensulfonic.
SO3Na OH
+ NaOH + 2 Na 2SO3
b-Naftolul are actiune antihelmintica, este germicid si fungicid, mai puternic decat fenolul, dar se foloseste mai ales ca paraziticid.
CAPITOLUL 3.
ANALIZA FENOLULUI
Fenolul se intrebuinteaza in industria organica de sinteza, in fabricarea materialelor plastice si a fibrelor sintetice.
3.1. Metode de analiza
Fenolul antrenabil cu vapori de apa se poate determona prin metode volumetrice, colotimetrice sau cromatografice in functie de concentratia in care se gasesc in apa. Pentru concentratie peste 50 mg/l se aplica metoda volumetrica iar pentru concentratia sub 50 mg/l metoda colorimetrica sau cromatografica.
1. Reactia de culoare - este o reactie de recunoastere a fenolilor.(vezi proprietatile fenolilor)
Fenolul in prezenta FeCl - Naftolul in prezenta FeCl3
b- Naftolul in prezenta FeCl3 Crezoli si hidrochinona in prezenta de FeCl3
Obs. Culoarea se datoreste cationului Ar- OFe] 2+ si este diferita in functie de natura fenolului.

2. Metoda de analiza volumetrica a fenolului
Fenolii separati din apa prin antrenare cu vapori de apa, tratati cu brom, formeaza tribrom-fenoli. Bromul ramas in exces este titrat cu tiosulfat, dupa adaugare de iodura de potasiu.
Mod de lucru:
Intr-un vas de bromurare se iau 100ml distilat si 50 ml solutie bromat- bromura, se adauga 5 ml acid sulfuric (H2SO4) 1:3, se inchide imediat vasul, se agita puternic si se lasa o ora in repaus, la intuneric la temperatura camerei. Se introduc 10 ml solutie de KI, se la 5 minute, se scoate dopul vasului si se face titrare cu solutie de tiosulfat de sodiu (Na2S2O3) 0,1N.
3.2. Determinari pentru fenol
Fenolul este supus urmatoarelor determinari:
a. Reactii de identificare si conditii de puritate
b. Punctul de congelare
c. Continutul in fenol
d. Solubilitatea in apa
e. Continutul in substante nevolatile
f. Continutul in sulf
a. Reactii de identificare si conditii de puritate. Aceasta determinare se realizeaza cu ajutorul indicatorului metil-oranj cand solutia de fenol trebuie sa se coloreze in galben.
Mod de lucru:
Se separa o solutie limpede din 1 g fenol si 20 cm3apa. Fenolul continut in solutie se supune urmatoarelor reactii de identificare:
3cm3 de solutie se trateaza cu o picatura de FeCl3 pana apare o coloratie albastra-violeta.
3cm3 solutie se trateaza cu 5 cm3 apa de brom si se formeaza un precipitat alb.
5cm3 solutie se trateaza cu o picatura de metil-oranj (indicator) iar solutia trebuie sa se coloreze in galben. Prin aceasta reactie se determina limita de aciditate.
b. Punctul de congelare: Aceasta determinare se realizeaza cu ajutorul unui aparat pentru determinarea punctului de congelare care este format din 2 eprubete de sticla, o eprubeta care este prevazuta cu o flansa metalica, un pahar Berzelius si un termometru.
Mod de lucru:
Pentru aceasta determinare se intrebuinteaza o proba de analizat deshidratata. Astfel, intr-un balon prevazut cu un refrigerent cu aer, se distila 50 cm3 fenol, pana la obtinerea unei cantitati de 1cm3 condens. Se inlocuieste apoi refrigerentul cu un tub de CaCl2 si se raceste proba deshidratata.
Intr-o eprubeta se introduc 20 cm3 fenol lichid deshidratat si se inchide eprubeta cu un dop prevazut cu termometru si agitator. Daca fenolul a inceput sa cristalizeze, se incalzeste usor eprubeta.
Se introduce eprubeta cu fenol in aparat la o temperatura de 6-8 grade mai mica decat punctul de congelare al fenolului. Printr-o agitare constanta, se observa in fenolul racit treptat aparitia primelor cristale care duc la o tulbureala a lichidului. Apoi se intrerupe agitarea.
c. Continutul in fenol: se determina volumetric prin titrare. Fenolul reactioneaza cu bromul, deoarece solutia apoasa de brom nu este stabila, se foloseste o solutie de bromura-bromat, care pune bromul in libertate intr-o solutie acida in timpul titrarii.
Mod de lucru
Se cantareste 0,5 g fenol la balanta analitica, se dizolva cu apa distilata intr-un balon cotat de 250 cm3 si se completeaza cu apa pana la semn. Se trateaza 25 cm3 solutie cu 50 cm3 solutie bromura -bromat de potasiu (KBr-KBrO3) 0,1N, 10cm3 H2SO3 (reactiv), intr-un flacon cu dop rodat si se lasa in repaus 15 minute. Se adauga 2g KI (reactiv), dizolvata in 10 cm3 apa distilata, se agita, se lasa 10 minute la intuneric si se titreaza cu tiosulfat de sodiu(Na2S2O3)
0,1 N pana la decolorarea solutiei in prezenta amidonului ca indicator.
Au loc reactiile: KBrO3 + 5KBr + 6HCl → 3Br2 + 6KCl + 3H2O
Br2 + 2KI → 2KBr + I2
I2 + 2Na2S2O3 → 2NaI + Na2S2O6
d. Solubilitatea in apa se determina prin observarea solutiilor cu ochiul liber la lumina zilei. Determinarea este diferita, in functie de domeniul de utilizare si de calitatea fenolului intrebuintat.
Mod de lucru:
In cazul fenolului reactiv se cantaresc 2 g fenol la balanta analitica, se incalzeste pana la topire si se amesteca cu un volum egal de cloroform (CHCl3) pana se obtine un lichid limpede.
In cazul fenolului tehnic se cantaresc 5g fenol care se introduc intr-un cilindru gradat de 100 cm3 cu dop slefuit (rodat) sau intr-un balon cotat, in care se adauga 100cm3 apa distilata, avand temperatura de 200C si se agita pana la dizolvarea fenolului.
Trebuie sa se formeze o solutie clara, fara opalescenta.
e. Continutul in substante nevolatile:
Mod de lucru
Intr-o fiola de sticla cantarita in prealabil la balanta analitica, se cantaresc 5g fenol. Fiola se incalzeste pe baie de apa pana la disparitia mirosului de fenol si apoi se introduce in etuva la 1050C , timp de 30-40 minute.
Se raceste in exsicator care contine CaCl2 si apoi se cantareste. Se repeta operatia pana la o masa constanta.
Calcul:
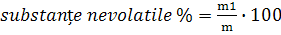
m = masa fenolului luat pentru determinare in g
m1= masa reziduului in g
f. Continutul in sulf: Analiza consta in determinarea cantitatii de iod corespunzatoare cantitatii de fenol si exprimarea acestuia in sulf. Aceasta se bazeaza pe faptul ca, combinatiile organice ala sulfului de tip R-SH (mercaptan) reactioneaza cu iodul, conform reactiei:
2R-SH + I2 → R2S2 + 2HI
Mod de lucru
Se cantaresc 5g fenol la balanta analitica intr-o fiola de cantarire si se aduc cantitativ intr-un pahar de titrare , de adauga 5 cm3 CH3COOH si se completeaza cu apa distilata pana la 100 cm3. Se lasa 5 minute , dupa care se adauga 0,5-1g KI, 1 cm3 amidon si se titreaza cu o solutie de I2 pana la aparitia culorii albastre.
CAPITOLUL 4.
UTILIZARILE FENOLULUI
Utilizarile fenolului
In 1865 fenolul a fost utilizat pentru prima data ca antiseptic la dezinfectia ranilor, dar din cauza caracterului iritant a fost inlocuit in chirurgie de alte antiseptice. Fenolul are un efect caustic asupra membranei celulei nervoase. Din cauza efectului bactericid se folosea ca dezinfectant, fiind folosit si la cultivarea plantelor producatoare de droguri ca erbicid.
Fenolul mai este folosit la producerea rasinilor artificiale precum bachelita care este un policondensat al fenolului si formaldehidei.
In timpul celui de al doilea razboi mondial, prinzionerii erau omorati in lagarele germane cu injectii intracardiace cu fenol. In tehnica microscopica se foloseste de asemenea formolul sau la conservarea organelor in anatomia patolgica. La constructiile de lemn se foloseste adezivul format din fenol-rezorcina-formaldehida.
Creolina, dezinfectant folosit in medicina - este un amestec de crezoli cu solutie de hidroxid
Lisolul folosit in medicina - este un amestec de crezoli in sapunuri obisnuite.
Creozotul un amestec de fenoli si crezoli - este folosit ca dezinfectant, la injectarea lemnului pentru a-l feri de putrezire. Conservarea carnii afumate se datoreste creozotului care se gaseste in fumul rezultat prin arderea lemnului
Fenolii sunt compusi cu abilitati anti-inflamatorii, anti-oxidante si anti-coagulante, si potrivit cercetatorilor spanioli, reprezinta cheia pentru reducerea riscului atacurilor de inima. Cantitati mari de fenoli se gasesc in uleiurile virgine si extravirgine de masline.

Se pare ca
in spatele efectelor miraculoase ale uleiurile de masline se afla o concentratie
ridicata a moleculelor de oxid nitric, al caror rol este sa dilate vasele de
sange, si un nivel redus de tensiune rezultat in urma oxidarii.
'Consumul alimentelor
bogate in fenoli imbunatateste sanatatea cardiovasculara si protejeaza
inima,' a concluzionat cercetatorul Francisco Perez Jimenez.
Fenolii sunt utilizati pentru producerea substantelor plastice policarbonate
(ex. sticle, cd-uri, casti), produse pentru igiena personala si a casei si a cosmeticilor. De asemenea fenolii sunt utilizati si pentru fabricarea hartiei, a lichidelor antigel si a lacurilor. Alte utilizari:
Fenolul - la fabricarea materialelor plastice (relon, bachelita), in industria medicamentelor, a antidaunatorilor, in industria colorantilor si a parfumurilor .
Crezolii sunt utilizati pentru obtinerea materialelor plastice de tipul bachelitelor si in industria explozivilor. Au actiune bactericida mai puternica decat fenolul, de aceea se folosesc ca antiseptici, mai ales sub forma de emulsie, cu o solutie de sapun in apa.
Naftolii se utilizeaza ca intermediari in industria colorantilor.
Hidrochinona este utilizata in tehnica fotografica si in industria colorantilor.
Pirogarol este folosit in dozarea oxigenului din amestecurile de gaze si ca revelator fotografic.
Utilizarea fenolului in tratamente de reintinerire a pielii.
Peelingul chimic este o tehnica neinvaziva ( nechirurgical) pentru a restaura o fata ridata , patati sau distrusa de soare, utilizand o solutie chimica care va indeparta straturile superficiale ale pielii. Noile celule ce se formeaza in timpul procesului de vindecare produc o suprafata a pielii mai neteda, mai intinsa, si cu aspect mai tanar.
Peelingul chimic poate fi utilizat pe toata fata sau in regiuni specifice, cum ar fi fruntea sau aria dinjurul gurii. Nu trebuie considerat un substitut pentru un lifting facial - nu elimina pielea lasata si in exces - dar multi oameni pot beneficia de ambele proceduri. Exista doua tipuri de solutii chimice utilizate in peeling: fenol si acid tricloracetic .
Peeling-ul cu fenol se utilizeaza pentru a trata riduri fine faciale, pete ale pielii cauzate de sarcina, anticonceptionale, boli virale, expunerea la soare, alte forme de distructii cronice ale pielii cauzate de soare incluzand si afectiuni precanceroase ale pielii. Pentru ca pateaza ariile tratate ale pielii fenolul este utilizat pentru peeling-ul intregii fete sau poate fi folosit pe arii limitate ale fetei pe o piele unde contrastul cu ariile netratate sa nu fie atat de evident.
Fenolul este utilizat exclusiv la fata. Daca se utilizeaza la gat sau in alta parte a corpului poate cauza cicatrici.

CAPITOLUL 5.
SECURITATEA SI SANATATEA IN MUNCA PREVENIREA SI STINGEREA INCEDIILOR
Masurile prin care se asigura supravegherea corespunzatoare a sanatatii lucratorilor in functie de riscurile privind securitatea si sanatatea in munca se stabilesc potrivit reglementarilor legale, a Legii securitatii si sanatatii in munca nr. 319/2006 .
In scopul asigurarii securitatii si sanatatii lucratorilor, trebuie sa se respecte masurile de S.S.M. :
TOXICITATEA FENOLULUI
Fenolul este un toxic protoplasmatic, care patrunde in interiorul celulei, prin solubilizarea lipidelor. Actioneaza asupra sistemului nervos central producand hipotermie si paralizia centrului vasomotor.
Contactul cu pielea:
Este un iritant puternic pentru piele. Local, fenolul exercita o actiune caustica asupra pielii provocand leziuni grave, albicioase, dureroase.
Gravitatea leziunilor este in functie de concentratia solutiei, timpul de contact si dimensiunea zonei de expunere. Solutiile diluate provoaca dermatite severe, mai ales la contact repetat.
Contactul cu ochii:
Este un iritant puternic pentru ochi. Patrunderea accidentala in ochi a fenolului, sau a solutiilor concentrate, provoaca o iritatie severa, care poate duce la distrugerea corneei.
Inhalare:
Inhalarea sub forma de vapori, in doze cronice, duce la iritarea cailor respiratorii si determina scleroza vaselor sanguine. .
Ingestia:
In caz de ingestie, produce efecte caustice asupra tubului digestiv, tulburari neurologice, cardiovasculare, hepatice, renale. Doza letala pentru om este de 10 g fenol.
FENOLUL este o substanta toxica si coroziva, emana vapori toxici, de aceea se va lua urmatoarele masuri de protectie:
purtati echipament de protectie: ochelari pentru protectia completa a ochilor; manusi; imbracaminte corespunzatoare de protectie; masca de protectie; aparat de respiratie.
fenolul se pastreaza numai in recipientul original, intr-un loc racoros si bine ventilat;
produsul nediluat nu trebuie utilizat intr-un spatiu inchis fara o buna ventilatie;
nu deversati fenolul in canalizare sau in mediu, duceti la un centru autorizat de colectare a deseurilor
pastrati containerele inchise atunci cand nu sunt utilizate si trebuie sa fie etichetate;
depozitati la temperatura ambianta ferit de soare si de umiditate sau alte deseuri;
conditiile de munca in spatii inchise trebuie bine aerisite;
nu inspirati vaporii/fumul.
IN CAZUL IN CARE:
la contactul cu ochii, se spala imediat cu multa apa si se consulta medical;
la contactul cu pielea, se spala imediat cu multa apa si sapun;
in caz de inghitire, a nu se provoca voma: se consulta imediat medicul si i se arata ambalajul (recipientul) sau eticheta .
CAPITOLUL 6.
PROBLEME DE POLUARE SI
PROTECTIA MEDIULUI
Fenolul polueaza aerul atmosferic, datorita utilizarii in cantitati mari in industrie, la obtinerea fenoplastelor, a colorantilor si a unor medicamente.
Pericolul fenolului activat de radiatiile ultraviolete ale soarelui, consta in provocarea de modificari patologice la plante.
Fenolul se intalneste in apele de suprafata sau subterane, unde ajung o data cu apele reziduuale industriale, provenite de la descompunerea pirogenetica a lemnului, de la fabricile de coloranti, materiale plastice, etc. De asemenea ei pot fi prezenti in apa ca urmare a descompunerii si putrefactiei organismelor vegetale.
Folosirea fenolilor este limitata doar pentru dezinfectia mediului (suprafete, aer). Nu este recomandata utilizarea lor pentru dezinfectia instrumentarului, datorita corozivitatii si nici utilizarea ca antiseptice, datorita toxicitatii.
Se folosesc, uneori, pentru dezinfectia instrumentarului utilizat in anatomia patologica si a echipamentelor contaminate cu bacilul tuberculozei, cand nu se poate folosi decontaminarea prin caldura.
Efectele toxice ale derivatilor fenolici sunt similare cu ale fenolului, actionand asupra sistemului nervos central.
Pot fi absorbiti de piele, mucoasele cailor respiratorii si tubului digestiv, dar rata de penetrare este in functie de suprafata expusa si de concentratie.
Solutiile concentrate sunt local corozive pentru piele si mucoase, iar solutiile diluate provoaca roseata si ulceratii ale pielei.
Fabricarea fenolilor impune luarea unor masuri de protectie a mediului inconjurator. Poluarea accidentala cu fenoli poate modifica mult calitatea factorilor de mediu:
In perioada de monitorizare a calitatii mediului, 27.02 - 04.03.2007, in zona raului Dambovnic si Neajlov indicatorii de calitate masurati: materii in suspensii, consum chimic de oxigen, substante extractibile, cianuri si fenoli, au avut valori care indicau evident o poluare a amediului.
Rezultatele sunt evidentiate grafic, dupa cum urmeaza:
Fig. 1. Variatia concentratiei de FENOLI (mg/l) in lungul raului Dambovnic si Neajlov, pe perioada poluarii accidentale
Din grafic se observa ca fenolii au avut valori de aproape 15 ori mai mari decat cele admisibile in sectiunille aflate imediat aval de descarcarea apelor in Dambovnic, scazand pe masura ce inaintau in aval.
Fig. 2. Imagini de la poluarea accidentala de la S.C.,,Arpechim'' 2007


CAPITOLUL 7.
CONCLUZII
In concluzie, fenolul este un compus organic in care grupa functionala -OH este legata de un atom de carbon apartinand unui nucleu aromatic.
De fapt fenolul este un benzol la care s-a substituit o grupare hidroxilica, de aceea are un caracter usor acid. La temperatura camerei fenolul apare sub forma de cristale incolore, care prin oxidare sau impuritati, pot avea o culoare roza pana la rosu brun.
Fenolul are un miros intepator caracterisic aromat si este de 1000 de ori mai activ ca benzolul.
Utilizat in mai multe domenii, cum ar fi industria:
medicamentelor;
colorantilor si a parfumurilor;
explozivilor;
industria fibrelor sintetice;
la fabricarea materialelor plastice;
in tehnica fotografica;
ca dezinfectant.
fenolul ramane un compus chimic toxic care poate modifica grav calitatea mediului.
Elaborarea proiectului cu aceasta tema, m-a ajutat sa inteleg mai bine proprietatile fenolului si de aici, multitudinea utilizarilor sale.
Fenolul este un intermediar organic important pentru industria chimica.

BIBLIOGRAFIE
Albu, C., Cosma I., Petrescu O. - Chimie, manual pentru clasa a X-a, Editura didactica si pedagogica, Bucuresti, 1984
Buchman A., Lupei E., Marincescu M. - Auxiliar curricular pentru clasa a IX-a SAM, domeniul chimie industriala, elaborat in cadrul CNDIPT-MEC, Bucuresti 2004
Colectiv - Standard de pregatire profesionala nivel 1, Domeniul Chimie industriala, varianta revizuita, Bucuresti, 2005
Colectiv - Curriculum clasa a X-a, Scoala de Arte si Meserii, Bucuresti, 2005
Cosma O. si col. - Manual de pregatire teoretica de baza, anul I Scoala profesionala, Chimie industriala, Editura Oscar Print, Bucuresti, 2000
Croitoru V., Vladescu L., Cismas R., Teodorescu M.- Chimie analitica si analize tehnice, Editura didactica si pedagogica, Bucuresti, 1997
Dobre L., Dragomir R., si col., Pregatire de Baza in Chimie Industriala, manual de practica, Ed. Oscar Print
Fatu, S., Stroe, F., Stroe, C., Chimie, manual pentru Scoala profesionala, Editura ALL, Educational 2000, Bucuresti, 2001
Halmanghi I., Zaharescu A.- Tehnologie chimica organica, Editura didactica si pedagogica, Bucuresti, 1962
Niculescu I., Dulca A., Rodeanu T., Vidrascu A. - Tehnologia fabricarii si prelucrarii produselor chimice, Editura didactica si pedagogica, Bucuresti, 1993
11. C.D. ALBU, O. PETRESCU, I. COSMA ,,CHIMIE - Manual pentru clasa a X-a", Editura Didactica si Pedagogica, Bucuresti, 1995
12. MIHAI ZAPAN ,,Chimie organica - Edith Beral" , Editura tehnica, Bucuresti 1973
ANEXA 1
Clasificarea compusilor organici

|
ALCANI |
|
ALCHENE |
|
ARENE |
|
ALCHINE |
|
CnH2n+2 |
|
CnH2n |
|
CnH2n-2 |
|
CnH2n-6 |
|
C2H4 etena C3H6 propena |
|
CH4 metan C2H6 etan |
|
C2H2 acetilena C2H6 etan |
|
C6H6 benzen |
|
Derivati halogenati |
|
Alcooli |
|
Aldehide si cetone |
|
Acizi carboxilici |
|
Alcooli polihidroxilici |
|
R - X |
|
R - OH |
|
R - CHO R - CO - Rl |
|
R - COOH |
|
CH2 - OH l CH - OH l CH2 - OH |


ANEXA 2
FENOL- UTILIZARI
a. La fabricarea medicamentelor

Pastile cu propolis, maces si sirop de zmeura. Pentru gat si iritatii ale mucoasei bucale. Flavonoidele si fenolii existenti in propolis actioneaza ca antioxidanti si intaresc imunitatea organismului. Macesul este o sursa naturala de Vitamina C usor absor
 Produs pe baza de fenol
utilizat in stomatologie.
Produs pe baza de fenol
utilizat in stomatologie.
Polienolii si fenolii poseda atat proprietati antioxidante cat si prooxidante. Dintre acestia flavonoizii se utilizeaza deja sub forma de medicamente (Troxevasin, Glivenol, Rutozid), desi potentialul lor terapeutic este doar in mica parte cunoscut.
PROPOLISUL, un produs secretat de albine, contine mari cantitati de flavonoizi si fenoli. Marea complexitate a compozitiei impiedica standardizarea unor preparate, desi sub forma de extracte partial purificate propolisul este utilizat mai ales pentru uz extern. Propolisul are pe langa un puternic efect antioxidant si proprietati bactericide, bacteriostatice, cicatrizante si antiinflamatorii.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 33666
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved