| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
REACTII REDOX
Reactiile redox sau de oxido-reducere sunt transformari ale substantelor in care se produce un transfer de electroni intre particulele reactante. Un exemplu de reactie redox este reactia dintre sodiul metalic si clorul gazos:
2Na(s) + Cl2(g) = 2NaCl(s) (9.1)
In cursul reactiei, atomii de sodiu cedeaza electroni, rezultand ioni de Na+:
Na = Na+ + e- (9.2)
In acelasi timp, moleculele de clor accepta electronii disponibilizati, transformandu-se in ioni de clorura:
Cl2 + 2e- = 2Cl- (9.3)
Transformarea in care o specie chimica (atomi, ioni sau molecule) cedeaza electroni se numeste oxidare, iar transformarea care se produce prin acceptare de electroni se numeste reducere.
Ecuatia reactiei globale dintre sodiul metalic si clorul gazos (9.1) se obtine prin insumarea ecuatiei reactiei de oxidare a sodiului cu cea de reducere a clorului molecular. Prin urmare, intr-o reactie redox, unul dintre reactanti se oxideaza, iar altul se reduce. Reactantul care se oxideaza se numeste reducator, iar reactantul care se reduce se numeste oxidant. In reactia (9.1) sodiul este reducator, iar clorul - oxidant.
Pentru a caracteriza starea la care ajunge un element prin cedare sau acceptare de electroni a fost introdusa notiunea de numar de oxidare (stare de oxidare).
Numarul de oxidare al unui atom dintr-o substanta reprezinta sarcina electrica formala pe care ar avea-o atomul respectiv daca electronii ar fi atribuiti atomilor substantei respective in mod conventional.
Atribuirea arbitrara a electronilor speciilor atomice ale unei substante se face pe baza urmatoarelor reguli:
1. Numarul de oxidare al unui atom dintr-o substanta elementara este zero. De exemplu: in hidrogenul molecular, in fier, in sulf si in fosforul alb, numerele de oxidare, trecute deasupra simbolului elementului respectiv, sunt 0:
![]() ,
, ![]() ,
, ![]() ,
, ![]()
2. Numarul de oxidare al unui element dintr-un ion simplu este egal cu sarcina electrica a acestuia. Astfel in clorura de potasiu, numarul de oxidare al potasiului va fi +1, iar al clorului -1, in clorura de calciu, numarul de oxidare al calciului va fi +2, iar al clorului -1, in dioxidul de plumb, numarul de oxidare al plumbului va fi +4, iar al oxigenului -2:
+1 -1 +2 -1 +4 -2
KCl, CaCl2, PbO2
3. Numarul de oxidare al unui atom dintr-un compus covalent este egal cu sarcina care ramane atomului atunci cand fiecare pereche de electroni participanta la legaturi chimice este atribuita elementului mai electronegativ.
In combinatie cu nemetalele, hidrogenul are starea de oxidare +1. De exemplu, in hidrogenul sulfurat, amoniac, apa, acid clorhidric:
+1 -2 -3 +1 +1 -2 +1 -1
H2S, NH3, H2O, HCl
In combinatiile cu metalele, hidrogenul are starea de oxidare -1, de exemplu, in hidrura de litiu, hidrogenul are starea de oxidare -1, iar litiul +1.
Oxigenul, in combinatiile sale, are starea de oxidare -2, intrucat este unul dintre cele mai electronegative elemente. Ca exemple se dau trioxidul de sulf, ionul permanganat, trioxidul de dialuminiu:
+6 -2 +7 -2 +3 -2
SO3, ![]() , Al2O3
, Al2O3
Oxidarea nu se poate desfasura independent de reducere. Intotdeauna, electronii cedati intr-un proces de oxidare sunt implicati intr-un proces de reducere. Prin urmare, orice proces de oxidare are loc concomitent cu un proces de reducere. De exemplu, reactia dintre oxidul de cupru (II) si hidrogen:
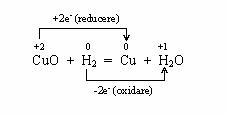
Stabilirea coeficientilor unei reactii redox
Consideram reactia redox dintre sulfatul de fier (II) si permanganatul de potasiu in mediu acid:
+7 +2 +2 +3
KMnO4 + FeSO4 + H2SO4 = MnSO4 + K2SO4 + Fe2(SO4)3 + H2O (9.4)
Elementele care isi modifica starea de oxidare sunt manganul si fierul, astfel incat semireactiile de oxidare si reducere pot fi scrise astfel:
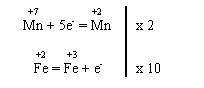
Numarul atomilor de fier trebuie sa fie par pentru ca ecuatia sa aiba coeficienti intregi. Pentru ca numarul de electroni cedati de fier sa fie egal cu numarul de electroni acceptati de mangan, prima semiecuatie se inmulteste cu 2, a doua cu 10. Inseamna ca KMnO4 va avea coeficientul 2, FeSO4 - 10, MnSO4 - 2, iar Fe2(SO4)3 - 1. Din bilantul atomilor de potasiu si oxigen, se obtin si coeficientii pentru K2SO4 - 1, H2SO4 - 8, H2O - 8. Ecuatia scrisa cu coeficienti va fi:
2KMnO4 + 10FeSO4 + 8H2SO4 = 2MnSO4 + K2SO4 + Fe2(SO4)3 + 8H2O (9.5)
In aceasta reactie permanganatul de potasiu este oxidant, iar sulfatul de fier (II) este reducator. Reactiile redox de mai sus poate fi scrisa ionic:
![]() + 5Fe2+ +
8H+ = Mn2+ + Fe3+ + 8H2O (9.6)
+ 5Fe2+ +
8H+ = Mn2+ + Fe3+ + 8H2O (9.6)
Reactia (9.2) poate fi descompusa in doua semireactii: una de reducere, alta de oxidare, prin a caror insumare rezulta procesul global.
![]() + 8H+ + 5e-
= Mn2+ + 8H2O (9.7)
+ 8H+ + 5e-
= Mn2+ + 8H2O (9.7)
5Fe2+ = 5Fe3+ + 5e-
Generalizand, semireactiile pot fi scrise sub forma:
Ox1 + me- = Red1 (9.8)
Red2 = Ox2 + ne-
Perechile Ox1/Red1 si Red2/Ox1 sunt denumite cupluri redox.
PROBLEME PROPUSE
9.1. Se considera urmatoarele reactii chimice:
(I) CaO + 2HCl CaCl2 + H2O
(II) 2Mg + O2 2MgO
(
(IV) 4HNO3 + 3C 4NO + 3CO2 + 2H2O
(V) Ca + S CaS
Care dintre aceste reactii sunt redox?
a) II, IV si V; b)
numai reactia IV; c) II si IV; d) I si
9.2. Care sunt numerele de oxidare ale oxigenului in combinatiile: SO2; H2O2; F2O; Na2O2?
a)
b)
c)
d)
e)
9.3. Indicati numerele de oxidare ale sulfului in urmatoarele substante: SOCl2; SO2; H2SO4; H2S; SO3.
a)
b)
c)
d)
e)
9.4.
In care dintre combinatiile urmatoare numarul de oxidare al sulfului este
negativ: H2SO3; H2SO4; H2S;
a) H2SO3 si SO2;
b) H2SO4 si SO3;
c) H2SO3 si H2S;
d) numai H2S;
e)
H2S
si
9.5. Care dintre speciile chimice date mai jos contin acelasi element la stari de oxidare diferite: Al4C3; Cr2O3; Fe3O4; Fe3[Fe(CN)6]2; Mn2O3?
a) Numai Fe3O4;
b) Al4C3 si Fe3O4;
c) numai Fe3[Fe(CN)6]2;
d) Fe3O4 si Fe3[Fe(CN)6]2;
e) Cr2O3 si Mn2O3.
9.6. Numerele de oxidare ale azotului in combinatiile (NH4)2SO4; NaNO3; N2O5; KNO2 si Mg3N2 sunt in ordine:
a)
b)
c)
d)
e)
9.7. Care din urmatoarele reactii nu reprezinta un proces de oxido-reducere?
a)
Fe + S =
b) MnO2 + 4HCl = MnCl2 + 2H2O + Cl2
c) 3Fe + 4H2O = Fe3O4 + 4H2
d) Na2SO4 + BaCl2 = BaSO4 + 2NaCl
e) N2 + 3H2 = 2NH3
9.8. Indicati care din urmatoarele ecuatii reprezinta o reactie de oxido-reducere:
a) FeCl3 + 3NaOH = Fe(OH)3 + 3NaCl
b) 2H2 + O2 = 2H2O
c) NH3 + HCl = NH4Cl
d) SO3 + H2O = H2SO4
e) CaCO3 = CaO + CO2
9.9. In care dintre compusii enumerati mai jos numarul de oxidare al carbonului este +4: CH4; CF4; CF3-CF3; CCl4; CH3OH?
a) CF3-CF3; CF4; CCl4;
b) CH4; CF4; CCl4;
c) CF3-CF3; CH3OH;
d) CF3-CF3; CH3OH; CH4;
e) CF4; CCl4.
9.10. Se considera reactiile:
Fe2O3 + 2Al = Al2O3 + 2Fe
2Na + 2H2O = 2NaOH + H2
4NH3 + 5O2 = 4NO + 6H2O
H2S + HClO = HCl + S + H2O
Reactantii care indeplinesc rolul de oxidant sunt in ordine:
a) Fe2O3; H2O; O2; H2S;
b) Fe2O3; Na; NH3; HClO;
c) Fe2O3; H2O; O2; HClO;
d) Al; Na; NH3; HClO;
e) Fe2O3; H2O; NH3; HClO.
9.11. Care dintre urmatoarele afirmatii privind reactia:
Mg + 1/2O2 MgO
este corecta?
a) magneziul este agent oxidant;
b) oxigenul este agent reducator;
c) magneziul se reduce;
d) oxigenul se oxideaza;
e) magneziul se oxideaza.
9.12. Care dintre urmatoarele afirmatii privind reactia dintre dioxidul de mangan si acid clorhidric este corecta?
a) manganul se oxideaza;
b) reactia serveste pentru obtinerea oxigenului in laborator;
c) clorul sufera un proces de oxidare;
d) reactia amintita este de neutralizare;
e) nici un element nu-si modifica numarul de oxidare in reactia amintita.
9.13. Se considera reactiile:
PbS + 4H2O2 = PbSO4 + 4H2O
2FeCl3 + SnCl2 = 2FeCl2 + SnCl4
H2SO3 + Cl2 + H2O = H2SO4 + 2HCl
H2SO4 + 8HI = 4I2 + H2S + 4H2O
Reactantii care indeplinesc rolul de reducator sunt:
a) PbS; SnCl2; H2SO3; HI;
b) PbS; SnCl2; H2SO3; H2SO4;
c) PbS; SnCl2; Cl2; HI;
d) H2O2; FeCl3; Cl2; H2SO4;
e) H2O2; FeCl3; H2SO3; HI.
9.14. Coeficientii ecuatiei reactiei:
aKMnO4 + bFeSO4 + cH2SO4 = mK2SO4 + nFe2(SO4)3 + pMnSO4 + rH2O
sunt in ordine:
a) 2; 10; 4; 1; 5; 1; 2;
b) 2; 5; 8; 1; 5; 2; 4;
c) 1; 10; 8; 1; 5; 1; 8;
d) 2; 10; 8; 1; 5; 2; 8;
e) 1; 5; 4; 1; 5; 1; 4.
9.15. Valorile coeficientilor ecuatiei reactiei:
mHI + nH2SO4 = xI2 + yH2S + zH2O
sunt in ordine:
a) 4; 1; 2; 1; 2;
b) 8; 1; 4; 1; 4;
c) 2; 1; 1; 1; 1;
d) 8; 2; 4; 2; 4;
e) 4; 2; 4; 2; 2.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 24657
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2024 . All rights reserved