| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
STRUCTURA INVELISULUI DE
ELECTRONI
1. Straturi electronice, orbitali
Luand in considerare modelul Bohr-Sommerfeld al atomului, pe baza datelor experimentale disponibile, este posibila construirea unei imagini intuitive asupra structurii atomilor diferitelor elemente. Pornind de la spectrul hidrogenului, s-a ajuns la concluzia ca invelisul electronic al atomilor are o structura stratificata. Electronii care graviteaza in jurul nucleului pe orbite eliptice se gasesc la distante medii diferite fata de nucleu. Electronii care se gasesc fata de nucleu la distante medii apropiate ca valoare alcatuiesc un strat electronic.
Apartenenta electronilor la un anumit strat este caracterizata de numarul cuantic principal n. Cel mai apropiat strat de nucleu este notat cu K pentru care n = 1. Urmatoarele straturi sunt: L (n = 2), M (n = 3), N (n = 4), O (n = 5), P (n = 6), Q (n = 7).
In atomul de hidrogen, in stare fundamentala (atom izolat in stare energetica minima), electronul se gaseste pe stratul K. In miscarea sa continua, electronul se poate gasi intr-o anumita regiune a spatiului din jurul nucleului. Aceasta portiune a spatiului in care exista probabilitatea de a se gasi electronul poarta numele de orbital. In fiecare orbital pot exista cel mult doi electroni caracterizati de o miscare de spin opus (miscare de rotatie). Aceasta miscare a electronilor este caracterizata de numarul cuantic de spin s, care poate lua valorile -1/2 si +1/2.
Stratul K (n = 1) este constituit dintr-un singur orbital de simetrie sferica numit orbital s (figura 1).
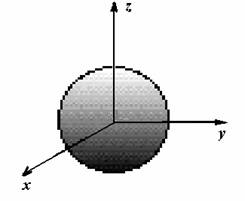
Fig. 1. Orbital s.
Stratul L (n = 2) este constituit din doua tipuri de orbitali de simetrii diferite, care alcatuiesc doua substraturi. Pentru a caracteriza tipul de simetrie a unui orbital s-a introdus numarul cuantic secundar (azimutal) l. Valorile numarului cuantic secundar l sunt functie de numarul cuantic principal n. Pentru n = k, numarul cuantic secundar l poate lua valorile 0, 1, 2, ., k-1. Prin urmare, pentru stratul K (n = 1) numarul cuantic secundar l are o singura valoare (l = 0), ceea ce inseamna ca stratul K este format dintr-un singur substrat s. Pentru stratul L (n = 2), l are valorile 0 si 1, adica stratul L contine doua substraturi, un substrat constituit dintr-un orbital s (l = 0) si un substrat format din trei orbitali p (l = 1). Orbitalii p au forma a doi lobi simetrici fata de nucleu (figura 2).
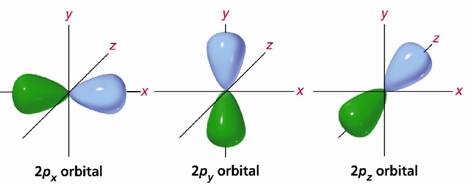
Fig.2. Orbitalii de tip p.
Orientarea orbitalilor este data de numarul cuantic magnetic m. Numerele cuantice magnetice pot lua valorile -l, - (l-1), ., -2, -1, 0, +1, +2, ., l-1, l. Pentru cazul orbitalilor p, numarul cuantic magnetic are valorile -1, 0, +1, care corespund orientarii orbitalilor dupa axele de coordonate.
Stratul M (n = 3) valorile numarului cuantic secundar si ale numarului cuantic magnetic sunt urmatoarele:
|
n |
l |
m |
|
l |
m |
|
|
l |
m |
Pe langa substraturile s (l = 0) si p (l
= 1), apar si orbitalii caracterizati de numarul cuantic secundar l = 2, care se numesc orbitali d. In numar de cinci, orbitalii d sunt formati in general din patru lobi cu orientare diferita in
spatiu dxy, dyz, dzx, ![]() , cu exceptia orbitalului
, cu exceptia orbitalului ![]() care are o forma
deosebita (figura 3).
care are o forma
deosebita (figura 3).
Pentru stratul N numerele cuantice au valorile:
|
n |
l |
m |
|
l |
m |
|
|
l |
m |
|
|
l |
m = |
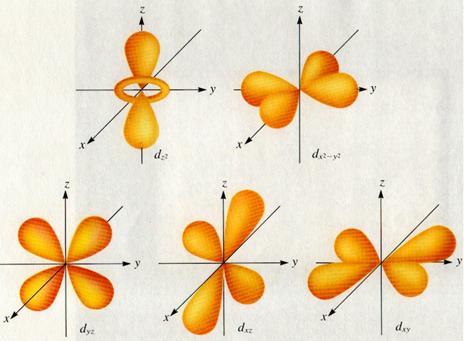
Fig. Orbitali d.
Orbitalii caracterizati de numarul cuantic secundar l = 3 se numesc orbitali f, care sunt in numar de sapte, asa cum rezulta din valorile numarului cuantic magnetic. Forma si simetria orbitalilor f este mai complicata (figura 4.).
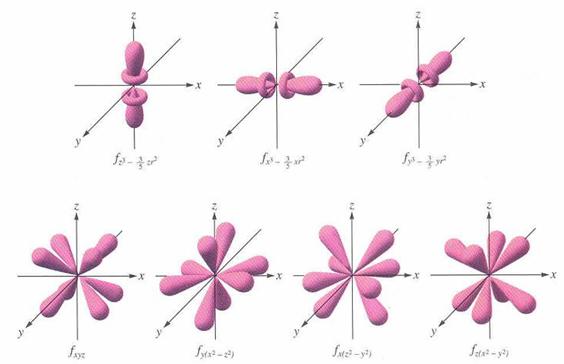
Fig.4. Orbitali f.
2. Ocuparea cu electroni a orbitalilor
Ordinea de ocupare cu electroni a orbitalilor unui atom in stare fundamentala se face pe baza urmatoarelor reguli:
- principiul ordinii crescatoare a energiei;
- principiul excluziunii al lui W.Pauli;
- regula lui Hund.
Principiul ordinii crescatoare a energiei
Numai in atomul de hidrogen ordinea crescatoare a nivelurilor energetice corespunde ordinii de dispunere a nivelurilor data de numarul cuantic principal n si numarul cuantic secundar l:
1s2s2p3s3p3d4s4p4d4f5s5p5d5f .
In atomii polielectronici se produce o modificare energetica a invelisului electronic, asa cum rezulta din diagrama energetica a substraturilor electronice (figura 5).
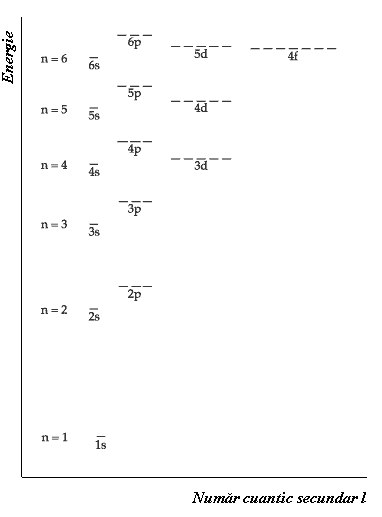
Fig.5. Nivele energetice ale orbitalilor.
Prin urmare, orbitalii vor fi ocupati cu electroni in ordinea:
1s2s2p3s3p4s3d4p5s4d5p6s4f5d6p .
Au fost propusi mai multi algoritmi de stabilire a succesiunii de ocupare a orbitalilor. Unul dintre acestia este "regula n l minim". Conform "regulii n l minim" substraturile electronice sunt ocupate cu electroni in ordinea crescatoare a valorii sumei dintre numarul cuantic principal n si numarul cuantic secundar l. La valori egale ale sumei, energia cea mai mica corespunde orbitalului cu n mai mic. Regula poate fi redata sub forma tabelara (tabelul 1).
Tabelul 1. Regula n l minim.
|
n | |||||||||||||||||||||
|
l | |||||||||||||||||||||
|
s |
s |
p |
s |
p |
d |
s |
p |
d |
f |
s |
p |
d |
f |
g |
s |
p |
d |
f |
g |
h |
|
|
n l | |||||||||||||||||||||
Cea mai sugestiva ilustrare a "regulii n l minim" este tabla de sah a lui Goldansky, in care pe diagonala principala se trec orbitalii s, iar pe urmatoarele diagonale - orbitalii p, d si f. Secventa ocuparii cu electroni a orbitalilor este indicata de sageata (figura 6).
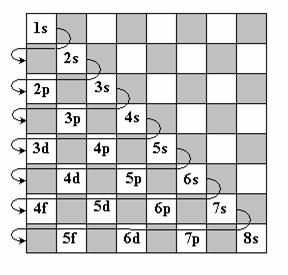
Fig.6. Tabla de sah a lui Goldansky.
Principiul excluziunii al lui Pauli stabileste ca in invelisul electronic al unui atom nu pot exista electroni care sa fie caracterizati de toate cele patru numere cuantice identice. Consecinta acestui principiu este faptul ca un anumit orbital nu poate fi ocupat decat cu cel mult doi electroni, care au spinul opus.
Regula lui Hund stabileste ca, in cazul orbitalilor de acelasi tip, electronii se dispun astfel incat modulul sumei numerelor cuantice de spin sa fie maxim. Prin urmare, orbitalii de acelasi tip vor fi completati mai intai cu cate un electron de acelasi spin, dupa care va incepe plasarea celui de-al doilea electron de spin opus pe orbitalul respectiv.
Atomul de hidrogen (Z = 1), are un singur electron plasat pe orbitalul 1s. Configuratia electronica se noteaza: 1s1. Pentru urmatorul element, heliu (Z = 2), configuratia electronica este 1s2. In continuare este redata ordinea de ocupare a orbitalilor pentru atomii elementelor pana la neon (Z = 10):
1s 2s 2px 2py 2pz
|
H (Z = 1) |
1s1 |
|||||||
|
He (Z = 2) |
¯ |
1s2 |
||||||
|
Li (Z = 3) |
¯ |
1s22s1 |
||||||
|
Be (Z = 4) |
¯ |
¯ |
1s22s2 |
|||||
|
B (Z = 5) |
¯ |
¯ |
1s22s22p1 |
|||||
|
C (Z = 6) |
¯ |
¯ |
1s22s22p2 |
|||||
|
N (Z = 7) |
¯ |
¯ |
1s22s22p3 |
|||||
|
O (Z = 8) |
¯ |
¯ |
¯ |
1s22s22p4 |
||||
|
F (Z = 9) |
¯ |
¯ |
¯ |
¯ |
1s22s22p5 |
|||
|
Ne (Z = 10) |
¯ |
¯ |
¯ |
¯ |
¯ |
1s22s22p6 |
Sodiul (Z = 11) are configuratia electronica 1s22s22p63s1, care poate fi redata simplificat: [10Ne]3s1, in care [10Ne] simbolizeaza configuratia neonului.
Electronul prin care un element se deosebeste de cel precedent se numeste electron distinctiv. Electronul distinctiv se afla pe nivelul energetic cel mai ridicat. Pozitia acestuia in invelisul electronic este de cea mai mare importanta pentru comportarea chimica a elementului respectiv.
Regula "regula n l minim" reda doar ordinea de ocupare a orbitalilor. Pentru elementele usoare aceasta corespunde configuratiei electronice. La elementele mai grele se produce o reasezare a nivelurilor energetice datorita fenomenului de ecranare a nucleului de electronii de pe straturile electronice inferioare. In felul acesta, la elementele cu Z mai mare, nivelurile energetice se dispun mai intai dupa numarul cuantic principal n, iar pentru acelasi n - dupa numarul cuantic secundar l. De exemplu, in cazul vanadiului (Z = 23), configuratia electronica devine: 1s22s22p63s23p63d34s2. Exista si cateva exceptii de la regulile care dau ordinea de ocupare cu electroni a orbitalilor. Astfel, cromul, conform regulii n+l, ar trebui sa aiba configuratia [18Ar]4s23d4. Dar, configuratia electronica a cromului, determinata din date experimentale, este [18Ar]4s13d5. Prin aceasta se realizeaza semicompletarea substratului 3d (3d5), ceea ce conduce la o structura electronica mai stabila. O situatie similara este intalnita in cazul molibdenului care are configuratia: [Kr]5s14d5. In cazul cuprului, conform regulii n+l, configuratia electronica ar trebui sa fie [Ar]4s23d9, in realitate este [Ar]4s13d10, care asigura un substrat 3d complet ocupat (3d10). Structuri electronice cu stabilitate ridicata sunt si cele cu substratul f semicomplet (f7) sau complet (f14).
Configuratiile electronice ale elementelor sunt date in tabelul 1.
Tabelul 1. Configuratiile electronice ale elementelor.
|
Z |
Denumire |
Simbol |
Configuratie electronica |
|
Hidrogen |
H |
1s1 |
|
|
Heliu |
He |
1s2 = [He] |
|
|
Litiu |
Li |
[He] 2s1 |
|
|
Beriliu |
Be |
[He] 2s2 |
|
|
Bor |
B |
[He] 2s22p1 |
|
|
Carbon |
C |
[He] 2s22p2 |
|
|
Azot |
N |
[He] 2s22p3 |
|
|
Oxigen |
O |
[He] 2s22p4 |
|
|
Fluor |
F |
[He] 2s22p5 |
|
|
Neon |
Ne |
[He] 2s22p6 =[Ne] |
|
|
Sodiu |
Na |
[Ne] 3s1 |
|
|
Magneziu |
Mg |
[Ne] 3s2 |
|
|
Aluminiu |
Al |
[Ne] 3s23p1 |
|
|
Siliciu |
Si |
[Ne] 3s23p2 |
|
|
Fosfor |
P |
[Ne] 3s23p3 |
|
|
Sulf |
S |
[Ne] 3s23p4 |
|
|
Clor |
Cl |
[Ne] 3s23p5 |
|
|
Argon |
Ar |
[Ne] 3s23p6 = [Ar] |
|
|
Potasiu |
K |
[Ar] 4s1 |
|
|
Calciu |
Ca |
[Ar] 4s2 |
|
|
Scandiu |
Sc |
[Ar] 4s23d1 |
|
|
Titan |
Ti |
[Ar] 4s23d2 |
|
|
Vanadiu |
V |
[Ar] 4s23d3 |
|
|
Crom |
Cr |
[Ar] 4s13d5 |
Tabelul 1. Configuratiile electronice ale elementelor (continuare).
|
Z |
Denumire |
Simbol |
Configuratie electronica |
|
Mangan |
Mn |
[Ar] 4s23d5 |
|
|
Fier |
Fe |
[Ar] 4s23d6 |
|
|
Cobalt |
Co |
[Ar] 4s23d7 |
|
|
Nichel |
Ni |
[Ar] 4s23d8 |
|
|
Cupru |
Cu |
[Ar] 4s13d10 |
|
|
Zinc |
Zn |
[Ar] 4s23d10 |
|
|
Galiu |
Ga |
[Ar] 4s23d104p1 |
|
|
Germaniu |
Ge |
[Ar] 4s23d104p2 |
|
|
Arsen |
As |
[Ar] 4s23d104p3 |
|
|
Seleniu |
Se |
[Ar] 4s23d104p4 |
|
|
Brom |
Br |
[Ar] 4s23d104p5 |
|
|
Kripton |
Kr |
[Ar] 4s23d104p6 |
|
|
Rubidiu |
Rb |
[Kr] 5s1 |
|
|
Strontiu |
Sr |
[Kr] 5s2 |
|
|
Ytriu |
Y |
[Kr] 5s24d1 |
|
|
Zirconiu |
Zr |
[Kr] 5s24d2 |
|
|
Niobiu |
Nb |
[Kr] 5s14d4 |
|
|
Molibden |
Mo |
[Kr] 5s14d5 |
|
|
Technetiu |
Tc |
[Kr] 5s24d5 |
|
|
Ruteniu |
Ru |
[Kr] 5s24d6 |
|
|
Rodiu |
Rh |
[Kr] 5s24d7 |
|
|
Paladiu |
Pd |
[Kr] 5s24d8 |
|
|
Argint |
Ag |
[Kr] 5s14d10 |
|
|
Cadmiu |
Cd |
[Kr] 5s24d10 |
|
|
Indiu |
In |
[Kr] 5s24d105p1 |
|
|
Staniu |
Sn |
[Kr] 5s24d105p2 |
|
|
Stibiu |
Sb |
[Kr] 5s24d105p3 |
|
|
Telur |
Te |
[Kr] 5s24d105p4 |
|
|
Iod |
I |
[Kr] 5s24d105p5 |
|
|
Xenon |
Xe |
[Kr] 5s24d105p6 = [Xe] |
|
|
Cesiu |
Cs |
[Xe] 6s1 |
|
|
Bariu |
Ba |
[Xe] 6s2 |
|
|
Lantan |
La |
[Xe] 6s25d1 |
|
|
Ceriu |
Ce |
[Xe] 6s24f2 |
|
|
Praseodim |
Pr |
[Xe] 6s24f3 |
|
|
Neodim |
Nd |
[Xe] 6s24f4 |
|
|
Prometiu |
Pm |
[Xe] 6s24f5 |
Tabelul 1. Configuratiile electronice ale elementelor (continuare).
|
Z |
Denumire |
Simbol |
Configuratie electronica |
|
Samariu |
Sm |
[Xe] 6s24f6 |
|
|
Europiu |
Eu |
[Xe] 6s24f7 |
|
|
Gadoliniu |
Gd |
[Xe] 6s24f75d1 |
|
|
Terbiu |
Tb |
[Xe] 6s24f9 |
|
|
Disprosiu |
Dy |
[Xe] 6s24f10 |
|
|
Holmiu |
Ho |
[Xe] 6s24f11 |
|
|
Erbiu |
Er |
[Xe] 6s24f12 |
|
|
Tuliu |
Tm |
[Xe] 6s24f13 |
|
|
Yterbiu |
Yb |
[Xe] 6s24f14 |
|
|
Lutetiu |
Lu |
[Xe] 6s24f145d1 |
|
|
Hafniu |
Hf |
[Xe] 6s24f145d2 |
|
|
Tantal |
Ta |
[Xe] 6s24f145d3 |
|
|
Wolfram |
W |
[Xe] 6s24f145d4 |
|
|
Reniu |
Re |
[Xe] 6s24f145d5 |
|
|
Osmiu |
Os |
[Xe] 6s24f145d6 |
|
|
Iridiu |
Ir |
[Xe] 6s24f145d7 |
|
|
Platina |
Pt |
[Xe] 6s14f145d9 |
|
|
Aur |
Au |
[Xe] 6s14f145d10 |
|
|
Mercur |
Hg |
[Xe] 6s24f145d10 |
|
|
Taliu |
Tl |
[Xe] 6s24f145d106p1 |
|
|
Plumb |
Pb |
[Xe] 6s24f145d106p2 |
|
|
Bismut |
Bi |
[Xe] 6s24f145d106p3 |
|
|
Poloniu |
|
[Xe] 6s24f145d106p4 |
|
|
Astatin |
At |
[Xe] 6s24f145d106p5 |
|
|
Radon |
Rn |
[Xe] 6s24f145d106p6 |
|
|
Franciu |
Fr |
[Rn]7s1 |
|
|
Radiu |
Ra |
[Rn]7s2 |
|
|
Actiniu |
Ac |
[Rn]7s26d1 |
|
|
Toriu |
Th |
[Rn]7s26d2 |
|
|
Protactiniu |
Pa |
[Rn]7s2d3 |
|
|
Uraniu |
U |
[Rn]7s26d15f3 |
|
|
Neptuniu |
Np |
[Rn]7s26d15f4 |
|
|
Plutoniu |
Pu |
[Rn]7s25f6 |
|
|
Americiu |
Am |
[Rn]7s25f7 |
|
|
Curiu |
Cm |
[Rn]7s26d15f7 |
|
|
Berkeliu |
Bk |
[Rn]7s26d15f8 |
|
|
Californiu |
Cf |
[Rn]7s25f10 |
Tabelul 1. Configuratiile electronice ale elementelor (continuare).
|
Z |
Denumire |
Simbol |
Configuratie electronica |
|
Einsteiniu |
Es |
[Rn]7s25f11 |
|
|
Fermiu |
Fm |
[Rn]7s25f12 |
|
|
Mendeleviu |
Md |
[Rn]7s25f13 |
|
|
Nobeliu |
No |
[Rn]7s25f14 |
|
|
Lawrenciu |
Lr |
[Rn]7s26d15f10 |
|
|
Kurceatoviu |
Ku |
[Rn]7s26d25f10 |
Sistemul periodic si periodicitatea proprietatilor elementelor
Sistemul periodic a fost elaborat pe baza a trei idei fundamentale care s-au dezvoltat in timp:
- posibilitatea unei clasificari naturale a elementelor,
convingerea ca exista o legatura stransa intre o marime fundamentala caracteristica fiecarui element si comportarea chimica a elementului respectiv,
- existenta unei periodicitati a proprietatilor elementelor.
Aceste idei au fost sintetizate pentru prima data de Mendeleev, care a intocmit un tabel al elementelor (in 1869), din care a rezultat (in 1871) sistemul periodic apropiat de forma actuala.
|
|
Dmitri Ivanovici Mendeleev (1834 - 1907) s-a nascut in orasul Tobolsk din
Sistemului periodic actual (forma lunga - pag. 27) este format din 18 coloane numite grupe si sapte linii orizontale numite perioade. Prima perioada contine doua elemente: hidrogenul, trecut de obicei in grupa 1 (grupa metalelor alcaline) si heliul, care apartine grupei a 18-a (grupa gazelor rare). Alte grupe care au un nume distinct sunt: grupa a 2-a (metale alcalino-pamantoase), grupa a 16-a (calcogeni), grupa a 17-a (halogeni). Perioadele 2 si 3 contin cate 8 elemente, repartizate in grupele 1, 2, 13-18, care au fost cunoscute sub numele de grupe principale. Perioadele 4, 5 si 6 contin cate 18 elemente, iar perioada a 7-a este deocamdata incompleta. Sistemul periodic este completat cu doua serii de cate 14 elemente cu caracter metalic numite lantanide si actinide, care dupa proprietatile lor ar trebui sa ocupe aceeasi casuta cu lantanul, respectiv actiniul.
In sistemul periodic se pot distinge diferite portiuni care cuprind elemente cu proprietati asemanatoare, denumite blocuri de elemente. Blocul s cuprinde elementele la care, in general, electronul distinctiv se plaseaza intr-un un orbital s. Din blocul s fac parte elementele din grupele 1 si 2. La aceste elemente, stratul exterior este constituit din orbitali s. Blocul p se caracterizeaza prin faptul ca, electronul distinctiv se plaseaza, cu mici exceptii, intr-un un orbital p, fiind alcatuit din elementele grupelor 13-18. Blocul d este format din elementele grupelor 3 - 12, cunoscute si sub numele de grupe secundare. La aceste elemente, denumite metale tranzitionale, electronul distinctiv este plasat intr-un un orbital d. Blocul f este constituit din cele doua doua serii de elemente: lantanidele si actinidele, la care electronul distinctiv este plasat, cel mai adesea, pe un orbital f.
Proprietati periodice
Volumul atomic poate fi calculat ca raportul dintre masa atomica si densitatea elementului. In figura 7 este redata variatia volumului atomic functie de numarul atomic Z. Se poate constata ca metalele alcaline ocupa maximele curbei, aceste elemente avand cel mai mare volum atomic. Pozitii apropiate de minimele curbei ocupa elementele grupei 13: B, Al, Ga, In, Tl. De asemenea, volume atomice reduse au elementele tranzitionale. Metalele alcalino-pamantoase, halogenii si gazele rare cu exceptia heliului, ocupa pozitiile intermediare.
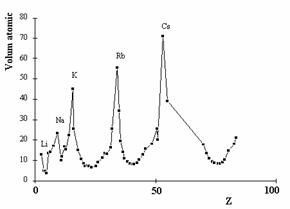
Fig.7. Volumul atomic functie de numarul atomic Z.
O reprezentare sugestiva a volumului atomic al elementelor din grupele principale este redata in figura 8. Pentru aceste elemente raza atomica, cu cateva exceptii, scade in perioade de la stanga la dreapta intrucat marirea numarului de electroni in stratul exterior, concomitent cu marirea sarcinii pozitive a nucleului, conduce la accentuarea fortei de atractie intre nucleu si electronii exteriori.
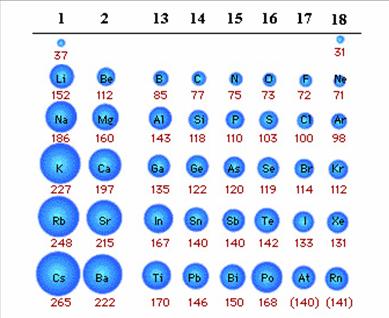
Fig.8. Razele atomice [in pm] ale elementelor din grupele principale.
Raza atomica este determinata de numarul de straturi electronice. Adaugarea unui nou strat electronic duce la marirea considerabila a razei atomice. Prin urmare, in grupele principale raza atomica va creste de sus in jos, regula mai putin evidenta la elementele tranzitionale.
In privinta razelor ionice, o proprietate generala este: anionii au raza, prin urmare si volumul, mai mari decat ale atomilor din care provin, iar la cationi, raza si volumul, sunt mai mici (figurile 9 si 10).
Razele anionilor scad in perioade de la stanga la dreapta intrucat pentru acelasi numar de electroni, cresterea sarcinii pozitive a nucleului duce la marirea fortei de atractie intre nucleu si invelisul electronic:
|
N-3 |
O2- |
F- |
|
|
Nr. de protoni | |||
|
Nr. de electroni | |||
|
Raza ionica [Å] |
Similar este si cazul cationilor:
|
Na+ |
Mg2+ |
Al3+ |
|
|
Nr. de protoni | |||
|
Nr. de electroni | |||
|
Raza ionica [Å] |
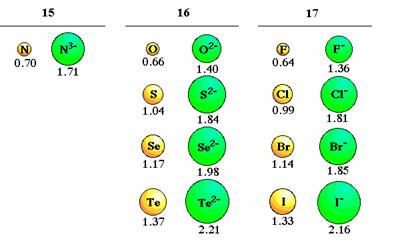
Fig.9. Marimile relative ale anionilor si atomilor din care provin.
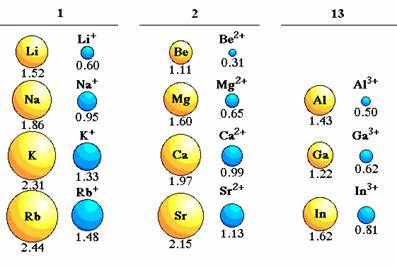
Fig.10. Marimile relative ale cationilor si atomilor din care provin.
O alta proprietate periodica este energia de ionizare, care reprezinta energia necesara pentru indepartarea unui electron dintr-un atom aflat in stare gazoasa. Energia de ionizare primara se refera la indepartarea electronului de pe nivelul energetic superior (prima treapta de ionizare), energia de ionizare secundara se refera la indepartarea unui electron din cationul rezultat (a doua treapta de ionizare). In fig. 11 este redata variatia energiei de ionizare primara functie de numarul atomic Z.
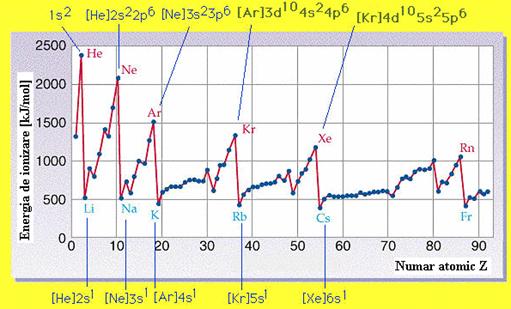
Fig.10. Variatia energiei de ionizare primara functie de Z.
Cele mai mici energii de ionizare le au metalele alcaline, iar cele mai mari le corespund gazelor rare. Acest fenomen este explicat de faptul ca, cu cat numarul de electroni de pe stratul exterior este mai mare, cu atat si energia necesara eliminarii unui electron este mai mare. La gazele rare, energia mare de ionizare este datorata si stabilitatii configuratiei exterioare 1s2 sau ns2np6. De asemenea, se poate constata ca, in cadrul unei grupe, energia de ionizare scade de sus in jos intrucat, cu cat electronul este mai indepartat de nucleu, cu atat forta cu care este atras de sarcina pozitiva a nucleului este mai mica.
Electronegativitatea reprezinta proprietatea unui atom al unui element dintr-o combinatie chimica de a atrage electronii. Elementele ale caror atomi atrag puternic electronii se numesc electronegative, iar elementele ale caror atomi au tendinta de a pierde electroni se numesc electropozitive.
Despre elementele electropozitive se spune ca au caracter metalic, in timp ce elementele electronegative au caracter nemetalic. Taria caracterului metalic sau nemetalic poate fi apreciata empiric pe baza intensitatii cu care se desfasoara unele reactii chimice la care participa elementele respective. O masura a caracterului elementelor este data de electronegativitatea c, definita in 3 moduri: Pauling, Allred-Rochow si Mulliken. In figura 11 sunt redate electronegativitatile Pauling.
|
H |
He |
||||||||||||||||
|
Li |
Be |
B |
C |
N |
O |
F |
Ne |
||||||||||
|
Na |
Mg |
Al |
Si |
P |
S |
Cl |
Ar |
||||||||||
|
K |
Ca |
Sc |
Ti |
V |
Cr |
Mn |
Fe |
Co |
Ni |
Cu |
Zn |
Ga |
Ge |
As |
Se |
Br |
Kr |
|
Rb |
Sr |
Y |
Zr |
Nb |
Mo |
Tc |
Ru |
Rh |
Pd |
Ag |
Cd |
In |
Sn |
Sb |
Te |
I |
Xe |
|
Cs |
Ba |
La |
Hf |
Ta |
W |
Re |
Os |
Ir |
Pt |
Au |
Hg |
Tl |
Pb |
Bi |
|
At |
Rn |
|
Fr |
Ra |
Ac |
Cel mai electronegativ element este fluorul (c = 3,98), iar cel mai electropozitiv este franciul (c = 0,7). In general, electronegativitatea creste in perioade de la stanga la dreapta. Prin urmare, metalele alcaline sunt cele mai electropozitive, iar halogenii sunt cele mai electronegative elemente. In grupe, electronegativitatea scade de sus in jos.
4. EXERCITII SI PROBLEME PROPUSE
1. Elementul chimic reprezinta:
a) specia de atomi cu acelasi numar de neutroni;
b) specia de atomi cu acelasi numar de masa;
c) specia de atomi cu acelasi numar atomic;
d) specia de atomi la care numarul electronilor este egal cu numarul neutronilor;
e) nici unul din raspunsurile a-d nu este corect.
2. Numarul de masa este dat de:
a) suma dintre numarul de electroni si numarul de protoni;
b) suma dintre numarul de electroni, numarul de neutroni si numarul de protoni;
c) suma dintre numarul de protoni si numarul de neutroni;
d) numarul protonilor;
e) numarul neutronilor.
Izotopii sunt specii atomice care au:
a) acelasi numar de protoni;
b) acelasi numar de neutroni;
c) acelasi numar de protoni si neutroni;
d) acelasi numar de neutroni si electroni;
e) nici unul din raspunsurile a-d nu este corect.
4. Numarul atomic al unui element se noteaza cu Z si este egal cu:
a) numarul de nucleoni;
b) numarul de protoni;
c) numarul de neutroni;
d) masa atomica;
e) nici unul din raspunsurile a-d nu este corect.
5. Relatia intre numarul de masa A, numarul atomic Z si numarul de neutroni din nucleul unui atom este data de expresia:
a) A = Z - N; b) Z = A + N; c) A = Z + N; d) N = Z - A;
e) Z = N - A.
6. Cei trei izotopi ai hidrogenului : protiu, deuteriu si tritiu difera prin:
a) numarul atomic;
b) numarul de protoni din nucleu;
c) numarul de masa;
d) numarul de electroni;
e) structura invelisului electronic.
7. Atomul de deuteriu contine:
a) 2 electroni, 2 protoni, 2 neutroni;
b) 2 electroni, 2 protoni, 1 neutron;
c) 1 electron, 1 proton, 1 neutron;
d) 1 electron, 1 proton, 2 neutroni;
e) 1 electron, 2 protoni, 1 neutron.
8. Care din urmatoarele afirmatii este falsa?
a) un orbital nu poate fi ocupat decat cu maximum doi electroni de spin opus;
b) un orbital nu poate fi ocupat cu doi electroni, decat dupa ce toti orbitalii substratului respectiv sunt ocupati cu cate un electron;
c) fiecare strat electronic este format din unul sau mai multe substraturi;
d) electronii de pe ultimul strat al unui atom sunt denumiti electroni de valenta;
e) electronul distinctiv al unui atom este cel cu energia cea mai mica.
9. Elementul cu Z=20 se gaseste in :
a) perioada 3 si grupa II;
b) perioada 2 si grupa II;
c)
perioada
2 si grupa
d) perioada 3 si grupa II;
e) perioada 4 si grupa II.
10. Elementele tranzitionale sunt:
a) elemente puternic electropozitive;
b) elemente puternic electronegative;
c) elemente la care electronul distinctiv ocupa orbitali de tip p;
d) elemente la care electronul distinctiv ocupa orbitali de tip s;
e) elemente la care electronul distinctiv ocupa orbitali de tip d.
11. Care din urmatoarele afirmatii, dedusa din comportarea chimica a elementelor, este corecta?
a) structurile electronice stabile corespund configuratiilor cu substraturi complet ocupate (s2, p6, d10, f 14 ) si substraturi pe jumatate ocupate (d5, f 7);
b) metalele tranzitionale sunt puternic electronegative;
c) lantanidele si actinidele sunt puternic electronegative;
d) elementele din grupele principale au caracter amfoter;
e) elementele din grupele secundare prezinta energie de ionizare mare.
12. Cunoscand ca pentru atomul de fier (Z=26) configuratia electronica este:
1s22s22p63s23p64s23d6,
inseamna ca pentru ionul Fe3+ configuratia electronica stabila va fi:
a) 1s22s22p63s23p64s23d3;
b) 1s22s22p63s23p63d5;
c) 1s22s22p63s23p64s13d4;
d) 1s22s22p63s23p63d6;
e) 1s22s22p63s23p64s23d4.
1 Care dintre urmatoarele configuratii electronice corespunde elementului Ti (Z=22)?
a) 1s22s22p63s23p64s23d2;
b) 1s22s22p63s23p64s13d3;
c) 1s22s22p63s23p63d4;
d) 1s22s22p63s23p64s23d3;
e) 1s22s22p63s23p64s23d4;
14. Dintre ionii 3Li+, 38Sr2+, 13Al3+, 37Rb+, 12Mg2+, raza ionica cea mai mare o are:
a) Li+; b) Mg2+; c) Al3+; d) Rb+; e) Sr2+;
16. Dintre ionii: 9F-, 34Se2+, 35Br-, 51Sb3+, 53I-, raza ionica cea mai mica o are:
a) I-; b) Br-; c) F-; d) Se2+; e) Sb3+.
17. Cati electroni necuplati pot exista pe un orbital f:
a) 7; b) 14; c) 1; d) 2; e) 5.
18. Numarul maxim de electroni de pe substratul d este:
a) 2; b) 6; c) 5; d) 10; e) 14.
19. Numarul maxim de electroni necuplati care pot ocupa substratul p este:
a) 1; b) 3; c) 6; d) 2; e) 4.
20. Numarul maxim de electroni de pe stratul electronic 4 (N) este:
a) 16; b) 4 ; c) 8; d) 14; e) 32.
21. Numarul maxim de electroni de pe stratul 3 (M) este:
a) 18; b) 10; c) 6; d) 3; e) 14.
22. Completarea cu electroni a substratului 3d incepe la elementul cu numarul atomic Z egal cu:
a) 21; b) 19; c) 20; d) 18; e) 22.
2 Care dintre configuratiile electronice de mai jos poate fi atribuita ionului Sr2+ stiind ca numarul de ordine ZSr=38:
a) 1s22s22p63s23p63d104s24p6;
b) 1s22s22p63s23p63d104s24p45s2;
c) 1s22s22p63s23p63d104s24p55s1;
d) 1s22s22p63s23p63d104s24p65s2;
e) 1s22s22p63s23p63d104p65s2.
24. Dintre elementele: I, Se, C, O, F, caracterul nemetalic cel mai pronuntat il are:
a) Se; b) C; c) F; d) I; e) O.
25. Dintre elementele: K, Al, Li, Sr, Cs, caracterul metalic cel mai pronuntat il are:
a) Li; b) Cs; c) Al; d) Sr; e) K.
26. Numerele de ordine ale elementelor: Ba, Cr, Fe, Zn, Ge, sunt: 56; 24; 26; 30; 32. Care dintre ionii: Ba2+, Cr3+, Fe3+, Zn2+si Ge4+ are configuratie de gaz rar:
a) Zn2+; b) Fe3+; c) Ba2+; d) Cr3+; e) Ge4+.
27. Numerele de ordine ale elementelor: Cu, Mo, S, Cd, Pb, sunt: 29; 42; 16; 48; 82.
Care dintre ionii Cu2+, Mo2+, S2-, Cd2+ si Pb2+ are configuratie de gaz inert:
a) Cd2+; b) S2-; c) Mo2+; d) Pb2+; e) Cu2+.
28. Sa se calculeze masa atomica a magneziului stiind ca acesta contine izotopii cu numarul de masa: 24; 25 si 26 in procent de 78 %, 10 % si 12 %.
a) 24,34; b) 24,00; c) 25; d) 26; e) 24,25.
29. Cati electroni se gasesc pe orbitalii 3d ai atomului de cupru (Z=29)?
a) 9; b) 4; c) 6; d) 8; e) 10.
30. Se dau urmatorii ioni ai elementelor din perioada a doua: Na+, Mg2+, Al3+, S2-, Cl-.
Raza ionica a acestor ioni scade in ordinea:
a) S2- > Cl- > Na+ > Mg2+ > Al3+;
b) Na+ > Mg2+ > Al3+ > S2- > Cl-;
c) S2- > Cl- > Al3+ > Mg2+ > Na+;
d) Al3+ > Mg2+ > Na+ > Cl- > S2-;
e) S2- > Cl- > Al3+ > Na+ > Mg2+.
31. Caracterul metalic al urmatoarelor elemente: Rb, K, Na, Mg, Al scade in ordinea:
a) Rb > K > Na > Mg > Al;
b) Al > Mg > Na > K > Rb;
c) Na > K > Rb > Al > Mg;
d) Rb > K > Na > Al > Mg;
e) Al > Mg > Rb > K > Na.
32. Configuratia electronica a atomului 29Cu este:
a) 1s22s22p63s23p63d94s2;
b) 1s22s22p63s23p63d54s24p4;
c) 1s22s22p63s23p64s24p63d3;
d) 1s22s22p63s23p63d104s2;
e) 1s22s22p63s23p63d104s1.
3 Configuratia electronica a atomului 24Cr este:
a) 1s22s22p63s23p63d44s2;
b) 1s22s22p63s23p33d9;
c) 1s22s22p63s23p63d6;
d) 1s22s22p63s23p64s13d5;
e) 1s22s22p63s23p64s23d4.
34. Electronul distinctiv al atomului 30Zn este plasat pe orbitalul:
a) 3d; b) 4d; c) 4s; d) 3p; e) 4p.
35. Numarul straturilor electronice ale unui atom este indicat de:
a) numarul grupei;
b) numarul perioadei;
c) numarul de electroni de valenta;
d) numarul atomic;
e) nici unul din raspunsurile a-d nu este corect.
36. Configuratia electronica 1s22s22p63s23p6 corespunde:
a) atomului de argon si ionului F-;
b) atomului de clor si ionului Na+;
c) ionilor Ca2+ si K+;
d) atomului de sulf si ionului K+;
e) ionului Cl+.
(Numere atomice Z : Ar - 18; F - 9; Cl - 17; Na - 11; K - 19; Ca - 20).
37. Care din ionii de mai jos contin 12 protoni si 11 electroni:
a) Na+; b) Al3+; c) Mg2+; d) Ne+; e) nici unul.
(Numere atomice Z : Na - 11; Al - 23; Mg - 12; Ne - 10).
38. Indicati seria in care toate speciile sunt izoelectronice:
a) H, He+, Li+, H2+, Be2+;
b) H-, Li+, H2, He, Be2+;
c) N2, CO, NO+, CN-, Ne;
d) N3-, O2-, F-, Ar, NH3;
e) N2, NH4+, HF, H2O, CO2.
39. Configuratia electronica a ionului Cu+ este:
a) 1s22s22p63s23p63d94s2;
b) 1s22s22p63s23p63d10;
c) 1s22s22p63s23p63d94s1;
d) 1s22s22p63s23p63d104s1;
e) 1s22s22p63s23p63d84s2.
(Numarul atomic Z pentru cupru este 29).
40. Configuratia electronica a ionului S2- este:
a) 1s22s22p63s23p23d1;
b) 1s22s22p63s23p33d1;
c) 1s22s22p63s23p33d3;
d) 1s22s22p63s23p4;
e) 1s22s22p63s23p6.
(Numarul atomic Z pentru sulf este 16).
41. Care din urmatoarele afirmatii este falsa:
a) in grupele principale razele atomice cresc de sus in jos;
b) razele ionilor cresc in grupele principale in acelasi sens cu razele atomice;
c) razele ionilor negativi scad in perioada de la stanga la dreapta;
d) razele cationilor sunt mai mici decat razele atomilor de la care provin;
e) razele anionilor sunt mai mici decat razele atomilor de la care provin.
42. La elementele din grupele principale sunt in curs de completare orbitalii:
a) numai orbitalii s;
b) numai orbitalii p;
c) s si p;
d) p si d;
e) s si d.
4 In general, la elementele din grupele secundare electronul distinctiv se plaseaza:
a) pe orbitalul s al ultimului strat electronic;
b) pe orbitalii d ai penultimului strat electronic;
c) pe orbitalii p ai stratului de valenta;
d) pe orbitalii s si p ai penultimului strat electronic;
e) pe orbitalii f de energie maxima.
44. Ordinea crescatoare a razelor ionilor Na+, Mg2+; si Al3+ este:
a) Na+, Mg2+, Al3+;
b) Mg2+, Al3+, Na+;
c) Al3+, Mg2+, Na+;
d) Na+, Al3+, Mg2+;
e) Al3+, Na+, Mg2+.
45. Intr-un atom energia electronilor este minima:
a) pe stratul electronic exterior;
b) pe stratul de valenta;
c) pe stratul cel mai apropiat de nucleu;
d) pe orbitalii s;
e) pe orbitalii f partial ocupati.
46. Cati electroni neimperecheati exista in invelisul de electroni al urmatoarelor specii chimice: 17Cl; 8O; 26Fe3+.
a) 1, 0, 1; b) 0, 2, 3; c) 1, 2, 5; d) 0, 4, 5; e) 1, 0,
47. Care din elementele cu configuratiile electronice de mai jos are cea mai mica energie de ionizare?
a) 1s22s22p63s2; b) 1s22s22p63s1; c) 1s22s22p6; d) 1s22s22p5; e) 1s22s22p
48. Care element din sistemul periodic formeaza cel mai greu un ion pozitiv?
a) H; b) Li; c) He; d) Cs; e) Xe.
49. Dupa completarea cu electroni a substratului 4p, electronul distinctiv se plaseaza pe substratul:
a) 4d; b) 5s; c) 3d; d) 5p; e) 5d.
50. Ocuparea cu electroni a substratului 3p incepe la atomii de:
a) Na; b) Si; c) P; d) Al; e) Mg.
51. Principiul excluziunii al lui Pauli prevede:
a) atomul unui element chimic se deosebeste de atomul elementului precedent prin electronul distictiv;
b) electronul distinctiv tinde sa ocupe in invelisul electronic al atomului locul vacant de energie minima;
c) intr-un orbital nu pot exista decat maximum 2 electroni de spin opus;
d) un orbital nu poate fi ocupat cu doi electroni decat dupa ce toti orbitalii substratului respectiv sunt ocupati cu cate un electron;
e) numarul maxim de electroni de pe un strat n este 2n2.
52. Perioada a 4-a a sistemului periodic este formata din:
a) 6 elemente; b) 2 elemente; c) 18 elemente;
d) 4 elemente; e) 8 elemente.
5 Indicati care din urmatoarele afirmatii este falsa:
a) numarul straturilor electronice ale unui atom este indicat de numarul perioadei din care acesta face parte;
b) elementele la care se completeaza orbitalii de tip s sau p ai ultimului strat (ns si np) se gasesc in grupele principale ale sistemului periodic;
c) elementele la care electronul distinctiv se plaseaza in orbitalii de tip d ai penultimului strat electronic formeaza grupele secundare ale sistemului periodic;
d) fiecare perioada se termina cu un gaz rar;
e) la elementele care fac parte din grupa lantanidelor si actinidelor este in curs de completare substratul f al penultimului strat (n-1)f.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 26674
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2024 . All rights reserved