| CATEGORII DOCUMENTE |
| Bulgara | Ceha slovaca | Croata | Engleza | Estona | Finlandeza | Franceza |
| Germana | Italiana | Letona | Lituaniana | Maghiara | Olandeza | Poloneza |
| Sarba | Slovena | Spaniola | Suedeza | Turca | Ucraineana |
LÉČIVA VEGETATIVNÍ NERVOVÉ SOUSTAVY
Nervový systém spolu se systémem endokrinním kontrolují a integrují veškeré tělesné funkce. Oba systémy jsou funkčně propojeny a ke kontrole a řízení tělesných funkcí využívají rozsáhlý systém negativních zpětných vazeb. Rozdílný však je způsob, kterým oba systémy přenášejí informace. Zatímco u endokrinního systému je přenos převážně chemický, pomocí krví přenášených hormonů (kap. 13), nervový systém využívá především elektrického přenosu signálu nervovými vlákny. Mezi nervovými buňkami navzájem nebo mezi neurony a efektory je signál přenášen chemicky, pomocí neurotransmitérů (kap. 5).
Vegetativní nervový systém, často nazývaný též autonomní nervový systém, je část nervového systému, která nepodléhá přímé volní kontrole, která však ovlivňuje základní životní funkce, jako srdeční výkon, průtok krve jednotlivými orgány, trávení, vylučování apod.
Z hlediska anatomického se vegetativní nervový systém dělí na dva celky (Obr. 8-1), na sympatický (sympatikus) a parasympatický (parasympatikus). Parasympatická nervová vlákna se druží k hlavovým nervům . Nervové uzliny (ganglia) parasympatiku se nacházejí ve stěnách inervovaného orgánu nebo v jeho blízkosti. Naproti tomu ganglia sympatiku se nacházejí v blízkosti míchy a jeho postgangliová vlákna jsou podstatně delší než u parasympatiku. Neurotransmitérem parasympatických i sympatických ganglií je acetylcholin (kap. 5). Je třeba zdůraznit, že sympatikus a parasympatikus jsou anatomické termíny, které však nemají zcela jednoznačný vztah k typu neurotransmitéru uvolňovaného z nervových zakončení ani k charakteru účinků vyvolaných agonistickým či antagonistickým působením farmak na receptory příslušného systému.
Pregangliová nervová vlákna jsou vyznačena čárkovaně Postgangliová nervová
vlákna jsou vyznačena plně Ach acetylcholin NA noradrenalin
Obr. 8-1 Schématické znázornění anatomických a farmakologických vlastností vegetativního nervového systému
Z hlediska typu přenašeče se nervová vlákna vegetativního nervového systému dělí na cholinergní (neurotransmitérem je acetylcholin) a adrenergní (neurotransmitérem je noradrenalin a adrenalin - kap. 5). Skutečnost, že většina postgangliových vláken sympatiku je adrenergního typu, zatímco většina postgangliových vláken parasympatiku je typu cholinergního (Obr. 8-1), vede k častému ztotožňování parasympatiku s cholinergním systémem a sympatiku s adrenergním systémem. Tomu odpovídá i klasifikace farmak působících na vegetativní nervový systém.
Adrenergika (sympatomimetika, adrenomimetika) jsou léčiva aktivující adrenergní receptory.
Antiadrenergika (sympatolytika, adrenolytika) jsou léčiva blokující adrenergní receptory.
Cholinergika (parasympatomimetika, cholinomimetika) jsou léčiva aktivující cholinergní receptory a látky inhibující acetylcholinesterázu.
Anticholinergika (parasympatolytika, cholinolytika) jsou léčiva blokující cholinergní receptory a látky působící jako reaktivátory acetylcholinesterázy.
Adrenergika
Sympatický nervový systém hraje důležitou roli při ovládání orgánů, jako je srdce, periferní krevní řečiště a respirační trakt. Aktivace sympatiku noradrenalinem a adrenalinem zvyšuje činnost srdce, vasokonstrikcí zvyšuje krevní tlak a dilatací bronchů zlepšuje plicní ventilaci. Tyto účinky mají svůj význam především v zátěžových situacích. Adrenalin, potřebný k vyvolání uvedené odezvy, se v případě stresu uvolňuje z dřeně nadledvinek a krví je transportován k cílovým tkáním. Látky částečně nebo úplně napodobující účinky nor-adrenalinu a adrenalinu se nazývají adrenergika nebo sympatomimetika. Jelikož struktury většiny sympatomimetik jsou podobné strukturám přirozených neurotransmitérů katechol-aminového typu, považujeme za vhodné na tomto místě znovu připomenout struktury těchto katecholaminů a zároveň uvést ve zjednodušené podobě jejich biosyntézu (Schéma 8-1).

a) L-fenylalanin-hydroxyláza; b) L-tyrosin-hydroxyláza; c) L-DOPA-dekarboxyláza;
d) dopamin-b-hydroxyláza; e) N-methyltransferáza
Schéma 8-1 Biosyntéza katecholaminových neurotransmitérů
Adrenergních receptorů existuje celá
řada. Rozvoj farmakologie vedl k jejich detail-nějšímu rozlišení, podle
selektivní odpovědi na různé typy agonistů a antagonistů. Jednotlivé podtypy
jsou označovány řeckými písmeny a čísly (a a b b apod.). Přesná charakteristika
těchto podtypů, jejich lokalizace v organismu a jejich vliv na funkci
příslušných orgánů přesahuje rámec těchto skript. Spokojíme se proto pouze s
velmi zjednodušeným konstatováním, že stimulace a-receptorů tzv. a-adrenergiky způsobuje převážně
vasokonstrikci a hypotenzi, stimulace b -receptorů tzv. b -adrenergiky podporuje především zvýšení síly a frekvence stahů srdce
(tachykardie) a stimulace b -receptorů
b -adrenergiky má bronchodilatační účinky.
|
|
Většina v praxi používaných
adrenergik má skelet b-fenethylaminu.
Charakter účinku (a-, resp. b-adrenergní) určuje především typ aminoskupiny. Primární aminy (R3
= H) vyka-zují selektivní účinek na a-receptory,
zatímco aminy sekundární jsou prakticky bez výjimky
b-adrenergiky. Deriváty s prodlouženým alifatic-kým řetězcem (Y =
alkyl) mají protrahovaný účinek. Pro presorickou aktivitu a-adrenergik jsou nezbytné
hydroxylové skupiny vázané na aromatickém jádře. Odstranění jednoho nebo obou
hydroxylů má za následek ztrátu afinity
k a-receptorům. Dalšími důsledky jsou zvýšení lipofility (a tím i
snazší pronikání do CNS přes hematoencefalickou bariéru - viz např. amfetamin, kap. 5.2.2 a 1.4) a
prodloužení doby účinku[2].
a-Adrenergika
Mezi a-adrenergiky zaujímají významné postavení zejména endoadrenergika (adrenergika přírodní,
organismu vlastní) - dopamin (1, 2-(3,4-dihydroxyfenyl)ethylamin,
DOPAMIN, TENSAMIN, CARDIOSTERIL), norepinefrin
(noradrenalin) (2,
2-amino-1-
-(3,4-dihydroxyfenyl)ethanol, NORADRENALIN, ARTERENOL) a epinefrin (adrenalin) (3,
1-(3,4-dihydroxyfenyl)-2-(methylamino)ethanol, ADRENALIN). Uvedené látky se
podávají v případech akutních srdečních nedostatečností a zástav srdeční
činnosti, různých forem šoku, těžkých hypotenzí apod. S ohledem na použití v
akutních případech a s ohledem na rychlou biodegradaci se látky 1 - 3 podávají výhradně intravenózně.
Syntéza dopaminu 1 vychází z 1,2-dimethoxybenzenu (veratrolu), který chlor-methylací poskytne benzylchlorid 4. Po převedení na nitril a katalytické hydrogenaci se získá amin 5. Posledním stupněm syntézy je deprotekce hydroxylových skupin účinkem bromovodíku (Schéma 8-2).

a) CH2=O, HCl, ZnCl2; b) KCN; c) H2, Ra-Ni; d) HBr
Schéma 8-2 Syntéza dopaminu 1
Adicí kyanovodíku na veratrový aldehyd a redukcí vzniklého
kyanhydrinu 6 násle-dovanou
demethylací se získá racemický noradrenalin 2. Přirodní (R)-(-)-isomer je 2 - 3x účinnější než racemát. Lze jej
připravit štěpením racemátu (+)-vinnou kyselinou
(Schéma 8-3).

Schéma 8-3 Syntéza norepinefrinu (noradrenalinu) 2
Syntéza epinefrinu (adrenalinu) 3 vychází z pyrokatecholu, který po
acylaci chloracetylchloridem, substituci chloru methylaminem a redukci poskytne
racemický adrenalin. Podobně jako v předchozím případě lze z racemátu získat
účinnější levotočivý
(R)-isomer štěpením kyselinou (+)-vinnou. (S)-(+)-Adrenalin zbylý po štěpení
lze recyklovat oxidací na keton 7
(Schéma 8-4).
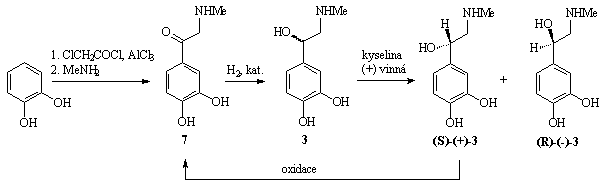
Schéma 8-4 Syntéza epinefrinu (adrenalinu) 3
Působení uvedených endoadrenergik 1 - 3 není zcela selektivní, neboť v organismu jsou
'univerzálními' neurotransmitéry, stimulujícími víceméně všechny typy
adrenergních receptorů. Na rozdíl od
nich a-exoadrenergika (syntetická analoga
přirozených adrenergik) vykazují selektivní účinky pouze na a-receptory. Jako příklady uvádíme korbadrin (8a,
(R)-(-)-2-amino-1-(3,4-dihydroxyfenyl)-1-propanol, CORBASIL, NORDEFRIN) a meta-raminol (8b, (R)-(-)-2-amino-1-(3-hydroxyfenyl)-1-propanol, ARAMINE,
PRESSONEX), které se připravují z propiofenonů 9a,b nitrosací (po
ochránění hydroxylových skupin benzylací), redukcí isonitrosoderivátu 10, hydrogenolýzou benzylové skupiny a
rezolucí pomocí kyseliny (+)-vinné. Syntézy obou látek se liší pouze v přípravě
propiofenonů 9 (Schéma 8-5).

Schéma 8-5 Syntéza korbadrinu 8a a metaraminolu 8b
b -Adrenergika
b -Adrenergika podporují především
srdeční činnost (zvýšení kontraktility srdečního svalu a frekvence stahů). Dále
působí na hladké svalstvo cév (vasodilatancia). Pro tyto účinky se používají
při léčení srdečních nedostatečností, infarktu myokardu a anginy pectoris
(kap. 10.3.3). Jako zástupce této skupiny léčiv uvádíme oxyfedrin (11,
(2'R,1'S)-3-[[(2-fenyl-
-2-hydroxy-1-methyl)ethyl]amino]-1-(3-methoxyfenyl)-1-propanon, ILDAMEN,
MYOFED-RIN) a poměrně nový preparát dobutamin
(12, ( )
4-[2-[[[3-(4-hydroxyfenyl)-1-methyl-propyl]amino]ethyl]-1,2-benzendiol,
DOBUTREX, INOTREX).
Oxyfedrin 11 se připravuje Mannichovou reakcí z (1R,2S)-(-)-norefedrinu, para-formaldehydu a m-methoxyacetofenonu (Schéma 8-6).

Schéma 8-6 Syntéza oxyfedrinu 11
Syntéza dobutaminu 12 vychází
z anisolu. Acylací chloridem kyseliny trans-2-
-butenové (krotonoylchloridem), Michaelovou adicí homoveratrylaminu 13 a redukcí karbonylové skupiny dle
Clemmensena se připraví amin 14,
který demethylací fenolických hydroxylových skupin bromovodíkem poskytne
dobutamin 12 (Schéma 8-7).

Schéma 8-7 Syntéza dobutaminu 12
b -Adrenergika
Nejvýznamnější skupinou mezi b-adrenergiky (co do počtu látek, i co do terapeutického významu) jsou b -adrenergika, která pro své bronchodilatační účinky nacházejí uplatnění především v terapii astmatu. Na rozdíl od b -adrenergik, vyznačujících se delším řetězcem na dusíku, jsou b -adrenergika N-substituována sekundární či terciární alkylovou skupinou.
První známou látkou této skupiny byl
isoprenalin (15a, 1-(3,4-dihydroxyfenyl)-2-
-(isopropylamino)ethanol, ISOPRENALIN, EUSPIRAN, ALUDRIN). Jedná se vlastně o
homolog epinefrinu 3, a proto se
syntetizuje zcela analogicky (Schéma 8-8). Podobně se syntetizuje i kolterol (15b, 2-(terc.butylamino)-1-(3,4-dihydroxyfenyl)ethanol).
Chránící benzylová skupina se odštěpuje hydrogenolyticky zároveň s redukcí
karbonylové skupiny (Schéma 8-8).
R1
15a
isoprenalin
i-Pr
15b
kolterol
t-Bu

Schéma 8-8 Syntéza isoprenalinu 15a a kolterolu 15b
Vyšší metabolickou stabilitu než uvedené deriváty pyrokatecholu, a tím i delší (protrahovanou) účinnost mají deriváty resorcinolu. Jako zástupce této skupiny uvádíme orciprenalin (metaproterenol) (16, 1-(3,5-dihydroxyfenyl)-2-(isopropylamino)ethanol, ASTMOPENT, ALUPENT). Výchozí látkou je 3,5-diacetoxyacetofenon, který se bromem převede na příslušný fenacylbromid. Ten se po substituci isopropylaminem a hydrolýze chránících acetylových skupin redukuje vodíkem na palladiu či Raneyově niklu (Schéma 8-9).

Schéma 8-9 Syntéza orciprenalinu 16
Stabilnější a zároveň i aktivnější
jsou deriváty, které mají fenolický hydroxyl v polo
ze 3 nahrazen skupinou hydroxymethylovou. Jako příklad může posloužit salbutamol
(17, 2-(terc.butylamino)-1-[4-hydroxy-3-(hydroxymethyl)fenyl]ethanol,
SULTANOL, VEN-TOLIN). Salbutamol 17
se připravuje acylací methylsalicylatu chloracetylchloridem, nukleofilní
substitucí chloru N-benzyl-terc.butylaminem
a redukcí karboxylu a fenonového karbonylu. Posledním stupněm syntézy je
hydrogenolytické odstranění chránicí benzylové skupiny (Schéma 8-10).

Schéma 8-10 Syntéza salbutamolu 17
Nepřímá adrenergika
Nepřímá adrenergika jsou látky,
které zvyšují v místě účinku koncentraci neurotransmitéru (noradrenalinu 2 v zakončeních sympatiku, resp.
dopaminu 1 v CNS) tím, že brzdí
jejich odbourávání (inhibitory MAO - kap. 5.2.1) nebo brzdí jejich zpětné
ukládání do zásobních vesikul v nervových synapsích. Nejvýznamnějšími představiteli
jsou deriváty
2-amino-3-fenylpropanu, a to amfetamin (18, 2-amino-3-fenylpropan, PSYCHOTON) a
efedrin (19, (1R,2S)-(-)-1-fenyl-2-(methylamino)propanol, ephedrin). Zatímco amfetamin 18 učinkuje výhradně jako nepřímé
andrenergikum s výraznými psychostimulačními účinky, které proniká díky své
lipofilitě snadno do CNS (kap. 5.2.2 a kap.1), efedrin 19 má výraznější b-adrenergní
(bronchodilatační) účinky a používá se k léčení astmatu a jiných dýchacích
potíží. Syntézy amfetaminu 18 i
efedrinu 19 byly již uvedeny v kap.
5.2.2.

Antiadrenergika
Antiadrenergika (sympatolytika,
adrenolytika) jsou látky, které působí v cílových orgánech jako antagonisté
neurotransmitérů katecholaminového typu. Podle mechanismu účinku se dělí na přímá, blokující přímo adrenergní receptory, a nepřímá, zasahující do biosyntézy katecholaminů, do procesu jejich
uvolňování či zpětného ukládání do presynaptických zakončení sympatiku. Podle
selektivity k typu receptoru se dělí na
a-antiadrenergika a b-antiadrenergika
a-Antiadrenergika
V této skupině léčiv zaujímají
dominantní postavení námelové alkaloidy,
produkované paličkovicí nachovou (Claviceps purpurea), houbou parazitující
na žitě. Námel vypěstovaný na žitě cíleně infikovaném paličkovicí nachovou je
jediným surovinovým zdrojem těchto alkaloidů. Námelové alkaloidy jsou deriváty
tetracyklického ergolenu, v jehož
struktuře je obsažen indolylethylamin. Vzájemné porovnání struktur ergolenu,
dopaminu
a serotoninu vysvětluje účinky námelových alkaloidů na adrenergní systém.

Námelové alkaloidy jsou amidy
kyseliny lysergové (20,
D-7-methyl-4,6,6a,7,8,9-
-hexahydroindolo[4,3-fg]chinolin-9-karboxylová kyselina); 'aminem' bývá tricyklický tripeptid 21, ve kterém jednou z aminokyselin je
prolin. Jako příklad uvádíme ergotamin ((5' )-12'-hydroxy-2'-methyl-(fenylmethyl)-8 -ergotaman-3',6',18-trion; ve vzorci 21 R1 =
= methyl, R2 = benzyl; CORNUTAMIN, součást přípravků ERGUTERIN a
ERGOFEIN, používaných jako uterotonikum[3],
resp. antimigrenikum).
|
|
|
Ergometriny jsou jednoduché amidy kyseliny lysergové, získávané převážně
polosyntetickou cestou z kyseliny lysergové 20 (Schéma 8-11). Takto se připravují např. ergometrin (22a, [8a(S)]-9,10-didehydro-N-(2-hydroxy-1-methylethyl)-6-methylergolin-8-
-karboxamid) a methylergometrin (22b, [8a(S)]-9,10-didehydro-N-(2-hydroxy-1-ethylethyl)-
-6-methylergolin-8-karboxamid) používané jako uterotonika.

Schéma 8-11 Syntéza ergometrinu 22a a methylergometrinu 22b
Přírodní i polosyntetické námelové alkaloidy vykazují bohatou škálu účinků. Kromě výše uvedeného použití (uterotonika a antimigrenika) působí řada z nich jako vasokonstrikční i jako vasodilatační agens, dopaminergika ovlivňující CNS apod. N,N-Diethylamid kyseliny lysergové je proslulý svou halucinogenní a psycholytickou aktivitou (LSD).
b-Antiadrenergika
Na rozdíl od a-antiadrenergik se struktury blokátorů b-adrenergních receptorů podstatně více podobají struktuře přirozených agonistů.
Arylethylaminy
se uplatňují především jako antihypertenzíva. Nejznámějším a nej-používanějším
farmakem z této skupiny je labetalol 23,
podávaný jako směs všech čtyř stereoisomerů. Stereoisomery S,S- a R,S- jsou
prakticky inaktivní, R,R- stereoisomer je
b-adrenolytikem a S,R-stereoisomer je a-adrenolytikem. Jedná se tedy o antihypertenzivum
s vyváženou a- a b-adrenolytickou aktivitou, působící jednak jako periferní
vasodilatans
(S,R-), jednak tlumící kontraktilitu srdečního svalu (R,R-). Syntéza labetalolu
23 je popsána
v kap. 10.4.1.

K antihypertenzním b-adrenolytikům arylethylaminového typu se často řadí i methyl-dopa (24, L-(-)-3-(3,4-dihydroxyfenyl)-2-amino-2-methylpropanová
kyselina, DOPEGYT, ALDOMET), třebaže bylo prokázáno, že účinným agens není
kyselina sama, nýbrž a-methyl-noradrenalin,
na který je v organismu dekarboxylována a který působí na a-receptory podobně jako
klonidin (kap. 10.4.1). Methyldopa 24
se připravuje z (3,4-dimethoxyfenyl)acetonitrilu, který kondenzací s
ethylacetatem, hydrolýzou a ketonotvorným štěpením poskytne keton 25. Ten s kyanidem draselným a
uhličitanem amonným cyklizuje na hydantoin 26,
jehož hydrolýza poskytne racemický derivát methyldopy 27. L-Methyldopa 24 se
získá po
N-acetylaci látky 27 rezolucí a
deprotekcí (Schéma 8-12).

a) AcOEt, EtONa; b) H+, H2O; c) KCN, (NH4)2CO3; d) Ba(OH)2; e) H+;
f) Ac2O; g) rezoluce; h) HBr, H2O
Schéma 8-12 Syntéza methyldopy 24
Zjištění, že b-antiadrenergní aktivita se nezmění, vloží-li se mezi aromatické
jádro a aminoethanolový zbytek oxymethylenová skupina, vedlo k přípravě celé
řady b-adrenolytik obecné struktury 28, tzv. aryloxyaminopropanolům. V této skupině nalezneme jak neselek-tivní b-adrenolytika působící na všechny typy b-adrenergních receptorů, tak kardioselektivní b -blokátory. Neselektivními b-adrenolytiky jsou např. propranolol (28a, 1-isopropylamino-
-3-(1-naftyloxy)-2-propanol, INDERAL), používaný při angině pectoris, srdečních
arytmiích a hypertenzi a metipranolol
(28b,
1-(4-acetoxy-2,3,5-trimethylfenoxy)-3-isopropylamino-2-
-propanol, TRIMEPRANOL), původní český preparát, používaný podobně jako
propranolol 28a. Kardioselektivním b-blokátorem je např. metoprolol
(28c,
1-isopropyl-amino-3-[4-(2-methoxyethyl)fenoxy]-2-propanol, VASOCARDIN,
BETALOC), používaný při hypertenzích, poruchách srdečního rytmu a angině
pectoris.
Aryloxyaminopropanoly se syntetizují
obecným postupem uvedeným ve Sché-
matu 8-13, zahrnujícím reakci příslušného fenolu s 2-chlormethyloxiranem
(epichlor-hydrinem) následovanou reakcí s isopropylaminem. Podle podmínek
reakce se buď nejprve substituuje atom chloru a teprve ve druhém reakčním
stupni dochází k nukleofilnímu otevření epoxidu nebo se nejprve otevřením
epoxidu získá chlorhydrin, ve kterém se provede nukleofilní substituce chloru
isopropylaminem.
|
Ar |
||
|
28a |
propranolol |
|
|
28b |
metipranolol |
|
|
28c |
metoprolol |
|


Schéma 8-13 Syntézy aryloxyaminopropanolů 28
Cholinergika
Cholinergika (parasympatomimetika,
cholinomimetika) jsou látky vyvolávající
v příslušných nervových zakončeních stejný účinek jako přirozený mediátor acetylcholin 29. Acetylcholin 29 je
nejrozšířenějším mediátorem v organismu, působícím nejen v post-gangliových
nervových vláknech parasympatiku, nýbrž i v gangliích a pregangliových
nervových vláknech parasympatiku i sympatiku. Účinky acetylcholinu 29 jsou proto velmi různorodé a podobně
široké spektrum účinků vykazují i cholinomimetika. Z hlediska mechanismu účinku
se cholinomimetika dělí na přímo
působící agonisty cholinergních receptorů a na nepřímo působící, zvyšující v synaptické oblasti koncentraci
acetylcholinu 29 inhibicí
acetylcholinesterázy.
Přímá cholinergika
Při studiu cholinergního systému
bylo zjištěno, že existují dva základní typy cholinergních receptorů, muskarinový a nikotinový. Jejich označení je dáno historicky, podle sloučenin, u
kterých byl pozorován agonistický účinek na cholinergní systém. Muskarin je alkaloid izolovaný z
muchomůrky červené (Amanita muscaria).
Muskarinové receptory se nacházejí převážně v efektorových tkáních (hladké
svalstvo, srdce, exokrinní žlázy ).
Nikotin, alkaloid izolovaný z tabáku
(Nicotiana tabacum), stimuluje
především receptory vegetativních ganglií a nervosvalových plotének (kap. 6).
Porovnáním struktur uvedených agonistů s příslušnou konformací acetylcholinu 29 je patrná jejich strukturní
příbuznost (nikotin je uveden v protonizované formě, ve které se nachází při
fyziolo-
gickém pH).

Muskarin a nikotin nemají praktický
terapeutický význam pro svoji toxicitu. Acetylcholin má omezené použití
vzhledem ke své nízké stabilitě; v krvi je rychle hydrolyzován celou řadou
nespecifických esteráz. Zpomalení rychlosti štěpení a zvýšení stability však
lze dosáhnout modifikací jeho strukury, a to buď v cholinové (alkoholické)
části nebo záměnou acetylové skupiny za karbamoyl. Jako příklady lze uvést methacholin
(30,
N-[2-(acetyloxy)propyl]trimethylamoniumchlorid, PROVOCHOLIN), karbachol (31a, N-[2-(karbamoyloxy)ethyl]trimethylamoniumchlorid, MIOSTAT) a bethanechol (31b, N-[2-
-(karbamoyloxy)propyl]trimethylamoniumchlorid, MYOCHOLIN, MYONACHOL,
URO-CHOLIN). Uvedené látky nalezly uplatnění především v očním lékařství při
léčení glaukomu a
dále při léčbě atonií
hladkého svalstva gastrointestinálního traktu a močového měchýře (bethanechol 31b).
Acetylcholin se připravuje acetylací
cholinu 32 získaného nukleofilním
otevřením oxiranu trimethylaminem (Schéma 8-14). Účinkem fosgenu na cholin 32 se získá chlorformiat, jehož
amonolýza poskytne karbachol 31a.
Alternativní syntézu karbacholu 31a,
použitelnou rovněž pro přípravu bethanecholu 31b, představuje reakce chlorhydrinu 33
s fosgenem, následovaná amonolýzou a kvarternizací vzniklého karbamatu
trimethylaminem. Z chlorhydrinu 33b lze
připravit též methacholin 30,
kvarternizací trimethylaminem následovanou acetylací (Schéma 8-14).

Schéma 8-14 Syntézy přímých cholinergik
Nepřímá cholinergika - inhibitory acetylcholinesterázy
Acetylcholinesteráza patří mezi tzv. serinové hydrolázy (Schéma 8-15). Nukleofilem atakujícím esterovou funkci acetylcholinu je deprotonizovaný hydroxyl aminokyseliny serinu (tzv. esteratické centrum enzymu). Vysokou afinitu acetylcholinu k enzymu zajišťuje coulombická interakce mezi kvartérním dusíkem substrátu a karboxylátovým aniontem asparagové kyseliny (tzv. anionické centrum).

Schéma 8-15 Mechanismus štěpení acetylcholinu acetylcholinesterázou.
Inhibitory acetylcholinesterázy mohou být principiálně dvojího druhu. První typ coulombickou interakcí obsadí anionické centrum enzymu, a tak brání přístupu acetylcholinu. Jedná se o kompetitivní inhibici, při které se nevytváří mezi inhibitorem a enzymem kovalentní vazba a proces je tedy vratný (reverzibilní). Druhý typ reaguje s esteratickým centrem. Vzniklá kovalentní vazba mezi inhibitorem a enzymem může být za fyziologických podmínek natolik stabilní, že se pak jedná o inhibici nevratnou (ireverzibilní).
Nejstarším známým nepřímým
cholinergikem je fysostigmin (34, PHYSOSTIGMIN, ANTICHOLIUM), který
se izoluje z kalabarských bobů (Physostigma
venenosum). Za fyziologických podmínek je protonizován na dusíku v poloze
1, a proto interaguje
s anionickým centrem acetylcholinesterázy. Kromě toho je jeho karbamatová
skupina transesterifikována serinovým hydroxylem (Schéma 8-16). Přestože v
tomto případě vzniká kovalentní vazba s esteratickým centrem enzymu, nejedná se
o ireverzibilní inhibici, neboť vzniklý karbamat acetylcholinesterázy se
postupně za fyziologických podmínek hydrolyzuje.
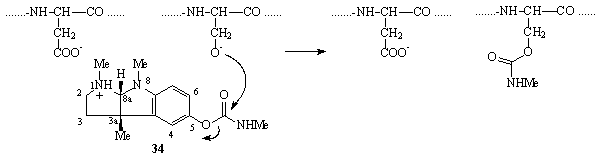
Schéma 8-16 Fysostigmin 34 a mechanismus jeho účinku na acetylcholinesterázu
Syntetickými karbamatovými cholinergiky jsou neostigminbromid (35, [3-dimethyl-aminokarbonyloxy)fenyl]trimethylamoniumbromid, SYNTOSTIGMIN, NEOSTIGMIN) a pyridostigminbromid (36, 3-(dimethylaminokarbonyloxy)-1-methylpyridiniumbromid, KA-LYMIN, REGONOL). Neostigminbromid 35 se připravuje z 3-dimethylamino-benzensulfonové kyseliny alkalickým tavením, převedením vzniklého 3-dimethylaminofenolu fosgenem na chlorformiat, aminolýzou a kvarternizací methylbromidem (Schéma 8-17). Analogicky se z 3-hydroxypyridinu připraví pyridostigminbromid 36 (Schéma 8-17).

Schéma 8-17 Syntéza karbamátových cholinergik
Příkladem nepřímého cholinergika, interagujícího pouze s anionickým centrem acetylcholinesterázy, je edrofoniumchlorid (37, N-(3-hydroxyfenyl)ethyldimethyl-amoniumchlorid, ENLON, TENSILON), dostupný kvarternizací m-(dimethylamino)fenolu, meziproduktu syntézy neostigminbromidu 35.

Všechna uvedená nepřímá cholinergika
se používají stejně jako cholinergika přímá
v očním lékařství a k léčení atonií gastrointestinálního traktu. Kromě toho
však slouží též jako antidota při předávkování nedepolarizujícími myorelaxancii.
V důsledku zvýšení koncentrace acetylcholinu v oblasti nervosvalových plotének
se 'vytěsní' inhibující myorelaxans -
- kap. 6.2.1.
Zvláštní skupinu inhibitorů acetylcholinesterázy tvoří reaktivní deriváty kyseliny fosforečné a fosfonové (obvykle nazývané souborně jako organofosfáty), které fosforylují, resp. fosfonylují serinový hydroxyl enzymu. Štěpení vazby P-O v inhibovaném enzymu probíhá za fyziologických podmínek nesmírně pomalu, takže uvedené látky lze považovat za ireverzibilní inhibitory acetylcholinestrázy. Terapeutický význam organofosforových sloučenin je (až na ojedinělé výjimky) nulový. Řada z těchto sloučenin se používá jako insekticida (např. paraoxon 38a, parathion 38b, malaoxon 39a a malathion 39b) a některé byly též vyráběny jako bojové chemické látky (např. sarin 40a, soman 40b). Ve strukturních vzorcích látek 38 - 40 jsou vyznačeny skupiny odstupující při fosfonylaci, resp. fosforylaci enzymu.
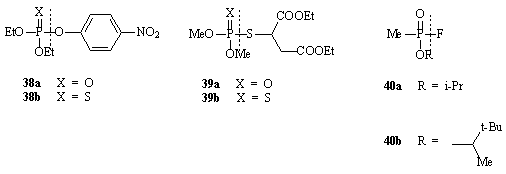
Je namístě zmínit zde stručně i látky, které se používají jako antidota při intoxikacích uvedenými vysoce toxickými sloučeninami fosforu, třebaže se de facto jedná o anti-cholinergika. Jsou to vesměs kvartérní a biskvartérní pyridiniové aldoximy, jako např. pralidoxim 41, trimedoxim 42a a obidoxim 42b. Tyto látky spolehlivě reaktivují inhibovanou acetylcholinesterázu, pokud jsou podány bezprostředně po intoxikaci.

Kvartérní pyridiniové aldoximy 41 a 42 se snadno připraví z příslušných pyridinkarbaldehydů reakcí s hydroxylaminem a kvarternizací vzniklých aldoximů (Schéma 8-18).
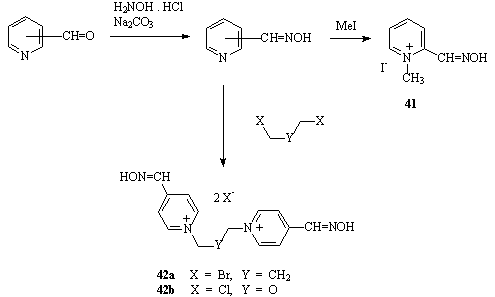
Schéma 8-18 Syntéza reaktivátorů acetylcholinesterázy
Mechanismus inhibice
acetylcholinesterázy a její reaktivace je znázorněn ve Sché-
matu 8-19. Oximátový anion vzniklý deprotonací poměrně kyselé
hydroxyiminoskupiny jako silný nukleofil atakuje atom fosforu. Výsledkem je
obnovení esteratického centra enzymu za současné fosfonylace oximu.

Schéma 8-19 Mechanismus inhibice acetylcholinesterázy sarinem a průběh její reaktivace účinkem pralidoximu
Anticholinergika
Anticholinergika (parasympatolytika, cholinolytika) kompetitivní inhibicí blokují účinek acetylcholinu a cholinomimetik v receptorech cílových orgánů (hladké svalstvo, srdce a exokrinní žlázy). Typickými vnějšími projevy působení anticholinergik jsou rozšíření zornic (mydriáza), zvýšená srdeční frekvence a snížená sekrece slz, slin a potu. Jedním z jejich nejvýraznějších účinků však je pokles napětí hladkého svalstva, čehož se využívá při uvolňování spasmů především u gastrointestinálního traktu. Tento typ léčiv se proto často označuje jako neurotropní či atropinová spasmolytika (na rozdíl od spasmolytik myotropních či muskulotropních (papaverinových) působících přímo na hladké svalstvo bez ovlivnění parasympatiku ).
Neurotropní a neurotropně-myotropní spasmolytika
Přírodními neurotropními
spasmolytiky jsou tropanové alkaloidy,
z nichž nejznámější je atropin (43, ester 3-tropanolu s kyselinou
(S)-2-fenyl-3-hydroxypropanovou, ATROPIN, součást přípravků BELLASPON,
SPASMOCYSTENAL a dalších). Hlavním zdrojem atropinu je rulík zlomocný (Atropa belladonna). Použití atropinu je
poměrně široké. Jeho mydriatického účinku se využívá k diagnostickým účelům v
očním lékařství. Vnitřně se používá jednak jako spasmolytikum při léčení kolik
zažívacího traktu, jednak jako antiparkinsonikum, neboť díky své lipofilitě
proniká snadno přes hematoencefalickou bariéru do CNS, kde svým
anticholinergním účinkem napomáhá znovuobnovení rovnováhy mezi účinky dopaminu
a acetylcholinu. Jako účinné anticholinergikum se rovněž používá
v kombinaci s trimedoximem 42a jako
antidotum při otravách organofosfáty.
Dalším známým přírodním anticholinergikem je skopolamin (44, 6,7-epoxyatropin, SCOPOLAMIN), který se izoluje z listů durmanu (Datura stramonium), jehož použití je obdobné jako u atropinu.

S jistou dávkou fantazie lze u
tropanových derivátů nalézt strukturní prvky acetylcholinu, a tak vysvětlit
jejich schopnost interagovat s cholinergními receptory (srovnej rovněž se
strukturou lokálních anestetik a myorelaxancií příčně pruhovaných svalů, kap.
6). Postupným zjednodušováním skeletu atropinu (Schéma 8-20) se dospělo k
syntetickým neurotropním spasmolytikům typu bazických esterů substituovaných
octových kyselin. Cílem uvedených strukturních zjednodušení nebyla pouze lepší
syntetická dostupnost, nýbrž
i zvýšení selektivity účinku. Alkaloidy tropanového typu jsou málo selektivní a
váží se prakticky na všechny typy muskarinových receptorů, jak ostatně dokazuje
šíře terapeutického využití atropinu.
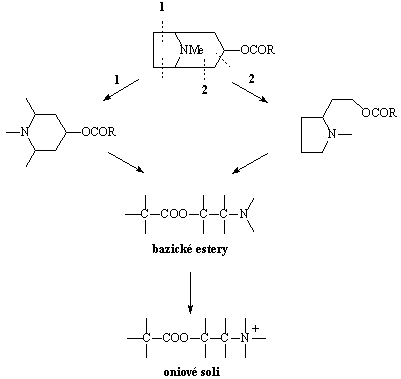
Schéma 8-20 Schéma zjednodušování tropanového skeletu
Z celé řady bazických esterů uvádíme pouze pro ilustraci adifenin 45a a drofenin 45b, neboť namísto tohoto typu farmak se dnes používají převážně spasmolytika typu oniových solí (viz dále).
|
R 45a adifenin fenyl 45b drofenin cyklohexyl
|
Kvarternizací farmak typu bazických
esterů se získají oniové soli, které mají vyšší spasmolytickou aktivitu díky
vyšší afinitě k receptorům jak muskarinového, tak nikotinového typu. Pro svůj
hydrofilní charakter tyto látky neprostupují přes hematoencefalickou bariéru,
a proto jsou prakticky prosty nežádoucích vedlejších účinků na CNS. Afinitu k
cholinergním receptorům vykazují nejen amoniové, nýbrž i sulfoniové soli.
Reprezentativními ukázkami spasmolytik typu oniových solí jsou např. oxyfenoniumbromid (46a,
2-[(cyklohexylfenyl-hydroxyacetyl)oxy]-N,N-diethyl-N-methylethanaminiumbromid,
OXYPHENON, ANTRE-NYL), hexasoniumjodid
(46b,
[2-[(cyklohexylfenylacetyl)oxy]ethyl]dimethylsulfoniumjodid, THIOSPASMIN) a poldinmethylsulfát (46c,
2-[[(difenylhydroxyacetyl)oxy]methyl]-1,1-
-dimethylpyrrolidiniummethylsulfat, NACTON). Uvedené látky nalezly uplatnění
nejen jako spasmolytika, nýbrž i jako antiulceróza (kap. 11.1.2), díky poměrně
selektivnímu antagonistickému působení na muskarinové receptory žaludeční
sliznice, vedoucímu
k potlačení sekrece žaludečních šťáv.
Oxyfenoniumbromid 46a se připravuje parciální hydrogenací benzilové kyseliny a esterifikací vzniklé a-cyklohexylmandlové kyseliny 47 diethylaminoethanolem. Posledním stupněm syntézy je kvarternizace esteru kyseliny 47 methylbromidem (Schéma 8-21).
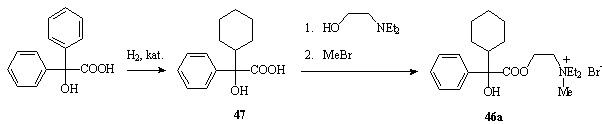
Schéma 8-21 Syntéza oxyfenoniumbromidu 46a
Hexasoniumjodid 46b se připravuje z kyseliny cyklohexylfenyloctové. 2-Methyl-thioethylester 48 (připravený buď O-alkylací sodné soli kyseliny 47 2-chlorethylmethyl-sulfidem nebo reakcí jejího chloridu s 2-methylthioethanolem) se alkyluje methyljodidem (Schéma 8-22).

Schéma 8-22 Syntéza hexasoniumjodidu 46b
Výchozí látkou syntézy
poldinmethylsulfátu 46c je
diethylglutamat, který termickou cyklizací a redukcí poskytne
2-pyrrolidinylmethanol (49).
Eschweilerovou-Clarkovou methylací a reakcí s chloridem thionylu se získá
pyrrolidinový derivát 50, kterým se
O-alkyluje sodná sůl benzilové kyseliny. Kvarternizace vzniklého esteru
dimethylsulfatem poskytne poldinmethylsulfát 46c (Schéma 8-23).

Schéma 8-24 Syntéza poldinmethylsulfátu 46c
Od výše uvedených anticholinergik se
strukturně odlišuje pirenzepin
(51,
5,11-dihydro-11-[(4-methyl-1-piperazinyl)acetyl]-6H-pyrido-(2,3-b)(1,4)-benzodiazepin-
-6-on, GASTROZEPIN), který (přestože spíše připomíná tricyklická antidepresiva)
je selektivním inhibitorem muskarinových cholinergních receptorů (tzv. typu M1)
žaludečního traktu a potlačuje sekreci žaludečních šťáv. Je proto významným
antiulcerózem doplňujícím H2 antihistaminika. Jeho syntézu uvádíme v
kap. 11.1.2.

Myotropní spasmolytika
Na tomto místě uvádíme i některá
známější myotropní spasmolytika, třebaže se jedná o farmaka, která neovlivňují
vegetativní nervový systém, nýbrž působí přímo na hladké svalstvo. Většina z
nich patří k derivátům isochinolinu a jejich nejznámějším zástupcem je alkaloid
papaverin (52, 1-(3,4-dimethoxybenzyl)-6,7-dimethoxyisochinolin, PAPAVERIN,
součást přípravků SPASMO-EUNALGIT, SPASMOVERALGIN a dalších). Papaverin je
v malé míře obsažen v opiu. Tento surovinový zdroj však nestačí krýt jeho
spotřebu, a proto se většina papaverinu získává postupem, jehož základem je
Bischlerova-Napieralského syntéza isochinolinu. Výchozí látkou je veratrol,
který chlormethylací a reakcí s kyanidem poskytne nitril 53. Ten se jednak redukuje na amin 54, jednak hydrolyzuje na kyselinu 55. Zahřátím kyseliny 55
s aminem 54 na teplotu cca 160 oC
vznikne amid 56, který cyklizací
účinkem fosforoxytrichloridu a následující dehydrogenací na palladiu poskytne
papaverin 52 (Schéma 8-24). Podobným
způsobem se připravují i další, od papaverinu odvozená myotropní spasmolytika
isochinolinového typu.

Schéma 8-24 Syntéza papaverinu 52
Hlavové nervy (např. trojklanný, bloudivý apod.) nevycházejí z míchy, nýbrž přímo z mozku.
b-Fenethylaminy, které nemají aromatické jádro substituováno hydroxylovými skupinami (zejména v poloze 3), nemohou být biotransformovány mechanismem, jehož prvním stupněm je methylace hydroxylové skupiny účinkem katechol-O-methyltransferázy (COMT).
Uterotonika jsou látky způsobující kontrakci děložního svalstva
Žlázy mající vývod buď na povrch těla nebo do dutiny některého orgánu, např. žlázy potní, slinné, žlázy vylučující žaludeční šťávy apod.
Tzv. zelený zákal, jehož průvodním jevem je zvýšený nitrooční tlak. Jedním z účinků cholinergik je kontrakce zornice (mióza), při které může lépe odtékat nitrooční mok z přední oční komory; důsledkem je pokles nitroočního tlaku.
pokles napětí, ochablost
křečovitých stahů
Na rozdíl od přírodních látek atropinu a papaverinu není možno většinu syntetických spasmolytik jednoznačně zařadit pouze do jedné z uvedených skupin, neboť často vykazují současně neurotropní i myotropní aktivitu.
Tato látka má přibližně stejnou toxicitu jako yperit.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 5311
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2024 . All rights reserved