| CATEGORII DOCUMENTE |
| Bulgara | Ceha slovaca | Croata | Engleza | Estona | Finlandeza | Franceza |
| Germana | Italiana | Letona | Lituaniana | Maghiara | Olandeza | Poloneza |
| Sarba | Slovena | Spaniola | Suedeza | Turca | Ucraineana |
UNIVERZITA P. J. ŠAFÁRIKA V KOŠICIACH
Prírodovedecká fakulta
Ústav chemických vied
RNDr. Miroslava Martinková, PhD., RNDr. Martin Humeník
Praktikum z organickej chémie I
Kryštalizácia je jednou z najpoužívanejších metód čistenia a delenia tuhých organických látok. Zakladá sa na rozdielnej rozpustnosti danej látky a jej prímesí vo vhodnom rozpúšťadle za rôznych teplôt (obyčajne za studena a pri teplote varu rozpúšťadla). Čistotu prekryštalizovanej látky posudzujeme podľa teploty topenia. Ak ostáva teplota topenia po viacerých kryštalizáciach nezmenená a ostrá (spravidla v rozmedzí 0-2oC), predpokladáme, že ide o čistú látku. Teplota topenia je teplota, pri ktorej je tuhá fáza v rovnováhe so svojou taveninou. Z praktického hľadiska teplotou topenia nazývame teplotu, pri ktorej prejde látka z kryštalického stavu na homogénnu kvapalinu. Pri jej ochladení prejde z kvapalnej do tuhej fázy pri rovnakej teplote (teplota tuhnutia).
Kryštalizácia acetanilidu a stanovenie jeho teploty topenia.
Úroveň
Čas 2 h
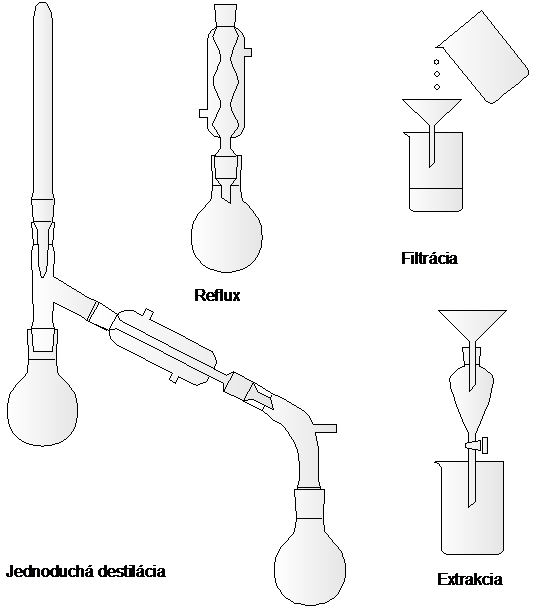
Príslušenstvo aparatúry pre: reflux, filtráciu, odsávanie
Chemikálie
|
Acetanilid (Mr 135,2, T.t. 113-115oC) |
1 g |
Xn - škodlivá |
|
H2O |
20 ml |
Postup práce
K 1 g acetanilidu (N-fenylacetamid) v 50 ml banke opatrenej spätným chladičom pridáme 20 ml vody a niekoľko varných kamienkov. Reakčnú zmes zahrejeme do refluxu. Ak sa všetka látka nerozpustila, pridáme cez spätný chladič ďalšie množstvo vody a opäť zmes zahrejeme do refluxu. Roztok prefiltrujeme cez skladaný filter do kadičky. Filtrát necháme ochladiť a vylúčené kryštály odsajeme na Büchnerovom lieviku. Získané kryštály necháme voľne vysušiť na vzduchu. Suché odvážime, vypočítame percentuálny výťažok kryštalizácie a stanovíme teplotu topenia.
Doporučená literatúra:
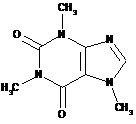
Použité aparatúry:

H a 13C NMR spektrum ACETANILIDU
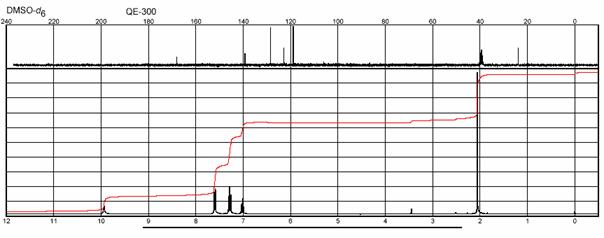
IČ spektrum ACETANILIDU
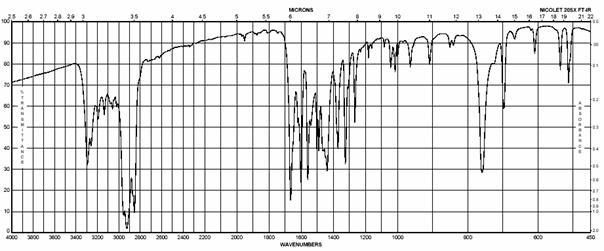
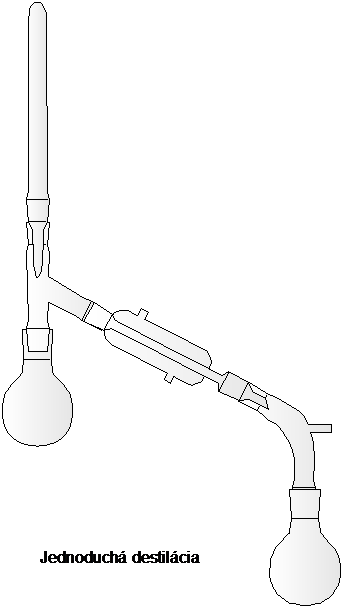
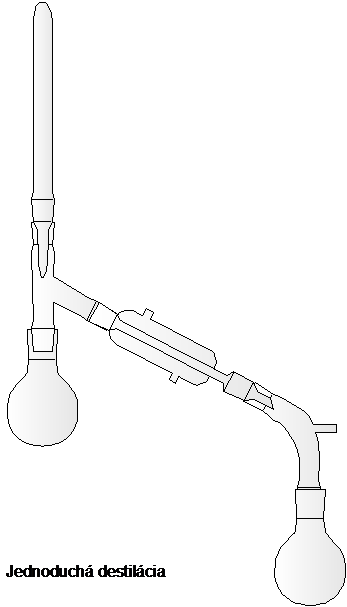
Destilácia je najdôležitejšia metóda čistenia a delenia kvapalných látok (alebo tuhých látok s nízkou teplotou topenia). Používa sa na oddelenie kvapalín od menej prchavých a neprchavých prímesí, alebo na oddelenie zmesí kvapalín s rôznou teplotou varu. V najjednoduchšom prípade sa kvapalina zahriatím do varu premieňa na paru, ktorá kondenzuje v chladiči na destilát. Pretože sa pritom pohybuje iba jedna fáza (para), hovoríme o jednoduchej destilácií. Zmesi látok s dostatočne rozdielnou teplotou varu možno už jednoduchou destiláciou rozdeliť na jednotlivé zložky – frakčná destilácia. Destiláciu možno uskutočniť za atmosferického alebo zníženého tlaku – vákuová destilácia.
Rozdelenie zmesi acetónu a vody, zostrojenie destilačnej krivky.
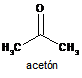
Úroveň
Čas 2 h
Príslušenstvo aparatúra pre: jednoduchú destiláciu
Chemikálie
|
acetón (T.v. 55-57oC) |
30 ml |
F – veľmi horľavá, Xi - dráždivá |
|
H2O |
30 ml |
Postup práce
V 250 ml varnej banke zmiešame 30ml vody a 30 ml acetónu. Pridáme varný kamienok, nasadíme zostupný chladič a pomaly destilujeme. Odoberáme 18 frakcií po 3 ml do odmerného valca a zaznamenávame teploty varu jednotlivých frakcií. Po skončení destilácie zostrojíme destilačnú krivku.
Doporučená literatúra:
Použitá aparatúra:
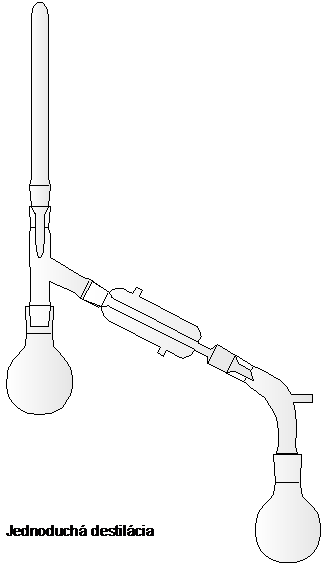
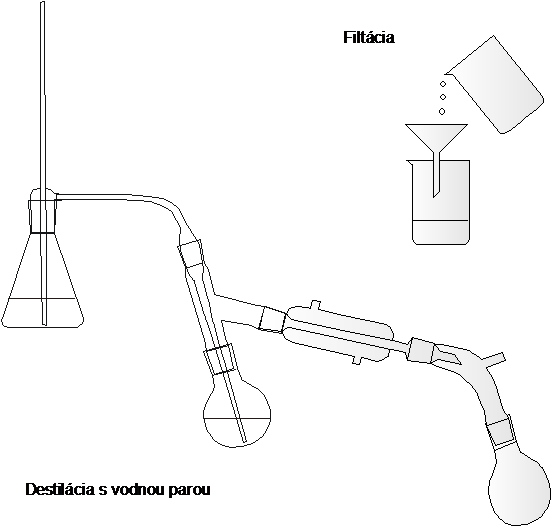
Destilácia s vodnou parou sa používa u vyššie vriacich organických kvapalín, ktoré sa
s vodou nemiešajú ani s ňou nereagujú a ktoré s vodnou parou prchajú – majú dostatočný tlak pár pri 100oC (aspoň 1 kPa). Teplota varu zmesi pri destilácii je vždy nižšia než teplota varu vody (platí Daltonov zákon). Aparatúra na destiláciu s vodnou parou má okrem častí známych z jednoduchej destilácie – destilačnej banky, chladiča a predlohy – naviac vyvíjač pary a nádstavec na preháňanie vodnou parou. Aparatúre chýba teplomer. Pri tejto destilácii sa vedie vodná para z vyvíjača čo najkratšou cestou do destilačnej banky. Para vzorku intenzívne premiešava a vyhrieva, pričom zo začiatku sama kondenzuje. Destilácia prebieha pomerne rýchle, a tak vyžaduje účinný chladič. Po skončení destilácie pevný produkt izolujeme z destilátu filtráciou, kvapalný produkt extrakciou.
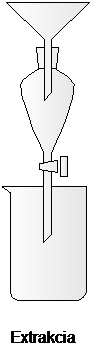
Extrakcia je metóda na delenie zmesi látok na základe rozdielnej rozpustnosti látok v dvoch vzájomne nemiešateľných rozpúšťadlách (obvykle voda a organické rozpúšťadlo). Najjednoduchšou formou extrakcie je vytrepávanie a robí sa spravidla v oddeľovacom lieviku.
Úroveň
Čas 4 h
Príslušenstvo aparatúry pre: destiláciu s vodnou parou, extrakciu, filtráciu, jednoduchú destiláciu
Chemikálie
|
anilín (T.v. 184oC) |
T- jedovatá, N- nebezpečná pre životné prostredie |
|
|
brómbenzén (T.v. 156oC) |
Xi- dráždivá, N – nebezpečná pre životné prostredie |
|
|
chloroform |
Xn – škodlivá, dráždivá, karcinogénna |
|
|
hydroxid sodný |
C- žieravá |
|
|
Zriedená kyselina chlorovodíková (1:1) |
C- žieravá |
|
|
síran sodný bezvodý (sušidlo) |
- |
|
|
chlorid sodný |
- |
Postup práce
Máme vzorku, ktorá je zmesou anilínu a brómbenzénu. Obe uvedené zlúčeniny sú vo vode nerozpustné, s vodou sa nemiešajú, majú vysoké teploty varu, teda sú vhodné na destiláciu s vodnou parou. Našou úlohou je oddeliť ich navzájom.
Zriedenou kyselinou chlorovodíkovou (1:1) okyselíme vzorku na pH približne 5 (kontrolujeme pomocou indikátorového papierika). Brómbenzén s HCl nereaguje, ale anilín dáva s HCl anilíniumchlorid.
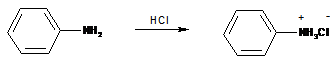
Anilíniumchlorid je kryštalická látka vo vode dobre rozpustná, ktorá s vodnou parou neprchá. Toto nám umožní jeho oddelenie od brómbenzénu. Destilačnú banku so vzorkou pripevníme k aparatúre a z kyslého prostredia pomocou vodnej pary vydestilujeme brómbenzén do destilačnej predlohy. Anilín vo forme anilíniumchloridu zostal v destilačnej banke rozpustený vo vode. Obsah destilačnej banky pridaním koncentrovaného roztoku NaOH (môže sa pridať aj pevný NaOH) zalkalizujeme na pH približne 11, čím uvoľníme anilín zo soli.
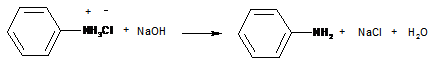
V destilácii s vodnou parou pokračujeme a z alkalického prostredia vydestilujeme do druhej predlohy anilín. Oba vydestilované roztoky nasýtime NaCl a separátne extrahujeme brómbenzén i anilín do chloroformu. Chloroformové roztoky vysušíme nad bezvodým síranom sodným a sušiace činidlo odfiltrujeme. Postavíme aparatúru na jednoduchú destiláciu a z vodného kúpeľa oddestilujeme z roztoku brómbenzénu chloroform. Anilín spracujeme analogicky. Obe látky odovzdáme ako surové produkty po oddestilovaní chloroformu. Odmeriame objemy produktov a stanovíme pomer oboch zložiek v zmesi.
Doporučená literatúra:
Organizácia cvičenia a metodické pokyny.
Študenti na 4-hodinovom cvičení izolujú zo zmesi len brómbenzén a stanovia jeho objem vo vzorke.
Študenti na 6-hodinovom cvičení izolujú obe látky a stanovujú objem jednotlivých zložiek a celkový objem.
Použité aparatúry:
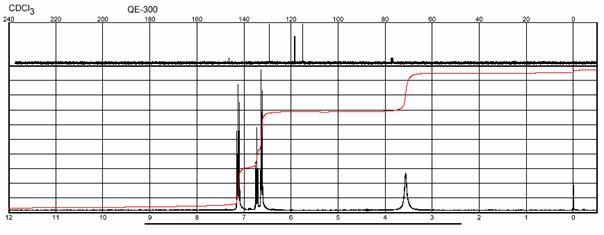
H a 13C NMR spektrum ANILÍNU
IČ spektrum ANILÍNU
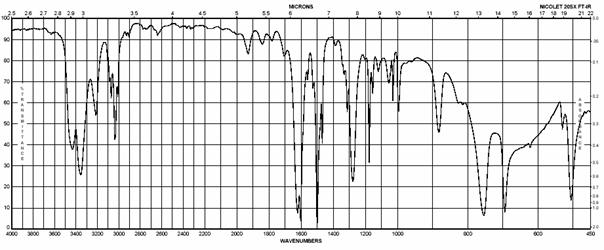
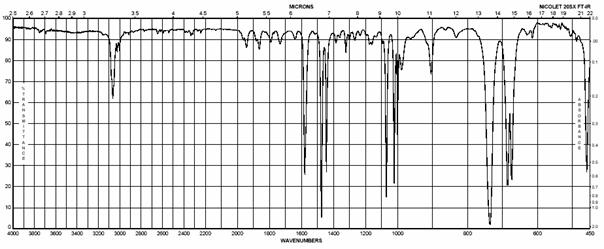
H a 13C NMR spektrum BRÓMBENZÉNU
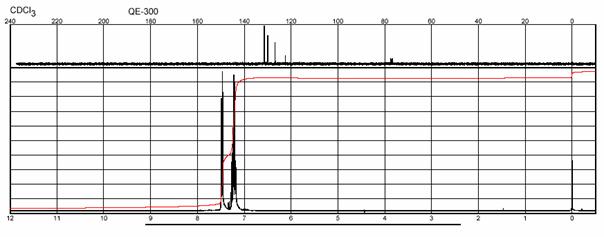
IČ spektrum BRÓMBENZÉNU
Estery karboxylových kyselín sú zvyčajne pripravené rekciou príslušnej karboxylovej kyseliny a alkoholu v prítomnosti kyslého katalyzátora (H2SO4, HCl, Lewisova kyselina) alebo reakciou funkčných derivátov karboxylových kyselín (chloridy a anhydridy) s alkoholmi. Estery sú veľmi často požívané v organickej syntéze, pretože esterová skupina môže byť jednoducho transformovaná na iné funkčné skupiny.
Octan etylový pripravíme esterifikáciou kyseliny octovej etanolom zahrievaním v prítomnosti kyseliny sírovej.

Úroveň
Čas 3 h
Príslušenstvo aparatúry pre: reflux, extrakciu, sušenie, filtráciu, destiláciu
Chemikálie
|
ľadová kyselina octová (Mr 60,1) |
15 g (0,25 mol) |
C - horľavá, žieravá |
|
etanol (96 %) |
20 ml |
F - veľmi horľavá |
|
H2SO4 (koncentrovaná) |
2,5 ml |
C - žieravá |
|
Na2CO3 (20-30 % vodný roztok) |
Xi - dráždivá |
|
|
CaCl2 (10 g v 12,5 ml H2O) |
Xi - dráždivá |
Postup práce
Do 250 ml jednohrdlovej banky dáme 15 g (14,3 ml) ľadovej kyseliny octovej a 20 ml etanolu. Za miešania pomaly pridáme 2,5 ml kyseliny sírovej. Na banku dáme spätný chladič a reakčnú zmes refluxujeme 30 minút na vodnom kúpeli. Banku ochladíme vodou a namiesto spätného chladiča použijeme destilačný chladič a destilujeme z vodného kúpeľa. V destilačnej banke zostane nezreagovaná kyselina octová a kyselina sírová. Destilát prelejeme do oddeľovacieho lievika a premývame vodným roztokom uhličitanu sodného. Pri premývaní postupujeme opatrne, pretože sa vyvíja CO2. Organickú vrstvu premývame dovtedy, kým nereaguje neutrálne na lakmus. Oddelenú organickú vrstvu potom premyjeme roztokom chloridu vápenatého, vysušíme nad bezvodým síranom sodným, prefiltrujeme a destilujeme za normálneho tlaku. Zachytávame frakciu pri teplote 75-78oC (literatúra uvádza 76-77oC). Produkt odvážime a vypočítame výťažnosť.
Meranie a interpretácia IČ a 1H NMR spektier sa uskutoční v rámci praktického cvičenia č. 7.
Octan etylový), (Mr 88,1, ρ 0,9), (Xi – dráždivá, F – veľmi horľavá) je bezfarebná, príjemne voňajúca kvapalina (tzv. octová esencia.).
Doporučená literatúra:
Použité aparatúry:
H a 13C NMR spektrum OCTANU ETYLOVÉHO
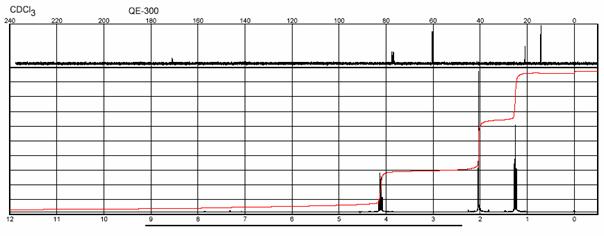
IČ spektrum OCTANU ETYLOVÉHO:
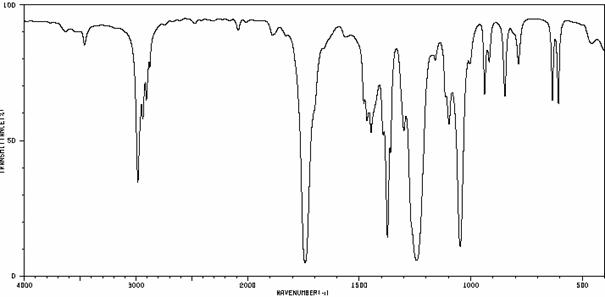
Kyselinu acetylsalicylovú pripravíme reakciou kyseliny salicylovej a anhydridu kyseliny octovej v prítomnosti kyseliny sírovej ako katalyzátora. Ide o esterifikačnú reakciu medzi hydroxyskupinou kyseliny salicylovej a acetanhydridom.
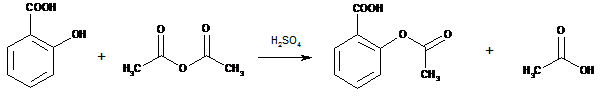
Úroveň 2
Čas 3 h
Príslušenstvo aparatúra pre: odsávanie
Chemikálie
|
kyselina salicylová (Mr 138,12) |
2,5 g (0,018 mol) |
Xn- škodlivá, dráždivá |
|
acetanhydrid (Mr 102,09, ρ1,082) |
5 ml (0,053 mol) |
C- škodlivá, žieravá |
|
kyselina sírová |
2 kvapky |
C - žieravá |
|
metanol |
2 ml |
F – veľmi horľavá, T - jedovatá |
Postup práce
Do 100 ml okrúhlej banky dáme 2,5 g kyseliny acetylsalicylovej, 5 ml anhydridu kyseliny octovej a 2 kvapky kyseliny sírovej. Reakčnú zmes dobre miešame. Teplota pritom samovoľne stúpa na 70-80oC a kyselina salicylová sa postupne rozpúšťa. Po 12-15 minútach teplota klesne na 35-40oC, pričom obsah banky stuhne. Do banky pridáme 25 ml vody a dobre rozmiešame. Produkt odsajeme na Büchnerovom lieviku, vysušíme, odvážime, vypočítame výťažnosť. Potom stanovíme teplotu topenia, ktorú porovnáme s údajom uvedeným v tabuľkách. Ak produkt nemá požadovanú čistotu prekryštalizujeme ho zo zriedenej kyseliny octovej (1:1).
Kyselina acetylsalicylová (Xn – škodlivá) je biela kryštalická látka s T.t. 138-140oC. Používa sa ako antipyretikum pod názvom Acylpyrín, alebo v kombinácií s kofeínom ako Acylcoffin. Jej identifikáciu uskutočňujeme pomocou chromatografie na tenkej vrstve (TLC) za použitia vyššie uvedených farmaceutických prípravkov ako štandardov.
Chromatografia na tenkej vrstve
Približne 0,1 g kyseliny acetylsalicylovej pripravenej na cvičení rozpustíme v 2 ml metanolu v malej skúmavke (roztoky štandardov Acylpyrínu a Acylcoffinu budú pripravené). Pre chromatografiu na tenkej vrstve použijeme Silufolové platničky LSL UV 254. Vystrihneme platničku 3 x 6 cm, označíme štart a poradie vzoriek. Na označené miesta nanesieme tenkou sklenenou kapilárou z každého roztoku tri krát. Platničku umiestnime do chromatografickej komôrky a vyvíjame v sústave hexán : octan etylový v pomere 1:3. Keď čelo rozpúšťadla dôjde na vzdialenosť 1 cm od horného okraja, platničku vyberieme a necháme voľne vysušiť. Identifikáciu robíme pomocou UV lampy pri vlnovej dĺžke 254 nm. Na silufolovej platničke budú tri fialové škvrny kyseliny acetylsalicylovej z jednotlivých vzoriek. Rovnaké RF hodnoty škvŕn potvrdzujú identitu látok. Charakteristická RF hodnota v danom vyvíjacom činidle pre kyselinu acetylsalicylovú je 0,85, pre kofeín z Acylcoffinu 0,04.
Doporučená literatúra:
Použitá aparatúra:
H a 13C NMR spektrum KYSELINY ACETYLSALICYLOVEJ
IČ spektrum KYSELINY ACETYLSALICYLOVEJ
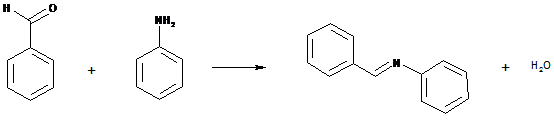
Pre úspešný priebeh adično-eliminačnej reakcie sú potrebné na atóme, ktorý atakuje karbonylový uhlík, dva ľahko odstupujúce substituenty – spravidla sú to vodíkové atómy. V takomto prípade pri eliminácií je odstupujúcou časticou voda. Tento typ reakcií sa často nazýva kondenzácia. Bežné adično-eliminačné reakcie aldehydov prebiehajú len s primárnymi amínmi, so sekundárnymi len v špecifických prípadoch. V reakcií vzniknuté azometíny sa nazývajú Schiffove zásady. Stabilné Schiffove zásady vznikajú z aromatických aldehydov a aromatických amínov.
Benzalanilín pripravíme reakciou benzaldehydu s anilínom.
Úroveň
Čas 2 h
Príslušenstvo aparatúra pre: odsávanie
Chemikálie
|
benzaldehyd (Mr 106,1, ρ 1,044) |
3,5 g (0,033 mol), 3,4 ml |
Xn - škodlivá |
|
anilín (Mr 93,1, ρ 1,022) |
3,1 g (0,033 mol), 3,0 ml |
T - jedovatá |
|
etanol (95 %) |
5,7 ml |
F – veľmi horľavá |
Postup práce
Do 50 ml okrúhlej banky dáme 3,5 g benzaldehydu a postupne za intenzívneho miešania pridáme 3,1 g čerstvo predestilovaného anilínu. Reakcia je exotermická. Po pridaní anilínu reakčnú zmes necháme stáť 15 minút a potom ju vlejeme za intenzívneho miešania do 5,7 ml etanolu v 100 ml kadičke. Postupne sa začnú vylučovať kryštáliky, pričom zmes necháme stáť asi 30 minút v ľadovej vode. Takmer tuhú hmotu odsajeme na Büchnerovom lieviku a necháme voľne sušiť na vzduchu. Zahustením kryštalizačnáho lúhu na polovicu pôvodného objemu za zníženého tlaku dostaneme ďalší podiel benzalanilínu. Zistíme výťažok a stanovíme teplotu topenia.
Benzalanilín (Mr 181,24, T.t. 52-54oC), (Xn – škodlivá)
Doporučená literatúra:
1. Kováč, J. a kol. Organická chémia, ALFA Bratislava 1992 (str. 588).
Použitá aparatúra:
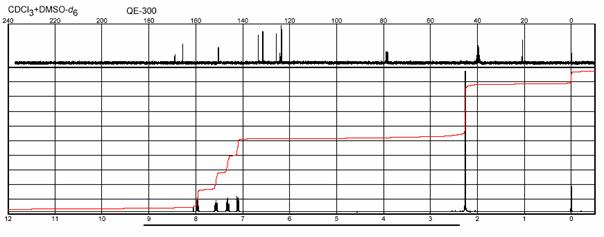
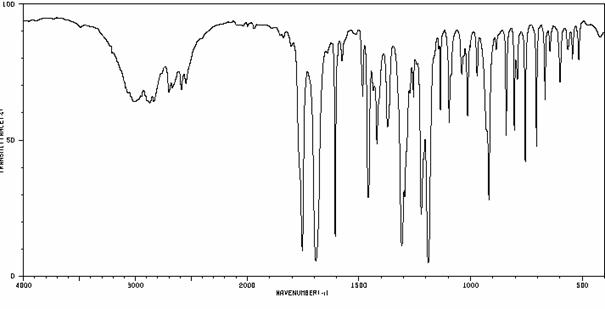
H a 13C NMR spektrum BENZALANILÍNU:
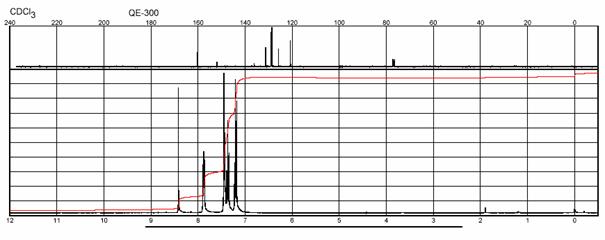
IČ spektrum BENZALANILÍNU:
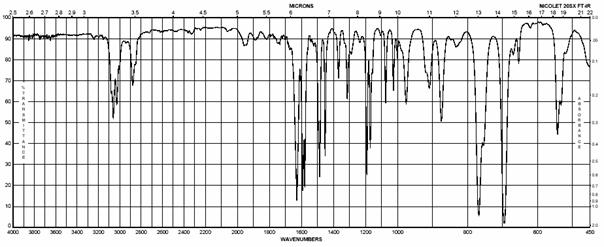
Princíp a použitie IČ a 1H NMR spektroskopie pre identifikáciu organických zlúčenín.
Organizácia cvičenia a metodické pokyny
Na tomto cvičení budú študenti oboznámení so základnými princípmi IČ a 1H NMR spektroskopie a zároveň budú namerané a interpretované IČ a 1H NMR spektrá octanu etylového pripraveného na praktickom cvičení č. 4.
Doporučená literatúra:
S hydroxylamínom (NH2OH) reagujú karbonylové zlúčeniny na oxímy. Rozoznávame aldoxímy, pripravené z aldehydov a ketoxímy, ktoré vznikli reakciou z ketónov. Acetofenónoxím (ketoxím) pripravíme reakciou acetofenónu s hydroxylamínom.
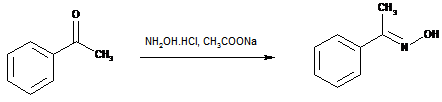
Úroveň
Čas 2 h
Príslušenstvo aparatúry pre: reflux, odsávanie
Chemikálie
|
acetofenón (Mr 120,15) |
3 ml (0,025 mol) |
Xn - škodlivá |
|
NH2OH.HCl (Mr 69,49) |
2 g (0,029 mol) |
Xn - škodlivá |
|
octan sodný (Mr 82,03) |
2,5 g (0.03 mol) | |
|
voda |
20 ml | |
|
etanol (95 %) |
2-5 ml |
F - veľmi horľavá |
Postup práce
Do 100 ml okrúhlej banky dáme 3 ml acetofenónu, 2 g hydroxylamínhydrochloridu, 2,5 g octanu sodného a 20 ml vody. Reakčnú zmes miešame, kým sa tuhé látky nerozpustia. Potom pridáme za miešania ešte 2-5 ml etanolu, aby sa rozpustil acetofenón. Obsah banky zahrievame na vriacom vodnom kúpeli 40 minút. Potom reakčnú zmes ochladíme studenou vodou a nakoniec ľadom. Vylúčené kryštáliky surového produktu odsajeme na Büchnerovom lieviku. Acetofenónoxím prekryštalizujeme z vody. Po vysušení zistíme výťažok a stanovíme teplotu topenia.
Acetofenónoxím Mr 135,16, T.t 58-60°C), (Xn – škodlivá)
Doporučená literatúra:
1. Kováč, J. a kol. Organická chémia ALFA, Bratislava 1992 (str. 588, 593).
Použité aparatúry:
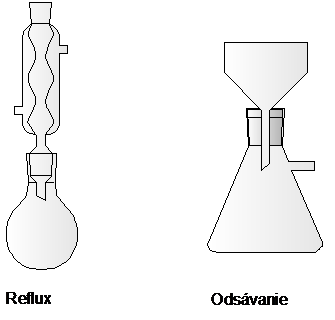
H a 13C NMR spetrum ACETOFENÓNOXÍMU:
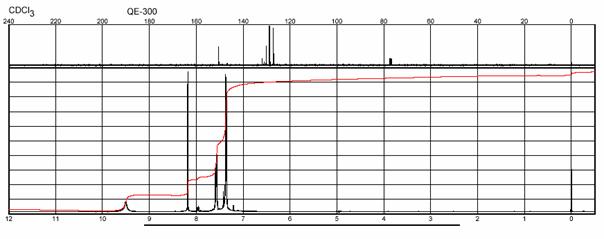
IČ spetrum ACETOFENÓNOXÍMU:
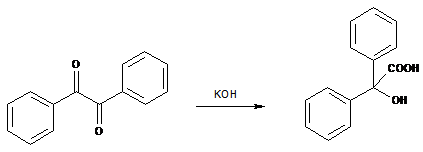
Kyselinu benzilovú pripravíme prešmykom benzilu v alkalickom prostredí. Hydroxylový anión atakuje uhlík jednej karbonylovej skupiny vicinálneho diketónu a vytvára O-anión. Tento anión sa môže buď rozložiť na pôvodné zložky, alebo odštiepiť arylanión, ktorý môže atakovať susednú karbonylovú skupinu, čím sa prešmyk skončí. Podľa východiskovej zlúčeniny benzilu sa táto reakcia nazýva benzilový prešmyk, ktorý prebieha pri všetkých aromatických a heterocyklických α-diketónoch.
Úroveň
Čas 2 h
Príslušenstvo aparatúry pre: reflux, filtráciu, odsávanie
Chemikálie:
|
benzil (Mr 210,2) |
2 g (0,01 mol) |
Xi - dráždivá |
|
etanol (96 %) |
5 ml |
F - horľavá |
|
hydroxid draselný (Mr 56,1) |
2 g (0,035 mol) |
C- žieravá |
Postup práce
K 2 g benzilu v 50 ml banke so spätným chladičom pridáme 5 ml etanolu a rozpustíme ho zahriatím na vodnom kúpeli. Potom prilejeme cez chladič po častiach vodný roztok KOH (2 g v 2 ml vody). Reakčnú zmes zahrievame na vriacom vodnom kúpeli 30 minút. Už asi po 5 minútach sa vylúčia kryštáliky draselnej soli kyseliny benzilovej, niekedy však soľ zostane v presýtenom roztoku a vylúči sa až neskoršie. Po ochladení sa vylúčené kryštáliky odsajú a čo najdokonalejšie zbavia kryštalizačného lúhu. Soľ potom rozpustíme v 10 ml horúcej vody, roztok odfiltrujeme od nezreagovaného benzilu a číry filtrát okyselíme potrebným množstvom zriedenej kyseliny chlorovodíkovej (1:1) na pH približne 2 až 3 (kontrolujeme pomocou indikátorového papierika). Vylúčenú kyselinu benzilovú odsajeme, dobre premyjeme vodou (produkt je potrebné dôkladne premyť vodou, aby sa odstránil chlorid draselný, ktorý ho znečisťuje). Kyselinu benzilovú vysušíme voľne na vzduchu. Po vysušení zvážime, vypočítame výťažnosť a stanovíme teplotu topenia, ktorú porovnáme s údajom v tabuľkách. Kyselinu benzilovú môžeme prekryštalizovať z horúcej vody.
Kyselina benzilová (Mr 228,3, T.t. 149-151oC), (Xn – škodlivá)
Doporučená literatúra:
Použité aparatúry:

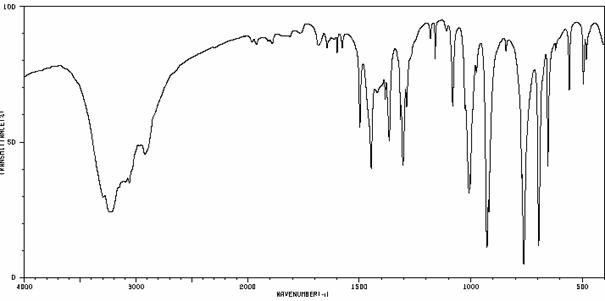
H a 13CNMR spektrum KYSELINY BENZILOVEJ:
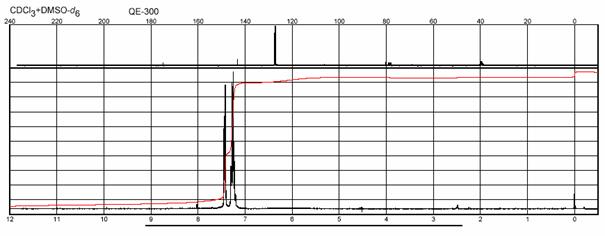
IČ spektrum KYSELINY BENZILOVEJ:
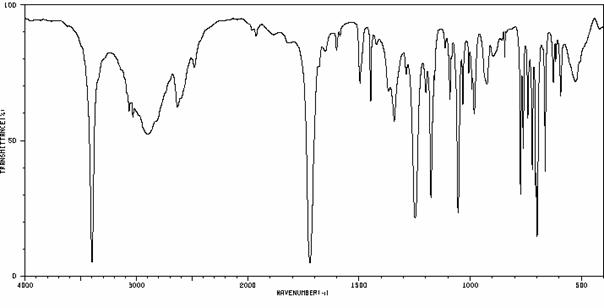
4,5-Difenylimidazol pripravíme reakciou benzilu, urotropínu a octanu amónneho v kyslom prostredí modifikovanou Radziszewského reakciou.
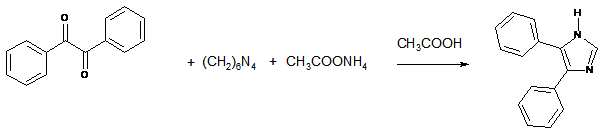
Úroveň
Čas 3 h
Príslušenstvo aparatúry pre: reflux, filtráciu, odsávanie
Chemikálie
|
benzil (Mr 210,24) |
1 g (0,00475 mol) |
Xi - dráždivá |
|
urotropín (Mr 141,09) |
0,133 g (0,00 mol) |
F – veľmi horľavá, Xn - senzibilizujúca |
|
octan amónny (Mr 77,08) |
2,93 g (0,057 mol) | |
|
25 % vodný roztok amoniaku |
C – žieravá, N – nebezpečná pre životné prostredie |
|
|
kyselina octová (99 %) |
25 ml |
C - žieravá |
Postup práce
V 100 ml okrúhlej banke zahrievame k varu 1 g benzilu, 0,133 g urotropínu, 2,93 g octanu amónneho v koncentrovanej kyseline octovej jednu hodinu. Vzniknutý roztok vylejeme do 190 ml vody a prefiltrujeme. Filtrát za chladenia zalkalizujeme na pH približne 9 (kontrolujeme pomocou indikátorového papierika). Vypadnutú zrazeninu odsajeme na Büchnerovom lieviku a premyjeme vodou. Po vysušení na vzduchu odvážime a vypočítame výťažnosť. Surový produkt môžeme kryštalizovať z horúceho pyridínu, ku ktorému sa pridáva opatrne horúca voda. Objemový pomer rozpúšťadiel je 1:1.
4,5-Difenylimidazol (Mr 220,28, T.t. 228-233oC), (Xn – škodlivá)
Doporučená literatúra:
1. Kováč, J. a kol. Organická chémia, ALFA Bratislava 1992 (str. 588, 599 ).
Použité aparatúry:
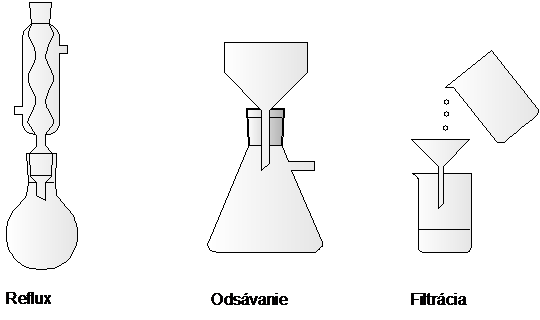
H a 13C NMR spektrum 4,5-DIFENYLIMIDAZOLU:
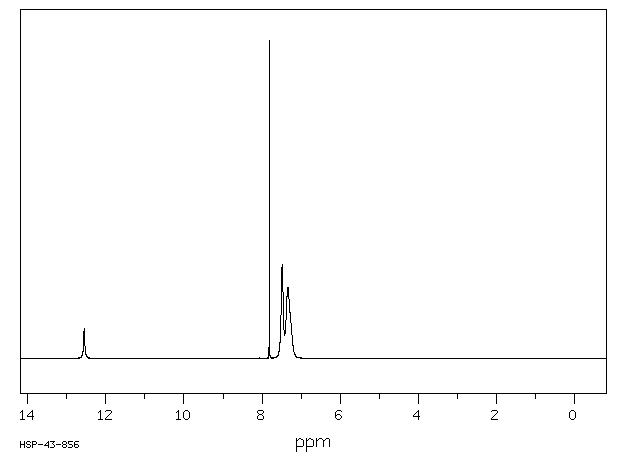
IČ spektrum 4,5-DIFENYLIMIDAZOLU:
Kofeín (1,3,7-trimetylxantín) patrí medzi dôležité xantínové deriváty. Nachádza sa v kávových zrnách a čajových listoch. V listoch čajovníka je 1,5 - 4,5 % kofeínu, podľa pôvodu a spracovania, viazaného na trieslovinu. Kofeín je veľmi často kombinovaný s kyselinou acetylsalicylovou a používaný pri liečbe bolestí hlavy.
Úroveň
Čas 3 h
Príslušenstvo aparatúry pre: extrakciu, odsávanie, destiláciu, sublimáciu
Chemikálie a materiál
|
chloroform |
24 ml |
Xn-karcinogénna, škodlivá, dráždivá |
|
čaj |
5 g | |
|
dusičnan bizmutitý (10 %) |
20 ml | |
|
síran sodný (sušidlo) |
Postup práce
Do 250 ml kadičky dáme 125 ml vody, 5 g čaju a varíme na sieťke 15 minút. K horúcemu čaju pridáme 20 ml 10 % vodného roztoku dusičnanu bizmutitého, sklenenou tyčinkou premiešavame a za horúca odsajeme na Bűchnerovom lieviku. Filtrát v kadičke varením zahustíme na 25 ml, ochladíme na laboratórnu teplotu a pridáme 12 ml chloroformu. Po dôkladnom premiešaní zmes prefiltrujeme na Bűchnerovom lieviku. Filtrát prenesieme do oddeľovacieho lievika, oddelíme organickú vrstvu a vodnú ešte raz extrahujeme chloroformom (12 ml). Spojíme organické extrakty, vysušíme nad síranom sodným, sušidlo odfiltrujeme a chloroform oddestilujeme. Odvážime surový produkt a stanovíme teplotu topenia. Surový produkt môžeme prečistiť sublimáciou pri normálnom tlaku a teplote 180-200oC.
Kofeín (Mr 194,20, T.t 235-239°C), (Xn- škodlivá)
Doporučená literatúra:
Použité aparatúry:
Trimyristín je tuk, ktorý je tvorený kyselinou myristovou - CH3(CH2)12COOH a glycerolom. Okrem muškátového orieška sa nachádza v kokosovom oleji (17,5 %) a palmojadrovom oleji (14,1 %). Používa sa na výrobu už vyššie uvedenej kyseliny myristovej a myristylalkoholu - CH3(CH2)13OH. Tieto dve zlúčeniny sú kľúčovými surovinami súčasného kozmetického priemyslu.
Úroveň
Čas 3 h
Príslušenstvo aparatúry pre: reflux, filtráciu, destiláciu, odsávanie
Chemikálie a materiál
|
muškátový orech |
2 g | |
|
dietyléter |
50 ml |
F+ mimoriadne horľavá, Xn- škodlivá |
|
acetón |
2,5 ml |
F- veľmi horľavá, Xi - dráždivá |
Postup práce
Do 250 ml varnej banky so spätným chladičom dáme 2 g rozdrveného muškátového orieška, 50 ml éteru a refluxujeme na vodnom kúpeli (teplota kúpeľa maximálne 45oC) jednu hodinu. Po prefiltrovaní éter oddestilujeme a zvyšok rozpustíme zahrievaním v 2,5 ml acetónu. Acetónový roztok necháme pomaly ochladiť na laboratórnu teplotu a potom ho dáme do ľadového kúpeľa. Produkt odsajeme na Büchnerovom lieviku a po vysušení odvážime a stanovíme teplotu topenia.
Trimyristín (T.t. 56,5oC)
Doporučená literatúra:
1. Brutovská, A. Cvičenie z metód organickej chémie, RUPJŠ Košice 1987 (str. 84).
Použité aparatúry:

Základné pravidlá v laboratóriu môžeme zhrnúť do dvoch základných skupín:
Vždy:
Dobre sa oboznámiť s laboratórnymi postupmi
Oboznámiť sa s bezpečnostným zabezpečením laboratória
Používať ochranné okuliare
Obliekať sa účelne a používať ochranný odev.
Umyť si ruky pred odchodom z laboratória
Prečítať si pozorne inštrukcie pred akýmkoľvek experimentom
Skontrolovať správne zostavenie aparatúr pre chemické pokusy
Veľmi opatrne narábať s chemikáliami
Upratať rozliate a rozsypané chemikálie
Pri akýchkoľvek pochybnostiach poradiť sa s vedúcim cvičenia
Nikdy:
Nejesť a nepiť v laboratóriu
Nefajčiť v laboratóriu
Neinhalovať a neochutnávať chemikálie
Nevyrušovať a nerozptyľovať kolegov vo svojom okolí
Nebehať po laboratóriu
Neuskutočňovať ľubovolné a vymyslené pokusy
Každé laboratórium ma isté zabezpečenie, pod ktoré spadajú únikové východy a rozmiestnenie systémov protipožiarnej ochrany, medzi ktoré patria hasiace prístroje, protipožiarna rúška, nádoby s pieskom na hasenie, bezpečnostné sprchy. Je potrebné sa dobre oboznámiť s rozmiestnením týchto bezpečnostných systémov v laboratóriu ako aj s ich používaním.
Ochrana očí
Počas práce v laboratóriu je potrebné používať ochranné okuliare. Oči patria k najcitlivejším miestam na tele v prípade zasiahnutia ostrými predmetmi ako sú napríklad kúsky rozbitého skla alebo rozprášenými a rozprsknutými chemikáliami. V chemickom laboratóriu sa nesmú používať kontaktne šošovky, pretože v prípade nehody sa môže chemikália dostať pod šošovku a vážne poškodiť oko ešte pred jej vybratím. V prípade veľmi nebezpečných pokusov sa vyžaduje použitie ochranného tvárového štítu.
Oblečenie
Najlepšou a nevyhnutnou ochranou je nosenie laboratórneho plášťa v prípade akejkoľvek činnosti v laboratóriu. Ďalšou nevyhnutnou podmienkou pre bezpečnú prácu v laboratóriu je pevné zopnutie dlhých vlasov, čím sa eliminuje riziko ich znečistenia, poškodenia alebo zapálenia. Takisto je nevyhnutná v laboratóriu vhodná obuv, ktorá ochráni nohu pred rozbitým sklom, rozliatymi a rozsypanými chemikáliami.
Zariadenia a aparatúry
Nikdy nepoužívať laboratórne zariadenie, ak nie sme plne oboznámený s jeho funkciou. To sa týka vákuových výviev, rotačných vákuových púmp, plynových tlakových fliaš a elektrických zariadení.
Pred zostavením aparatúry pre experiment je potrebné skontrolovať sklo, či nie je prasknuté alebo nalomené. Je potrebné taktiež skontrolovať, či je aparatúra dobre upevnená v držiakoch a na stojanoch.
Najväčším nebezpečenstvom v laboratóriu je oheň. Väčšina organických zlúčenín začne horieť, ak je vystavená otvorenému ohňu a mnohé z nich, obzvlášť organické rozpúšťadlá, ktoré sa bežne používajú, sú mimoriadne horľavé. V laboratórnej praxi je potrebné vyhnúť sa používaniu otvoreného ohňa a využívať v závislosti od potreby vodné a olejové kúpele, elektrické variče, prípadne elektrické topné hniezda.
V prípade potreby použitia otvoreného ohňa nikdy nezapaľovať kahan predtým ako skontrolujeme, či sa v blízkosti nenachádza otvorená fľaša s rozpúšťadlom prípadne inou organickou zlúčeninou.
Je potrebné vyhnúť sa inhalácii výparov organických látok a vždy, ak je to možné, pracovať s chemikáliami v digestóriu. V prípade použitia vysoko toxických látok a látok, ktoré produkujú toxické a dráždivé výpary je nevyhnutné pracovať v digestóriu.
Je potrebné sa vyhnúť kontaktu chemikálii s pokožkou, čo je obzvlášť dôležité pri použití žieravín a látok, ktoré sa ľahko absorbujú cez pokožku. Najlepšou ochranou je použitie gumených rukavíc pre rutinné laboratórne operácie.
V prípade rozliatia alebo rozsypania chemikálii je nevyhnutné ich okamžite odstrániť. Pevné látky je potrebné pozametať a uložiť do odpovedajúcej odpadovej nádoby. Porozlievané kyseliny je potrebne pred utretím zneutralizovať s pevným Na2CO3 prípadne s NaHCO3. Zásady je najlepšie zneutralizovať s Na2S2O3. Ak došlo k rozliatiu veľmi prchavých látok, je najlepšie hneď upozorniť kolegov, uhasiť kahany a opustiť miestnosť.
Chemikálie a nebezpečenstvo.
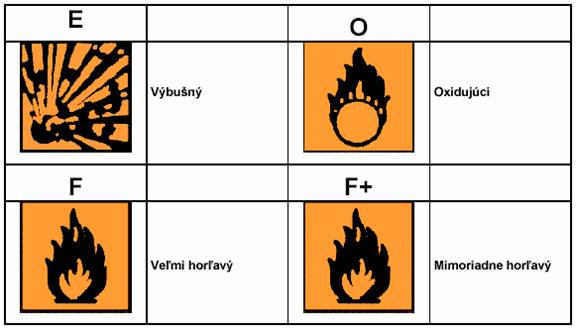
Každá chemikália používaná v chemickom laboratóriu predstavuje isté nebezpečenstvo. Pre označenie každého druhu nebezpečenstva sa používajú grafické symboly a skratky podľa výnosu Ministerstva hospodárstva Slovenskej republiky č. 2/2002 :
- výbušné: E
- oxidujúce: O
- mimoriadne horľavé: F+
- veľmi horľavé: F
- horľavé: R10
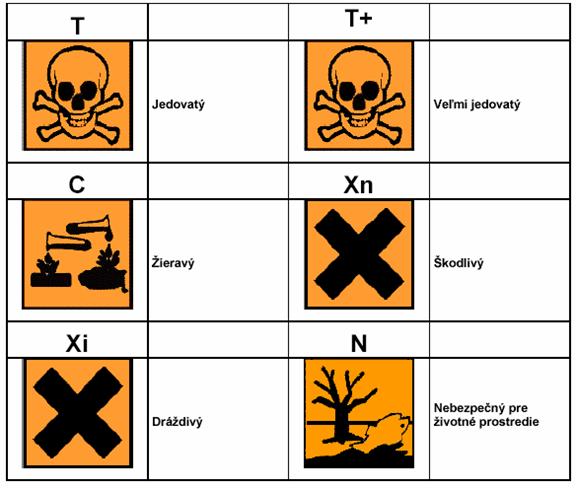
- jedovaté: T
- škodlivé: Xn
- žieravé: C
- dráždivé: Xi
- senzibilizujúce: R42 a/alebo R43
- karcinogénne: Karc. kat.
- mutagénne: Muta. kat.
- látky poškodzujúce reprodukciu: Repr. kat.
- látky nebezpečné pre životné prostredie: N alebo/a R52, R53, R59.
Grafické zobrazenie výstražných symbolov pre nebezpečné chemické látky:
Horľavé chemikálie
Základným pravidlom pri používaní horľavých chemikálii je presvedčiť sa, či sa v ich blízkosti nenachádza otvorený oheň.
Bežne používané organické rozpúšťadlá ako sú uhľovodíky napr. hexán, petroléter, benzén, toluén, alkoholy napr. metanol a etanol, estery ako napr. etylacetát a ketóny, napr. acetón patria medzi mimoriadne horľavé.
Zvlášť nebezpečné sú étery kvôli ich tendencii vytvárať explozívne peroxidy pokiaľ boli vystavené dlhodobejším účinkom vzduchu a svetla. Z tohto hľadiska sú obzvlášť nebezpečné dietyléter a tetrahydrofurán.
Explozívne chemikálie
K tomuto typu chemikálii patria tie, ktoré reagujú veľmi prudko a explozívne s vodou, napr. sodík alebo draslík, hydrid sodný prípadne lítiumalumíniumhydrid.
Výbušnosť iných typov zlúčenín je daná ich zložením a štruktúrou. Môžu obsahovať v molekule relatívne vysoký pomer kyslíka alebo dusíka a z týchto dôvodov môžu podliehať oxidačno-redukčným reakciam, prípadne uvoľňovať stabilné molekuly napr. N2. Takéto zlúčeniny sú zväčša citlivé na nárazy a zahriatie obzvlášť ak sú suché, bez rozpúšťadla. Patria sem napríklad polynitrozlúčeniny, kyselina pikrová, acetylidy kovov, azidy, diazozlúčeniny, peroxidy a perchlorované soli.
V prípade práce s týmto typom zlúčenín je nevyhnutné používať ochranný tvarový štít a pracovať za ochranným sklom v digestóriu.
Oxidujúce chemikálie
Oxidujúce chemikálie môžu spôsobiť požiar v prípade kontaktu s horľavým materiálom ako je napríklad papier.
Do tejto kategórie spadajú napr. peroxid vodíka, ozón, peroxokyseliny, Cr2O3, KMnO4, ale aj koncentrované kyseliny ako napr. kyselina sírová a dusičná.
Žieraviny
Pri narábaní so žieravinami je potrebné použiť ochranné rukavice a v prípade zasiahnutia pokožky opláchnuť ju veľkým množstvom vody.
Medzi najnebezpečnejšie žieraviny patria kyseliny sírová, dusičná, chlorovodíková, bromovodíková, fosforečná ale aj organické karboxylové a sulfónové kyseliny.
Fenol spôsobuje takisto poleptanie a je vysoko toxický, pretože sa ľahko absorbuje cez pokožku.
Medzi žieraviny tiež zaraďujeme zásady ako sú napr. hydroxid sodný, draselný, amónny, ale aj organické zásady napr. trietylamín alebo pyrolidín.
Bróm je veľmi nebezpečnou žieravinou, spôsobuje veľmi ťažké poleptanie pokožky a silno dráždi dýchacie cesty. Je veľmi prchavý preto je nevyhnutné pracovať v digestóriu.
Tionylchlorid a chlorid hlinitý uvoľňujú pri kontakte s vodou alebo vzdušnou vlhkosťou plynný HCl, preto môžu silno dráždiť dýchacie cesty. Je rovnako nevyhnutné pracovať s nimi iba v digestóriu.
Škodlivé a toxické chemikálie
Väčšina organických zlúčenín je označovaná ako škodlivá, v prípade, že sú extrémne zdraviu škodlivé, sú označené ako toxické.
Medzi najnebezpečnejšie patria anilín, benzén, bróm, chlorid uhličitý, dimetylsulfát, H2S, metyljodid, soli ortuti, metanol, nitrobenzén, fenol, fenylhydrazín, kyanid draselný a sodný.
Dráždivé chemikálie
Mnohé z organických zlúčenín sú dráždivé pre pokožku, oči prípadne dýchacie cesty. Nasledujúce chemikálie je najbezpečnejšie používať v digestóriu, aby sme čo najviac znížili riziko vystavenia sa týmto chemikáliám alebo ich výparom:
benzyl a alylhalogenidy, a-halogénkarbonylové zlúčeniny, izokyanidy, tionylchlorid a acylchloridy.
Niektoré z chemikálií majú veľmi nepríjemný zápach, medzi najnepríjemnejšie patria pyridín, kyselina fenyloctová, dimetylsufid a mnoho iných zlúčenín osahujúcich síru.
Karcinogény
Sú látky, ktoré po dlhodobejšej expozícii na zdravé bunky spôsobujú vznik rakoviny. Čas medzi expozíciou a vznikom tumoru je u ľudí aj niekoľko rokov.
Medzi karcinogény zaraďujeme:
epoxidy, dimetylsulfát, formaldehyd, benzén, aromatické amíny napr. 2-naftylamín, benzidín, kondenzované aromatické zlúčeniny napr. benzpyréen, azozlúčeniny, Cr2O3, chlórované uhľovodíky napr. CCl4 a CHCl3, tiomočovinu a iné.
Popáleniny
Prípadný požiar v laboratóriu je potrebné ihneď hlásiť vedúcemu cvičenia a opustiť miesnosť. Na hasenie drobných požiarov je vhodné použiť piesok, protipožiarnu rúšku pripadne penový, resp. snehový hasiaci prístroj. Na hasenie sa nikdy nepoužíva vodný hasiaci pristroj, obzvlášť pri horení elektrických zariadení a organických rozpúšťadiel, ktoré nie sú miešateľné s vodou.
Drobné popáleniny od variča, nádob vodného prípadne olejového kúpeľa sa ošetrujú chladením pod prúdom studenej tečúcej vody po dobu 10-15 minút. Na popáleniny nikdy nepoužívajte nijakú masť ani krém a vytvorené pľuzgiere neporušujte.
Chemikálie na pokožke
V prípade, že sa na pokožku dostali akékoľvek chemikálie, zasiahnuté miesto opláchnite prúdom studenej vody po dobu 15 minút. V prípade zasiahnutia väčšej časti tela je potrebné použiť okamžite bezpečnostnú sprchu. Akékoľvek zasiahnuté oblečenie musí byť odstránené.
Chemikálie v oku
V prípade zasiahnutia oka chemikáliou je potrebné oko vypláchnuť veľkým množstvom tečúcej vody po dobu 15 minút.
Porezanie
Drobné porezania napríklad rozbitým sklom sa musia vypláchnuť prúdom tečúcej vody po dobu aspoň 10 minút, aby sme z rany odstránili prípadné drobné úlomky skla alebo chemikálie. Malé porezania zvyčajne prestane krvácať samo pomerne rýchlo a môže byť prelepené náplasťou, prípadne previazané hygienickým obväzom.
Veľké rany nevyplachujte vodou, odstráňte viditeľné ľahko prístupné cudzie telesá, nepokúšajte sa však vytiahnuť hlboko zakliesnené teleso. Ranu silno stlačte vankúšikom gázy a jej okraje pritisnite k sebe. Ak ostalo v rane nejaké teleso, priamo na ranu netlačte. Vankúšik gázy pevne obviažte elastickým alebo iným obväzom.
Otrava
V prípade požitia chemikálie, ak je postihnutý pri vedomí, dajte mu vypiť pohár vlažnej vody. Nikdy sa nepokúšajte vyvolať zvracanie. Ak postihnutý zvracia spontánne držte ho prehnutého, aby nedošlo k vdýchnutiu obsahu žalúdka.
V prípade otravy vdychovaním dráždivých látok preneste postihnutého na čerstvý vzduch a dbajte, aby nedošlo k ďalšiemu vdychovaniu škodlivín zo zamoreného odevu. Oči a ústa vyplachujte vodou.
V prípade vážneho poranenia v laboratóriu a po poskytnutí prvej pomoci okamžite zavolajte lekársku pomoc.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 8124
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved
Distribuie URL
Adauga cod HTML in site