| CATEGORII DOCUMENTE |
| Bulgara | Ceha slovaca | Croata | Engleza | Estona | Finlandeza | Franceza |
| Germana | Italiana | Letona | Lituaniana | Maghiara | Olandeza | Poloneza |
| Sarba | Slovena | Spaniola | Suedeza | Turca | Ucraineana |
DOCUMENTE SIMILARE |
|
Biochemijos laboratoriniai darbai
Glikolizës tyrimas
Darbo tikslas:
Ištirti glikolizës procesą raumens audinyje.
Nustatyti slopiklio MJAR poveiká glikolizës procesui.
Apskaičiuoti gliukozës skaldymo bei fruktozës ir pieno rűgšties susidarymo greičius.
Raumenř ekstrakto paruošimas
Tirpalai
Darbo eiga
BALTYMO KIEKIO NUSTATYMAS BREDFORDO METODU
REAGENTAI:
DARBO EIGA:
1 lentelë. Optinio tankio priklausomybë nuo albumino koncentracijos.
|
Serumo albumino tűris (μl) |
serumo albumino koncentracija (mg/ml) |
Optinis tankis |
1 pav. Optinio tankio priklausomybë nuo albumino koncentracijos.
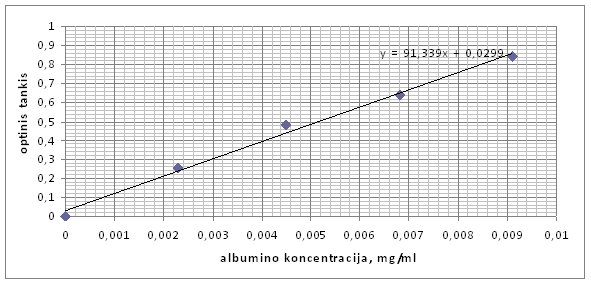
2 lentelë. Optinio tankio priklausomybë nuo baltymo kiekio frakcijos
|
Skiedimo koficientas |
Optinis tankis |
Baltymo kiekis mg/ml |
|
vidurkis | ||
BANDYMAS SU GLIKOGENU
Tirpalai
Darbo eiga
Á 8 mëgintuvëlius stovinčius lede supilame 1 lentelëje nurodytus kiekius glikogeno, ekstrakto, monojodacto rűgšties ir trichloracto rűgšties. Inkubuojami 30 min. 370C temperatűroje. Kontroliniuose mëginiuose tricloracto rűgštá pripilame pradžioje iki ekstrakto pripylimo. Tiriant glikolizës poveiká á atitinkamus mëgintuvëlius pripilame monojodacto rűgšties, kuri slopina glicerolio aldehido fosfato dehidrogenazës aktyvumą.
3 lentelë. Mëginiř sudëtis.
|
Mëginio numeris |
||||||||
|
1 | ||||||||
|
glikogenas |
0,5 ml |
0,5 ml |
0,5 ml |
0,5 ml |
0,5 ml |
0,5 ml |
0,5 ml |
0,5 ml |
|
ekstraktas |
1,5 ml |
1,5 ml |
1,5 ml |
1,5 ml |
1,5 ml |
1,5 ml |
1,5 ml |
1,5 ml |
|
MJAR |
0,1 ml |
0,1 ml |
|
0,1 ml |
0,1 ml |
|||
|
H2O |
0,1 ml |
0,1 ml |
0,1 ml |
0,1 ml | ||||
|
Trichloracto r. |
3,0 ml |
3,0 ml |
3,0 ml |
3,0 ml |
3,0 ml |
3,0 ml |
3,0 ml |
3,0 ml |
Po inkubacijos baltymai nusodinami pridedant 3 ml 12% trichloracto rűgšties. Baltymř nuosëdos centrifuguojamos ir filtrate nustatomas gliukozës, fruktozës bei pieno rűgšties kiekis. Gliukozës kiekis nustatomas kolorimetriniu metodu su antroniniu reagentu, fruktozës kiekis kolorimetriniu metodu su rezorcinu, o pieno rűgšties kiekis nustatomas fermentiniu metodu su laktato dehidrogenaze. Iš substrato ir produkto kiekio pokyčio galima spręsti apie glikolizës intensyvumą. Baltymo koncentracija pradiniame baltyminiame ekstrakte nustatoma Bredfordo metodu. Apskaičiuojame gliukozës skaidymo, fruktozës bei pieno rűgšties susidarymo greičius (μmol/min. mg baltymo). Gautus duomenis surašome á 9 lentelę.
GLIKOGENO NUSTATYMAS
Metodas remiasi tuo, kad angliavandeniai, paveikti sieros rűgštimi, virsta furfurolo dariniais, kurie su antronu sudaro spalvotus junginius. Iš spalvos intensyvumo galima spręsti apie angliavandeniř kieká.
Tirpalai
Darbo eiga
c = D1/D2 cx,
kur D1 – tiriamojo tirpalo optinis tankis, D2 – standartinio gliukozës tirpalo optinis tankis, cx – standartinio gliukozës tirpalo koncentracija.
4 lentelë. Gliukozës koncentracija mëginiuose
|
Mëginio nr. |
Sugertis 620 nm |
Gliukozës koncentracija, mg/ml |
Gliukozës koncentracija, mol/ml** |
|
2 | |||
|
3 | |||
|
4 | |||
|
5 | |||
|
6 | |||
|
7 | |||
|
8 |
![]() ; čia Ast=0,09; cst=0,005 mg/ml.
; čia Ast=0,09; cst=0,005 mg/ml.
* trichloracto rűgštis pripilama prieš pilant ekstraktą (kontroliniai mëginiai); **Mgliukozës=180 g/mol.
FRUKTOZËS NUSTATYMAS
Šildant tirpalą su koncentruota HCl, susidaro oksimetilfurfurolas, kuriam reaguojant su rezorcinu, atsiranda rožinë spalva. Ši Selivanovo pasiűlyta spalvinë reakcija taikoma tiek kiekybiniam tiek kokybiniam fruktozës bei jos fosfatř nustatymui.
Tirpalai
Darbo eiga
5 lentelë. Fruktozës koncentracija mëginiuose
|
Mëginio nr. |
Sugertis (490 nm) |
Fruktozës koncentracija (mg/ml) |
Vidutinë fruktozës koncentracija (mg/ml) |
Vidutinë fruktozës koncentracija ( mol/ml) |
|
| ||||
PIENO RŰGŠTIES NUSTATYMAS
Pieno rűgštis, veikiant fermentui laktato dehidrogenazei oksiduojama iki piruvo rűgšties. Oksiduojantis piruvo rűgščiai, NAD+ redukuojamas iki NADH, kurio koncentraciją galime išmatuoti spektrofotometriškai. Oksiduojantis vienam moliui pieno rűgšties, susidaro vienas molis NADH. Matuojant susidariusio NADH optiná tanká 340 nm bangos ilgyje ir žinant NADH molinës ekstinkcijos koeficientą galime apskaičiuoti susidariusio pieno rűgšties kieká. Laktato dehidrogenazës katalizuojamos reakcijos pusiausvyra yra pastumta á pieno rűgšties susidarymo pusę. Tačiau esant terpëje hidrazino arba semikarbazido, su kuriais piruvo rűgštis sudaro hidrazinus arba semikarbazonus cheminës reakcijos pusiausvyra yra pastumiama á piruvo rűgšties susidarymo pusę ir galime kiekybiškai išmatuoti laktato kieká.
Tirpalai
Darbo eiga
Paruošiami tirpalai pagal 7 lentelę.
6 lentelë. Mëginiř sudëtis.
|
Mëginio sudëtis |
Kontrolë (ml) |
Tiriamasis tirpalas (ml) |
|
Glicino – hidrazino buferis |
2,7 | |
|
NAD+ tirpalas | ||
|
Laktato dehidrogenazës tirpalas | ||
|
Tiriamasis tirpalas |
Tirpalai sumaišomi ir termostatuojami 60 min. 250C temperatűroje. Po inkubacijos su spektrofotometru išmatuojame tiriamo mëginio optiná tanká. Pieno rűgšties kieká mëgintuvëlyje apskaičiuojame pagal formulę:
M = (D/6,22),
kur M – nustatomos medžiagos kiekis μmol/ml, D – tiriamojo mëginio optinis tankis, V – tiriamo mëginio tűris, 6,22 – optinis tankis tirpalo, kuriame yra 1 μmol/ml NADH.
8 lentelë. Pieno rugšties kiekis
|
Mëginio Nr. |
Sugertis (340 nm) |
cpr, μmol/ml |
Vidutinë cpr, μmol/ml |
REZULTATAI:
9 lentelë. Gliukozës, fruktozës ir pieno rűgšties kitimas glikolizës tyrimo eigoje.
|
Kontrolë |
30 min. inkubacija |
Greitis (μmol/min. mg baltymo) |
Kontrolë (su MJAR) |
30 min. inkubacija (su MJAR) |
Greitis (μmol/min. mg baltymo) |
|
|
Gliukozë (μmol/ml) | ||||||
|
Fruktozë (μmol/ml) | ||||||
|
Pieno rűgštis (μmol/ml) |
IŠVADOS:
LITERATŰRA:
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 2262
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2024 . All rights reserved