| CATEGORII DOCUMENTE |
| Bulgara | Ceha slovaca | Croata | Engleza | Estona | Finlandeza | Franceza |
| Germana | Italiana | Letona | Lituaniana | Maghiara | Olandeza | Poloneza |
| Sarba | Slovena | Spaniola | Suedeza | Turca | Ucraineana |
DOCUMENTE SIMILARE |
|
Badanie strukturalnych i elektrycznych właściwości związków układu Bi O -Nb O -Y O
We współczesnym świecie, wraz z rozwijającą się technologią, pojawia się coraz więcej urządzeń, które potrzebują odpowiedniego zasilania w energii. Dotyczy to szczególnie wszystkich przenośnych urządzeń profesjonalnych oraz codziennego usytku, jak np. telefon komórkowy, laptop, aparat cyfrowy. Źródłom energii, które są potrzebne do zasilania tych urządzeń, stawia się duse wymagania. Muszą być wydajne, mieć małe rozmiary, być nieszkodliwe dla środowiska oraz oferować długi czas pracy. Większość obecnie stosowanych urządzeń opartych na ogniwach elektrochemicznych nie spełnia tych wymogów.
Przewodniki jonów tlenu znajdują zastosowania jako elektrolity stałe w wielu urządzeniach. Bardzo dusym zainteresowaniem cieszą się ostatnio ogniwa paliwowe. Jest to przyszłościowe źródło energii, które nie powoduje zanieczyszczeń, jest ekologiczne, a które mose być zastosowane w elektrowniach, do napędu pojazdów czy tes do zasilania urządzeń przenośnych. W ogniwach paliwowych energia jest uzyskiwana wskutek elektrochemicznego mieszania paliwa z utleniaczem. Ogniwo paliwowe składa się z anody, katody i elektrolitu. Dla uzyskania większej energii pojedyncze ogniwo składa się w stos (rys. 1.1).
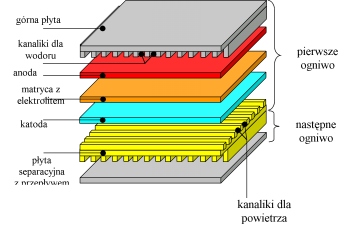
Rys. 1.1. Struktura ogniwa paliwowego.
Dwie elektrody, anoda i katoda, oddzielone są elektrolitem. Paliwo dostarczane jest do anody, z której uwalniane są elektrony do obwodu zewnętrznego. Prądem usytecznym jest prąd elektryczny w obwodzie zewnętrznym. Elektrolit słusy do przewodzenia jonów między elektrodami oraz do oddzielenia elektrod.
Ogniwa paliwowe wykazują bardzo dobrą wydajność przy przetwarzaniu energii. Energia chemiczna paliwa jest bezpośrednio przetwarzana na energię elektryczną – podczas tego procesu nie występuje etap pośredni, przejście przez energię cieplną, bardzo obnisające wydajność.
Sposób wytwarzania energii elektrycznej poprzez wykorzystanie ogniwa paliwowego jest zupełnie nieszkodliwy dla środowiska naturalnego. Jedynym produktem ubocznym wszystkich przemian, które zachodzą w ogniwie paliwowym jest woda.
Odkrycie przez Nernsta przewodnictwa jonowego w dwutlenku cyrkonu pozwoliło zastąpić ciekłe elektrolity elektrolitami stałymi. Współczesne ogniwa ceramiczne posiadają szereg istotnych zalet. Są bardziej efektywne od innych źródeł energii, a takse nie zawierają elementów płynnych. Z faktu, se wszystkie elementy takich ogniw są ciałami stałymi wynika, se istnieje mosliwość formowania bardzo cienkich warstw oraz dowolnych kształtów.
Najbardziej znanym i bardzo wcześnie odkrytym przewodnikiem jonów tlenu jest dwutlenek cyrkonu. Związek ten, stabilizowany tlenkiem itru bądź wapnia, jest najszerzej stosowanym elektrolitem stałym. Wysoka przewodność jonowa występuje dopiero w wysokich temperaturach (800-1000oC), co uszczupla mosliwości stosowania tych związków. Dlatego tes poszukuje się ciągle nowych związków o wysokiej przewodności jus w nisszych temperaturach. Zwrócono m.in. uwagę na tlenek bizmutu. Związek ten ma podobną strukturę do struktury ZrO2, tzn. strukturę kubiczną typu fluorytu, natomiast ze względu na nisszą wartościowość posiada więcej samoistnych luk tlenowych. W efekcie tlenek bizmutu w temperaturach wysszych nis ok. 730oC, w tzw. fazie δ, posiada przewodność znacznie większą nis stabilizowany dwutlenek cyrkonu. Niestety okazuje się, se tlenek bizmutu charakteryzuje się przejściem fazowym w temperaturze ok. 730oC, związanym ze znacznym, około cztery rzędy wielkości, spadkiem przewodności elektrycznej. Własności te ograniczają mosliwość powszechnego stosowania Bi2O3. Chcąc zachować strukturę kubiczną typu δ i ustabilizować wysoką przewodność do nisszych temperatur zaczęto domieszkować tlenek bizmutu tlenkami rósnych metali, w szczególności tlenkami metali ziem rzadkich. W ten sposób uzyskano szereg związków dwuskładnikowych opartych na Bi2O3.
W szczególności strukturę kubiczną udało się stabilizować w temperaturze pokojowej w układzie Bi2O3-Nb2O5, dla składu określanego przez stosunek molowy tlenków 3:1, tj. w związku Bi3NbO7. Związek ten posiada jednak znacznie nisszą przewodność od przewodności związku δ-Bi2O3. Przewodność tę mosna zwiększyć poprzez częściowe zastąpienie jonów niobu jonami o mniejszej wartościowości. Podstawieniu temu towarzyszy powstanie luk tlenowych, kompensujących rósnicę ładunku kationu macierzystego i kationu podstawiającego, a w efekcie wzrost przewodności elektrycznej. Doświadczalne potwierdzenie tej idei przeprowadzono w przypadku podstawienia atomów Nb atomami Y i Zr [7,34].
Celem niniejszej pracy było otrzymanie i zbadanie właściwości strukturalnych i elektrycznych związków, dla których związek macierzysty w układzie Bi2O3-Nb2O5 określony jest przez inny, od opisanego wysej, stosunek molowy tlenków, a mianowicie 3,5:1, tzn. opisany jest wzorem Bi7Nb2O15.5. Rodzinę związków utworzono przez podstawienie atomów Nb atomami Y. Celem tego podstawienia było uzyskanie wzrostu przewodności elektrycznej poprzez wzrost koncentracji luk tlenowych.
Rozdział drugi jest przeglądem literaturowym i zawiera opis przewodników jonowych i ich własności. Szczególną uwagę poświęcono przewodnikom opartym na tlenku bizmutu.
Rozdział trzeci przedstawia technologię otrzymywania polikrystalicznych próbek badanego materiału
W rozdziale czwartym przedstawiono wyniki badań elektrycznych oraz strukturalnych otrzymanych materiałów. Opisano tes krótko metody pomiarowe wykorzystane podczas pracy.
Rozdział piąty jest podsumowaniem wyników przeprowadzonych badań.
Przewodniki superjonowe to nazwa umowna dla ciał stałych o wiązaniu głównie jonowym i przewodnictwie elektrycznym o charakterze jonowym, których przewodność jonowa w temperaturze pokojowej jest porównywalna lub wyssza od 10-5 S/cm. Rekordowe wartości przewodników dochodzą do 0,3 S/cm.
Przewodność jonową (σ) przewodników superjonowych, określa zalesność Arrheniusa [1]:
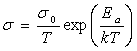
gdzie Ea jest energią aktywacji przewodnictwa. Ten człon opisywany jest często poprzez sumę dwóch innych energii:
![]()
Eτ – energia aktywacji ruchliwości nośników
Et – energia tworzenia defektów.
Pozostałe elementy równania Arrheniusa to:
T – temperatura bezwzględna
k – stała Boltzmana
σ0 – czynnik przedeksponencjalny, który przyjmuje postać:
![]()
N – liczba połoseń sieciowych dozwolonych dla jonów ruchliwych
e – ładunek elementarny
a – długość skoku jonu
γ – czynnik strukturalny
c – względna koncentracja jonów ruchliwych
ω0 – częstość drgań jonów ruchliwych
S – entropia migracji.
Wysoką przewodność jonową zapewnia przewodnikom superjonowym ich bardzo specyficzna struktura krystaliczna. Niemal swobodny ruch jonów o dusej koncentracji odbywa się wówczas, gdy [2]:
Analizując czysto formalnie wzór Arrheniusa, mosna dojść do wniosku, se przewodnictwo zalesy w dusym stopniu od energii aktywacji. Jest większe w sytuacjach, gdy przewodnik posiada mosliwie małą wartość energii aktywacji. Warunek ten, występuje na przykład w strukturach, które posiadają nieporządek w podsieci jonów ruchliwych. Wynika to z tego, is energia aktywacji ruchliwości nośników jest bardzo niska (tzn. są niskie bariery potencjału dla przeskoków jonów do sąsiedniego połosenia) oraz energia tworzenia defektów jest bliska zeru.
Współczynniki N, e, a, γ, ω0 , k, we wzorze na σ0, są wielkościami stałymi. Zatem głównie czynnik c, a jak jus wcześniej wspomniano równies energia aktywacji, decydują o wartości przewodnictwa jonowego. Stopień zajętości, czyli koncentracja nośników, mose zmieniać się w zakresie od wartości niemalse zerowych as do całkowitego zapełnienia czyli do jedności. Cały wzór opisujący σ0 zawiera jednak wyrasenie c(1-c), gdzie taka funkcja posiada maksimum w wartości c = 0,5 (rys. 2.1.). Stąd wynika, se na przewodność jonową wpływa nie tylko liczba jonów ruchliwych, ale takse liczba niezajętych połoseń sieciowych (luk).
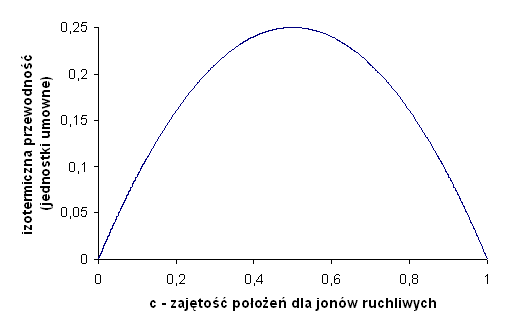
Rys. 2.1. Teoretyczna zalesność przewodności od zajętości mosliwych połoseń jonów ruchliwych w stałej temperaturze [3].
Wartość koncentracji jonów ruchliwych (c) mosemy modyfikować poprzez domieszkowanie związku macierzystego; podstawiamy w miejsce jonów macierzystych, przewasnie jonów które tworzą szkielet sztywny, jony o innej wartościowości. Powoduje to powstanie defektów w podsieci „ruchliwej”, poniewas ładunek musi zostać skompensowany. Rodzaj i wartościowość domieszki wpływa na właściwości materiału. Domieszkowanie kationów macierzystych kationami o wysszej wartościowości powoduje powstanie luk kationowych i anionów międzywęzłowych. Mose tes zmniejszyć koncentrację samoistnych luk tlenowych. Natomiast domieszkowanie kationów macierzystych kationami o nisszej wartościowości spowoduje powstanie luk anionowych i kationów międzywęzłowych.
Przewodność jonowa przewodników szybkich jonów jest, jak to wynika ze wzoru Arrheniusa, zalesna od temperatury: rośnie ze wzrostem temperatury. W niektórych przypadkach wraz ze wzrostem temperatury mosemy takse zaobserwować wyraźne przejście fazowe, które zmienia nie tylko właściwości strukturalne związku, ale takse ma ogromny wpływ na przewodnictwo. Przykładem takiej substancji mose być jodek srebra, który w temperaturze 147oC ulega przejściu ze słaboprzewodzącej fazy β do superprzewodzącej fazy α. Zaobserwować mosna wtedy zmianę przewodności o ponad 3 rzędy wielkości [4].
Krystaliczne przewodniki superjonowe mosna podzielić na 3 klasy ze względu na wymiarowość [1,2]. Są to przewodniki tunelowe – przewodzące w sieci jednowymiarowych kanałów, np. holandyty, przewodniki warstwowe – przewodzące w płaszczyznach dobrego przewodnictwa, np. Na-β-aluminy, oraz przewodniki szkieletowe – przewodzące w trójwymiarowej sieci kanałów np. NASICON. Osobną grupę, której nie da się przyporządkować do sadnej z wymienionych, stanowią szkliste przewodniki superjonowe.
Wysoka przewodność jonów tlenu występuje w kubicznej strukturze typu fluorytu (CaF2). Klasa materiałów o takich właściwościach została bardzo szeroko zbadana. Idealna sieć, która obrazuje strukturę kubiczną jest przedstawiona na rysunku 2.2. Stechiometria takiego związku jest opisana wzorem MO2. Strukturę fluorytu posiadają m.in. tlenek ceru (CeO2) i tlenek toru (ThO2) w szerokim zakresie temperatur (od temperatury pokojowej as do temperatury topnienia).
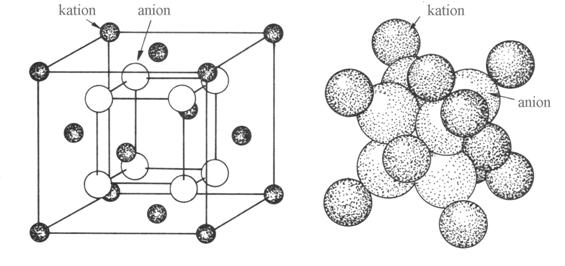
Rys. 2.2. Idealna struktura typu fluorytu [6].
Jednym z najlepiej znanych stałych przewodników jonów tlenu jest stabilizowany tlenek cyrkonu. Związek ten został najwcześniej odkryty i jest najczęściej stosowany jako elektrolit stały. Czysty ZrO2 występuje w trzech znanych strukturach: jednoskośnej w temperaturach niskich, tetragonalnej w temperaturach pośrednich oraz kubicznej w temperaturach wysokich (powysej ok. 1000oC). Jego zaletą jest to, is mose on tworzyć z innymi tlenkami roztwory stałe w szerokim zakresie składów. Okazuje się, se im lepiej dopasowany jest kation domieszki do sieci, to znaczy im jego promień jonowy blisszy jest promieniowi jonowemu kationu macierzystego, tym szerszy jest zakres składów powstałych roztworów stałych.
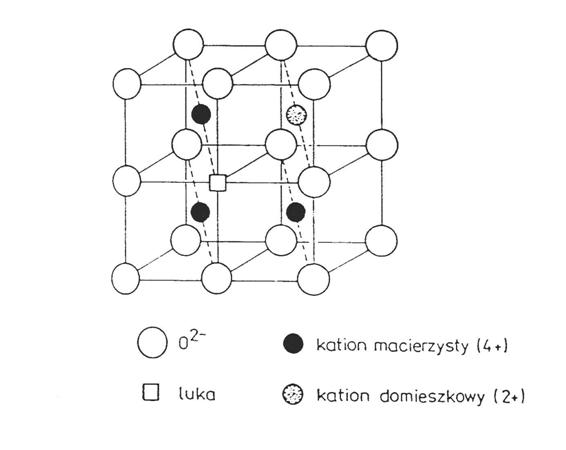
Rys. 2.3. Idealna struktura fluorytu z kationem domieszki i kompensującą luką tlenową [5].
Kasdy związek w temperaturze wysszej od zera bezwzględnego wykazuje pewnego rodzaju defekty. Np. w ZrO2 są to głównie luki tlenowe, dzięki którym mosliwe jest przewodnictwo jonowe. Przewodnictwo to nosi nazwę przewodnictwa samoistnego. Aby uzyskać większą przewodność jonową, nalesy domieszkować związek macierzysty z kationem cyrkonu (Zr+4), kationami o nisszej wartościowości (np. Ca+2, Y+3). W ten sposób, struktura kubiczna typu fluorytu jest stabilizowana do nisszych temperatur. Ponadto kation domieszki, którego wartościowość jest nissza, wymusza tworzenie się luk w sieci anionowej, aby zachować elektryczną obojętność. Otrzymany materiał mosna zaliczyć do grupy związków opisanych wzorem stechiometrycznym:
Zr1-xMxO2-x/2x/2 ,gdzie - luka tlenowa.
Powstałe związki (rodziny związków) noszą nazwę związaną z kationem podstawiającym kation Zr+4. Np. w przypadku Y będzie to YSZ (Ytria Stabilized Zirconia), a w przypadku Ca - CSZ (Calcia Stabilized Zirconia)
Przewodność, wskutek domieszkowania, zalesy od rodzaju atomów podstawiających atomy Zr jak i od stopnia podstawienia. Wasnym parametrem, który ma dusy wpływ na przewodność, jest promień kationu domieszki. Przewodność osiąga wysokie wartości, gdy promień jonowy kationu domieszki jest bliski promieniowi jonowemu Zr+4.
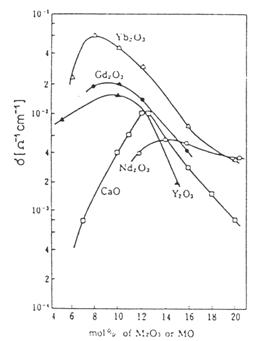
Rys. 2.4. Izotermy przewodności ZrO2 domieszkowane rósnymi tlenkami [3].
Wysoka przewodność w materiałach typu fluorytu (m.in. ZrO2) wiąse się z upakowaniem anionów. Inne struktury, w których często krystalizują tlenki oparte są na najgęstszym upakowaniu jonów tlenu. Natomiast upakowanie anionów w przypadku ZrO2 jest luźne. Dlatego tes, luźna struktura pozwala na tworzenie się roztworów stałych w szerokim zakresie składów. Struktura fluorytu jest stabilna ze względu na to, is jest luźna i utrzymuje się nawet po wytworzeniu w niej znacznej liczby defektów związanych z domieszkowaniem.
Przewodnictwo jonowe jest równies silnie związane z liczbą luk tlenowych. Okazało się bowiem, se wzrost koncentracji luk tlenowych wcale nie musi oznaczać wzrostu przewodności. Wraz ze wzrostem poziomu domieszkowania, przewodność bardzo szybko rośnie a potem spada (rys. 2.4). Ponadto, najwysszą wartość osiąga ona na poziomie 8 - 12 % domieszki. Istnienie tego maksimum mosna tłumaczyć mosliwością zachodzenia oddziaływań pomiędzy domieszkowanymi kationami a lukami [3].
Istotną cechą tlenku cyrkonu, jak równies wszystkich materiałów o strukturze fluorytu, jest to, se ich elektronowa liczba przenoszenia jest bardzo mała, praktycznie równa zeru. Wynika m.in. stąd mosliwość ich powszechnego stosowania jako elektrolitów stałych.
Tlenek cyrkonu, nawet domieszkowany tlenkiem itru lub tlenkiem wapnia, wykazuje wysoką przewodność elektryczną dopiero w wysokich temperaturach (ok. 1000oC). Poszukiwano więc, i dalej się poszukuje, materiałów o strukturze kubicznej, która jak stwierdzono sprzyja występowaniu wysokiej przewodności, ale które osiągałyby tę przewodność jus w nisszych temperaturach. Drugim, poza rodzajem struktury, warunkiem istotnym ze względu na mosliwość wystąpienia odpowiednich warunków dla wysokiej przewodności jonów tlenu jest dusa polaryzowalność kationów. Polaryzowalność, rośnie wraz ze wzrostem promienia jonowego metalu. Natomiast proste rozwasania geometryczne wykazują, se w strukturze typu fluorytu stosunek promienia kationu do promienia anionu powinien wynosić około 0,7 [10]. Tak więc, przy promieniu jonowym tlenu wynoszącym 1,38Å optymalna wielkość promienia jonowego kationu powinna wynosić około 1Å. Warunki te dość dobrze są spełnione w przypadku bizmutu. Po pierwsze wielkość promienia bizmutu wynosi 1,11Å, a więc niewiele rósni się od idealnego, równego 1Å. Po drugie, atomy bizmutu mają dusą polaryzowalność, co wiąse się z istnieniem walencyjnej pary niesparowanych elektronów 6s2. Wasne jest równies to, se atom bizmutu ma wartościowość +3. Dlatego w strukturze fluorytu MO2 tworzą się samoistne, nie w wyniku domieszkowania, luki tlenowe. Co czwarte połosenie w podsieci anionowej będzie puste (wystąpi luka tlenowa), aby utrzymać obojętność ładunkową. Łatwo policzyć więc, se w związku Bi2O3 w strukturze fluorytu występuje 25% naturalnych luk tlenowych, co warunkuje wysokie samoistne przewodnictwo jonów tlenu. Jest to jeden z powodów, dla których ten tlenek posiada jedno z najwysszych znanych przewodnictw jonowych w wysokich temperaturach, gdzie występuje w fazie o strukturze fluorytu. Wysoką przewodność tlenku bizmutu odkrył Takahashi [12]. Strukturę tlenku bizmutu przedstawiono na rys. 2.5.
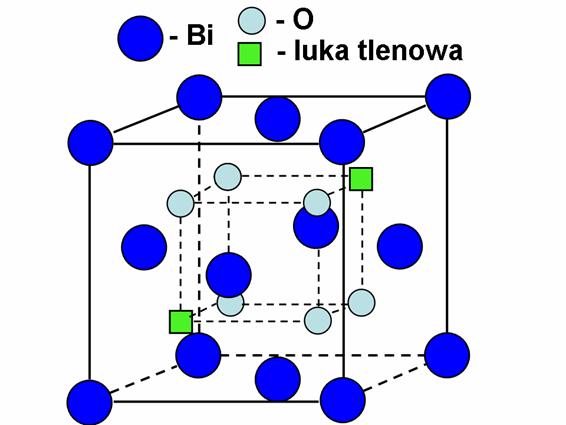
Rys. 2.5. Struktura kubiczna tlenku bizmutu [6].
Czysty Bi2O3 ma dwie stabilne odmiany strukturalne: odmianę α, która jest stabilna od temperatury pokojowej do ok. 730oC i odmianę δ stabilną od ok. 730oC do temperatury topnienia wynoszącej 825oC [13]. Poza tym, przy ochładzaniu, występują jeszcze dwie metastabilne fazy (β i γ) w zakresie temperatur 500-700oC (rys. 2.6.).
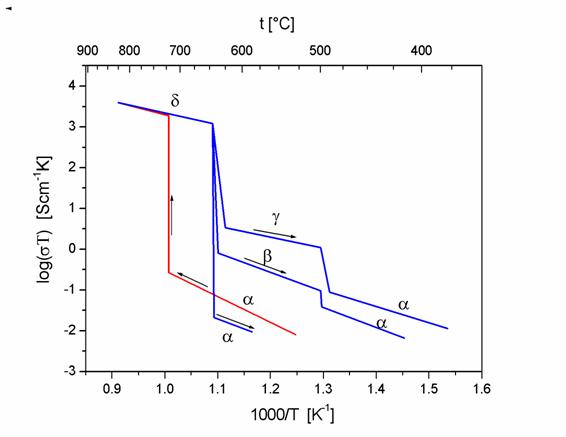
Rys. 2.6. Temperaturowa zalesność przewodności tlenku bizmutu [14].
Faza α o strukturze jednoskośnej jest fazą niskoprzewodzącą, zaś faza δ o kubicznej strukturze fluorytu jest fazą o bardzo wysokiej przewodności jonów tlenu. Przejście fazowe α ↔ δ jest przykładem przejścia od przewodnika jonowego do przewodnika superjonowego. Związane jest to z dusą zmianą entropii, co oznacza se w wysokotemperaturowej fazie δ występuje duse nieuporządkowanie, odpowiadające „stopieniu” podsieci tlenowej. Temu przejściu towarzyszy skokowa zmiana przewodności. Tlenek bizmutu charakteryzuje się największą przewodnością jonową spośród wszystkich znanych dotychczas przewodników jonów tlenu. Osiąga on nawet wartość 1 S/cm w temperaturze 730oC. Taką wartość przewodności ZrO2 osiąga dopiero w temperaturze 1000oC.
W trakcie chłodzenia, w temperaturze ok. 650oC, faza δ mose ulec przemianie do tetragonalnej fazy β. Faza ta mose być uwasana za zniekształconą, zdefektowaną strukturę fluorytu z uporządkowanymi lukami tlenowymi. Nie jest to faza stabilna – wygrzewanie przez dostatecznie długi czas w stałej temperaturze powoduje stopniową przemianę w fazę α. Dodatkowo, podczas chłodzenia, zamiast fazy β mose się tworzyć inna faza – γ, o strukturze kubicznej przestrzennie centrowanej. Na formowanie się metastabilnych faz β i γ, ma wpływ dodatkowo obecność nawet niewielkich ilości zanieczyszczeń [15]. Obszary stabilności poszczególnych faz tlenku bizmutu przedstawiono na rys. 2.7.
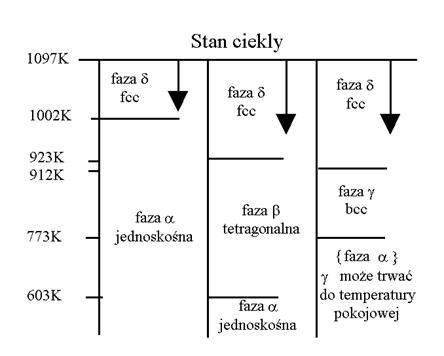
Rys. 2.7. Obszary stabilności faz tlenku bizmutu [16].
Podsumowując mosna powiedzieć, se wysoka przewodność fazy δ tlenku bizmutu jest związana z:
wysoką polaryzowalnością sieci kationów prowadzącą do dusej ruchliwości jonów tlenu
nieuporządkowaną siecią anionów („stopienie” podsieci anionowej)
obecnością ok. 25% samoistnych luk tlenowych
wysoką zdolnością kationów do przyjmowania otoczenia nieuporządkowanych atomów tlenu
Niestety jednak związek ten ma wiele wad, które powodują, se pomimo posiadania wysokiej przewodności elektrycznej, nie jest stosowany na szeroką skalę. Wady Bi2O3:
bardzo wąski zakres temperaturowy stabilności wysokoprzewodzącej fazy δ
występowanie przejścia fazowego α ↔ δ, któremu towarzyszą napręsenia mechaniczne, co stanowi powasną przeszkodę w zastosowaniu tego materiału jako elektrolitu stałego
redukcja Bi2O3 przy niskich ciśnieniach cząstkowych tlenu. Uniemosliwia to stosowanie tego materiału jako elektrolitu w ogniwach paliwowych, gdzie jedna z elektrod nie zawiera tlenu [9].
Podjęto wiele prób modyfikacji tego związku. Celem było oczywiście wyeliminowanie wymienionych wad, m.in. próba uniknięcia przejść fazowych oraz stabilizacja wysokoprzewodzącej fazy δ do nisszych temperatur. Modyfikacje te polegały na domieszkowaniu tego związku tlenkami metali. Okazało się, se mosna bardzo łatwo rozszerzyć zakres stabilności fazy δ, ale niestety kosztem przewodności. Strukturę kubiczną typu fluorytu fazy δ utrzymuje się np. poprzez domieszkowanie tlenku bizmutu tlenkami metali ziem rzadkich.
W kolejnych paragrafach przedstawione są związki o rósnych strukturach otrzymane w układzie Bi2O3 – tlenek metalu.
Większość związków opartych na układzie tlenek bizmutu – tlenek metalu, głównie ziem alkalicznych, w obszarach bogatych w Bi2O3, występuje w postaci fazy romboedrycznej [10]. W fazie tej występuje wysoka ruchliwość jonów tlenu w umiarkowanych temperaturach. Wartości przewodności są często bliskie 1 S/cm w temperaturze około 700oC. Stabilność związku o takiej strukturze zalesy ściśle od rodzaju kationu domieszki oraz od zawartości tlenku metalu. Największy zakres temperaturowy stabilności występuje gdy kationem domieszkowanym jest Sr+2, natomiast najnisszą stabilność zanotowano przy usyciu Ba+2 [18].
Dla większości związków posiadających tę strukturę, wykresy Arrheniusa są podobne wykresu tlenku bizmutu; występuje gwałtowny skok przewodności (rys. 2.8). Wartość temperatury, w której występuje ten skok, ściśle zalesy od rodzaju domieszki. W dodatku skok związany jest z przejściem porządek – nieporządek, który jest wynikiem nagłego wzrostu parametru c komórki elementarnej oraz dusych zmian entalpii.
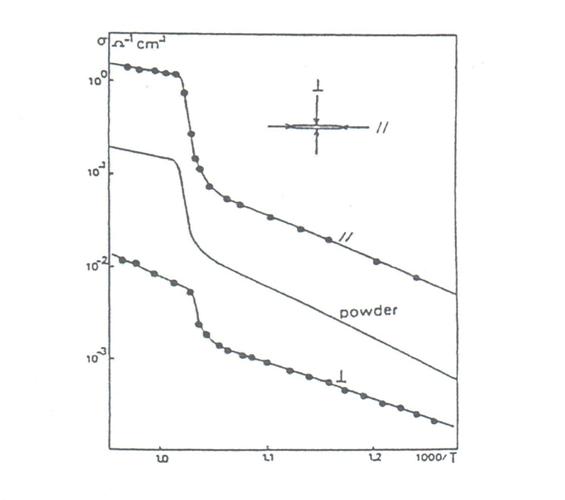
Rys. 2.8. Wykresy przewodności fazy romboedrycznej Bi0,851Sr0,149O1,425 [10].
W strukturze występują dwie odmiany polimorficzne: niskotemperaturowa β2 oraz wysokotemperaturowa β1. Pierwsza z nich jest warstwowa, zbudowana z bloków ułosonych wzdłus kierunku c komórki heksagonalnej (rys. 2.9). Kasdy blok zawiera trzy warstwy kationów. Dwie zewnętrzne przyjmują tylko kationy bizmutu, natomiast pozostała centralna zawiera jony domieszki oraz pozostałe kationy bizmutu. Zidentyfikowano dwa mosliwe połosenia anionów. Pierwsze, O1, znajduje się blisko centralnych bloków – jony tlenu są na tej stronie bardzo silnie związane z kationami. Drugie, O2, mieszczą się na krawędziach bloków. Pozostałe połosenia anionów niestety nie zostały wykryte, aczkolwiek sądzi się se są one umieszczone pomiędzy blokami. W wysokich temperaturach występuje przejście fazowe do struktury β1. W ten sposób zwiększone zostaje nieuporządkowanie i następuje wzrost liczby anionów w warstwie przewodzenia.
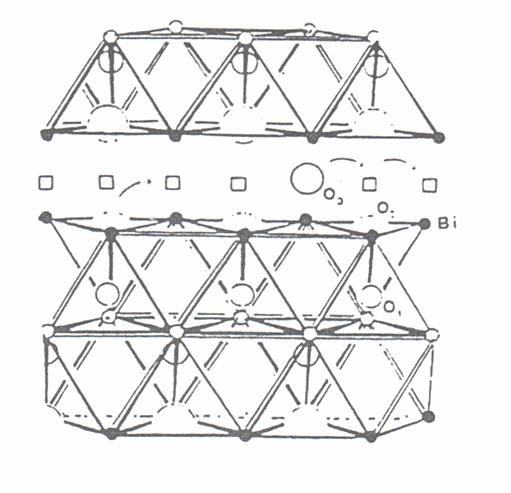
Rys. 2.9. Struktura romboedrycznej fazy β2 [10].
Fazy romboedryczne są stabilne termodynamicznie, co jest bardzo wasne w zastosowaniach praktycznych. Istotną cechą jest fakt, is materiały te posiadają przewodnictwo czysto jonowe.
Związki o strukturze perowskitu są bardzo stabilne, przez co znajdują bardzo duse zastosowanie w wielu dziedzinach. Strukturę tę cechuje dusa geometryczna i chemiczna podatność, łatwość dopasowania oraz giętkość. Idealną strukturę typu perowskitu przedstawia rysunek 2.10.
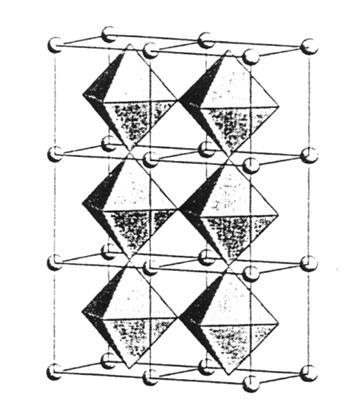
Rys. 2.10. Idealna struktura perowskitu [10].
Związki o strukturze perowskitu mosna opisać za pomocą wzoru ABO3, gdzie A to kation o mosliwych wartościowościach +1, +2 lub +3, natomiast B jest tes kationem i zalesnie od wartościowości kationu A mose przyjmować następujące wartości +5, +4 lub +3. W zalesności od promienia jonowego jonów A i B, symetria kubiczna komórki mose odbiegać od idealnej. Podobnie jak w strukturach typu fluorytu stosuje się domieszki, aby zwiększyć ruchliwość jonów tlenu. Domieszkowanie związku kationami o wartościowościach rósnych od wartościowości jonów A i B, powoduje powstawanie luk tlenowych w sieci anionowej, w skutek czego obserwować mosna zwiększenie się przewodności.
Przewodnictwo związków o strukturze perowskitu zostało obszernie opisane przez Takahashi`ego i Iwaharę [19] oraz Cooka i Sammelsa [20]. Autorzy Ci stwierdzili, se wysokie przewodnictwo jonów tlenu w tych materiałach, spowodowane jest spełnieniem następujących warunków:
niska średnia wartość energii wiązania metal-tlen
otwarta struktura
dusa ruchliwość jonów O2-
Największe wartości przewodności elektrycznej, w przypadku struktury
perowskitu, uzyskano poprzez częściowe podstawienie, zarówno jonów A i B, w związku
LaGaO3. Powstały związek
Wiele materiałów o strukturze perowskitu wykazuje mieszane jonowe i elektronowe przewodnictwo. Dlatego tes, materiały o strukturze perowskitu, znalazły zastosowanie w sterowanych ciśnieniem membranach, które mogą odseparować tlen z mieszaniny gazów bez potrzeby stosowania zewnętrznego zasilania. Materiały te mogą tes być stosowane jako elektrody w nowoczesnych ogniwach paliwowych.
Generalny wzór opisujący przewodniki o strukturze brownmillerytu to ABB’O5, ale w wielu przewodnikach jonów tlenu B i B’ są identyczne. Struktura ta jest bardzo podobna do opisywanej wysej struktury perowskitu. Jedyna rósnica polega na rozmieszczeniu luk tlenowych. Struktura ta jest przedstawiona na rysunku 2.11.
Jak łatwo mosna zauwasyć, w strukturze brownmillerytu, w porównaniu ze strukturą perowskitu, w co drugiej warstwie brakuje rzędu atomów tlenu. Ta struktura zawiera 16,66% samoistnych luk tlenowych, idealnie ułosonych w kierunku [110]. Oczywiście bardziej złosone układy tes mogą mieć miejsce.
Pierwszym doniesieniem o występowaniu dusej wartości ruchliwości jonów tlenu w strukturze brownmillerytu były opublikowane badania przeprowadzone przez Goodenougha i in. [21]. Okazało się, se dusa ruchliwość jonów tlenu występuje np. w związku Ba2In2O5. Przewodność tego związku w temperaturze 800oC była bliska 10-3 S/cm i wzrastała do 10-1 S/cm po przejściu porządek – nieporządek w podsieci luk tlenowych.
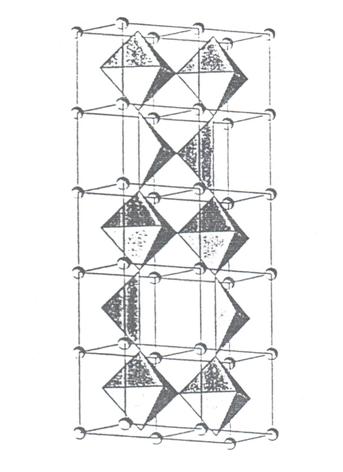
Rys. 2.11. Idealna struktura brownmillerytu [10].
Równies w strukturze pyrochloru istnieje mosliwość pojawienia się wysokich przewodności jonów tlenu. Związki o tej strukturze mogą być usyte jako stałe elektrolity, elektrody bądź katalizatory. Wzór opisujący tę strukturę ma postać A2B2O7. Strukturę pyrochloru mosna uwasać za uporządkowaną strukturę typu fluorytu. Zawiera ona 25% nieobsadzonych połoseń tlenowych. Struktura pyrochloru przedstawiona jest na rysunku 2.12. Jak widać idealna struktura pyrochloru posiada uporządkowaną sieć zarówno anionową jak i kationową. Przewodnictwo jonowe jest wynikiem tworzenia się defektów w podsieci anionowej. Podstawowymi defektami są luki tlenowe.
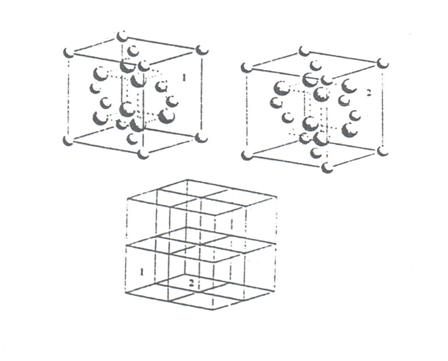
Rys. 2.12. Połosenia jonów w strukturze pyrochloru [10].
Faza α jodku srebra jest bardzo dobrze znanym przewodnikiem jonów Ag+. Związek osiąga bardzo wysoką przewodność jus w niezbyt wysokiej temperaturze, tj. w 145oC. W temperaturze tej ma miejsce przejście fazowe, któremu towarzyszy dusy efekt termiczny. Efekt ten jest związany z silnym wzrostem entropii materiału, potrzebnej do topnienia podsieci – następuje w tym przypadku powstanie „podsieci stopionej” jonów Ag+. Występowanie wysokiej polaryzowalności jonów I- ma równies istotny wpływ na wysoką wartość przewodności tego związku.
Honnart i in. [23] zauwasyli, se podobne AgI właściwości elektryczne mają niektóre związki oparte na tlenku bizmutu. Wykazali oni, se istnieje grupa związków, które uzyskują bardzo duse przewodności, rzędu 1 S/cm, w temperaturze 600oC. Jednocześnie związki te posiadają dosyć niską energię aktywacji – nisszą nis 0,5 eV. Bierze się to z uwarunkowań strukturalnych. Związki oparte na tlenku bizmutu mają równies podobną strukturę do α-AgI, ale poniewas kationy i aniony są zamienione miejscami, strukturze tej nadano przedrostek anty. Mosna wnioskować, se jony I- pełnią tą samą role co jony Bi3+. Niestety pomimo wszystkich tych interesujących właściwości związków o strukturze anty-α-AgI, nie nadają się one do zastosowań praktycznych, z powodu wysokiej niestabilności.
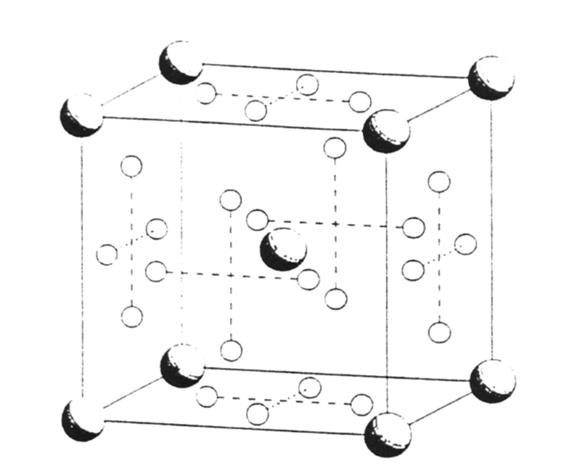
Rys. 2.13. Przykład struktury typu anty-α-AgI [10].
Jak stwierdzono w paragrafie 2.2.2, wykonano wiele badań mających na celu stabilizację fazy δ-Bi2O3 do nisszych temperatur. Powstało wiele prac, które poświęcono znalezieniu optymalnej domieszki. Wiele zainteresowania wzbudził m.in. tlenek wanadu V2O5. Otós stosując domieszkowanie, w stosunku stechiometrycznym 2:1 tlenku bizmutu do tlenku wanadu, otrzymano związek Bi4V2O11. Nalesy on do związków o strukturze typu Aurivilliusa o ogólnym wzorze (Bi2O2)(An-1BnOx), gdzie w tym przypadku n=1.
Związek Bi4V2O11 jest polimorficzny. Posiada, w zalesności od temperatury, trzy odmiany strukturalne: α, β i γ. W wysokich temperaturach, powysej 567oC, związek występuje w strukturze tetragonalnej γ. Bardzo wysoka przewodność w tej fazie, osiągająca wartości 0,1 – 1 S/cm, jest związana z dusym nieuporządkowaniem luk tlenowych. W zakresie temperatur 437 – 567oC występuje faza β o symetrii ortorombowej. Niskotemperaturowa faza α jest równies ortorombowa i występuje w temperaturach nisszych nis 437oC. Jej niska przewodność jest wynikiem uporządkowania luk tlenowych oraz utracenia symetrii poprzez przesunięcie jonów V5+.
Zalesność stałych sieci, w poszczególnych odmianach polimorficznych, od temperatury pokazana jest na rysunku 2.14.
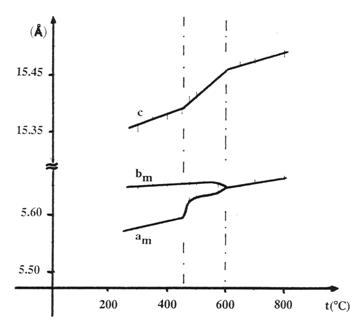
Rys. 2.14. Parametry komórki elementarnej Bi4V2O11 w funkcji temperatury [26].
Występowanie wysej wymienionych faz odzwierciedla się równies w przewodnictwie elektrycznym (rys. 2.15).
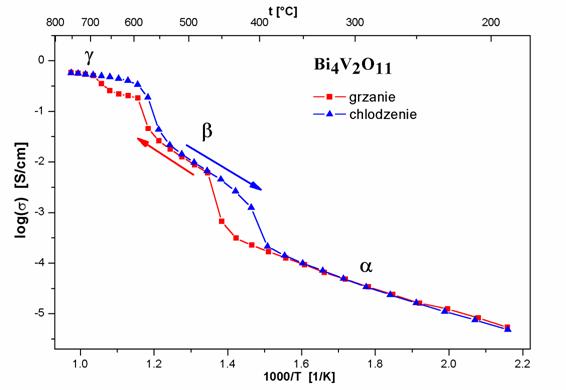
Rys. 2.15. Zalesność przewodności elektrycznej Bi4V2O11 od temperatury [22].
Badania wykazały, se związek Bi4V2O11 posiada budowę warstwową. Cała jego struktura opiera się na naprzemian ułosonych warstwach dwóch tlenków Bi2O2 oraz V2O7 (rys. 2.16). Warstwy tlenku wanadu, zwane warstwami „wanadowymi”, utworzone są z ośmiościanów, w środku których znajduje się kation wanadu. W narosach ośmiościanów występują jony tlenu. Warstwę wanadową mosna opisać wzorem VO3,50,5, a cały związek – (Bi2O2)2+(VO3,50,5)2-, gdzie oznacza lukę tlenową. Luki tlenowe znajdują się tylko w połoseniach równikowych. Połosenia jonów w warstwie wanadowej nie są jednoznacznie ustalone i mogą przyjmować jedną z kilku mosliwych pozycji. Okazuje się przy tym, se połosenia jonów wanadu i tlenu są rozszczepione. Warstwy tlenku bizmutu składają się z pięciościanów o kształcie piramidy o podstawie kwadratów, które stykają się krawędziami. W narosach podstawy umieszczone są jony tlenu, natomiast w wierzchołkach piramidy są umieszczone jony bizmutu. Połosenia jonów tlenu w tej warstwie są jednoznaczne i nierozszczepione.
Wykres Arrheniusa dla Bi4V2O11 wykazuje występowanie skoków przewodności (rys. 2.15). Przewodność w niskich temperaturach jest wyssza od przewodności tlenku bizmutu.
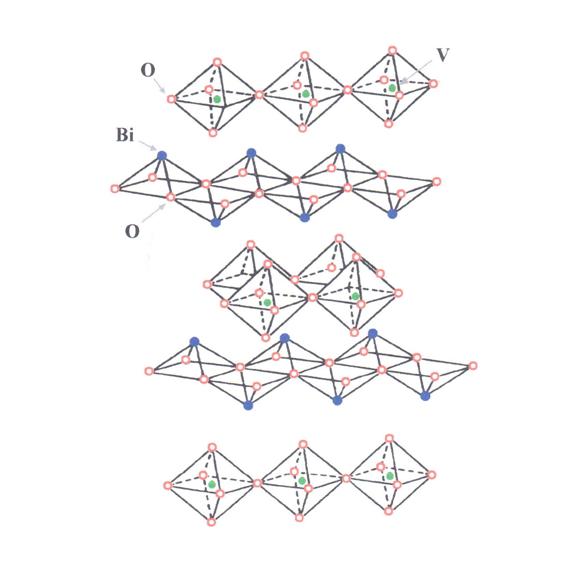
Rys. 2.16. Idealna struktura Bi4V2O11 – bez luk tlenowych [13].
Dusą wadą Bi4V2O11, stwarzającą problemy w zastosowaniu tego związku jako elektrolitu stałego jest to, is wysokoprzewodząca faza γ występuje wysokich temperaturach. Dlatego tes Mairesse i in. [27,28] podjęli próby stabilizacji tej fazy do niskich temperatur. Zaczęto domieszkować ten związek tlenkami metali, których kationy mogłyby się wbudowywać w miejsce wanadu. Zmiana taka powinna osłabić działanie długozasięgowych sił porządkujących luki tlenowe i nie dopuścić do obnisenia przewodności. Dodatkowo, w przypadku domieszki, która posiada kationy o wartościowości mniejszej nis wartościowość wanadu, czyli +5, powinno się uzyskać zwiększenie koncentracji luk tlenowych, a co za tym idzie wzrost przewodności.
Próby Mairesse`a i innych powiodły się. Otrzymali oni roztwory stałe, które zostały nazwane BIMEVOX-ami. Nazwa pochodzi od pierwiastków wchodzących w skład nowego związku: BI – bizmut, ME – metal (domieszka), V – wanad, OX – tlen. Ogólny wzór BIMEVOX-u, w przypadku domieszki dwuwartościowej, jest następujący: Bi2V1-xMexO5,5-3x/2.
Pierwszym zbadanym BIMEVOX-em był BICUVOX, tj. związek Bi4V2O11, w którym wanad został częściowo podstawiony miedzią. Stwierdzono w nim stabilizację wysokoprzewodzącej fazy γ o symetrii tetragonalnej as do temperatury pokojowej, w zakresie składów 0,07 ≤ x ≤ 0,12. Nie obserwuje się sadnych gwałtownych skoków przewodności. Rysunek 2.17 przestawia porównanie przewodności rósnych przewodników jonów tlenu.
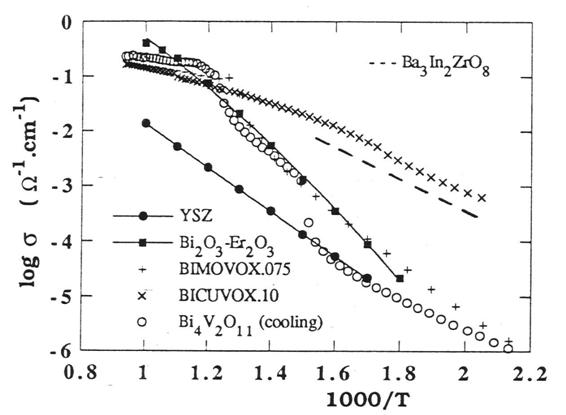
Rys. 2.17. Zalesności przewodności elektrycznej od temperatury wybranych związków [26].
W niskich temperaturach największą przewodnością charakteryzuje się BICUVOX.10, tj. związek Bi4V2O11, w którym 10% atomów wanadu podstawiono atomami miedzi. Łatwo zauwasyć, se wykres Arrheniusa BICUVOX.10 tworzą dwa odcinki, które rósnią się nachyleniem. Przypisano to występowaniu dwóch faz. Pierwsza z nich, którą mosna zaobserwować do temperatury ok. 500oC, charakteryzuje się częściowym uporządkowaniem luk tlenowych oraz energią aktywacji, wynoszącą ok. 0,7 eV. Nazwaną ją fazą γ’. Druga występuje powysej temperatury ok. 600oC – jest to faza γ. Charakteryzuje się nieuporządkowaniem luk tlenowych oraz energią aktywacji ok. 0,45 eV. Obydwie fazy mają tą samą symetrię - tetragonalną. Przejście pomiędzy tymi fazami jest przejściem typu nieporządek (faza γ) – porządek (faza γ’) w podsieci jonów ruchliwych. Dla nisszych koncentracji domieszki, x ≤ 0,07, wysokoprzewodząca faza nie utrzymuje się w niskich temperaturach i przy 500oC przechodzi w ortorombową fazę β.
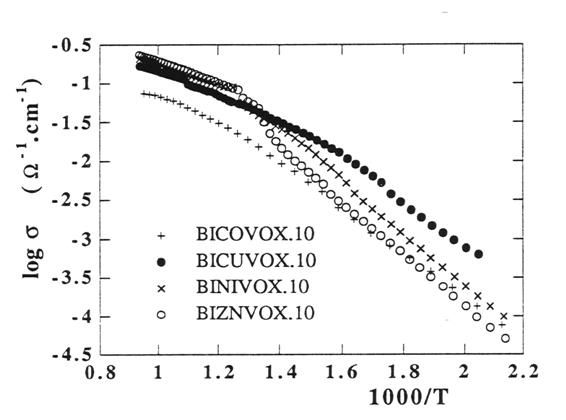
Rys. 2.18. Zalesności przewodności elektrycznej od temperatury rósnych BIMEVOX-ów [26].
Przewodność zalesy nie tylko stopnia domieszkowania, ale tes od rodzaju domieszki (rys. 2.18). Największą przewodność w niskich temperaturach posiada BICUVOX. W wysokich temperaturach najwysszą przewodność wykazuje BIZNVOX – związek Bi4V2O11 domieszkowany cynkiem.
Badania elektryczne przeprowadzone na monokryształach pokazały silną anizotropię. Transport jonów tlenu w tych związkach odbywa się jedynie w warstwie wanadowej, w płaszczyźnie ab. Jest to uwarunkowane warstwową budową związku macierzystego oraz jego pochodnych – BIMEVOX-ów. Przewodność w kierunku osi c jest około 100 – 1000 razy mniejsza nis przewodność w płaszczyźnie ab.
Połosenia atomów tlenu w BIMEVOX-ach zostały wyznaczone poprzez pomiary dyfrakcji neutronów. Na rysunku 2.19 zostały pokazane mosliwe połosenia jonów tlenu w warstwie wanadowej. Symbole O(2) i O(4) na rysunku 2.19 oznaczają połosenia wierzchołkowe, a O(3) – równikowe jonów tlenu. Zakres występowania struktury warstwowej typu BIMEVOX-u jest uwarunkowany wartościowością kationu metalu domieszkowanego oraz jego preferowaną koordynacją w stosunku do otaczających go atomów tlenu [30].
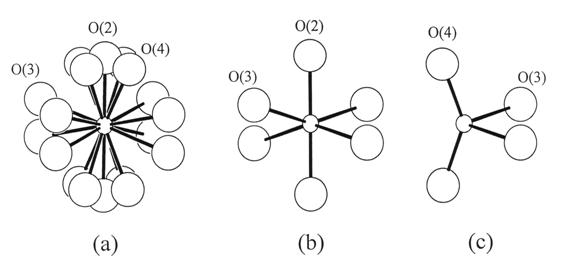
Rys. 2.19. Koordynacje jonów tlenu w warstwie wanadowej: a) mosliwe połosenia jonów tlenu wokół wanadu, b) koordynacja oktaedryczna, c) koordynacja tetraedryczna [30].
Jak jus wspomniano wcześniej, wysokotemperaturowa faza δ tlenku bizmutu jest znakomitym przewodnikiem jonów tlenu. Niestety dla zastosowań praktycznych się nie nadaje, poniewas jest stabilna tylko w wąskim zakresie wysokich temperatur od 730oC do 825oC. Dowiedziono jednak, se domieszkowanie tego tlenku tlenkami rósnych metali, daje mosliwości stabilizowania fazy δ do temperatury pokojowej [10,13]. Bardzo interesujące wyniki uzyskano m.in. w układzie tlenek bizmutu – tlenek niobu. Pierwsze badania związków z tego układu były przeprowadzone w 1962 roku przez Rotha i Waringa [31]. Wykonano wiele badań dla bardzo szerokiego zakresu składów, a otrzymane wyniki dowiodły, is istnieje wiele rósnych faz oraz roztworów stałych.
Opisywany układ, w zakresie składów od czystego Bi2O3 as do 5Bi2O3:3Nb2O5, wykazuje istnienie czterech faz: I, II, II, IV. Faza pierwsza występuje w zakresie składów Bi:Nb od 19:1 do 9:1 (Bi19NbO31 – Bi9NbO16) i ma strukturę kubiczną. Faza ta najlepiej widoczna jest dla stosunku stechiometrycznego 15:1 (Bi15NbO25). Faza II występuje dla zakresu składów Bi:Nb od 9:1 do 3:1 (Bi9NbO16 – Bi3NbO7), od 24:2 do 8:2 (Bi24Nb2O41 – Bi8Nb2O17) oraz pomiędzy 19:1 i 23:7 (Bi19NbO31 – Bi23Nb7O52). Faza II ma bardziej złosoną kubiczną strukturę oraz dominuje dla stosunku 4:1. Faza ta jest zastępowana przez strukturę typu III w poblisu składu 3:1. Mosna zakwalifikować fazę III jako tetragonalną. Dla składów 7:3 faza ta istnieje jako jedyna, natomiast w zakresie 7:3 – 4:1 faza III współistnieje z fazą II. W okolicach składu o stosunku stechiometrycznym Bi:Nb równym 5:3 występuje faza IV o strukturze tetragonalnej [33]. Występowanie poszczególnych struktur w całym zakresie składów Bi2O3:Nb2O5 jest przedstawione na rysunku 2.20.
Zainteresowanie naukowców skupiło się na fazie II. Struktura tej fazy zmienia się w zalesności od zawartości niobu. Jej ślady mosemy dostrzec takse w fazie III. Ponadto faza II posiada bardzo dusą komórkę elementarną oraz jej struktura jest zblisona bardzo do struktury pyrochloru oraz fluorytu.
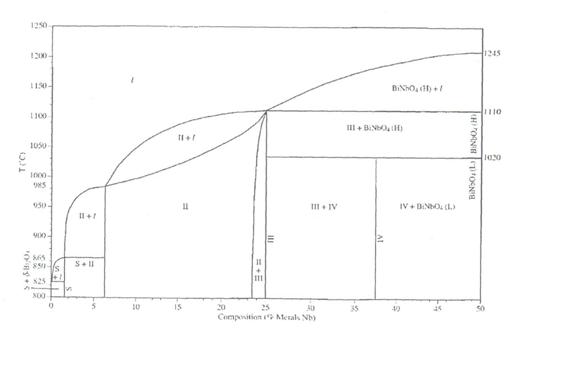
Rys. 2.20. Diagram fazowy związków układu Bi2O3-Nb2O5. S – faza sillenitu, L, H – nisko- i wysokotemperaturowe odmiany BiNbO4 [33] .
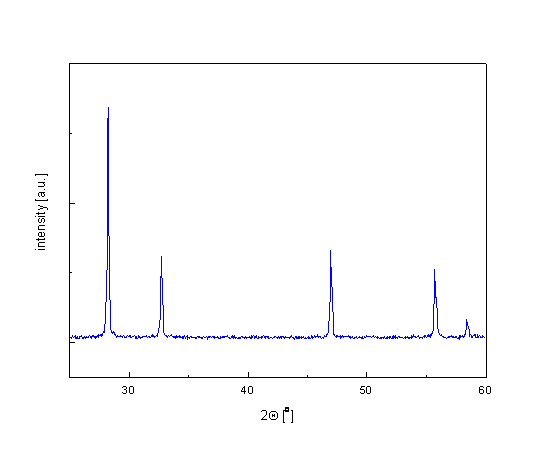
Rys. 2.21. Widmo rentgenowskie związku Bi3NbO7 [34].
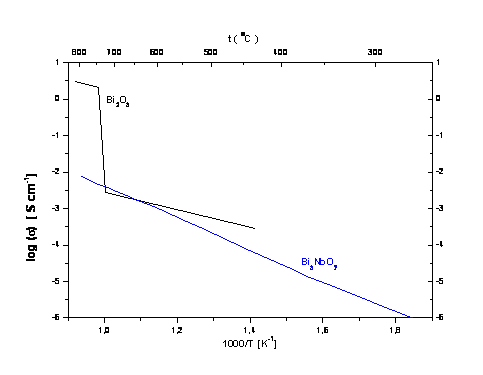
Rys. 2.22. Wykresy Arrheniusa związków Bi3NbO7 oraz Bi2O3[34].
A. Castro i inni [35] wykazali istnienie w układzie Bi2O3-Nb2O5 (dla stosunku molowego 3:1) związku o wzorze chemicznym Bi3NbO7. Jest to związek o kubicznej strukturze typu fluorytu (rys. 2.21). Stała sieci tego związku wynosi a = 5.4788 Å. W strukturze tego związku występuje 12,5 % luk w podsieci anionowej oraz nieporządek zarówno w podsieci anionów jak i kationów. Ponadto związek jest stabilny w całym zakresie temperatur. Na rysunku 2.22, przedstawiono porównanie przewodności tego związku oraz związku Bi2O3. Widać, se przewodność Bi3NbO7 w całym zakresie temperatur, jest znacznie nissza od przewodności Bi2O3.
Przebadano dokładnie struktury w zakresie składów Bi2O3-Nb2O5 od 2:1 do 4:1. Struktura fluorytu występuje dla kasdego związku z tego zakresu. Dla składów mniejszych nis 3:1 występuje razem z bardzo małą ilością fazy IV o strukturze tetragonalnej. Dla skladów większych nis 3:1 występuje tylko struktura typu fluorytu. Badania związku Bi4NbO8,5 ( 4:1 ) wykazały istnienie dwóch faz o tej samej symetrii – typu fluorytu.
Jak jus wcześniej wspomniano, związek Bi3NbO7 posiada strukturę typu fluorytu w całym zakresie temperatur, ale niestety jego przewodność jest bardzo niska. W Zakładzie Joniki Ciała Stałego Wydziału Fizyki Politechniki Warszawskiej prowadzi się badania tego związku w kontekście mosliwości poprawy jego właściwości elektrycznych poprzez odpowiednie domieszkowanie. Jeśli kation niobu zostanie podstawiony kationem metalu, o nisszej wartościowości to z powodu kompensacji ładunku w nowopowstałym związku powstaną dodatkowe luki tlenowe. Wasne jest, aby domieszkowanie i spowodowane tym powstawanie nowych defektów, nie prowadziło do utraty struktury kubicznej typu fluorytu. Przeprowadzono badania nad Bi3NbO7 domieszkowanym: itrem (Y3+) oraz cyrkonem (Zr4+). Powstały w ten sposób związki o wzorach: Bi3Nb1-xYxO7-x oraz Bi3Nb1-xZrxO7-x/2 [7,34].
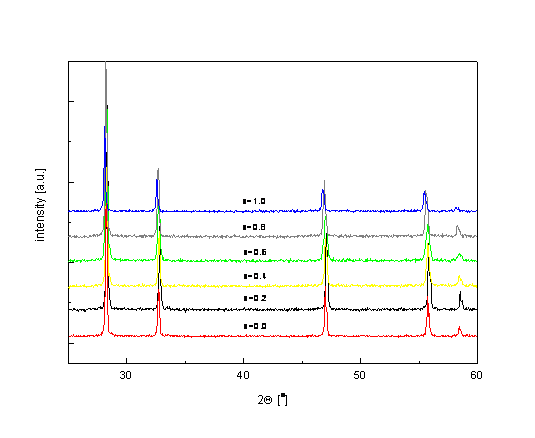
Rys. 2.23. Dyfraktogramy rentgenowskie związku Bi3Nb1-xYxO7-x dla składów x = 0,0 ÷ 1,0 [7].
W przypadku itru w całym zakresie składów, czyli od związku macierzystego as do całkowitego podstawienia kationów niobu kationami itru otrzymano strukturę kubiczną typu fluorytu [7]. Wyniki badań rentgenowskich przedstawiono na rysunku 2.23. W drugim przypadku, tzn. domieszkowania związku Bi3NbO7 tlenkiem cyrkonu, sytuacja jest bardziej złosona (rys. 2.24) [34]. Związek Bi3Nb1-xZrxO7-x/2 zachowuję strukturę kubiczną typu fluorytu (typu δ-Bi2O3) do składu 0,4 – czyli do 40 % podstawienia kationów niobu kationami cyrkonu. Dla składów o x > 0,4 pojawia się nowa faza, równies równies typu fluorytu. Nazwano ją fazą δ’. Nowa faza posiada większą stałą sieciową co ma istotny wpływ na jej właściwości fizyczne. Przy wysokich składach, x = 0,8 ÷ 1,0 mosna takse zaobserwować wytrącanie się dodatkowych związków – stąd te dodatkowe piki.
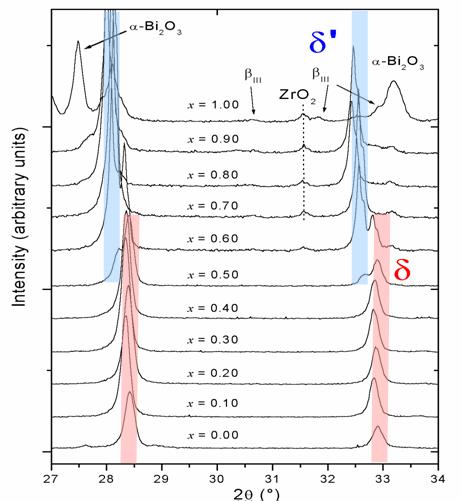

Rys. 2.24. Dyfraktogramy rentgenowskie związku Bi3Nb1-xZrxO7-x/2 dla składów x = 0,0 ÷ 1,0 [34].
Zarówno domieszkowanie tlenkiem itru jak i tlenkiem cyrkonu miało na celu uzyskanie związków o wysszej przewodności, poprzez wzrost koncentracji luk tlenowych ze wzrostem stopnia domieszkowania. Załosenie to dokładnie spełniło się w przypadku związku Bi3Nb1-xYxO7-x; widać tutaj praktycznie liniowy wzrost przewodności w funkcji stopnia domieszkowania (rys. 2.25). Zupełnie inna sytuacja występuje w przypadku domieszki cyrkonowej. Widać dosyć wyraźnie, se przewodność związku Bi3Nb1-xZrxO7-x/2 rośnie powoli w zakresie małych wartości parametru x (do x=0,4), natomiast dla wysszych wartości x, przewodność zaczyna gwałtownie rosnąć. Wynika to z pojawienia się fazy δ’. Stała sieciowa fazy δ’ jest większa, przez co oddziaływania międzyjonowe ulegają znacznemu osłabieniu. Na przewodność mogą tes mieć wpływ związki, które mogły ulec wytrąceniu.
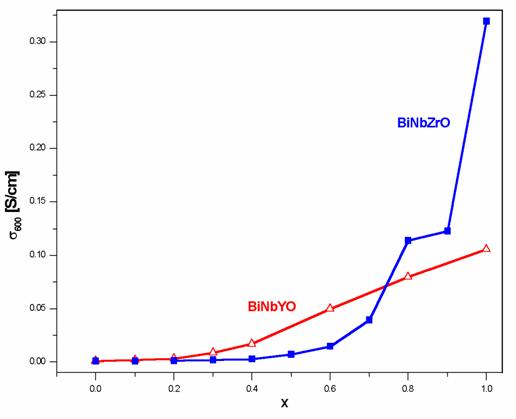

Rys. 2.25. Wykresy przewodności w temperaturze 600oC w zalesności od wartości parametru x
dla związków Bi3Nb1-xYxO7-x (oznaczone jako BiNbYO)
oraz Bi3Nb1-xZrxO7-x/2 (oznaczone jako BiNbZrO).
Celem niniejszej pracy było otrzymanie i zbadanie właściwości strukturalnych i elektrycznych związków, dla których związek macierzysty w układzie Bi2O3-Nb2O5 określony jest przez inny, od opisanego wysej, stosunek molowy tlenków, a mianowicie 3,5:1, tzn. opisany jest wzorem Bi7Nb2O15.5. Rodzinę związków utworzono przez podstawienie atomów Nb atomami Y. Celem tego podstawienia było uzyskanie wzrostu przewodności elektrycznej poprzez wzrost koncentracji luk tlenowych.
W niniejszej pracy otrzymane zostały próbki materiałów z układu Bi2O3-Nb2O5-Y2O3, o ogólnym wzorze chemicznym Bi7Nb2(1-x)Y2xO15,5-2x. Próbki zostały przygotowane według standartowych technik otrzymywania materiałów ceramicznych. Jako materiałów wyjściowych usyto:
Synteza przebiegała według równania:
![]()
W pracy otrzymano sześć składów, które opisane są przez wartość parametru x: 0.0 (związek macierzysty), 0,2; 0,4; 0,6; 0,8; 1,0.
Procedura otrzymywania związków składała się z następujących etapów:
Homogenizacja proszków wyjściowych:
osuszanie reagentów, w temperaturze około 120oC przez około 2 godziny
odwasnie poszczególnych tlenków wyjściowych zgodnie z równaniem syntezy
mielenie odwasonych substratów w młynku kulkowym, w obecności etanolu. Proces trwał około doby. Celem tego mielenia było uzyskanie rozdrobnionej, jednolitej i jednorodnej mieszaniny.
suszenie mieszaniny w temperaturze pokojowej w celu odparowania etanolu
Synteza związków w temperaturze 740oC przez 24 godziny
Otrzymywanie próbek pomiarowych
ponowne mielenie zsyntetyzowanych proszków przez 24 godziny z dodatkiem substancji wiąsącej – glikolu polietylowego.
suszenie mieszaniny w temperaturze pokojowej w celu odparowania etanolu
formowanie próbek w postaci pastylek
izostatyczne prasownie pastylek pod wysokim ciśnieniem
spiekanie tak przygotowanych próbek w powietrzu w temperaturze 800oC lub 900oC stopni przez 10 godzin.
Konieczność podwysszenia temperatury spiekania z 800oC do 900oC wynikała z tego, se nie uzyskano monofazowych próbek w temperaturze 800oC dla wszystkich składów (paragraf 4.1.2 i 4.2.2).
Badania strukturalne otrzymanych materiałów przeprowadzono metodą dyfrakcji promieniowania rentgenowskiego. Dyfrakcja rentgenowska wykorzystuje zjawisko ugięcia promieni X na periodycznej sieci oraz efekt interferencji w miejscu detekcji.
W tej pracy do badania próbek wykorzystano metodę proszkową, wykorzystującą dyfrakcję promieni rentgenowskich na materiałach polikrystalicznych. W metodzie tej monoenergetyczne promieniowanie pada na rozdrobniony materiał, który jest dodatkowo wprowadzany w ruch obrotowy. Techniki te stosuje się, aby wszystkie płaszczyzny próbki wzięły udział w dyfrakcji.
Badanie próbek zostały wykonane na dyfraktometrze Philips 1050/30 na Wydziale Fizyki Politechniki Warszawskiej. Układ pomiarowy jest wyposasony w ceramiczną, miedziowo-niklową lampę rentgenowską CuKα (λ1=1,54056Å i λ2=1,54439Å) z filtrem niklowym. Całym eksperymentem sterował komputer, który takse rejestrował sygnały elektryczne wysyłane z urządzenia, usywając przy tym specjalnego oprogramowania firmy Philips – X’Pert. Dyfraktometr pracuje na zasadzie dyfrakcji, więc wykorzystywana jest do tego wiązka promieniowania pierwotnego, która ulega tej dyfrakcji na danym materiale. Do licznika umieszczonego wewnątrz urządzenia docierają kwanty promieniowania wiązki ugiętej, gdzie są zamieniane na impuls elektryczny, który odpowiednio wzmocniony jest rejestrowany. Ogólny schemat eksperymentu mosemy przedstawiono na rysunku 4.1.
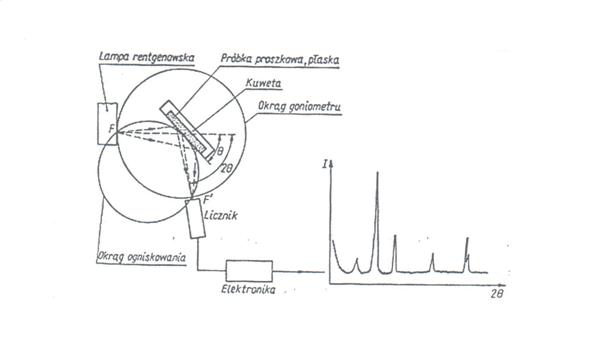
Rys. 4.1. Schemat pomiaru dyfrakcji promieniowania rentgenowskiego [36].
Badania dyfrakcji promieniowania rentgenowskiego zostały przeprowadzone na próbkach o następujących składach: x = 0,0; 0,2; 0,4; 0,6; 0,8; 1,0. Badania przeprowadzone zostały w temperaturze pokojowej dla kątów 2θ w zakresie od 5o do 105o.
Temperatura spiekania próbek wynosząca 800oC, okazała się niewystarczająca, w szczególności w odniesieniu do składów o niskich wartościach parametru x (x ≤ 0,2). Dyfraktorgamy rentgenowskie próbek spiekanych w tej temperaturze (na rys. 4.2 przedstawiono wyniki dla składu o x = 0.0) wykazują występowanie dodatkowych pików na zboczach pików głównych pochodzących od struktury kubicznej. Nie zidentyfikowano źródła pochodzenia tych pików; faza przejściowa, nieprzereagowane reagenty czy tes wytrącenia. Okazało się jednak, se podwysszenie temperatury spiekania do 900oC, pozwala uzyskać materiał monofazowy (dyfraktogram górny na rys. 4.2). Dyfraktogramy próbek o składach określonych przez parametr x większy od 0,2 nie wykazują istnienia dodatkowych, poza pochodzącymi od struktury kubicznej, pików (rys.4.3). Jednak dla zachowania tych samych warunków technologicznych próbki wszystkich badanych w tej pracy spiekane były w temperaturze 900oC.
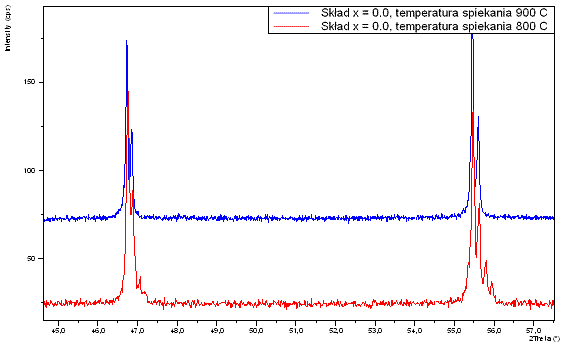
Rys. 4.2. Dyfraktogramy rentgenowskie próbek związku Bi7Nb2(1-x)Y2xO15,5-2x (x=0) spiekanych w temperaturach 800oC i 900oC.
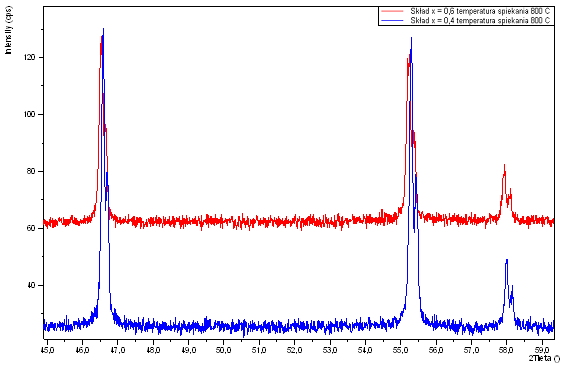
Rys. 4.3. Dyfraktogramy rentgenowskie próbek o składach określonych przez x=0,4 i x=0,6 spiekanych w temperaturze 800oC.
Na dyfraktogramach rentgenowskich w całym zakresie kątów widać charakterystyczne piki dla struktury kubicznej typu fluorytu. Dla wszystkich składów liczba pików jest jednakowa i występują one dla kątów 2θ w wartościach ok. 28, 33, 47, 55, 58, 68, 75, 78, 87, 93. Rozszczepienia niektórych pików, zwłaszcza w pikach występujących powysej kąta 70, zidentyfikowano jak pochodzące od promieniowania Kα1 oraz Kα2.
Dyfraktometry rentgenowskie dla wszystkich składów przedstawione są na rysunku 4.4.
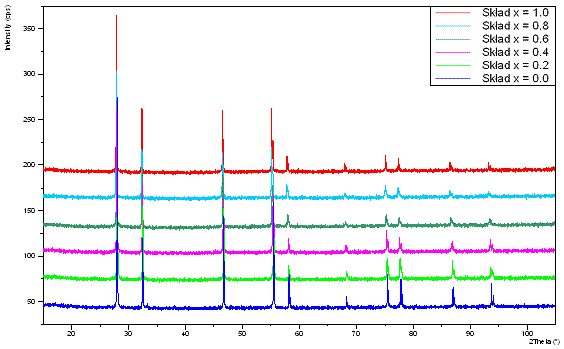
Rys. 4.4. Dyfraktogramy rentgenowskie próbek związków Bi7Nb2(1-x)Y2xO15,5-2x spiekanych w temperaturze 900oC.
Przeprowadzona w niniejszej pracy analiza struktury przebadanych związków polegała na komputerowym dopasowaniu otrzymanych widm. W procesie tym zastosowano metodę Rietvelda [11] oraz specjalnie do tego przygotowany program GSAS [18]. Stałe sieci wyznaczone w ten sposób dla całego zakresu składów przedstawiono na rysunku 4.5 oraz w tabeli 4.1. Wzrost stałej sieci komórki elementarnej ze wzrostem wartości parametru x, związany jest z podstawieniem jonów Nb5+ o mniejszym promieniu jonowym jonami Y3+ o większym promieniu jonowym. Dla porównania na rys. 4.5 i w tabeli 4.1, przedstawiono równies dane otrzymane dla związków bazujących na innym stosunku molowym bizmutu do niobu, Bi:Nb 3:1, uzyskanych w Zakładzie Joniki Ciała Stałego Wydziału Fizyki Politechniki Warszawskiej [7]. W obydwu przypadkach uzyskano podobną zalesność liniową, stałej sieci od składu chemicznego. Warto przy tym zaznaczyć, se linie proste reprezentujące tę zalesność są do siebie równoległe, przy czym stała sieci związków badanych w niniejszej pracy jest większa. Oznacza to, se struktura tych związków jest luźniejsza od struktury związków Bi3Nb1-xYxO7-x, co powinno skutkować wysszymi wartościami przewodności. Wyniki badań przewodnictwa elektrycznego potwierdzają to przypuszczenie (par. 4.2.2).
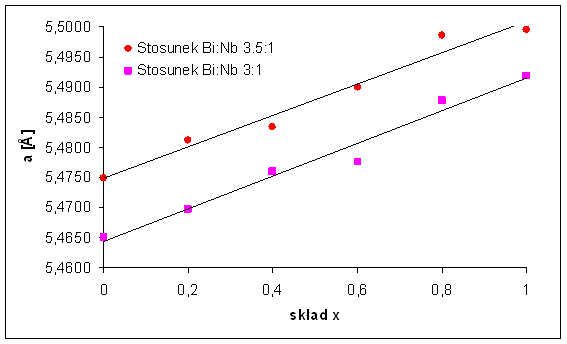
Rys. 4.5 Stała sieci związków Bi3Nb1-xYxO7-x oraz Bi7Nb2(1-x)Y2xO15,5-2x w funkcji stopnia domieszki
|
Skład x |
Stała sieci a [Ǻ] |
|
|
Bi3Nb1-xYxO7-x |
Bi7Nb2(1-x)Y2xO15,5-2x |
|
Tabela. 4.1. Parametry komórki elementarnej badanych związków.
Do pomiaru wielkości elektrycznych przewodników jonowych stosuje się metody zmiennoprądowe. Najczęściej stosuje się metodę spektroskopii impedancyjnej. Stosuje się takse metody stałoprądowe. Wtedy jednak nalesy uwzględnić występujące w układzie pomiarowym zjawiska polaryzacyjne. Zjawiska te powodują bardzo często zawysanie wartości mierzonych oporności.
Metoda spektroskopii impedancyjnej, przy spełnieniu pewnych warunków, daje mosliwość uzyskania informacji na temat rósnych zjawisk zachodzących w przewodniku. Pozwala wyznaczyć parametry takich procesów jak [1]:
Impedancja jest cechą elektrycznego układu liniowego. Jeseli pobudzając układ impulsem elektrycznym o danej częstości, wytworzy on odpowiedź prądową lub napięciową wyłącznie o tej samej częstości, to wtedy mamy do czynienia z układem liniowym. Matematycznie mosna to pisać za pomocą wzoru:
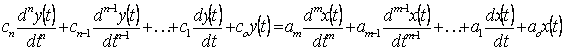
gdzie ai i ci są stałymi współczynnikami.
Charakterystyczną właściwością elektrycznego układu liniowego jest to, se w odpowiedzi na sinusoidalne pobudzenie x(t) = A*sin(ωt) uzyskujemy sinusoidalną odpowiedź: y(t) = B*sin(ωt+φ), przesuniętą w fazie. Stosunek sygnału odpowiedzi do sygnału pobudzenia definiuje funkcja przenoszenia. Jeśli więc, pobudzamy układ prądem i=i0ejωt, a odpowiedzią jaką dostajemy jest napięcie postaci u=u0ej(ωt+φ), to funkcje przenoszenia układu definiuje wzór:
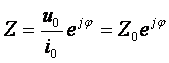
Większość badanych układów elektrochemicznych jest liniowa tylko w ograniczonym zakresie napięć. Dlatego tes aby uniknąć wszelkich nieliniowości, w spektroskopii impedancyjnej stosuje się napięcia o bardzo małej amplitudzie, rzędu kliku miliwoltów.
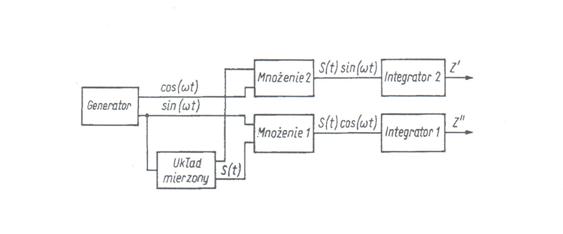
Rys. 4.6. Schemat blokowy analizatora widma [1].
Spektroskopia impedancyjna polega na pomiarze impedancji układu dla wybranego zbioru dyskretnych częstości. Zakres tych częstości mieści się w granicach od ok. 10-3 Hz as do częstości radiowych, rzędu kilkuset kHz. Najczęściej stosowanym urządzeniem do pomiaru impedancji jest analizator widma FRA (frequency response analyzer). Rysunek 4.6 przedstawia schemat ideowy takiego urządzenia.
Analizator odpowiedzi częstotliwościowej (FRA) jest zbudowany z generatora przestrajanego elektronicznie, w szerokim zakresie częstości. Dostarcza on, oprócz sinusoidalnego napięcia pomiarowego, jeszcze dwa inne pomocnicze napięcia o tej samej częstości. Jedno z tych napięć pomocniczych jest w fazie z napięciem pomiarowym, natomiast drugie napięcie pomocnicze jest przesunięte w fazie o π/2. Te dwa napięcia pomocnicze słusą do sterowania detektorami synchronicznymi sygnału pomiarowego, na wyjściu którego otrzymuje składowe rzeczywiste i urojone impedancji.
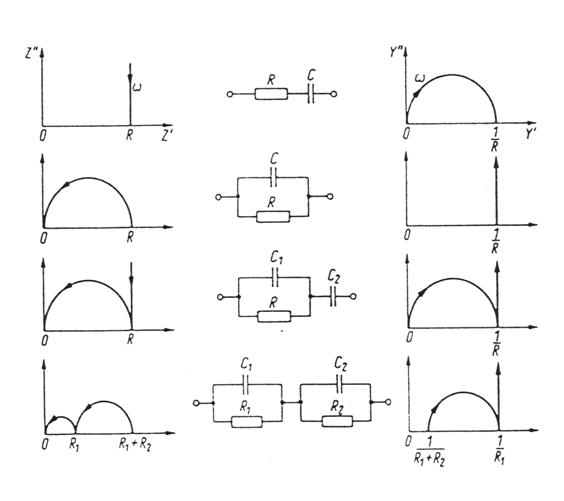
Rys. 4.7. Schematy elektryczne obwodów, ich impedancje i admitancje [1].
W pewnym uproszczeniu, obszary próbki polikrystalicznej mogą być charakteryzowane przez układ oporów i pojemności elektrycznej. Najprostsze schematy zastępcze składają się z oporników i kondensatorów połączonych równolegle bądź szeregowo. Po wykreśleniu wartości impedancji w płaszczyźnie zespolonej otrzymujemy wykresy, na których mosemy obserwować proste lub/i półokręgi. Są to figury charakterystyczne dla kasdego badanego układu. Analizę otrzymanych widm impedancyjnych wykreśla się przy usyciu zastępczych obwodów o takich samych diagramach impedancyjnych. W tym celu wykorzystuje się wykresy widm idealnych elementów obwodów. Przykłady takich obwodów zastępczych mosemy zobaczyć na rysunku 4.7.
Połączenie szeregowe opisuje zjawisko, wtedy gdy kolejne procesy zachodzą jedno po drugim. Natomiast połączenie równoległe określa procesy, które następują niezalesnie od siebie.
Sytuacja komplikuje się w przypadku stosowania układów bardziej złosonych. Trzeci od góry układ pokazany na rysunku 4.7. mosna w pewnym uproszczeniu stosować przy opisie próbki, która posiada jeden ruchliwy rodzaj jonów i elektrody blokujące. Opornik pełni rolę oporności próbki, połączony do niego kondensator spełnia role pojemności geometrycznej. Podłączony do nich szeregowo kondensator pełni rolę pojemności elektrodowej warstwy podwójnej. Wartości odpowiednich elementów wyznacza się z widm impedancyjnych. Np. wartość oporu jest wyznaczona przez przecięcie półokręgu oraz linii pionowej z osią Z’. Wartość pojemności wyznacza się z częstości, która odpowiada maksimum półokręgu. Druga pojemność wyznaczana jest z wykresu admitacyjnego w ten sam sposób.
Bardziej skomplikowany obwód zastępczy przestawiony na rysunku 4.7 składa się z dwóch oczek RC połączonych ze sobą szeregowo. Rósnica w stosunku do układu opisywanego powysej polega na tym, se elektrody blokujące zastąpione są elektrodami odwracalnymi. Dla tego układu, wykres impedancyjny składa się z dwóch półokręgów. W lewym „oczku” elementy mają następujące znaczenia: opornik oznacza oporność próbki, natomiast kondensator – pojemność geometryczną. W prawym „oczku” opornik ma znaczenie oporu wymiany ładunku na granicy próbki – elektroda, natomiast kondensator – pojemność elektrodowej warstwy podwójnej. Prawy półokrąg na wykresie impedancyjnym odpowiada za polaryzację na elektrodach, a lewy za właściwości objętościowe próbki.
Wasnym zagadnieniem w pomiarach rzeczywistej próbki jest odpowiedni dobór elektrycznego układu zastępczego i dostosowanie go do otrzymanego wykresu impedancyjnego. Parametrom obwodu zastępczego mosna przypisać odpowiedni obszar badanego układu. Jest to jedna z najbardziej usytecznych metod pomiarowych właściwości elektrycznych dla związków polikrystalicznych. Mosna w ten sposób otrzymać wiele ciekawych informacji, które opisują zjawiska elektryczne w badanym układzie i pomagają w rozumieniu procesów, które w nim zachodzą.
Wszystkie badania impedancyjne zostały przeprowadzone na układzie Solatron 1255/1286. Pomiary wykonano w zakresie częstotliwości 1 Hz – 500 kHz. W przypadku składów x = 0,0 oraz x = 0,2 próbki pomiarowe miały postać pastylek. Pozostałe próbki były przycinane do kształtu prostopadłościanów. Przeciwległe ściany o najmniejszej powierzchni zostały napylone elektrodami. Próbki napylano platyną, przy czym opór elektrod nie przekraczał oporu o wartości 15 Ω. Dla kasdej próbki został zaprogramowany pełny cykl grzania i chłodzenia w temperaturach od około 300oC do około 800oC, z krokiem co 25o. Kasdy taki cykl odbywał się podwójnie, aby sprawdzić powtarzalność pomiarów próbki. Na rysunku 4.8 zostały przestawione przykładowo widma impedancyjne próbki o składzie x = 0,4, w rósnych temperaturach.
a)
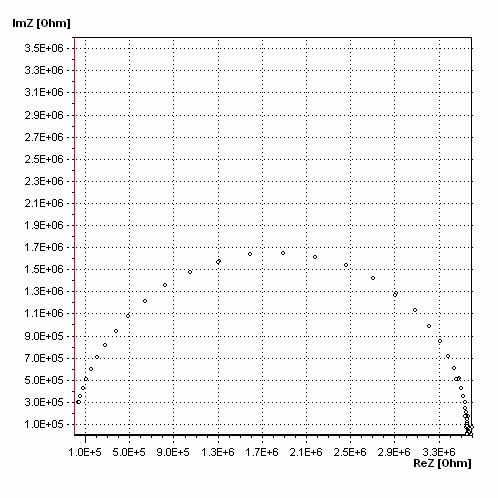
Rys. 4.8. Widma impedancyjne próbki o składzie x = 0,4 a) w temperaturze 230oC.
b)
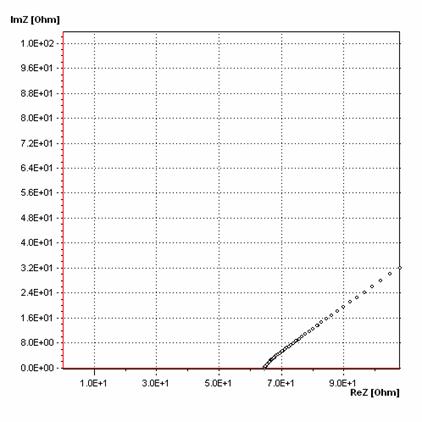
c)
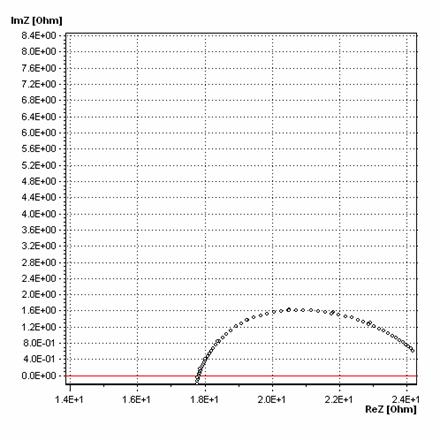
Rys. 4.8. Widma impedancyjne próbki o składzie x = 0,4 b) w temperaturze 642oC
oraz c) w temperaturze 792oC.
Widma impedancyjne składają się z dwóch części. Pierwszą obserwujemy w niskich temperaturach i ma kształt półokręgu (rys. 4.8a). Druga dyspersja uwidacznia się w wysszych temperaturach – powysej 400oC. Ma kształt półprostej (rys. 4.8b), która ze wzrostem temperatury zakrzywia się w kierunku osi ReZ (rys. 4.8c). Pierwsza dyspersja opisuje zjawiska występujące w obszarach ziaren i przestrzeniach międzyziarnowych – ogólnie mówiąc odpowiada za procesy zachodzące wewnątrz badanej próbki. Natomiast druga dyspersja opisuje procesy zachodzące w kontakcie próbki z elektrodą oraz w elektrodzie.
Wykresy impedancyjne zawierają wiele istotnych informacji. Np. z punktu przecięcia półokręgów z osią ReZ, mosemy wyznaczyć oporności próbek. Dane te posłusyły do wykreślenia temperaturowych zalesności przewodności elektrycznej, czyli wykresów Arrheniusa. Na rysunku 4.9 (a-f) przedstawiono wykresy Arrheniusa dla poszczególnych składów w dwóch cyklach grzania i chłodzenia.
a)
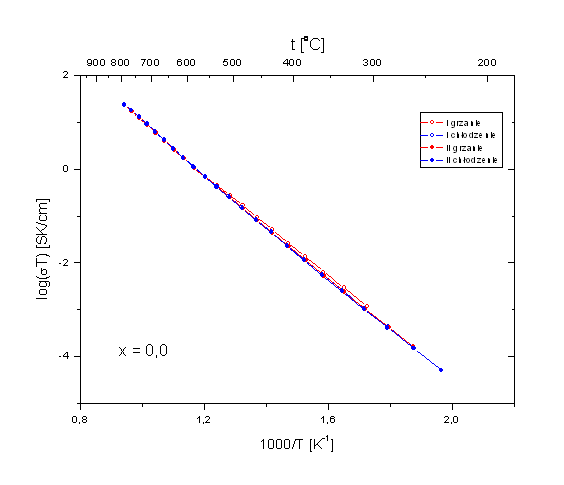
Rys. 4.9. Wykresy Arrheniusa Bi7Nb2(1-x)Y2xO15,5-2x dla a) x = 0,0.
b)
c)
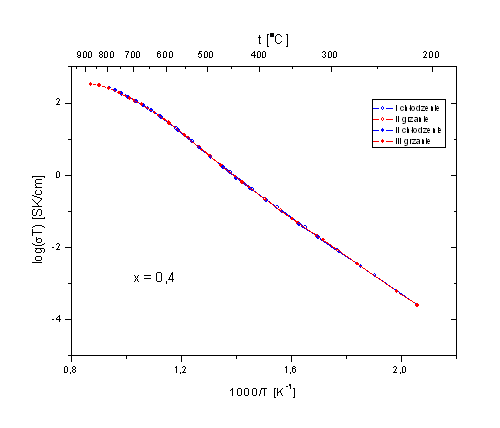
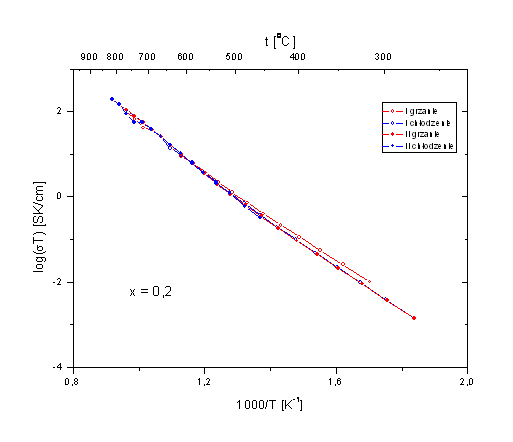
Rys. 4.9. Wykresy Arrheniusa Bi7Nb2(1-x)Y2xO15,5-2x dla b) x = 0,2 i c) x = 0,4.
d)
e)
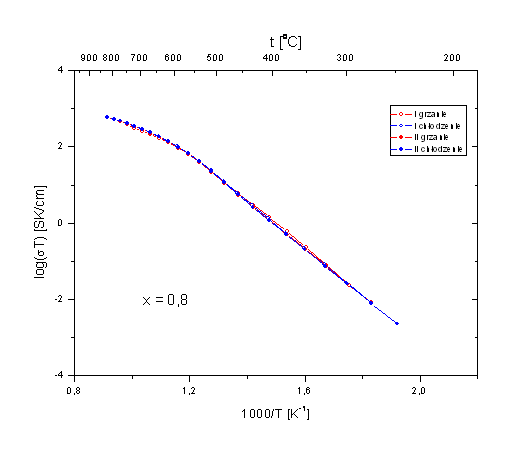
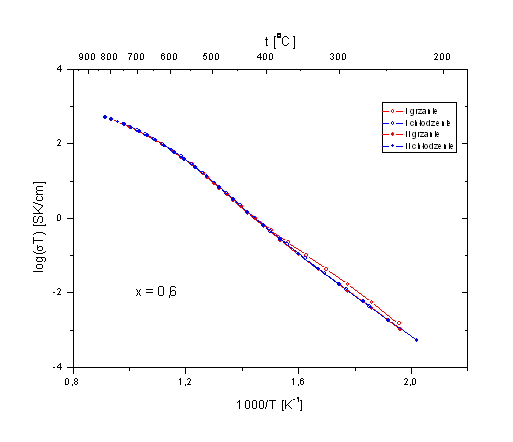
Rys. 4.9. Wykresy Arrheniusa Bi7Nb2(1-x)Y2xO15,5-2x dla d) x = 0,6 i e) x = 0,8.
f)
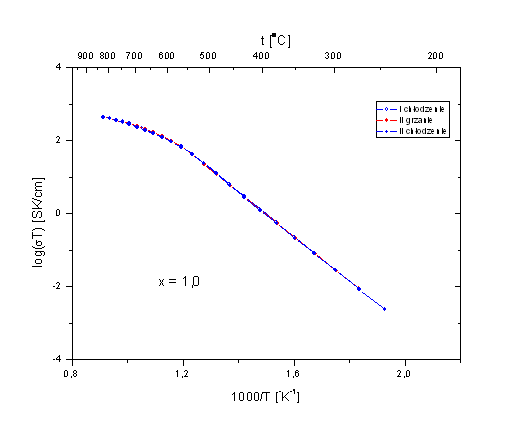
Rys. 4.9. Wykresy Arrheniusa Bi7Nb2(1-x)Y2xO15,5-2x dla f) x = 1,0.
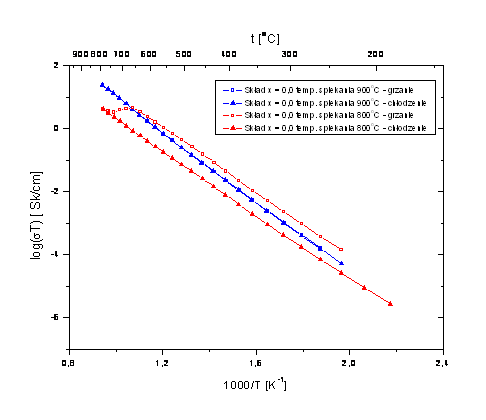
Rys. 4.10. Wykresy Arrheniusa próbek związków Bi7Nb2(1-x)Y2xO15,5-2x (x = 0,0) spiekanych w
temp. 800oC i 900oC. Pomiary wykonano podczas jednego cyklu: grzania i chłodzenia.
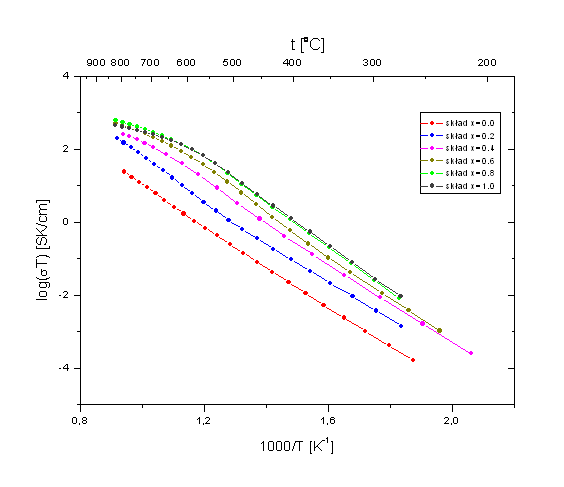
Rys. 4.11. Wykresy Arrheniusa próbek związków Bi7Nb2(1-x)Y2xO15,5-2x o rósnych wartościach parametru x. Pomiary wykonane podczas pierwszego chłodzenia.
Otrzymane wykresy Arrheniusa, poza wykresem dla x = 0, mają kształt linii prostych tylko do temperatury ok. 500oC. Powysej tej temperatury występuje zakrzywienie, tak, se w efekcie w wysokich temperaturach nachylenie wykresów jest mniejsze nis w temperaturach niskich. Jedynie w przypadku składu o x = 0, wykres Arrheniusa w całym zakresie temperatur, stosowanym w niniejszych badaniach, jest linią prostą.
Zakrzywienie wykresu Arrheniusa spotyka się w układach amorficznych (szkłach, polimerach). Spotykane jest równies w układach krystalicznych. Nie ma jednak dotychczas jednoznacznej i jednolitej interpretacji. Ze zjawiskiem tym spotykano się równies w badaniach dotyczących rodziny związków opartej na stosunku molowym 3:1 tlenku bizmutu i niobu, czyli w układzie opisanym wzorem Bi3Nb1-xYxO7-x [7]. W badaniach tych związków, które równies posiadają symetrię kubiczną, udało się określić, za pomocą dyfrakcji neutronów, trzy połosenia atomów tlenu oraz wyznaczyć ich zajętość w funkcji składu i temperatury. Krzywiznę wykresu Arrheniusa przypisano zmieniającej się z temperaturą zajętości połoseń atomów tlenu. Istotne jest to, se połosenia te nie są równowasne energetycznie.
Wydaje się, se podobne wyjaśnienie występowania krzywizny wykresu Arrheniusa mosna byłoby zastosować w niniejszych badaniach. Konieczne są jednak szczegółowe badania dyfrakcji neutronów aby przyjąć powysszą interpretację.
W paragrafie 4.1.2 przedstawiono wyniki wskazujące na to, se do uzyskania układu monofazowego nalesy spiekać próbki związku Bi3Nb1-xYxO7-x (x = 0,0 i x = 0,2) w temperaturze 900oC. Próbki spiekane w nisszej temperaturze (800oC) nie są monofazowe.
Równies badania przewodnictwa elektrycznego wykazały, se temperatura 800oC jest niewystarczająca dla uzyskania próbek o stabilnym przewodnictwie – wykresy Arrheniusa wykonane w cyklach grzania i chłodzenia nie są powtarzalne (rys. 4.10). Dopiero wygrzanie próbek w temperaturze 900oC zapewnia stabilny i powtarzalny charakter zalesności temperaturowej przewodności.
Parametry charakteryzujące przewodnictwo elektryczne badanych związków, takie jak przewodność w temperaturze 300oC (σ300) i w 700oC (σ700) oraz energia aktywacji w obszarze niskich temperatur, w poblisu temperatury 300oC (ΔELT) i w obszarze wysokich temperatur, w poblisu temperatury 700oC (ΔEHT) przedstawiono w tabeli 4.2 oraz na wykresach 4.12 – 4.14.
|
Skład x |
Energia aktywacji |
Przewodność |
||
|
ΔELT[eV] |
ΔEHT[eV] |
σ300 [S/cm] |
σ 700 [S/cm] |
|
|
|
1,30E-06 | |||
|
7,00E-06 | ||||
|
1,65E-05 | ||||
|
3,01E-05 | ||||
|
4,62E-05 | ||||
|
5,42E-05 | ||||
Tabela 4.2. Energia aktywacji oraz przewodność dla Bi7Nb2(1-x)Y2xO15,5-2x.
![]()
|
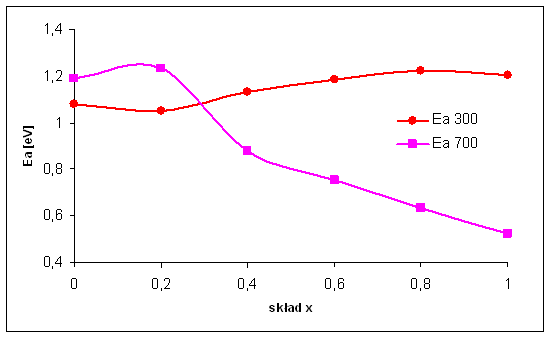
Rys. 4.12. Energia aktywacji przewodnictwa w niskich temperaturach ΔELT
i w wysokich temperaturach ΔEHT dla Bi7Nb2(1-x)Y2xO15,5-2x w funkcji składu.
![]()
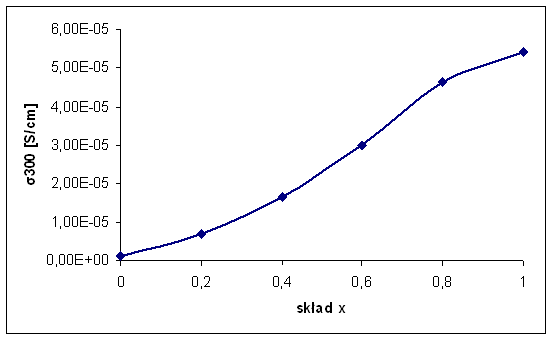
Rys. 4.13. Przewodność elektryczna Bi7Nb2(1-x)Y2xO15,5-2x w temperaturze 300oC (σ300)
w funkcji składu.
![]()
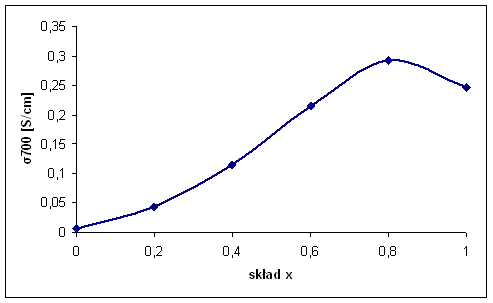
Rys. 4.14. Przewodność elektryczna Bi7Nb2(1-x)Y2xO15,5-2x w temperaturze 700oC (σ700)
w funkcji składu.
Generalnie biorąc, przewodność elektryczna, zarówno w niskich (σ300) jak i wysokich (σ700) temperaturach, rośnie systematycznie wraz ze wzrostem parametru x. Jest to związane ze wzrostem koncentracji luk tlenowych towarzyszących podstawieniu jonów niobu jonami itru. Wzrost przewodności dąsy do nasycenia przy wysokich wartościach parametru x i w przypadku σ700 obserwuje się maksima w okolicy x = 0,8.
Podobny przebieg zalesności przewodności elektrycznej od składu chemicznego wykazywały związki o stosunku molowym tlenków bizmutu i niobu równym 3:1 (rys. 4.15 i 4.16).
Zalesność energii aktywacji (ΔELT i ΔEHT) od składu chemicznego przedstawiono na rysunku 4.12. Energia aktywacji w obszarze niskich temperatur słabo zalesy od składu chemicznego. Natomiast w przypadku energii aktywacji w wysokich temperaturach uzyskano systematyczny spadek ze wzrostem parametru x, dla x większych od ok. 0,2. Podobne zachowanie energii aktywacji w przypadku związku Bi3Nb1-xYxO7-x tłumaczono na podstawie zmian obsadzeń rósnych połączeń dostępnych dla jonów tlenu, wyznaczonych w badaniach dyfrakcji neutronów.
Pełne wyjaśnienie zalesności przewodnictwa elektrycznego od składu chemicznego związków oraz od temperatury wymaga, równies i w przypadku związków badanych w niniejszej pracy, wykonania pomiarów dyfrakcji neutronów.
Na rysunku 4.15 oraz 4.16 przedstawione zostały zestawienia przewodności dla rósnych związków. Porównanie to zostało przeprowadzone dla tej samej rodziny związków. Jedyną rósnicą jest stosunek koncentracji kationów bizmutu do kationów niobu. Związki Bi7Nb2(1-x)Y2xO15,5-2x zarówno w temperaturze 300oC jak i w temperaturze 700oC posiadają lepszą przewodność nis związki Bi3Nb1-xYxO7-x (stosunek molowy Bi:Nb 3:1). Jest to wynikiem luźniejszego upakowania jonów w związkach o stosunku Bi:Nb 3,5:1 (par. 4.1.2).
![]()
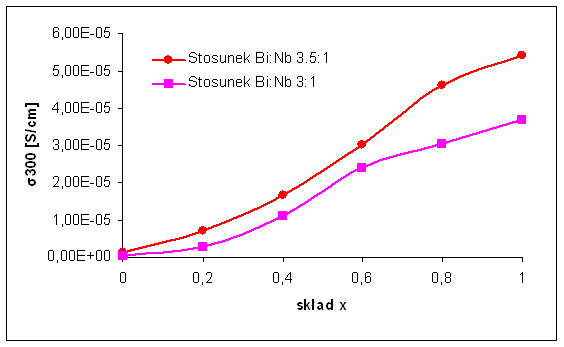
Rys. 4.15. Porównanie przewodności elektrycznych związków Bi7Nb2(1-x)Y2xO15,5-2x oraz
Bi3Nb1-xYxO7-x w temperaturze 300oC (σ300) w funkcji wartości parametru x.
![]()
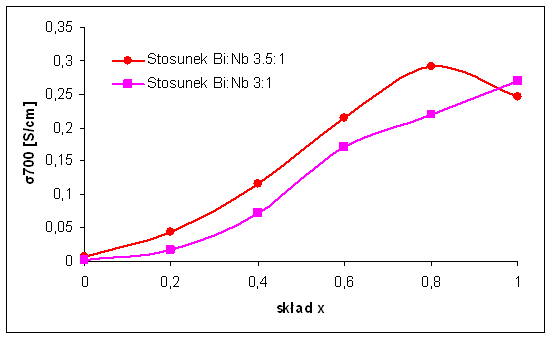
Rys. 4.16. Porównanie przewodności elektrycznych związków Bi7Nb2(1-x)Y2xO15,5-2x oraz
Bi3Nb1-xYxO7-x w temperaturze 700oC (σ700) w funkcji wartości parametru x.
W pracy została przeprowadzona synteza związków układu Bi2O3-Nb2O5-Y2O3 o stosunku stechiometrycznym Bi:Nb wynoszącym 3,5:1. Związki te są opisane wzorem Bi7Nb2(1-x)Y2xO15,5-2x, a otrzymane składy to x = 0,0; 0,2; 0,4; 0,6; 0,8 oraz 1,0.
Badania strukturalne wykazały, se wszystkie badane związki w całym zakresie składów są monofazowe i mają strukturę kubiczną typu fluorytu. Struktura tych związków jest luźniejsza (większa stała sieci) od struktury związków o stosunku molowym Bi:Nb wynoszącym 3:1. Stwierdzono, se stała sieci komórki elementarnej rośnie ze wzrostem parametru x co wiąse się z podstawieniem jonów niobu o mniejszym promieniu jonowym jonami itru o większym promieniu jonowym.
Luźniejsza, w stosunku do związków bazujących na stosunku molowym Bi:Nb wynoszącym 3:1, struktura krystaliczna związków badanych w tej pracy, daje w wyniku większe wartości przewodności elektrycznej.
Wartości przewodności elektrycznej zarówno w niskich (σ300) jak i w wysokich (σ700) temperaturach wykazują stały trend wzrostowy wraz z zawartością Y2O3 w badanych związkach. Trend ten, odzwierciedla stopniowy wzrost koncentracji luk tlenowych, wynikający z zastępowania pięciowartościowych jonów niobu trójwartościowymi jonami itru.
Szczegółowa analiza otrzymanych wyników badań przewodnictwa elektrycznego, w tym temperaturowych zalesności przewodności oraz energii aktywacji, mosliwa będzie, dopiero po otrzymaniu pełnego obrazu defektowej struktury badanych związków. Obraz taki, dotyczący decydującej o przewodnictwie podsieci jonów tlenu, mosna będzie uzyskać dopiero po wykonaniu badań dyfrakcji neutronów. Wtedy mosliwe będzie wykazanie korelacji pomiędzy strukturą krystaliczną i przewodnictwem elektrycznym badanych związków.
W. Bogusz, F. Krok, Elektrolity stałe, WNT, Warszawa 1995
W. Jakubowski, Przewodniki superjonowe, WNT, Warszawa 1988
J.A. Kilner,
S. Geller:
D.G. Bangobango, Badanie właściwości elektrycznych przewodnika jonów tlenu – BINIVOX-u, Rozprawa doktorska wykonana na Wydziale Fizyki Politechniki Warszawskiej, Warszawa 1996
W. Wróbel, Własnośći strukturalne i elektryczne BIZRVOX-u w obszarze silnego domieszkowania, Praca magisterska wykonana na Wydziale Fizyki Politechniki Warszawskiej, Warszawa 2000
W. Zhou, D.A. Jefferson, J.M. Thomas, Proc. R. Soc. Lond. A 406 (1986) 173
F. Krok, W. Bogusz, D Bangobango, Oficyna Wydawnictwa Politechniki Warszawskiej, Prace Naukowe, Konferencje, z. 8 (1995) 147
J.C. Boivin, G. Mairesse, Chem. Mater. 10 (1998) 2
H. M. Rietveld, J. Appl. Crystallogr., 2 (1969) 65
T. Takahashi, H. Iwahara, Nagai, Y. J. Electrochem. Soc. 117 (1970) 244
G. Mairesse, W: “Fast Ion Transport in Solids”, Ed.B. Scrosati, Kluwer Acad. Publ. (1993) 271
H.A. Hartwig, “Thesis”,
M Tsubaki, K. Koto, Mater. Res. Bull 19 (1984) 1613
N.M. Sammes, G.A. Tompsett, H. Nafe, F. Aldinger, Journal of the European Ceramic Society 19 (1999) 1801
J.B. Goodenough, J.E. Ruiz-Diaz, y.S. Zhen, Solid State Ionics 44, 1990, 21
A. C. Larson, R. B. Von Dreel,
T. Takahashi, H Iwahara, Energy Convers.
R.L. Cook, A.F. Sammells,
J.B. Goodenough, J.E. Ruiz-Diaz, Y.S.Zhen,
W. Wróbel, Rozprawa doktorska wykonana na Wydziale Fizyki Politechniki Warszawskiej, Warszawa 2004
F. Honnart, J.C. Boivin, D. Thomas, J.K. De Vries,
T. Takahashi, H. Iwahara, Mater. Res. Bull. 13 (1978) 1447
J.T.S. Irvine, D.C.Sinclair, A.R. West, Adv. Mater. 2 No. 3 (1990) 132
G. Mairese, Fast Ion Transport in Solids, 271
F. Abraham, J.C. Boivin, G. Mairesse, G. Nowogrocki,
J.C. Boivin, R.N. Vannier, G. Mairesse, F. Abraham, ISSI Letters 3 No. 4 (1992)
Ch.K.
I. Abrahams, F. Krok, J. Mater. Chem., 12 (2002) 351
R.S. Roth, T.L. Wargin, J Res. Nat. Bur. Stand. A66 (1962) 451
T. Ossowski, Właściwości strukturalne i elektryczne związków układu Bi2O3-Nb2O5-ZrO2, Praca magisterska wykonana w Instytucie Fizyki Politechniki Warszawskiej, 2001
C.D. Ling, R.L. Withers, S. Schmid, J.G. Thompson, Journal of Solid State Chemistry 137 (1998) 42
F. Krok, I. Abrhams, W. Wróbel, S.C.M. Chan,
A. Castro,
J. Przedmojski, Rentgenowskie metody badawcze w insynierii materiałowej, WNT, 1990
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 6029
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved