| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Sinteza ATP dependenta de gradientul protonic
Starea energizata a membranei este folosita direct pentru activitati fiziologice (transportul ionic, rotatia flagelului) sau pentru conversia ADP la ATP.
Ideea conversiei ADP la ATP, dependenta de gradientul protonic a fost propusa sub denumirea de teoria chemiosmotica sau chemiosmoza (Mitchell, l961). Procesul este rezultatul unei serii de reactii chimice ce se produc in si pe cele doua fete ale unei membrane.
Chemiosmoza are loc atat in membrana celulei procariote, cat si la nivelul membranei interne a mitocondriilor celulei eucariote.
Gradientul de concentratie protonica pe cele doua fete ale membranei genereaza un gradient electrochimic, o stare energizata a membranei, denumita forta proton-motrice*, care se exprima in volti si face ca membrana sa devina o baterie biologica.
*Reactiile fosforilarii oxidative, producatoare de E, sunt cuplate cu reactiile consumatoare, printr-o stare intermediara bogata in E, si nu printr-un compus chimic. Dupa Mitchell, starea intermediara este gradientul electrochimic de H+ prin membrana citoplamatica sau prin membrana mitocondriala interna, care cupleaza fluxul de E de la transportorii de e-, cu sinteza ATP. Substratul cuplarii este membrana intacta. E libera inmagazinata in gradientul de protoni s-a denumit forta proton-motrice.
Forta proton-motrice este convertita in energie chimica prin sinteza ATP din ADP, sub actiunea ATP-sintazei (ATP-aza). ATP-sintaza, localizata pe fata citoplasmatica a membranei, este considerata cel mai mic motor biologic cunoscut. Enzima este un complex format din cel putin l0 catene polipeptidice si are actiune reversibila pentru ca sintetizeaza ATP din ADP si Pi, dar catalizeaza si reactia inversa, de hidroliza a ATP la ADP, Pi, cu eliberarea energiei.
ATP-aza este alcatuita din subunitatea F1(formata din 5 polipeptide: α-3 copii, β-3 copii, g d e localizata pe fata interna a membranei si subunitatea Fo, transmembranara, ce formeaza un canal prin care trec protonii. Trecerea H+ prin Fo genereaza o forta de rotatie, transmisa subunitatii F1 prin subunitatea g Subunitatea g este rotorul care mediaza conversia intre curgerea H+ si sinteza ATP, iar F1 este statorul motorului ATP-azei. Energia de rotatie a motorului ATP-azei nu este folosita pentru propulsie, ci pentru sinteza ATP.
Evenimentele transportului de e- sunt influentate de doua clase de agenti chimici: inhibitori si decuplanti.
Inhibitorii blocheaza fluxul e- si astfel inhiba chiar forta proton-motrice: CO si CN-(cianida) se leaga strans de anumiti citocromi si inhiba functionarea lor.
Decuplantii inhiba sinteza ATP fara sa afecteze transportul e-: substantele liposolubile ca dinitrofenolul si dicumarolul cresc permeabilitatea membranei si astfel forta proton-motrice este anulata.
In compusii fosforilati, grupul fosfat este atasat prin atomul de O legat esteric. Nu toate legaturile fosfat sunt macroergice (fosfoenol-piruvatul).
Oxidoreductazele care folosesc alti acceptori de e-
Nitrat-reductaza este enzima implicata in respiratia anaeroba a nitratului, cupleaza fosforilarea respiratorie cu reducerea NO3-, in absenta O2. E. coli are 2 izoenzime nitrat-reductaze: NAR membranara si NAR periplasmica;
Nitrit-reductaza (periplasmica), catalizeaza doua reactii de transfer al e-:
reducerea NO2- --- NO (oxid nitric) + H2O
reducerea O2 ---- H2O
Reductaza oxidului nitric (NOR) converteste NO --- N2O, in reactia de denitrificare.
Dimetil sulfoxid reductaza (DMS), ancorata de membrana printr-un citocrom b.
Reductazele compusilor cu sulf, implicate in reducerea respiratorie a compusilor cu S.
Fumarat-reductaza reduce fumaratul ca acceptor final al unei catene transportoare de e-, rezultand succinatul.
Reactiile de oxido-reducere a componentelor catenei transportoare indeplinesc doua functii:
accepta e- de la un donor si ii transfera unui acceptor
conserva o parte din energie in procesele de fosforilare oxidativa.
Cantitatea mare de energie produsa in respiratie rezulta din transferul e- prin catena transportoare, de la un component cu nivel redox mai crescut, la altul cu nivel redox mai scazut. Energia este captata in legaturi macroergice, prin combinarea Pi cu ADP si formarea ATP.
Fosforilarile oxidative au loc concomitent cu transferul protonilor(H+) intre NADH-dehidrogenaza si flavoproteina, la jonctiunea CoQ/citocrom si la jonctiunea citocrom-oxidaza/O2.
Unele componente ale catenei de respiratie - flavoproteinele si quinonele - accepta numai protoni(H+), iar citocromii accepta numai e-.
In prezenta O2, setul de enzime al catenei de respiratie este abundent la bacteriile strict aerobe si la cele facultativ anaerobe, cand cresc in conditii de aerobioza.
Numeroase bacterii heterotrofe (chimioorganotrofe) realizeaza un metabolism aerob. Ele oxideaza substraturi organice, acceptorul final de e- fiind O2: M. tuberculosis, Bacillus sp., Pseudomonas, Agrobacterium etc.
Mecanisme de conservare a energiei
Functia chimica esentiala a proceselor metabolice producatoare de energie este aceea de a furniza compusi organici cu legaturi chimice cu continut energetic ridicat. Metabolitii fosforilati acumuleaza o cantitate variabila de energie libera.
Molecula cea mai importanta cu rol de transportor de energie este ATP, cu un continut de energie libera de 8 kcal/mol pentru fiecare legatura fosfat. ATP realizeaza un transfer de energie intre moleculele cu continut ridicat de energie libera si cele care participa la reactiile consumatoare de energie.
Reactiile de fosforilare in cursul carora sunt sintetizate molecule cu continut energetic ridicat si in special ATP prezinta un interes special pentru metabolismul energetic bacterian.
Valoarea energetica a unei cai metabolice se estimeaza dupa numarul de molecule de ATP sintetizate prin oxidarea unei molecule de substrat (de exemplu, glucoza).
Reactiile de fosforilare sunt de trei feluri si au sedii celulare distincte:
reactii de fosforilare la nivelul substratului, catalizate de enzime citoplasmatice;
reactii de fosforilare oxidativa, catalizate de enzimele localizate la nivelul membranei citoplasmatice si a intruziilor sale;
reactii de fosforilare fotosintetica.
Ciclul Krebs este initiat prin condensarea acetil-CoA cu oxaloacetatul, pentru a forma acidul citric (fig. 55). Intr-o succesiune de reactii ciclice se produce oxidarea aeroba a gruparii acetil, care provine nu numai din glicoliza sau din suntul hexozo-monofosfatului, ci si din beta-oxidarea acizilor grasi, ca si din degradarea catenei de carbon a majoritatii aminoacizilor. Ciclul Krebs furnizeaza compusii care initiaza caile de biosinteza.
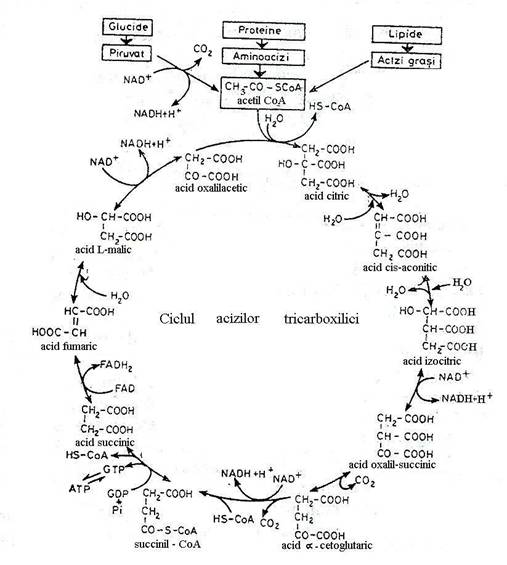
Fig. 55. Reactiile ciclului acizilor tricarboxilici (ciclul Krebs).
Fiecare tur al ciclului, pornind de la acetil-CoA elibereaza doua molecule de CO2 si 8 H+, sub forma a doua molecule de NADH + H+, una de NADPH + H+ si una de FADH2.
Experientele pe preparate mitocondriale denota ca in timpul transportului unei perechi de e- intre NAD si O2 se sintetizeaza 3 molecule de ATP. Randamentul energetic global al oxodarii unei molecule de glucoza prin glicoliza si prin ciclul Krebs este de 38 molecule ATP.
La bacterii, numarul real de molecule de ATP sintetizate nu este cunoscut, datorita prezentei ATP-azei. Determinarile indirecte sugereaza un bilant identic, dar masuratorile directe evidentiaza l6 molecule ATP/o molecula de glucoza.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 4754
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved