| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Aplicatia legii lui Hess
Principiul lucrarii:
Reactia de ardere a magneziului este reprezentata prin ecuatia reactiei urmatoare:
Mg(s) + ½O2(g) → MgO(s) (3.4.1)
Dar aceasta reactie se poate obtine prin combinarea urmatoarelor reactii chimice:
MgO(s) + 2 HCl(aq) → MgCl2(aq) + H2O (3.4.2)
Mg(s) + 2 HCl(aq) → MgCl2(aq) + H2(g) (3.4.3)
H2(g) + ½O2(g) → H2O(l) (3.4.4)
Scopul lucrarii: se va urmari determinarea entalpiei de reactie, utilizand legea lui Hess, pentru reactia de combustie a magneziului.
Aparatura si substante:
Aparatura: termometru, cilindru gradat,
bagheta de sticla, balanta analitica, vas Dewar, pahar Berzelius
Substante: Mg pulbere, MgO pulbere,
solutie HCl
Modul de lucru:
l intr-un pahar Berzelius, plasat in vasul Dewar, se pun 100 mL HCl 1 M si se citeste dupa cateva minute temperatura solutiei (T1);
l se adauga apoi 1g MgO pulbere sub agitare si se citeste dupa cateva minute temperatura amestecului (T2);
l se repeta operatia de mai sus, dar pentru 1g de Mg pulbere.
Calcule si rezultate:
Tabelul 3.4.1
|
A |
VHCl [mL] |
mMgO |
T1 [0C] |
T2 [oC] |
DT [oC] |
Q [kcal] |
nMgO |
DH [kcal/mol] |
|
B |
VHCl [mL] |
MMg |
T1 [0C] |
T2 [oC] |
DT [oC] |
Q [kcal] |
nMg |
DH [kcal/mol] |
unde:
Q - cantitatea de caldura din calorimetru (cal)
n - numarul de moli de substanta dizolvata (mol)
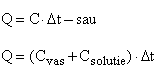 (3.4.5)
(3.4.5)
![]()
Cvas= 20 cal/grad
Csolutie= 100 cal/grad
Aratati combinarea ecuatiilor reactiilor chimice (3.4.2), (3.4.3) si (3.4.4), astfel incat sa se obtina ecuatia reactiei de combustie a Mg.
Tema de casa:
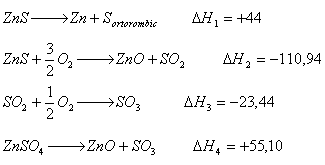
![]()
Daca se cunosc efectele termice ale urmatoarelor reactii:
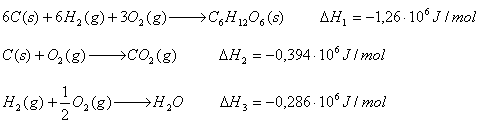
![]()
Calculati caldura de reactie care apare la obtinerea a 10m3 acetilena, daca se cunosc efectele termice ale urmatoarelor reactii chimice:
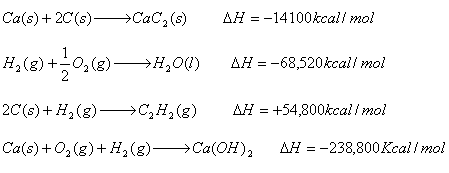
Sa se calculeze caldura de formare standard a H2SO4 conform reactiei :
S(s) + 2O2(g) + H2(g) H2SO4(l)
Daca se cunosc entalpiile standard ale urmatoarelor reactii :
1) S (s) +O2(g) SO2 (g) DH298= -70,96 kcal/mol
2) SO2(g) +1/2O2(g) SO3 (g) DH298 = -23,49Kcal/mol
3) SO3(g) +H2O(l) H2SO4(l) DH298 = -31,14 kcal/mol
4) H2 (g) + ½ O2(g) H2O (l) DH298 = -68,32 kacl/mol
Sa se calculeze caldura de formare a benzenului lichid in starea standard din elemente.
6C(s) + 3H2(g) → C6H6(l) (a) ;
Reactia de ardere a benzenului lichid din elemente este:
C6H6 +15/2 O2(g) →6CO2(g) + 3H2O(l) (b) cu cHC6H6=781kcal/mol .
Reactiile de ardere ale ale carbonului si hidrogenului sunt:
C(s) + O2(g) → CO2 (g) (c) ; cu Δ cHC=- 94,1 kcal/mol iar
H2(g)+1/2O2(g) → H2O(l) (d) ; cu ΔcHH2= - 68,3 kcal/mol.
Calculati entalpia standard de formare a dioxidului de carbon cunoscand entalpiile standard de reactie pentru :
C+1/2O2 CO DH298 = -110,63 Kj/mol
CO +1/2O2 CO2 DH298 = -283,63 Kj/mol
- precizati daca procesele in discutie sunt endoterme sau exoterme
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 5017
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2026 . All rights reserved