| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Notiuni de termodinamica si fizica statistica
1. Definitii
Termodinamica,
fizica statistica si termocinetica se ocupa cu studiul
proceselor fizice care au loc in sistemele macroscopice. Sunt considerate
sisteme macroscopice, sistemele mari in comparatie cu dimensiunile atomice
si care contin astfel foarte multi atomi sau molecule. Spre
deosebire de lumea macroscopica, pe care o cunoastem cu ajutorul
simturilor noastre, nivelul microscopic apartine obiectelor care au
dimensiuni atomice (![]() m). Un sistem macroscopic tipic contine aproximativ
m). Un sistem macroscopic tipic contine aproximativ ![]() atomi in
interactiune.
atomi in
interactiune.
Termodinamica studiaza proprietatile generale ale sistemelor fizice aflate in echilibru termic. Este o metoda fenomenologica de studiu care face abstractie de cauza fenomenelor termice. Porneste de la trei legi fundamentale, numite principiile termodinamicii, la care adauga un set de rezultate experimentale.
Fizica statistica porneste de la structura atomica a substantelor. Nu isi propune sa studieze un atom sau o molecula individuala, ci corpuri macroscopice constituite dintr-un numar foarte mare de atomi, folosind metodele teoriei probabilitatilor. Stabileste legile termice macroscopice pe baza cunoasterii structurii atomo-moleculare a sistemului. Sta la baza termodinamicii din punct de vedere teoretic.
Atat termodinamica cat si fizica statistica studiaza starile de echilibru ale corpurilor macroscopice (stari stationare) care sunt lipsite de transport de masa, de energie, de sarcina electrica etc. Spre deosebire de ele, termocinetica se ocupa cu studiul starilor de neechilibru si a proceselor de trecere a sistemului din starile de neechilibru in stari de echilibru.
Prin sistem fizic, in general, se intelege o portiune finita din Univers. Sistemul termodinamic este orice sistem fizic care indeplineste urmatoarele conditii: a) Contine un numar suficient de mare de microsisteme (atomi, molecule, ioni etc.) astfel incat, la echilibru, fluctuatiile parametrilor microsistemelor sa fie neglijabile. b) Este limitat spatial si contine un numar finit de microsisteme. Prin aceasta definitie, se exclud din randul sistemelor termodinamice atat sistemele fizice cu un numar mic de particule, cat si Universul infinit.
Starea unui sistem termodinamic este data de totalitatea proprietatilor lui la un moment dat si este descrisa de un anumit numar de parametri. Parametrii de stare ai unui sistem termodinamic sunt acele marimi fizice care caracterizeaza atat sistemul cat si relatiile lui cu sistemele inconjuratoare.
Daca sistemul este, de exemplu, o cantitate de gaz, asupra caruia nu actioneaza un camp electric sau magnetic, iar actiunile gravifice se neglijeaza, experienta arata existenta a trei parametri: volumul, presiunea si temperatura. Dintre acestia doar doi sunt independenti, deoarece cei trei parametrii sunt legati prin ecuatia de stare.
Parametrii de stare pot fi impartiti in parametrii externi (sau parametrii de pozitie) si parametrii interni. Parametrii externi depind de mediul exterior. Volumul si intensitatea unui camp exterior (gravitational, electric, magnetic) fac parte din categoria parametrilor externi. Parametrii interni depind de proprietatile interne ale sistemului, mai precis de miscarea in ansamblu si de distributia particulelor ce compun sistemul. Exemple de parametrii interni ar fi presiunea, temperatura, energia interna etc. Starea sistemului termodinamic va fi complet determinata, la un moment dat, prin cunoasterea tuturor parametrilor interni si externi. Legat de acesti parametrii se introduce notiunea de sistem simplu, caracterizat printr-un singur parametru extern si un singur parametru intern.
Daca parametrii de stare raman constanti in timp, cand nu se schimba conditiile exterioare, sistemul se afla in echilibru termodinamic. Parametrii macroscopici care caracterizeaza sistemul in starea de echilibru pot fi extensivi si intensivi. Parametrii extensivi sunt proportionali cu dimensiunea sau extinderea sistemului. Exemple de astfel de parametrii sunt volumul si masa. Parametrii intensivi nu depind de dimensiunea sistemului. Presiunea medie si temperatura sunt parametrii intensivi. Raportul a doi parametri extensivi este un parametru intensiv. De exemplu densitatea, care este raportul dintre masa si volum, este un parametru intensiv.
Marimile fizice care sunt determinate numai de starea sistemului la un moment dat fiind functii numai de grupul complet al parametrilor de stare, se numesc functii de stare sau marimi de stare. Exemple de marimi de stare sunt energia interna, entropia, entalpia etc.
In cazul in care un sistem termodinamic evolueaza de la o stare termodinamica la alta, parametrii de stare ai sistemului se schimba. Aceasta evolutie se numeste proces termodinamic si este caracterizata de marimi specifice numite marimi de proces. Marimile de proces depind de toate starile intermediare ale sistemului atinse in timpul procesului.
Procesele termodinamice se clasifica:
a) dupa marimea variatiei relative a parametrilor de stare: in procese diferentiale, pentru care variatia relativa a parametrilor de stare este foarte mica si procese finite, cand cel putin un parametru de stare sufera o variatie relativ mare;
b) din punctul de vedere al naturii starilor intermediare: in procese cvasistatice (de echilibru), in cazul in care starile intermediare pot fi considerate suficient de apropiate de starile de echilibru in tot timpul procesului si in procese nestatice, pentru care starile intermediare nu pot fi complet caracterizate din punct de vedere termodinamic;
c) din punctul de vedere al trecerii sistemului din starea initiala in starea finala si invers: in procese reversibile si procese ireversibile. Daca un sistem trece din starea initiala in starea finala printr-un proces cvasistatic si daca este posibila si trecerea inversa a sistemului de la starea finala la cea initiala prin aceleasi stari intermediare atunci procesul se numeste reversibil. Numai procesele cvasistatice pot fi reversibile pentru ca implica o succesiune de stari de echilibru. Procesele care nu indeplinesc aceasta conditie sunt ireversibile.
In toate cazurile reale procesele termodinamice sunt nestatice si ireversibile. Procesele cvasistatice reversibile sunt procese idealizate care sunt importante deoarece permit stabilirea marimilor de stare si a principiilor termodinamicii.
Dupa starea lor de agregare, substantele se impart in solide si fluide. Un fluid este o substanta care poate curge. Prin urmare termenul de fluid include lichidele si gazele. Aceasta clasificare nu este intotdeauna exacta. Unele fluide cum este rasina sau smoala, curg asa de incet incat, practic, se comporta ca solide in intervale de timp lungi. Plasma, care reprezinta un gaz puternic ionizat, nu se potriveste in nici una din cele doua categorii astfel incat este considerata a patra stare a materiei, pe langa starile solida, lichida si gazoasa.
Exista o diferenta in modul in care o forta actioneaza asupra suprafetei unui fluid sau a unui solid. Pentru un solid nu exista restrictii privind directia unei astfel de forte, dar pentru un fluid in repaus, aceasta forta trebuie sa actioneze intotdeauna perpendicular pe suprafata. Din acest motiv este convenabil sa descriem forta care actioneaza asupra unui fluid specificand presiunea, care este definita ca raportul dintre marimea fortei care apasa normal si uniform pe o suprafata si aria acelei suprafete. Presiunea se transmite prin sectiuni arbitrare ale fluidului (sau catre frontierele solide ale fluidului), perpendicular pe aceste sectiuni in fiecare punct.
Presiunea este o marime scalara. Se
masoara in SI in ![]() (se numeste
pascal:
(se numeste
pascal: ![]() ). Exista mai multe unitati de
masura tolerate pentru presiune. Cateva exemple sunt:
). Exista mai multe unitati de
masura tolerate pentru presiune. Cateva exemple sunt:
1 torr = 1 mm Hg = ![]()
1 bar = ![]() (unitate folosita
mai ales in meteorologie)
(unitate folosita
mai ales in meteorologie)
1 atm = ![]() (atmosfera fizica
sau atmosfera)
(atmosfera fizica
sau atmosfera)
1 at = ![]()
Se observa ca 760 torr = 1 atm.
Un fluid sub presiune exercita o forta
asupra oricarei suprafete in contact cu el. Sa consideram o
suprafata inchisa continand un fluid. Un element de
suprafata poate fi reprezentat printr-un vector ![]() a carui modul
este aria elementului de suprafata si a carui directie
este paralela cu normala exterioara la elementul de
suprafata. Forta exercitata de fluid asupra elementului de
suprafata este:
a carui modul
este aria elementului de suprafata si a carui directie
este paralela cu normala exterioara la elementul de
suprafata. Forta exercitata de fluid asupra elementului de
suprafata este: ![]() . Deoarece
. Deoarece ![]() si
si ![]() au aceeasi
directie putem scrie:
au aceeasi
directie putem scrie: ![]() , iar la limita,
, iar la limita, ![]() . Daca forta este constanta si
suprafata finita, relatia devine:
. Daca forta este constanta si
suprafata finita, relatia devine: ![]() .
.
Masurarea presiunii
Evangelista Torricelli a inventat in 1643 barometrul cu mercur, aparat utilizat pentru masurarea presiunii atmosferice. Presiunea atmosferica intr-un punct este numeric egala cu greutatea unei coloane de aer cu aria sectiunii transversale egala cu unitatea care se intinde de la acel punct pana la extremitatea superioara a atmosferei. Aceasta presiune descreste cu altitudinea.
Barometrul cu mercur este un dispozitiv simplu, format dintr-un tub lung de sticla, care se umple cu mercur si se rastoarna intr-o cuva cu mercur (fig.1). Mercurul coboara in tub si se stabileste la o anumita inaltime. Inaltimea coloanei de mercur din tub masoara presiunea atmosferica. La nivelul marii coloana de mercur va avea o inaltime de aproximativ 760 mm.
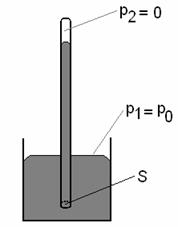
Deasupra mercurului din
tub se formeaza un gol care contine vapori de mercur a caror
presiune, ![]() , este asa de mica la temperaturi obisnuite,
incat poate fi neglijata. Presiunea care se exercita asupra
mercurului din cuva este presiunea atmosferica,
, este asa de mica la temperaturi obisnuite,
incat poate fi neglijata. Presiunea care se exercita asupra
mercurului din cuva este presiunea atmosferica, ![]() . Mercurul din tub coboara pana cand greutatea
mercurului din tub devine egala cu produsul intre presiunea
. Mercurul din tub coboara pana cand greutatea
mercurului din tub devine egala cu produsul intre presiunea
Fig. 1
atmosferica si suprafata transversala a tubului pe care actioneaza:
![]()
Dar
![]()
de unde rezulta:
![]()
![]()
Exercitiu. Sa calculam "presiunea de 760 mm coloana de mercur"
(adica presiunea echivalenta cu cea exercitata de o coloana
de mercur de 760 mm), la temperatura (normala) de 0C si in camp
gravitational normal (standard), pentru care acceleratia
gravitationala este ![]() m s Densitatea mercurului la temperatura normala este
m s Densitatea mercurului la temperatura normala este ![]() kg/m3.
Aceasta este presiunea de o atmosfera (1 atm - unitate de masura
tolerata pentru presiune).
kg/m3.
Aceasta este presiunea de o atmosfera (1 atm - unitate de masura
tolerata pentru presiune).
Prin urmare:
![]()
Observatie. In meteorologie, presiunea este indicata prin specificarea inaltimii unei coloane de mercur, dar sa nu uitam ca presiunea nu este o lungime ci raportul dintre forta si arie.
![]()
Aparatele pentru masurarea presiunii se numesc manometre. Majoritatea acestor aparate folosesc presiunea atmosferica ca nivel de referinta si masoara de fapt, diferenta dintre presiunea existenta in vas si presiunea atmosferica. Rezultatul acestui tip de masuratoare se numeste presiune manometrica (sau diferentiala), iar manometrul corespunzator este manometrul in forma de U cu un capat deschis (fig.2).
Diferenta de presiune intre presiunea din vas si presiunea atmosferica este proportionala cu diferenta de inaltime a coloanelor de lichid din tubul in forma de U a manometrului.
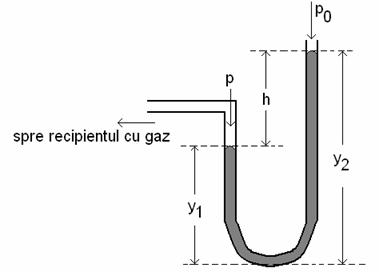
Fig.2
Din fig.2 se
observa ca ![]() este diferenta de
inaltime a coloanelor de lichid din manometru. Astfel, presiunea p
din recipient este echilibrata de presiunea atmosferica,
este diferenta de
inaltime a coloanelor de lichid din manometru. Astfel, presiunea p
din recipient este echilibrata de presiunea atmosferica, ![]() , la care se adauga presiunea datorata
greutatii coloanei de lichid din ramura din dreapta a manometrului:
, la care se adauga presiunea datorata
greutatii coloanei de lichid din ramura din dreapta a manometrului:
![]()
Daca recipientul contine gaz la presiune mare, se foloseste un tub manometric cu lichid cu densitate mare cum este mercurul; daca gazul are presiune mica, atunci se poate folosi ca lichid manometric, apa.
Din punct de vedere microscopic, gazul exercita o presiune asupra peretilor vasului (recipientului) datorita ciocnirilor dintre moleculele de gaz si peretii vasului. Aceasta presiune este determinata de forta medie cu care moleculele gazului actioneaza in procesul de ciocnire asupra unei suprafete a peretelui de arie egala cu unitatea, in directie normala (perpendiculara) la aceasta suprafata.
Formula fundamentala a teoriei cinetice a gazelor exprima presiunea ca functie de marimi microscopice caracteristice gazului:
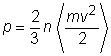
unde n este
concentratia moleculelor gazului (numarul de molecule din unitatea de
volum), iar 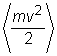 este energia
cinetica medie a unei molecule.
este energia
cinetica medie a unei molecule.
Din punctul de vedere al teoriei cinetice, presiunea gazului, ca proprietate macroscopica a sistemului de molecule, este un parametru obtinut in urma unei medieri efectuate pe tot ansamblul de molecule, ceea ce arata caracterul statistic al presiunii.
Simtul tactil este calea cea mai simpla prin care distingem corpurile calde de corpurile reci, putand astfel sa aranjam corpurile in ordinea gradului lor de incalzire. Dar procedeul este subiectiv si limitat. De exemplu, daca o persoana isi cufunda o mana in apa calda si pe cealalta in apa rece, iar apoi introduce ambele maini in apa calduta, va avea senzatia de apa mai rece pentru prima mana si apa mai calda pentru a doua mana. Aceasta arata nesiguranta unei masuratori bazata pe simtul tactil.
Sa consideram un obiect A pe care il simtim rece fata de mana si un obiect identic B pe care il simtim cald, puse in contact unul cu altul. Dupa un timp suficient de lung, corpurile A si B genereaza aceeasi senzatie de temperatura. Spunem ca A si B sunt in echilibru termic unul cu altul. Verificarea echilibrului termic se realizeaza folosind un al treilea corp numit si corp de proba (de exemplu, un termometru). Situatia este rezumata intr-un postulat, numit si principiul zero al termodinamicii:
"Daca A si B sunt in echilibru termic cu un al treilea corp C (termometrul) atunci A si B sunt in echilibru termic unul cu altul"
Aceasta proprietate a sistemelor este descrisa de marimea fizica numita temperatura. Temperatura este o marime scalara; egalitatea temperaturilor este o conditie necesara si suficienta pentru echilibru termic.
Exista mai multe proprietati fizice masurabile care variaza atunci cand temperatura unui corp se modifica: volumul unui lichid, lungimea unei bare metalice, rezistenta electrica a unui conductor, presiunea unui gaz mentinut la volum constant etc. Oricare dintre aceste proprietati poate fi folosita pentru confectionarea unui termometru, adica pentru stabilirea unei scari de temperatura.
O scara de temperatura se stabileste prin alegerea unei substante termometrice particulare (corp termometric) si a unei proprietati a acesteia. Definim scara temperaturilor stabilind relatia (monotona) intre proprietatea aleasa a substantei si temperatura corespunzatoare.
Unul dintre cele mai raspandite termometre foloseste un lichid (mercur) intr-un tub capilar de sticla (Fig.1). Proprietatea termometrica este lungimea coloanei de lichid.
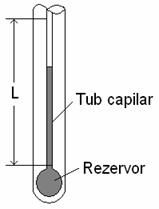
Fig.1
Sa presupunem ca am ales un corp termometric care are proprietatea X dependenta liniar de temperatura:
![]()
unde a este o constanta pe care trebuie sa o evaluam. Astfel, diferente de temperatura egale corespund la variatii egale ale lui X. Sau cu alte cuvinte, ori de cate ori coloana de lichid din termometru variaza ca lungime cu o unitate, temperatura masurata variaza cu o cantitate bine definita.
A determina constanta a inseamna a etalona termometrul. Etalonarea necesita precizarea unui punct fix standard la care toate termometrele trebuie sa indice aceeasi temperatura. In prezent se foloseste punctul la care gheata, apa si vaporii de apa coexista in echilibru si care se numeste punctul triplu al apei. Aceasta stare, univoc determinata, este caracterizata de urmatorii parametri:
![]() mm col. Hg,
mm col. Hg, ![]() K (0,01 sC)
K (0,01 sC)
a) Scara de temperatura a gazului ideal
Marimea care caracterizeaza starea sistemului si care variaza cu temperatura este presiunea gazului al carui volum este mentinut constant. Daca volumul unui gaz este mentinut constant, presiunea sa depinde de temperatura si creste continuu cu cresterea temperaturii.
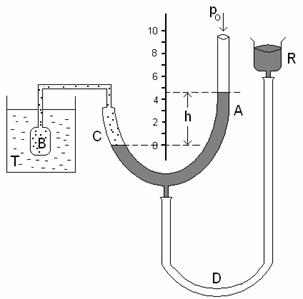
Figura 2
Gazul, de obicei heliu, se afla in balonul B, iar presiunea lui se masoara cu un manometru cu tub deschis.
Pe masura ce temperatura gazului creste,
acesta se dilata impingand mercurul in jos in tubul C si in sus in
tubul A. Tuburile A si C comunica, printr-un tub de cauciuc D, cu
rezervorul de mercur R. Ridicand sau coborand rezervorul R, nivelul de mercur
in tubul C este mentinut la aceeasi valoare care reprezinta un
nivel de referinta. Pe scara gradata se citeste
diferenta de inaltime din cele doua ramuri ale manometrului
(tuburile A si C) si cunoscand presiunea atmosferica po,
se calculeaza presiunea gazului din B:![]() .
.
Temperatura indicata de termometru este:
![]()
![]()
![]()
Aparatul este laborios, se foloseste in laboratoarele de cercetare si serveste la stabilirea scarii de temperatura a gazului ideal.
S-a constatat ca indicatiile de temperatura ale unui termometru cu gaz la volum constant depind de gazul folosit in cazul valorilor obisnuite ale presiunii de referinta. Daca insa presiunea de referinta este mica, indicatiile de temperatura ale termometrelor cu gaz la volum constant, care folosesc diferite gaze, tind catre aceeasi valoare. Prin urmare valoarea temperaturii depinde numai de proprietatile generale ale gazelor si nu de un gaz particular. Se defineste astfel o scara de temperatura a gazului ideal prin relatia:
![]() (V = const.)
(V = const.)
Temperatura cea mai
coborata care poate fi masurata cu termometrul cu gaz este de ![]() K. Pentru a
obtine aceasta temperatura trebuie folosit heliu la presiuni
joase, deoarece heliul devine lichid la o temperatura (4,216 K) mai
coborata decat oricare alt gaz.
K. Pentru a
obtine aceasta temperatura trebuie folosit heliu la presiuni
joase, deoarece heliul devine lichid la o temperatura (4,216 K) mai
coborata decat oricare alt gaz.
b) Scara Celsius
Scara Celsius se defineste cu ajutorul scarii Kelvin care constituie scara fundamentala a temperaturilor in stiinta. Astfel, temperatura in grade Celsius se calculeaza conform relatiei:
t (sC) = T (K) - 273,15
Gradul Celsius, ca unitate de temperatura, se obtine impartind la 100 diferenta intre temperatura la care vaporii de apa si apa lichida sunt in echilibru la presiunea atmosferica normala (1atm) - numit punctul de fierbere al apei si temperatura la care gheata si apa sunt in echilibru la presiune atmosferica normala - numit punctul de inghet al apei. Cele doua temperaturi sunt 100 sC, respectiv 0 sC.
Scara Celsius foloseste un grad care are aceeasi marime ca si gradul de pe scara Kelvin. Cu alte cuvinte, diferenta a doua temperaturi este aceeasi daca este exprimata in grade Kelvin sau in grade Celsius.
c) Scara Fahrenheit
Aceasta scara este folosita in tarile de limba engleza, cu exceptia Angliei care a adoptat scara Celsius in 1964. Relatia intre o temperatura exprimata in grade Fahrenheit si grade Celsius este:
![]() (sF) =
(sF) = ![]() (sC)
(sC)
Conform acestei scari punctul de fierbere al apei este 212 (sF), iar cel de inghet este 32 (sF).
Cele doua temperaturi caracteristice apei fac parte dintr-o serie de puncte de referinta numite puncte fixe fundamentale folosite pentru masuratori de temperatura; cateva asemenea puncte sunt indicate in tabelul urmator:
Substanta |
Punctul de transformare |
Temperatura(K) |
|
oxigen |
punct de fierbere normal | |
|
apa |
punct triplu | |
|
apa |
punct de fierbere normal | |
|
sulf |
punct de fierbere normal | |
|
argint |
punct de topire normal | |
|
aur |
punct de topire normal |
Din punct de vedere microscopic, temperatura unei substante este direct legata de energia moleculelor sale; cu cat temperatura este mai mare, cu atat energia creste si miscarea moleculelor este mai intensa. Temperatura nu are inteles pentru o singura molecula. Ea exprima energia medie a unui numar foarte mare de molecule.
Conform teoriei cinetice a gazelor, un gaz consta dintr-un numar N, foarte mare, de particule aflate in miscare rectilinie cu viteze mari. Particulele nu interactioneaza unele cu altele decat in timpul ciocnirilor dintre ele sau cu un perete. Din formula fundamentala a teoriei cinetice rezulta:
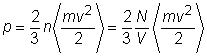 T
T 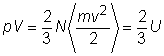
unde U este energia medie totala a particulelor care, in acest caz, este in intregime energie cinetica de translatie.
Pentru
ca acest rezultat sa fie in concordanta cu ecuatia de stare
a gazului ideal, ![]() , in conditii de echilibru, energia medie totala
trebuie sa fie egala cu:
, in conditii de echilibru, energia medie totala
trebuie sa fie egala cu:
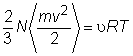 . Obtinem:
. Obtinem: 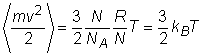 , unde am inlocuit numarul de moli cu
, unde am inlocuit numarul de moli cu ![]() ,
, ![]() fiind numarul lui
Avogadro si am tinut cont ca
fiind numarul lui
Avogadro si am tinut cont ca ![]() este constanta lui
Boltzmann.
este constanta lui
Boltzmann.
Deoarece miscarea
de translatie are trei grade de libertate (ceea ce corespunde la trei
componente ale vitezei), fiecarui grad de libertate i se atribuie, in
medie, o energie egala cu ![]() .
.
Afirmatia ca fiecarui grad de libertate a
miscarii unei molecule i se asociaza la echilibru o energie
medie egala cu ![]() constituie principiul
echipartitiei energiei.
constituie principiul
echipartitiei energiei.
Rezultatul obtinut pentru moleculele unui gaz este generalizat de fizica statistica. In mecanica statistica nu este necesar sa se precizeze daca particulele sunt moleculele unui gaz sau ioni care ocupa pozitii fixe intr-o retea cristalina, electroni sau alte entitati microscopice. Important este ca aceste particule sa fie aproape independente si ca interactia (slaba) dintre ele sa fie suficienta pentru a permite particulelor sa schimbe energie si sa ajunga in cele din urma la echilibru.
Metodele mecanicii statistice ne permit sa
gasim valoarea la echilibru a energiei medii a unei particule pe baza
cunoasterii tipurilor de energie ale particulelor individuale. Daca o
astfel de energie se exprima ca suma unui numar de termeni
patratici (de exemplu: ![]() - energie medie de
translatie,
- energie medie de
translatie, ![]() - energie medie de
rotatie,
- energie medie de
rotatie, ![]() - energie medie de
vibratie), atunci se poate demonstra riguros ca, la echilibru,
energia medie a unei particule asociata fiecarui termen
patratic, este
- energie medie de
vibratie), atunci se poate demonstra riguros ca, la echilibru,
energia medie a unei particule asociata fiecarui termen
patratic, este ![]() .
.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 3848
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved