| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Clasificarea reactoarelor electrochimice
1. Reactoarelor electrochimice ideale
Pentru a estima performantele unui RE este util sa adoptam un model. In acest scop vom folosi clasificarea reactoarelor chimice care are in vedere numarul de faze prezente, conditiile transportului de masa si temperatura de lucru.
Din punct de vedere al modului de operare RE poate sa functioneze discontinuu, continuu sau semicontinuu, de aceea vom vorbi despre:
(i) Reactorul electrochimic discontinuu (REDS),
(ii) Reactorul electrochimic continuu sau cu deplasare (REDP) si
(iii) Reactorul electrochimic cu amestecare perfecta (REAP).
Fata de aceste modele ideale in practica vom intalni RE care se apropie mai mult sau mai putin de acestea. Tot din considerente de simplificare vom aprecia ca RE sunt operate izoterm.
Tot dupa modul de operare al RE pot fi clasificate in:
(i) Discontinue
(ii) Cu recirculare
(iii) Cu o singura trecere
(iv) Aranjate in cascada de n reactoare identice.
|
|
|
Fig. 1. Reactoare ideale impreuna cu evolutia concentratiei reactantului si produsului in functie de timp sau de distanta de la intrarea in reactor: (a) Reactorul discontinuu (REDS); (b) Reactorul cu deplasare (REDP); (c) Reactor cu amestecare perfecta (REAP). |
1.1. Reactorul electrochimic discontinuu
Acest tip de RE este incarcat cu reactanti si cu solutia de electrolit iar acestea sunt amestecate pe durata cat are loc reactia. Apoi amestecul de reactie este scos din RE si produsii sunt recuperati fie prin izolarea lor din solutie fie prin indepartarea de pe electrozi.
Pe durata functionarii REDS concentratia reactantului sau a reactantilor respectiv a produsului sau a produsilor se modifica de o maniera ce depinde de cinetica reactiilor de la electrozi, de geometria electrozilor, de conditiile de curgere si de volumul de electrolit. Se considera ca in fiecare moment compozitia solutiei de electrolit in REDS este uniforma in intreg volumul sau. Timpul de sedere al solutiei de electrolit este egal cu timpul de reactie.
Acest tip de RE ideal solicita operatii repetate de incarcare - descarcare si este folosit in urmatoarele cazuri:
(i) in timpul cercetarii unui proces, cand se studiaza cinetica in diverse conditii de operare;
(ii) cand utilizarea altor reactoare sofisticate nu este recomandata, de exemplu, datorita toxicitatii sau costului electrolitului, reactantilor sau produsilor;
(iii) cand electrosinteza / elctroliza trebuie oprita din timp in timp (la intervale de timp bine stabilite) datorita unor cerinte specifice - de exemplu, pentru recoltarea produsului de pe electrozi sau inlocuirea anozilor consumabili.
1.2. Reactorul electrochimic cu deplasare
RED este denumit, uneori, si RE continuu, RE tubular sau RE cu curgere piston. Curgerea solutiei de electrolit prin RED este continua, cu o viteza constanta si se considera ca nu are loc o amestecare a electrolitului pe directia de curgere intre intrarea si iesirea din RED. Din aceste motive, concentratia produsului si a reactantilor este functie de distanta parcursa de la intrarea in RED si de timpul de sedere in RED.
Exemple de RE care sunt exploatate in conditii foarte apropiate de modelul RED sunt: RE cu electrozi cilindrici statici, RE cu electrozi plani paraleli - tip filtru-presa si unele RE cu electrozi porosi sau tridimensionali (3D).
1.3. Reactorul electrochimic cu amestecare perfecta
in cazul REAP, dupa cum arata si numele, are loc o amestecare continua si energica a electrolitului in conditii in care se adauga continuu reactant si se extrage continuu produs - de fapt se introduce si se scoate continuu solutie de electrolit. Datorita amestecari perfecte se considera ca avem aceeasi concentratie atat la intrare cat si la iesire, schimbarea de concentratie realizandu-se chiar la intrarea in REAP.
In practica, cazurile foarte apropiate de REAP corespund RE cu electrozi cilindrici rotitori sau modelelor in care agitarea este foarte viguroasa, asigurata cu ajutorul unui gaz insuflat in REAP sau generat la electrod/electrozi. Tot un comportament apropiat de REAP intalnim si in cazul reactoarelor cu electrozi in strat fluidizat.
1.4. Ecuatiile conversiei in RE ideale
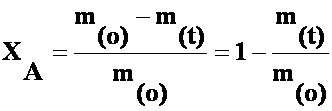 (1)
(1)
unde m(o) si m(t) sunt cantitatile de A la timpul initial, t = 0, si la un timp, t, mai mare decat zero; iar in termeni de concentratie:
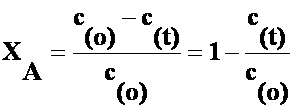 (2)
(2)
iar in cazul RED avem:
 (3)
(3)
in care c(i) si c(e) sunt concentratiile reactantului la intrarea si, respectiv, la iesirea din RED.
Conversia in REDS
 (4)
(4)
respectiv:
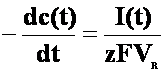 (5)
(5)
unde I(t) este curentul instantaneu la timpul t iar Vr este volumul REDS. Daca procesul este controlat de transportul de masa:
I(t) = IL = zFAkmc(t) (6)
si deci:
![]() (7)
(7)
de unde rezulta ca:
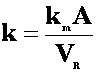 (8)
(8)
Daca integram ecuatia (7) intre limitele: t = 0 si t = t respectiv c = c(0) si c = c(t) se obtine:
c(t) = c(0) exp 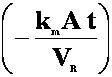 (9)
(9)
ceea ce indica o scadere exponentiala a concentratiei reactantului in raport cu timpul.
Daca se noteaza:
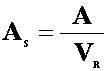 (10)
(10)
ca fiind aria electrodica pe unitatea de volum de reactor, atunci:
c(t)
= c(0) exp ![]() (11)
(11)
Cand se analizeaza date experimentale se prefera forma logaritmata:
ln 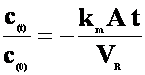 (12)
(12)
care evidentiaza
(i) o dependenta liniara semilogaritmica avand panta ![]() si (ii) care trece prin origine, aceste doua
argumente fiind necesare pentru validarea comportamentul de tip REDS..
si (ii) care trece prin origine, aceste doua
argumente fiind necesare pentru validarea comportamentul de tip REDS..
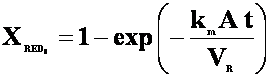 (13)
(13)
Conversia in RED
NV c(i) - NV c(e)
= ![]() (14)
(14)
sau
Dc = c(i)
- c(e) = 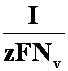 (15)
(15)
Pentru un RED:
I = f(x) = 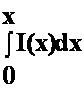 (16)
(16)
I = IL = zFAkmc(x) (17)
iar:
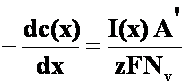 (18)
(18)
unde A' este aria electrodica pe unitatea de lungime de RED. Daca inlocuim pe I(x) cu IL, rezulta ca:
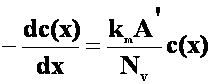 (19)
(19)
c(i) = c(e)
exp 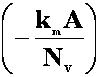 (20)
(20)
unde A = A'∙L - suprafata electrodului, conform ecuatiei (3) conversia devine:
![]()
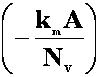 (21)
(21)
iar curentul limita:
IL= zFNV c(i) XRED (22)
sau:
IL= zFNVc(in)
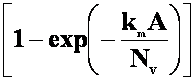 (22a)
(22a)
t = ![]() , (23)
, (23)
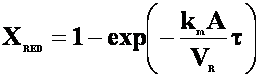 (24)
(24)
Se observa ca, pentru valori date ale lui km, si VR, RED si REDS realizeaza aceeasi conversie daca timpul de sedere in RED este acelasi cu timpul de procesare din REDS.
Conversia in REAP
IL= zFAkmc(e) (25)
iar:
Dc = c(i)
- c(e) = 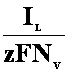 (26)
(26)
sau:
c(i) - c(e)
= 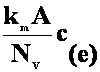 (27)
(27)
de unde se poate explicita:
c(e) = 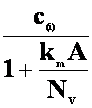
![]() (28)
(28)
iar conversia este:
 (29)
(29)
Se observa ca, pentru realizarea unor conversii ridicate in conditiile unei viteze de curgere date, este importanta asigurarea unor valori mari pentru km si a.
Tabel 1. Clasificarea RE in functie de modul de operare
Tipul de RE |
Modul de operare |
Expresia conversiei fractionare, X |
Nr. ecuatie |
|
REDs |
Discontinuu |
| |
|
RED |
Recirculare |
| |
|
REAP |
Recirculare |
| |
|
RED |
Cu o singura trecere |
| |
|
REAP |
Cu o singura trecere |
| |
|
RED |
Cascada de n reactoare |
1-exp [-n (kmA/Nv)] | |
|
REAP |
Cascada de n reactoare |
|
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 2003
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved