| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
1.1. Ce este biochimia?
Biochimia este stiinta care se ocupa cu studiul chimiei sistemelor biologice. Cu alte cuvinte, scopul principal al biochimiei este de a explica in termeni chimici fenomenele care apar in formele biologice. Ea se bazeaza pe chimie, stiinta care studiaza schimbul, transferul sau rearanjarea electronilor in/sau intre molecule sau atomi. Sistemele vii, pentru a exista, trebuie sa fie capabile de a determina schimburi de materie si energetice care sa sustina ceea ce generic definim drept viata.
1.2. Ce sunt sistemele biologice?
Sistemele biologice nu reprezinta altceva decat ierarhizarea structurala, complicata dar organizata a sistemelor din natura spre o entropie cat mai joasa, in sensul:

De subliniat ca din aceasta serie doar celule sunt considerate a avand viata. Celulele sunt reprezentarea vie a organizarii atomilor, moleculelor sau organoletelor, elemente care sunt considerate neavand viata. Spre deosebire de sistemele nevii, organismele vii poseda proprietati deosebite, care reprezinta de fapt obiectul studiilor biochimiei.
Dintre proprietatile remarcabile ale organismelor vii trebuiesc remarcate:
gradul mare de complexitate si organizare: celulele lor poseda o structura interna complicata ca urmare a unor interactiuni dintre o multitudine de tipuri de molecule complexe;
specificitatea functiei lor in sistem, cu "tinta" bine determinata;
capacitatea de a interactiona cu mediul din care isi procura resursele de energie si materie;
capacitatea de a se reproduce precis. Aceasta este de fapt deosebirea esentiala si ceea mai importanta care desparte cea ce definim astazi lume vie (viata) de asa denumita "lume nevie".
In consecinta, sistemele vii sunt sisteme termodinamic deschise, schimband energie si materie cu vecinatatile lor asa cum este reprezentat generic in Figura 1.1.
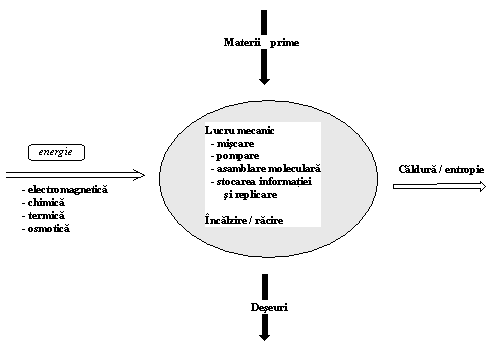
Figura 1.1. Interactiunea sistemelor biologice cu mediul inconjurator
Pe de alta parte, apar o serie de intrebari firesti privind interactiunile chimice dintre celulele vii si anume:
- ce tip de molecule apar si care este proportia lor in celulele vii;
- care este structura acestor molecule;
- cine influenteaza reactivitatea chimica ale acestor molecule, atat in starea lor intrinseca dar mai ales in formele prezente in celule;
- care sunt formele de interactiune dintre biomolecule si cine le influenteaza?
Dar cea mai incitanta dintre toate este intrebarea urmatoare: cum si unde au aparut primele forme ale vietii vii si oare din care biomolecule?
Doua postulate sunt fundamentale raspunsului la aceste intrebari:
1. sistemele vii au nevoie de apa lichida;
2. sistemele vii se bazeaza pe chimia compusilor carbonului.
Sistemele vii au nevoie de apa lichida!
Oare de ce starea lichida este preferata intre cele trei stari de agregare, solida (gheata), lichida si gazoasa (vapori), intalnite pe Pamant? Sa analizam putin cele trei stari pentru a intelege mai bine acest postulat.
Starea gazoasa presupune interactiuni foarte slabe intre particulele prezente in sistem. Aceste interactiuni fiind mai mult de tipul ciocnirilor elastice, contactul dintre particule este practic infim, ne permitand formarea unor grupari moleculare mari. In consecinta starea poate fi caracterizata drept un "haos" din punct de vedere al organizarii.
Starea solida presupune in schimb interactiuni foarte puternice intre particulele existente, practic "inghetarea" in forme rigide a moleculelor sau a particulelor constitutive. Acest mod de organizare determina o foarte slaba posibilitate de interactiuni moleculare, fiind astfel nefavorabila interactiunilor care apar in sisteme vii, mai ales atunci cand este vorba de replicare.
In fine, starea lichida ofera posibilitatea unor interactiuni intra si intermoleculare suficient de puternice pentru ca molecule vecine sa poata interactiona, dar insuficient de puternice pentru a le rigidiza dupa interactiune. Sunt indeplinite premizele interactionarii care duc la formarea de ansambluri de molecule complexe, dar si existenta posibilitatilor de interactiune dintre acestea.
Daca starea lichida este cea care este favorabila unor astfel de interactiuni apare o alta intrebare la care trebuie raspuns: oare orice sistem lichid, ca de exemplu oxigenul lichid cu punct de fierbere -1830C sau fierul topit, cu punctul de topire de 15350C, este potrivit? Evident ca nici unul dintre aceste sisteme lichide nu vor putea sa sustina sistemele vii deoarece acestea sunt conditionate si de o temperatura cuprinsa intre anumite limite si anume limitele ambientale de pe Pamant. Singurul sistem lichid capabil de a sustine astfel de interactiuni in conditiile normale de temperatura este apa! Despre calitatile si proprietatile specifice ale apei drept solvent universal, practic "leaganul" vietii vii, vom discuta intr-un alt capitol.
1.2.2. Sistemele vii se bazeaza pe chimia compusilor carbonului
Care sunt argumentele pentru care carbonul sta la baza formarii ansamblurilor moleculare care permit existenta vietii vii? De ce nu alte elemente, cum ar fi siliciul, mult mai raspandit mai ales in scoarta pamantului, nu prezinta aceasta proprietate.
Daca vom analiza cele 90 de elemente cel mai des intalnite in natura, vom observa ca doar 30 dintre aceste elemente sunt elemente care apar in formele vii. Caracteristic este faptul ca circa 90% din ponderea masica celulara este determinata de elemente capabile sa formeze de la una pana la patru legaturi covalente si anume: hidrogenul, carbonul, azotul si oxigenul. Substantele elementare care apar in organismele vii pot fi clasificate in functie de abundenta lor in aceste sisteme in doua categorii:
componente principale (sau permanente): hidrogenul, carbonul, azotul, oxigenul, fosforul, sulful, clorul, sodiul, potasiul si calciu;
componente in urme (sau secundare): magneziul, cromul, manganul, fierul, cobaltul, nichelul, cuprul, zincul, seleniul si iodul.
Cu toate ca din aceasta ultima categorie de elemente, acestea apar doar in cantitati uneori infime in organismele vii (la nivelul partilor per milion - ppm), rolul lor este deosebit de important si esential in desfasurarea proceselor biologice. Aceste elemente apar in special in molecule sau ansambluri moleculare cu foarte inalta specificitate in chimia sistemelor vii, mai ales intr-o grupa speciala de catalizatori biochimici - enzimele. Spre exemplificare, fierul care are o pondere masica doar de 0,3 % din masa hemoglobinei, este elementul indispensabil pentru transportul oxigenului in organismele superioare.
Majoritatea sistemelor biologice au ca elemente constitutive ansambluri moleculare compuse din atomi de carbon care stabilesc legaturi fie cu atomi de carbon, fie cu atomi de hidrogen, oxigen, azot sau fosfor. Diversitatea posibilitatilor de legare determina aparitia unor game vaste de combinatii moleculare. Considerate unitati monomere ale macromoleculelor care apar in sistemele vii ca proteinele, acizii nucleici si polizaharidele, moleculele cu masa moleculara mai mica de 500 unitati atomice de masa, amino acizii, nucleotidele, si monozaharurile, sunt caramizile, constituentii de baza a sistemelor biologice.
Pentru a raspunde totusi la intrebarea de la inceputul acestui capitol va trebuie sa analizam in detaliu caracteristicile si proprietatile elementelor din grupa componentelor principale, elemente capabile sa permita aparitia de ansambluri macromoleculare caracteristice sistemelor vii. Raspunsul deriva din proprietatea fundamentala a elementelor carbon, azot, oxigen, fosfor sau sulf de a stabilii asa numitele legaturi covalente prin redistribuirea electronilor de pe ultimul strat si aparitia a ceea ce se defineste drept stare de hibridizare.
1.3. Hibridizarea unor elementelor constitutive ale biomoleculelor
Forma structurala adoptata de moleculele organice poate fi usor recunoscuta daca se va analiza hibridizarea adoptata de fiecare atom constituent al moleculei. Gradul de hibridizare se poate calcula simplu insumand numarul atomilor legati cu numarul de perechi de electroni nelegati. Principalele hibridizari care se intalnesc in biomolecule sunt reprezentate mai jos (Tabelul 1.1.).
Tabelul 1.1. Principalele moduri de hibridizare care se regasesc in formarea legaturilor chimice intre atomii care formeaza biomolecule
|
Nr. atomi legati + |
hibridizare |
Compozitia orbitalilor hibrizi |
|
sp3 |
1 s + 3 p |
|
|
sp2 |
1 s + 2 p |
|
|
sp |
1 s + 1 p |
In tabelul 1.2. sunt reprezentate principalele stari de hibridizare care se regasesc in ansamblurile biomoleculare.
Tabelul 1.2. Moduri de hibridizare ale atomilor principali la formarea legaturilor in biomolecule
|
atom |
Nr. atomi legati |
Nr. perechi de electroni neparticipante |
hibridizare |
forma |
|
carbon |
sp3 |
tetraedrica |
||
|
sp2 |
trigonala |
|||
|
sp |
lineara |
|||
|
azot |
sp3 |
piramidal trigonala |
||
|
sp2 |
planar 120 |
|||
|
oxigen |
sp3 |
planar 109 |
||
|
sulf |
sp3 |
planar 109 |
1.3.1. Hibridizarea carbonului
Hibridizare sp3
Atunci cand carbonul este legat la alti patru atomi si care nu contin perechi electroni neparticipanti hibridizarea sp3 are o aranjare spatiala tetraedrica (Figura 1.2.)
|
|
|
|
metan |
etan |
|
Figura 1.2. Simetria tetraedrica a atomului de carbon in hibridizarea sp3 |
Hibridizare sp2
Daca un atom de carbon este legat de alti trei atomi formand doua legaturi simple si una dubla hibridizarea este de tip sp2. Aranjamentul spatial este unul trigonal sau triunghiular, cu unghiuri intre legaturi de 1200. Dupa cum se observa, in molecula acidului acetic vom gasi un atom de carbon in hibridizarea sp3 si unul in hibridarea sp2.
|
etena |
|
|
acid acetic |
|
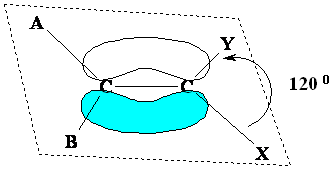
Figura 1.3. Simetria trigonala a atomului de carbon in hibridizarea sp2
Hibridizare sp
O ultima posibilitate de rearanjare a orbitalilor carbonului este hibridizarea sp care apare atunci cand carbonul este legat de alti doi atomi fie prin doua duble legaturi, fie printr-o tripla legatura. Aceasta hibridizare confera o aranjare liniara a moleculei cu unghi de 1800.
|
Acetilena |
|
|
dioxid de carbon |
|
Trebuie mentionat ca tripla legatura este mai rar intalnita in compusii naturali, fapt pentru care nici nu am insistat asupra ei.
1.3.2. Hibridizarea hidrogenului
Fenomenul hibridizarii orbitalilor apare in special atunci cand un atom se leaga de mai multi atomi. In cazul hidrogenului, el avand un singur electron intr-un singur stat electronic, de tip s, nu se pune problema hibridizarii deoarece el nu poate forma decat un singur tip de legatura, anume legatura de tip s
|
metan (CH4) |
amoniac (NH3) |
apa (H2O) |
|
|
|
|
1.3.3. Hibridizarea azotului, oxigenului si sulfului
Hibridizare sp3 a azotului
Atomul de azot poate adopta si el hibridizarea sp3, dar difera de carbon prin faptul ca poseda o pereche de electroni neparticipanti la formare de legatura. Geometria este in acest caz una trigonala.
|
amoniac |
|
||
|
metilamina |
|
||
Hibridizare sp2 a azotului
Atunci cand doar doi atomi sunt legati de azot acesta va adopta si el configuratia hibridizarii sp2 . Si in acest caz, pereche de electroni nu participa la formare de legatura. Ca rezultat geometria este una planara cu unghi intre doua legaturi de 1200.
|
piridina |
|
Hibridizarea oxigenului
Legarea la doi atomi ai oxigenului determina adoptarea hibridizarii sp3, regasindu-se cele doua perechi de electroni neparticipante. Geometria este cea planara cu unghi intre legaturi de cca. 1090, asa cum s-a dovedit pentru molecula de apa si metanol. Oxigenul poate stabili insa si dubla legatura cu un alt atom, situatie intalnita in cazul compusilor carbonilici sau carboxilici, cand starea de hibridizare adoptata este cea de sp2.
|
apa |
|
|
metanol |
|
|
acid acetic |
|
Hibridizare sp3 a sulfului
In biomolecule sulful adopta cel mai adesea hibridizare sp3. Geometria adoptata seamana cu cea a oxigenului in aceiasi stare de hibridizare, dupa cum se poate bine observa in exemplele urmatoare.
|
Hidrogen sulfurat (H2S) |
|
|
metantiol |
|
1.4. Exemple de structuri biomoleculare
Mai jos sunt redate cateva structuri de compusi biomoleculari pentru a intelege mai bine diversitatea legaturilor care pot aparea in aceste tipuri de compusi chimici. Cu cat o molecula poseda mai multe grupari functionale, cu atat posibilitatile de a se lega de alte molecule devin mai favorabile.
|
aspirina (acid acetilsalicilic) |
|
|
cisteina (un amino acid) |
|
|
adenina (o baza azotata gasita in DNA si RNA) |
|
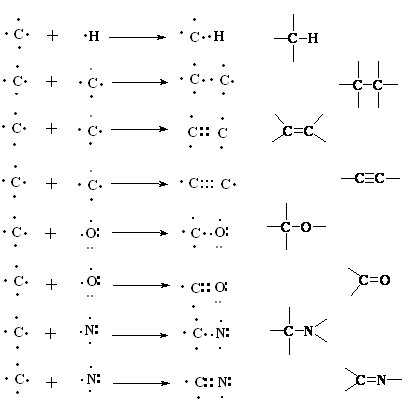
Revenind acum asupra faptului ca toata chimia vietii se grupeaza in jurul chimiei atomului de carbon, care practic are o pondere mai mare decat 50% din masa uscata a celulei, observam posibilitatile acestuia de a forma legatura simpla (legatura s), legatura dubla (legatura s p) sau legatura tripla cu un atom de carbon, legatura simpla sau dubla (legatura s p) cu atomul de azot sau oxigen. Dar poate cea mai importanta observatie care trebuie scoasa in evidenta este proprietatea carbonului de a forma legaturi covalente cu alti atomi de carbon (Figura 1.4.).
Energii ale legaturilor covalente
Energie ( kJ/mol)
H-H 436
C-H 414
C-C 343
C-O 351
Figura 1.4. Tipuri de legaturi stabilite de atomul carbon si energii de legatura ale unor legaturi
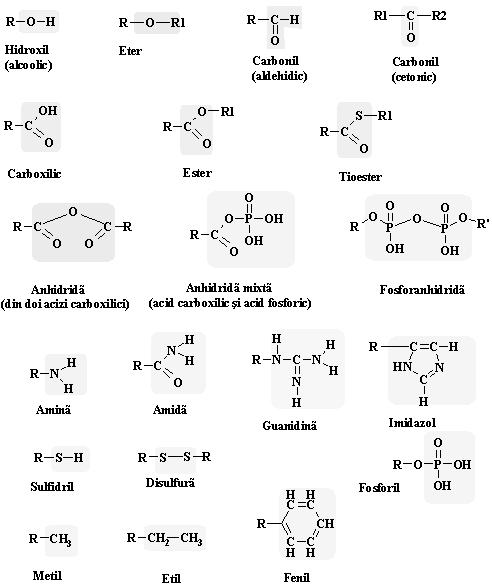
![]() Figura 1.5. Posibilitatea legarii
atomului de carbon de alti atomi
Figura 1.5. Posibilitatea legarii
atomului de carbon de alti atomi
cu formarea gruparilor functionale
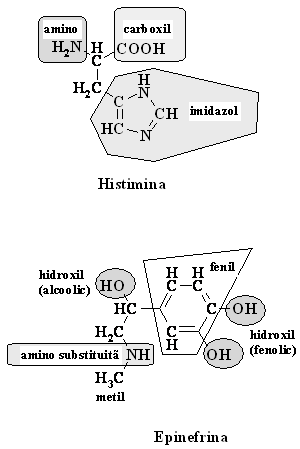
Figura 1.6. Biomolecule cu grupari functionale multiple
In compusii biologici carbonul este regasit atat sub forma unor compusi cu catena liniara sau ramificata, cat si sub forme ciclice, constituite numai din atomi de carbon, dar si sub forme mixte, cand intre atomii de carbon se insereaza un alt atom, denumit de obicei drept heteroatom. Diversitatea mare de combinare ale atomilor prezenti in biomolecule este conferita si de ale caracteristici ale biomoleculelor de baza si anume asa numitele grupari functionale (Figura 1.5.), grupari care la baza lor au tot un atom de carbon.
Aceste grupari functionale dau specificitatea reactivitatii unei biomolecule deoarece modul lor de interactiune cu alte biomolecule sunt imprimate si de prezenta acestora. De multe ori pe o singura biomolecula se pot afla mai multe astfel de grupari functionale (Figura 1.6.). In acest caz reactivitatea lor va fi determinata si de tipul de molecula cu care intra in contact, cu alte cuvinte ele vor reactiona cu aceea grupare functionala cu care poate "comunica" cu biomolecula invecinata.
Drept consecinta biodiversitatea si gradul de interactionare biochimica a diferitelor biomolecule fac ca ierarhizarea biomoleculara sa decurga de la molecule simple, ca de exemplu apa, pana la ansambluri moleculare deosebit de complexe ale organismului viu. Biodiversitate ofera insa o selectivitate proprie, fapt care permite ca aceleasi reactii sa aiba loc cu aceleasi caracteristici. Interventia diferitilor factori, in special al celor externi, pot duce la perturbarea acestor mecanisme complexe de impachetare - despachetare, cu consecinte serioase asupra starii generale a organismului.

|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 1989
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2024 . All rights reserved