| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
 Reactii specifice
Reactii specificeReactia acizi-baze.
Trebuiesc intelese ca reactii la care participa 2 cupluri; pentru ca un acid sa poata ceda protoni, trebuie ca in solutie sa existe o baza care sa-i fixeze, deoarece protonii am observat ca nu pot exista liberi in solutie:
![]()
![]()
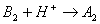
![]()
Facand abstractie de prezenta apei, in sistemul de echilibru, reactia de mai sus poate reprezenta interactia dintre acidul unui cuplu si baza altui cuplu, fara ca vreunul din cele doua cupluri sa fie cel al apei:
![]()
![]()
![]()
![]()
Aminele, (compusi organici) a caror solutii au caracter bazic, genereaza in solutii apoase ioni oxidril.
La dizolvarea in apa a unui acid, acesta va genera ioni hidroniu, iar la dizolvarea in apa a unei baze, aceasta va elibera ioni hidroxil. Cologaridmii cu semn schimbat ai concentratiilor acestor ioni, va indica mediul acid sau bazic al solutiei finale.
Se observa ca prin cedare de protoni, acidul initial se transforma in baza sa conjugata, astfel ca, cu cat un acid este mai tare cu atat baza sa conjugata va fi mai slaba, si invers. De exemplu, cel mai tare acid in solutie apoasa este ionul hidroniu H3O+ (Ka = 1) a carei baza conjugata este apa H2O. Astfel, daca vom aseza acizii in ordinea crescatoare a tariei lor (Ka), va rezulta o ierarhie descrescatoare a tariei bazelor lor conjugate. Un acid va reactiona cu orice baza care se gaseste deasupra lui in aceasta ierarhie.
Consecutiv, in solutii apoase baza cea mai tare este ionul hidroxil HO- (Kb = 1), al carui acid conjugat este apa. Asadar in solutii apoase nu pot exista acizi mai tari ca H3O+ si baze mai tari ca HO-, si consecutiv acizi mai slabe ca H2O si baze mai slabe ca H2O.
In solutiile apoase apa este componentul predominant (in exces). Din aceasta cauza, acizii tari ionizeaza total, in solutii apoase ei elibereaza ionul hidroniu si baze conjugate, care sunt foarte slabe, chiar neutre din punct de vedere al bazicitatii (Cl-, NO3-, SO42-, ClO4- sunt practic neutre). In cazul bazelor tari, acestea in solutii apoase elibereaza ionul hidroxil si acizii conjugati (Na+, K+, Ca2+), care sunt acizi foarte slabi, chiar neutru din punct de vedere al aciditatii.

Reactia de hidroliza.
Este reactia inversa a reactiei de neutralizare, interactiunea are loc intre ionii apei si ionii sarii. Toate reactiile chimice la care iau parte molecule de apa, se numesc reactii de hidroliza.
![]()
![]()
![]()
Aceasta ecuatie este valabila numai cand, in urma interactiunii dintre ionii sarii si ionii apei se obtine un electrolit slab sau greu solubil.
Astfel, pot exista trei cazuri:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Asadar, cand se obtine un electrolit putin disociat, rezulta ca sarea a hidrolizat; daca se obtin numai electroliti tari, reactia de hidroliza nu are loc, ci are loc ionizarea sarii.
Exista patru tipuri de saruri:
I. saruri provenite de la acizi slabi - baze tari, rezulta o solutie cu caracter bazic: CH3COONa, KCN, Na3PO4, etc;
II. saruri provenite de la acizi tari - baze slabe, rezulta o solutie cu caracter acid: NH4Cl, NH4NO3, FeCl3, AlCl3, etc;
III. saruri provenite de la acizi slabi - baze slabe, caracterul solutiei poate fi slab acid, bazic sau neutru (in functie de taria acidului): NH4CN, CH3COOAl, etc;
IV. saruri provenite de la acizi tari - baze tari, nu hidrolizeaza, in urma ionizarii sarii, va rezulta o solutie cu caracter neutru.
Unele reactii de hidroliza pot servi la reactia de identificare pentru unii ioni: BiCl3, SbCl3, SnCl2. In analiza chimica calitativa precipitatele de sulfuri, carbonati, fosfati, oxalati, se spala cu solutii de electroliti adecvati, pentru prevenirea reactiilor de hidroliza, in urma carora se formeaza precipitati.

Reactia redox.
Sunt acelea in care reactantii sufera transformari ale starilor de oxidare, prin transfer de electroni.
![]()
Donorul este reducator (Red) si acceptorul este oxidant (Ox): Red = Ox + ē. Astfel se defineste cuplul reducator-oxidant (redox).
![]()
![]()
![]()
![]()
![]()
Acceptarea de electroni este un proces de reducere, iar cedarea de electroni este oxidare. Substanta care sufera un proces de oxidare se numeste agent reducator, iar cea care sufera un proces de reducere se numeste agent oxidant.
Intr-o reactie chimica un partener este oxidat cand sarcina sa pozitiva creste sau sarcina sa negativa scade. Trecerea metalelor in solutii, sub forma de cationi, este o reactie de oxidare:
![]()
![]()
Un partener este redus, atunci cand sarcina sa pozitiva scade sau sarcina sa negativa creste. Trecerea ionilor metalici de la o stare superioara de oxidare la una inferioara este un proces de reducere:
![]()
![]()
![]()
![]()
![]()
![]()
Din ultimele doua reactii se observa ca reactiile redox sunt influentate de prezenta ionilor de H+, care induce un mediu acid.
Asemanator protonilor, nici electronii nu pot exista liberi, de aceea pentru ca un reducator sa poata ceda electroni, trebuie sa existe in solutie un oxidant care sa-i accepte; in reactiile redox trebuie sa aiba loc simultan ambele fenomene de cedare si acceptare de electroni. Numai descriptiv cele doua fenomene se scriu separat.
![]()
![]()
![]()
![]()
Daca in solutia unui oxidant si a unui reducator, de introduce un electrod inert (metal inatacabil Au, Pd, Pt), acesta joaca rol de suport de electroni angajati in reactia redox si astfel, capata un potential de electrod numit potential redox.
Conventional, potentialul normal pentru H+/H2 se ia ca referinta si are valoarea o. pe baza lui s-au putut calcula potentialele pentru orice cuplu redox.
![]()
![]()
![]() ε = -3,040 mV
ε = -3,040 mV
![]()
![]()
![]() ε = -2,900 mV
ε = -2,900 mV
![]()
![]()
![]() = -2,710 mV
= -2,710 mV
![]()
![]()
![]() = -0,760 mV creste potentialul redox
= -0,760 mV creste potentialul redox
![]()
![]()
![]() = -0,760 mV creste taria oxidantilor
= -0,760 mV creste taria oxidantilor
![]()
![]()
![]() = 0,00 mV scade taria
reducatorilor
= 0,00 mV scade taria
reducatorilor
![]()
![]()
![]() ε = 0,570 mV
ε = 0,570 mV
![]()
![]()
![]() ε = 1,280 mV
ε = 1,280 mV
![]()
![]()
![]() ε = 1,360 mV
ε = 1,360 mV
![]() ε = 1,500 mV
ε = 1,500 mV
Cu cat un cuplu are potentialul redox mai mare cu atat oxidantul cuplului este mai puternic si reducatorul mai slab.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 1666
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2024 . All rights reserved