| CATEGORII DOCUMENTE |
| Aeronautica | Comunicatii | Electronica electricitate | Merceologie | Tehnica mecanica |
SURSE DE ENERGIE NECONVENTIONALE REGENERABILE. OBTINEREA HIDROGENULUI PRIN FOTODISOCIEREA APEI
HIDROGENUL
T. N. Veziroglu /1/, editor al revistei specializate in probleme de energetica hidrogenului "International Journal of Hydrogen Energy" sintetizeaza cateva proprietati care recomanda utilizarea hidrogenului ca vector energetic produs pe baza de tehnologii neconventionale:
- hidrogenul concentreaza surse (energetice) de energie primara pe care o prezinta la consumator intr-o forma convenabila
cost de productie relativ ieftin ca urmare a perfectionarilor de ordin tehnologic
- posibilitatea de conversie in diverse forme de energie prin procedee caracterizate de eficienta maxima
- este o sursa inepuizabila, avand in vedere ca se obtine din apa, iar prin utilizare se transforma in apa. Productia si consumul hidrogenului reprezinta un ciclu inchis, care mentine constanta sursa de productie - apa, si reprezinta un ciclu clasic de recirculare a materiei prime (spre exemplificare se prezinta schema de principiu de mai jos)
- este cel mai usor si mai curat combustibil. Arderea hidrogenului este aproape in intregime lipsita de emisii poluante, cu exceptia NOx-ului, care poate si el fi eliminat prin reglarea corespunzatoare a conditiilor de ardere. Are o densitate energetica gravimetrica mult superioara oricarui alt combustibil
- hidrogenul poate fi stocat in mai multe moduri: gaz la presiune normala sau la inalta presiune, ca hidrogen lichid sau sub forma de hidruri solide
- poate fi transportat pe distante mari in oricare din formele prezentate anterior
- deoarece se poate combina fara probleme cu oxigenul care, in cazul unei pile de combustie, are o eficienta de combustie de peste 60 %, ofera perspectiva depozitarii electricitatii in afara varfurilor de sarcina, prin electroliza apei in scopul obtinerii hidrogenului.
La inceputul noului secol si mileniu, cei interesati de problemele globale cu care se confrunta civilizatia trebuie sa recunoasca importanta poluarii datorate surselor de energie fosile si necesitatea reducerii emisiilor toxice prin inlocuirea acestora cu noi surse de energie. Aproximativ 80% din energia mondiala este reprezentata de sursele fosile. Acestea sunt responsabile de emisiile de CO2 din atmosfera, care sunt daunatoare unui climat ecologic. Multi combustibili sintetici pot sa nu polueze atmosfera ambianta, dar hidrogenul indeplineste cel mai bine aceste conditii.
Sistemele bazate pe hidrogen reprezinta una din cele mai atractive directii ale energiei viitorului. Producerea hidrogenului din materiale ieftine, cum ar fi apa, este un proiect care va fi sustinut in viitor.
Actualmente, hidrogenul se obtine prin reformarea cu abur a gazului metan. Prin utilizarea apei ca materie prima de obtinere a hidrogenului se va realiza economisirea gazului metan, cu atat mai mult cu cat in viitor se preconizeaza utilizarea hidrogenului drept carburant nepoluant.
Sistemele bazate pe hidrogen solar reprezinta una din cele mai atractive directii ale energiei viitorului. Astazi, ecologistii privesc la deteriorarea ecosistemelor si observa necesitatea restructurarii economiei, necesitatea unei paradigme schimbate. Spre exemplu, stabilirea climei planetare depinde acum de reducerea emisiilor de carbon, prin trecerea de la combustibilii fosili spre o economie bazata pe energie solara/hidrogen /2/.
Pe plan international cercetarea producerii hidrogenului este inclusa in programul retelei internationale de energie regenerabila, care a luat nastere la 12 septembrie 1992 in Anglia (World Renewable Energy Network), autoarea prezentei lucrari fiind membru fondator /3/.
OBTINEREA HIDROGENULUI
Disocierea termica directa a apei si disocierea apei cu ajutorul cuantelor de lumina sunt metode neconventionale de obtinere a hidrogenului. Utilizarea energiei luminoase pentru disocierea apei este posibila deoarece vaporii de apa absorb lumina de cca. 1860 si fotonii de radiatii ultraviolete de 1949 . In aceste conditii se rupe legatura H-OH cu un randament de formare a hidrogenului de cca. 0,4 %.
'Hidrogenul solar' are posibilitati reale de a deveni mai rentabil ca sursa energetica decat energia furnizata de centralele atomoelectrice.
Autoarea prezentei lucrari, impreuna cu profesorul T.N. Veziroglu au publicat in 2002 un studiu amplu privind starea curenta a obtinerii si utilizarii hidrogenului ca sursa alternativa de energie ("Current status of hydrogen energy", Renewable and Sustainable Energy Reviews, 6, 141-179(2002)).
Structura zeolitilor
Un
zeolit este definit ca o retea tridimensionala de tetraedri de SiO4
si AlO4 care se intalnesc in fiecare varf, punand in
comun un atom de oxigen. Cel care a denumit
aceste noi materiale folosind acest termen a fost suedezul Axel Cronstedt /4/. Denumirea
provine din limba greaca si inseamna piatra care fierbe. Cronstedt s-a dovedit a fi inspirat deoarece
descrie una din proprietatile remarcabile ale zeolitilor,
capacitatea de a absorbi masiv apa si de a o elimina la temperaturi de
peste
Studiu pentru selectarea zeolitului activ in reactia de fotodisociere a apei: zeolitul A
Zeolitul A a fost primul zeolit obtinut prin sinteza, ca rezultat al cercetarilor de pionierat ale lui Barre /5/. Zeolitul A, sintetizat prin cristalizarea hidrotermala a gelurilor de aluminosilicat in sistemul Na2O-Al2O3-SiO2-H2O, se caracterizeaza la temperatura ridicata printr-o structura cuboctaedrica, raport molar SiO2/Al2O3 = 2, capacitate inalta de adsorbtie a apei si proprietati remarcabile de schimb ionic.
O importanta clasa a catalizatorilor acizi solizi o constituie zeolitii sintetici (sitele moleculare). Diferitele structuri cristalografice permit clasificarea sitelor moleculare in tipurile A, X si Y /6/. Unitatea cristalografica de baza este tetraedrul, cu un atom se siliciu in centru si atomi de oxigen in varfuri; atomul de siliciu poate fi inlocuit izomorf cu un atom de aluminiu (fig. 4). Unitatea structurala cristalina a sitelor moleculare este celula sodalitica formata din 24 tetraedri (fig.5).
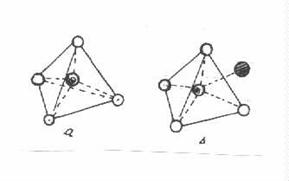
Figura 4
Site moleculare: a - tetraedrul de SiO4- ; b - tetraedrul de Al O4 Na
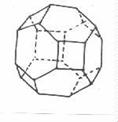
Figura 5
Unitatea structurala cuboectaedrica formata prin unirea a 24 tetraedri
Daca fiecare fata patrata a celulei se leaga cu o alta fata patrata structura rezultata va fi cubica (fig.6) cu axe ortogonale si este caracteristica sitelor moleculare de tip A. Daca unitatile sodalitice se leaga intre ele cu fetele hexagonale fata in fata, structura obtinuta este proprie sitelor moleculare de tip X si Y (fig.6).
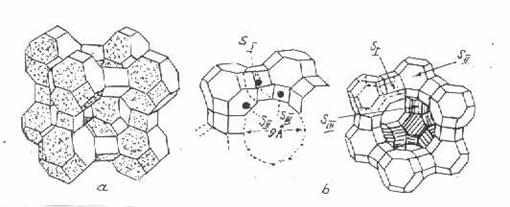
Figura 6
Site moleculare: a - tip A, b- tip X sau Y
Sitele moleculare de tip A prezinta trei tipuri de cavitati. Cavitatile tip α sunt cele mai mari, ocupa centrul celulelor elementare, prezinta pori cu diametrul de 4,2 A si fiecare comunica cu alte sase cavitati. Cavitatile β sunt cavitati sodalitice si au forma octaedrica. Deschiderea ferestrelor sodalitice este de 2,3 A. Cavitatile γ au de asemenea forma cubica si unesc fetele patrate ale cavitatilor sodalitice, rezultand astfel cavitatile α (fig. 7 si 8).
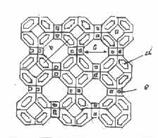
Figura 7
Structura sitei moleculare tip A
a - unitati cuboctaedrice; b - cavitati mari (α) c - deschideri inelare (pori sau "ferestre" mari) (β); d - cavitati mici (γ) cu deschideri inelare mici; e - punti de oxigen
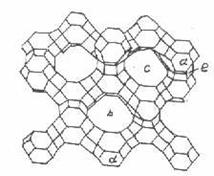
Figura 8
Structura sitei moleculare tip X si Y
a - unitati cuboctaedrice; b - cavitati mari (α); c - deschideri inelare (pori sau "ferestre" mari) (β) ; d - cavitati mici (γ) cu deschideri inelare mici; e - punti de oxigen
REALIZAREA INSTALATIEI DE LABORATOR PENTRU OBTINEREA HIDROGENULUI PRIN FOTODISOCIEREA APEI
S-a construit o instalatie experimentala alcatuita din urmatoarele componente :
reactor din cuart special construit, cu ferestre slefuite optic, prevazut cu robinet acces gaz purtator (argon sau azot), robinet pentru colectarea gazelor rezultate din reactie (hidrogenul) si robinet de siguranta
suport metalic special pentru reactorul din cuart care sa asigure atat stabilitatea reactorului pe timpul desfasurarii reactiei cat si detasarea de instalatie, necesara echiparii reactorului cu diverse probe preparate, pe care se studiaza reactia de fotodisociere a apei
sistem de agitare continua a probei cu apa, in reactorul din cuart; plita magnetica si agitatoare magnetice
sistem de iradiere in UV: s-a montat o lampa UV cu vapori de mercur, prevazuta cu droser si cu diferite filtre UV in domeniul 300 - 450 nm
ecran de protectie UV
sistem de colectare a gazelor rezultante din reactie (hidrogen, oxigen), alcatuit din mai multe gazometre si vase de nivel. Controlul producerii hidrogenului s-a urmarit prin metode cromatografice, analizand periodic hidrogenul colectat in timpul reactiei .
Producerea fotochimica a hidrogenului din apa are loc in concordanta cu urmatoarea schema cinetica:
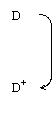
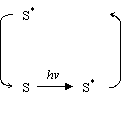

unde D este un electron donor de sacrificiu, S este sensibilizatorul, A este un electron acceptor si C un catalizator redox.
FOTOSISTEME PENTRU GNERAREA HIDROGENULUI DIN APǍ
Dioxidul de titan
TiO2 este un conductor de tip n (Δn ≤3.2 eV), care absoarbe fotonii in domeniul ultraviolet apropiat, ceea ce limiteaza aplicarea lui in sisteme care utilizeaza energia solara; cu toate acestea, sisteme fotocatalitice pe baza de TiO2 cu surse UV artificiale au fost aplicate pentru decontaminarea surselor de apa /7,8/. Prin iluminarea TiO2 cu radiatii avand lungimea de unda mai mica de 400 nm se pot genera perechi de electroni (e-)/goluri pozitive (h+) in banda de conductie, care migreaza spre suprafata, participand la reactiile redox care au loc intr-un proces fotocatalitic.
TiO2 + hν (≤3.2 eV) → e - + H +
e - + H + → recombinare
Pentru a obtine un fotocatalizator eficient trebuie evitat consumul perechilor de sarcini fotoexcitante in procese de recombinare, prin marirea vitezei de transfer a acestora catre speciile din solutie. Se pot utiliza in acest scop catalizatori de transfer de sarcina pe suprafata TiO2; imprastierea rapida a sarcinilor h + poate fi promovata de adsorbtia unor intermediari oxido-reducatori in solutie, prin incorporarea unor centri de adsorbtie mai eficienti decat TiO2, pe suprafata catalizatorului. Acesti centri trebuie sa se situeze in apropierea centrilor de TiO2, astfel incat oxidantii generatori de sarcini h+ ( de exemplu, radicalii hidroxil) sa poata ajunge la centrii TiO2 inainte ca acesti intermediari sa se consume intr-o reactie (recombinarea cu electroni).
Compozitii mixte: dioxid de titan/suport zeolitic
Lucrarile publicate pana acum indica folosirea unor concentratii mari de TiO2 in compozitia catalizatorilor de tipul TiO2/suport zeolitic /9/. Unul dintre cele mai importante aspecte privind prepararea fotocatalizatorilor pe baza de zeoliti este metoda de preparare a compozitiilor mixte TiO2 - suport zeolitic, care trebuie sa asigure atat pastrarea fotosensibilitatii TiO2 cat si a proprietatilor de adsorbtie ale zeolitului /10/.
S-au efectuat experimente pe urmatorii compusi:
TiO2 + zeolit de tip A modificat cu 15% TiO2
TiO2 + zeolit de tip A modificat cu 15% TiO2 + aditivi anorganici
TiO2 + aditivi anorganici de tip Na2CO3 si NaHCO3.
La compusii de TiO2 + zeolit de tip A modificat cu 15% TiO2 + aditivi anorganici cantitatea totala de hidrogen obtinuta a fost cuprinsa intre 4,95 si 6,75 ml. La compusii de TiO2 + aditivi anorganici de tip Na2CO3 si NaHCO3 s-a obtinut cea mai mare cantitate de hidrogen : 21,70 - 25,90 ml H2.
CONCLUZII
1) S-au selectat din literatura cele mai eficiente fotosisteme de obtinere a hidrogenului. S-a efectuat un studiu pentru selectarea zeolitului activ in reactia de fotodisociere a apei: zeolit tip A. Anatasul este cea mai activa faza de TiO2
2) S-au efectuat experimentari pe amestecuri preparate de zeolit de tip A modificat cu TiO2 si probe de TiO2 aditivat cu saruri de sodiu
3) S-au efectuat cercetari de fotodisociere a apei pe o instalatie de laborator alcatuita din urmatoarele componente: reactor din cuart de constructie speciala; lampa UV cu vapori de mercur; instalatie de vid; butelie de gaz (argon/azot); gazometre pentru colectarea hidrogenului
4) S-a testat comportarea sub iradiere a compusilor preparati (probe de dioxid de titan si zeoliti modificati cu TiO2) si utilizati in generarea hidrogenului. Activitatea fotocatalitica a dioxidului de titan suportat pe zeoliti (ZSM-5 si zeolit A) este mai mare comparativ cu TiO2 pur. La compusii de TiO2 + zeolit de tip A modificat cu 15% TiO2 + aditivi anorganici, cantitatea totala de hidrogen obtinuta a fost cuprinsa intre 4,95 si 6,75 ml. La compusii de TiO2 + aditivi anorganici de tip Na2CO3 si NaHCO3 s-a obtinut cea mai mare cantitate de hidrogen: 21,70 - 25,90 ml H2.
BIBLIOGRAFIE
1. T. N. Veziroglu, International Journal of Hydrogen Energy, 2000, 1143
2. I. Iliescu, Prefata
3. M. Momirlan, L. Muresan, A. A. M. Sayigh, T. N. Veziroglu, Renewable Energy: Renewable Energy, Energy Efficiency and the Environment, 2, 1258 (1996)
6. M. Cruceanu, E. Popovici, N. Balba, N. Naum, L. Vladescu, A. Vasile, E. R. Russu, Site moleculare
zeolitice, Editura Stiintifica si Enciclopedica, Bucuresti, 1986
7. V. F. Stone, R. J. Davis, Chem Mater., 10, 1468 (1998)
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 1216
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved