| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Alti agenti chimioterapeutici
Hidrazida acidului nicotinic (izoniazida, INH), introdusa in clinica inainte de 1950, impreuna cu rifampina, formeaza baza chimioterapiei antituberculoase. Izoniazida este un derivat al nicotinamidei. Mecanismul de actiune al izoniazidei nu este cunoscut, dar influenteaza sinteza lipidelor, acizilor nucleici si acidului micolic la M. tuberculosis.
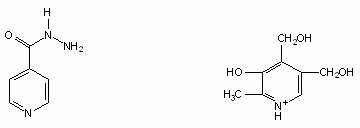
Izoniazida Piridoxina (vitamina B6)
Se presupune ca izoniazida este activa prin competitie cu piridoxina (vitamina B6) necesara cresterii celulelor de M. tuberculosis, sau inhiba sinteza acizilor micolici (acizi grasi specifici acestor bacterii). Este bactericida fata de celulele care cresc si se divid si are actiune bacteriostatica fata de celulele care nu se multiplica. Toate cele trei (PASA, dapsone si izoniazida) se folosesc pentru tratamentul infectiilor cu Mycobacterium.
Etambutolul, pirazinamida si etionamida blocheaza reactiile enzimatice in celula bacteriana, deoarece sunt similare dar nu identice cu vitaminele bacteriene.
Etambutolul inhiba arabinozil-transferaza, enzima implicata in biosinteza arabinogalactanului si lipoarabinomananului. Alte efecte atribuite actiunii etambutolului sunt inhibitia metabolismului ARN si sintezei fosfolipidelor, inhibitia transferului acizilor micolici la arabinogalactanul legat de peretele celular mureinic, sinteza spermidinei si inhibitia unei trepte timpurii a conversiei glucozei in monozaharidele utilizate pentru sinteza polizaharidelor parietale (arabinogalactan, arabinomanan) si a peptidoglicanului. Este un medicament foarte specific si eficient, utilizat in asociatie cu izoniazida, pentru tratamentul tuberculozei. Are efect bacteriostatic. Nu se cunoaste mecanismul care determina rezistenta la etambutol (J. A. Musser, 1995).
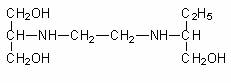
Etambutolul
Pirazinamida este un derivat sintetic al nicotinamidei. Nu se cunoaste mecanismul de actiune, nici baza moleculara a rezistentei. Unele tulpini sensibile la pirazinamida au o enzima specifica (pirazinamidaza), ce metabolizeaza pirazinamida la acidul pirazinoic, intermediarul activ antibacterian. Tulpinile rezistente la pirazinamida au pierdut activitatea pirazinamidazica. S-au identificat si tulpini foarte rezistente la pirazinamida, care au si activitate pirazinamidazica. Aceasta sugereaza ca, in plus fata de pierderea capacitatii de sinteza a pirazinamidazei, exista si alte mecanisme de rezistenta.
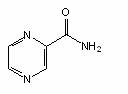
Pirazinamida
Etionamida, derivata a acidului izonicotinic, este activa fata de M. tuberculosis si alte micobacterii. In vitro, celulele tratate cu etionamida, celulele de M. tuberculosis isi pierd acidorezistenta. Se crede ca mecanismul sau de actiune implica inhibitia sintezei acizilor micolici.
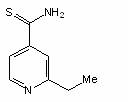
Etionamida
Nu se cunosc mecanismele rezistentei la etionamida si la izoniazida.
Metronidazolul a fost introdus in clinica in 1959 pentru tratamentul infectiei cu Trichomonas vaginalis. Ulterior s-a demonstrat eficienta sa fata de infectiile cu bacterii anaerobe si fata de alte infectii parazitare. Difuzeaza bine in tesuturi, inclusiv in sistemul nervos. Are cea mai buna activitate bactericida, dintre toate medicamentele active fata de bacteriile anaerobe.
Actiunea sa consta in activarea reductiva a grupariii nitro. Metronidazolul actioneaza ca acceptor preferential de electroni(e-), fiind redus de proteinele transportoare de e- cu potential redox scazut. Reducerea scade concentratia sa, ceea ce mentine un gradient ce favorizeaza incorporarea medicamentului in celula si generarea produselor intermediare ale reducerii, cu efecte toxice pentru celula.
Toxicitatea se datoreaza compusilor intermediari sau radicalilor liberi ce interactioneaza cu ADN si probabil cu alte molecule, producand leziuni. Intermediarii citotoxici se descompun in produse finale netoxice si inactive: acetamida si acidul 2-hidroxietil oxamic. Efectul asupra microbiotei intestinale este minim, deoarece medicamentul este redus in conditii anaerobe.
Methenamina este produsul ciclic de condensare a formaldehidei si amoniului. Are activitate antibacteriana slaba, dar la pH acid, fiecare molecula hidrolizata genereaza 4 molecule de amoniu si 6 molecule de formaldehida:
![]()
Este excretata in urina acida, unde este hidrolizata si formaldehida eliberata este bactericida. Este disponibila ca sare a acidului mandelic sau hipuric pentru acidifierea urinii. Nu s-a descris rezistenta la formaldehida, dar tulpinile de Proteus, care produc frecvente infectii urinare sunt rezistente, deoarece ureaza lor cliveaza ureea la CO2 si NH3 si alcalinizeaza urina.
Derivatii nitrofuranului (furazolidon, nitrofurantoina, nitrofuratel, nitrofurazon) au efect bacteriostatic fata de bacteriile Gram pozitive si Gram negative. Cel mai utilizat este nitrofurantoina.
Derivatii nitrofuranului se folosesc pentru terapia infectiilor tractului urinar, deoarece realizeaza concentratii suficient de mari in urina. Nu au actiune sistemica. Un intermediar redus al nitrofuranilor produce ruperea catenei de ADN, ceea ce explica efectele mutagene ale acestor compusi in vitro. Sunt activate mecanismele de reparare a ADN. Metabolitii reactivi redusi ai nitrofurantoinei interfera nu numai cu ADN, ci par a fi capabili sa se lege cu proteinele ribosomale si inhiba sinteza proteinelor. Inhiba respiratia bacteriana si metabolismul piruvatului.
Nitroimidazolii au spectru larg de actiune (bacterii, fungi, protozoare, helminti). Cei cu activitate antibacteriana sunt 5-nitroimidazolii: 2-metronidazolul, furazolidonul si tinidazolul.
Furazolidonul este unul din numarul foarte mare de compusi (de ordinul miilor) de nitrofuran, introdusi in clinica dupa descoperirea acestei clase de compusi in anii '40. Este activ fata de Klebsiella, E. coli, Campylobacter spp., S. aureus, Giardia lamblia.
Efectul lor antibacterian este dependent de reducerea gruparii nitro in conditii anaerobe. Compusii capteaza e- din feredoxina redusa, generata in reactia de decarboxilare a piruvatului. Produsul reducerii are efect letal, probabil prin ruperea catenei de ADN. Unele bacterii microaerofile sunt deosebit de sensibile, dar mecanismul mortii lor nu se cunoaste.
Aceste substante au spectru antibacterian redus, limitat la bacterii anaerobe, cu doar doua exceptii: Helicobacter pylori si Gardnerella vaginalis, bacterii microaerofile sensibile la nitroimidazol. Conditia esentiala pentru ca nitroimidazolii sa actioneze, este reducerea partiala a gruparii nitrat prin sistemul intracitoplasmatic transportor de electroni. Bacteriile aerobe sunt incapabile sa realizeze aceasta reducere, ceea ce explica rezistenta lor naturala.
Nitrofuranii sunt agenti antibacterieni a caror structura si mod de actiune sunt similare cu cele ale nitroimidazolilor. Activitaea lor este legata de reducerea gruparii NH2.
Intreaga cantitate administrata, pe cale orala sau parenterala ramane disponibila actiunii antimicrobiene. Perioada de injumatatire permite administrarea a doua doze/zi. Datorita mecanismului unic de actiune, nu exista fenomene de rezistenta incrucisata. Bacilii Gram negativi poseda rezistenta intrinseca pentru ca au pompe de eflux eficiente fata de Linezolid.
Un parametru esential al unui agent chimioterapeutic este indexul terapeutic, adica raportul dintre doza toxica minima si doza cu eficienta maxima. Valoarea mare a acestui raport este caracteristica agentilor chimioterapeutici foarte eficienti.
Oxazolidinonele reprezinta o clasa unica de agenti antimicrobieni sintetici. Utilizarea lor in clinica a fost impusa de necesitatea tratarii infectiilor produse de stafilococii rezistenti la meticilina, de pneumococii rezistenti la penicilina, de enterococii rezistenti la vancomicina.
Acesti agenti au un mecanism unic de actiune, ceea ce elimina riscul rezistentei incrucisate cu agentii antimicrobieni disponibili. Deoarece nu sunt molecule naturale, genele de rezistenta specifica nu preexista in genofondul natural.
Oxazolidinonele au fost initial utilizate in terapie ca inhibitori ai monoamin-oxidazei, pentru tratamentul depresiei, dar ulterior s-a descoperit ca au si activitate antimicrobiana. Primul agent al acestei clase a fost produs de compania DuPont de Nemours, la sfarsitul anilor '70 pentru controlul bolilor foliare bacteriene si fungice la diferite plante, inclusiv la tomate. Modificarea chimica a oxazolidinonei a dus la descoperirea a doi agenti - eperezolid si linezolid, cu activitate in vitro si toxicitate diminuata.
Linezolid are activitate in vitro, fata de N. gonorrhoeae si N. meningitidis si are o eficienta buna fata de multe bacterii Gram pozitive anaerbe (Bacteroides fragilis). Bacteriile Gram negative sunt probabil intrinsec rezistente, deoarece poseda pompe de eflux, eficiente fata de linezolid. In vitro, linezolid are o eficienta relativ buna fata de M. tuberculosis si foarte buna fata de Nocardia.
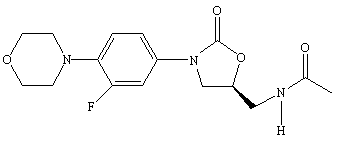
Linezolid
Concentratiile subinhibitorii de linezolid diminua producerea hemolizinei si coagulazei la S. aureus si inhiba sinteza streptolizinei O si DN-azei la streptococi.
Mecanismul de actiune si rezistenta. Oxazolidinonele sunt inhibitorii sintezei proteinelor ribosomale la bacterii, dar spre deosebire de alti agenti antimicrobieni cu actiune asupra ribosomilor, oxazolidinonele au un mecanism unic de actiune deoarece blocheaza prima treapta a asamblarii ribosomilor din subunitatile disociate. Oxazolidinonele se leaga de un situs al subunitatii 50S, la interfata sa cu subunitatea 30S si previn formarea complexului de initiere 70S, care cuprinde ARN-fMet, ARNm si cele doua subunitati ribosomale.
Linezolid se leaga de subunitatea 50S, la sau langa situsul care leaga cloramfenicolul si lincomicina, deoarece cele 3 molecule intra in competitie pentru situsurile de legare din domeniul V al ARN 23S al subunitatii 50S. Domeniul V este centrul peptidil-transferazei, care catalizeaza formarea legaturii peptidice. Spre deosebire de cloramfenicol si lincomicina, linezolid nu inhiba formarea legaturilor peptidice si intre ele nu exista rezistenta incrucisata.
Asemanator majoritatii inhibitorilor sintezei proteinelor ribosomale, activitatea linezolidului fata de bacterii in vitro este considerata bacteriostatica, deoarece bacteriile sunt omorate mai incet decat de agentii bactericizi.
Linezolid este metabolizat prin oxidarea inelului morfolino si se formeaza doi metaboliti: acidul aminoetoxi-acetic si hidroxi-etil glicina.
Linezolid este un agent antimicrobian cu spectru larg de activitate, virtual fata de toate bacteriile Gram pozitive.
Intreaga cantitate administrata, pe cale orala sau parenterala ramane disponibila actiunii antimicrobiene. Perioada de injumatatire permite administrarea a doua doze/zi. Datorita mecanismului unic de actiune, nu exista fenomene de rezistenta incrucisata. Bacilii Gram negativi poseda rezistenta intrinseca pentru ca au pompe de eflux eficiente fata de Linezolid.
Un parametru esential al unui agent chimioterapeutic este indexul terapeutic, adica raportul dintre doza toxica minima si doza cu eficienta maxima. Valoarea mare a acestui raport este caracteristica agentilor chimioterapeutici foarte eficienti.
Antibioticele (anti + bios = cu efecte nefavorabile) sunt un grup heterogen de substante chimice cu greutate moleculara mica, produse de microorganisme prin procese de biosinteza, care omoara sau inhiba cresterea altor specii de microorganisme.
Definitia initiala s-a completat ulterior, deoarece antibioticele sunt substante chimice obtinute prin biosinteza, semisinteza sau prin sinteza chimica, care in concentratie mica inhiba multiplicarea sau omoara microorganismele. Definitorie pentru notiunea de antibiotic, ramane capacitatea de a fi produs prin biosinteza de catre microorganisme.
Fenomenul de antibioza (inhibitia dezvoltarii unui microorganism de catre altii) a fost descris de Pasteur (l877). Gratia si Dath (1924)au studiat microorganismele din sol si in filtratul acelular al culturii de actinomicete au evidentiat efectul inhibitor al unei substante pe care au denumit-o actinomicetina.
Fleming (l928), in cautarea unor compusi cu potential antibacterian, a observat inhibitia cresterii coloniilor de Staphylococcus aureus in vecinatatea coloniilor fungice de Penicillium notatum. Apoi a aratat ca mediul lichid al culturii de P. notatum, diluat de 800 de ori, a inhibat cresterea culturii de Staphylococcus. A descoperit "medicamentul miracol" - pe care l-a denumit penicilina, dar n-a izolat-o, pentru care a fost distins cu premiul Nobel. Calitatile ei de medicament "miraculos" au fost evidentiate de catre Ernst Chain si Howard Florey (1939), care au izolat-o si au folosit-o in tratamentul infectiilor bacteriene in timpul celui de al II-lea razboi mondial. Productia industriala a inceput in l943. Noul medicament a fost introdus in circuitul clinic general in 1944 si a avut un impact urias asupra starii de sanatate a populatiei umane.
R. Dubos (1939) a izolat gramicidina si tirocidina din Bacillus brevis, active fata de bacteriile Gram pozitive.
S. Waksman (1944-1945) a izolat streptomicina din Str. griseus, un microorganism izolat din sol, pentru care a primit premiul Nobel. Streptomicina este activa fata de unele bacterii Gram pozitive si fata de Mycobacterium tuberculosis. El a propus denumirea de antibiotic, cu sensul de compus chimic produs de un microorganism, care la concentratie mica, inhiba sau omoara alte microorganisme.
Antibiotice au fost esentiale in lupta cu maladiile infectioase si au contribuit esential la cresterea sperantei de viata in secolul 20. Dupa introducerea penicilinei in clinica generala (1944), infectiile grave (faringita streptococica) pana atunci, au devenit vindecabile. Azi, dependenta omului de antibiotice este totala. Numai in SUA, in 1998, pentru uzul uman s-au folosit circa 12,5 tone de antibiotice. Daca se adauga cele administrate in hrana animalelor si in agricultura, se apreciaza ca in ultimii 50 de ani s-au produs si s-au utilizat peste un milion de tone.
Antibioticele sunt produse de trei grupe de microorganisme: actinomicete, bacili Gram pozitivi si fungi filamentosi microscopici. Actinomicetele sunt cele mai bune producatoare de antibiotice si alti metaboliti secundari cu activitate biologica. Genul cel mai reprezentativ - Streptomyces - s-a izolat din tubul digestiv al unui pui de gaina. Cephalosporium a fost izolat din apa marii, langa un canal de deversare a apelor menajere, iar Bacillus, dintr-o rana tegumentara a unei fetite (Tracy) si de aici s-a dat denumirea antibioticului bacitracina.
Estimarile numarului de substante antibiotice variaza: unii au inventariat circa 5000 antibiotice identificate, iar altii evalueaza cifre net superioare de ordinul a 10 000. Actinomicetele produc peste 2/3 din totalul antibioticelor, iar speciile g. Streptomyces produc 70-80% dintre metabolitii secundari. Pentru terapia infectiilor umane si animale se foloseste un numar restrans (circa l00), produse de reprezentantii a 5 genuri de microorganisme: Bacillus, Streptomyces, Micromonospora, Penicillium, Cephalosporium. Celelalte sunt toxice ori au efecte defavorabile asupra organismului sau sunt lipsite de selectivitate.
Izolarea microorganismelor producatoare de antibiotice este foarte laborioasa. Din l34 700 tulpini bacteriene izolate din circa 5000 de probe diferite de sol, o singura tulpina a prezentat interes practic.
In perioada descoperirii celor mai multe antibiotice (anii 1950-'60) s-au identificat tetraciclina, eritromicina si kanamicina, agentii antifungici candicidina si nistatinul, precum si substante cu efect antineoplazic (adriamicina).
Marea majoritate a antibioticelor se obtine in procese industriale, pe cale microbiologica.
In prezent, numai portiunea majora a moleculei de antibiotic este sintetizata de microorganisme, iar restul moleculei este sintetizata pe cale chimica. Se obtin astfel antibiotice de semisinteza sau prin metode de bioconversie. In unele cazuri (de exemplu, cloramfenicolul), intreaga molecula se sintetizeaza pe cale chimica, datorita structurii sale moleculare simple.
Conventional, in categoria antibioticelor sunt incluse si substantele de semisinteza sau cele sintetizate artificial, dar pe care microorganismele le pot sintetiza total sau partial. Aceasta mentiune (ca microorganismele le pot sintetiza total sau partial) este necesara, pentru ca din categoria antibioticelor sa se excluda compusii cu efect antibacterian sintetizati numai pe cale chimica (sulfamidele) sau cei produsi in organismele superioare (lizozimul).
Structurile moleculare complexe ale antibioticelor combina derivati a doua sau mai multe grupe de metaboliti: aminoacizi, glucide, bazele acizilor nucleici, intermediari ai sintezei lipidelor. Acetil-CoA si propionil-CoA formeaza catene lungi (ca in sinteza acizilor grasi) si rezulta poli-b cetone (RCO - CH2 - CO - CH2 - ), care se condenseaza pentru a forma inelele macrolidelor, polienelor, tetraciclinelor sau portiuni ale moleculei altor antibiotice.
Substantele biogene preluate de celula sub o forma simpla, sunt folosite de celula in urmatoarele directii esentiale:
pentru sinteza metabolitilor primari (aminoacizi, baze purinice si pirimidinice, enzime, acizi grasi), necesari biosintezei constituientilor structurali, rezultatul fiind cresterea celulei. Acesti compusi se sintetizeaza faza de crestere primara, denumita si trofofaza;
pentru producerea energiei, in metabolismul energetic si a produselor metabolismului energetic (produsi de fermentatie alcoolica, lactica, butirica, propionica, acida etc.);
pentru producerea (uneori) a metabolitilor secundari (antibiotice, alcaloizi, ergotina, giberelina).
Metabolitii secundari se sintetizeaza in faza de crestere secundara - idiofaza - dupa epuizarea unui nutrient major (sursa de C sau de N), nu sunt esentiali pentru cresterea celulei si sinteza lor este expresia procesului de diferentiere biochimica.
Metabolitii primari si secundari pot fi denumiti ''generali'' si ''speciali''. Metabolismul primar implica activitatea unei serii de cai interconectate de anabolism, de catabolism si amfibolice, catalizate de enzime care furnizeaza intermediari de biosinteza si energie si convertesc precursorii in macromolecule esentiale: ADN, ARN, proteine, lipide si polizaharide. Metabolismul primar este acelasi pentru toate organismele vii.
Pe langa metabolitii generali, unele organisme ale diferitelor grupari taxonomice sunt capabile sa sintetizeze metaboliti de tip special, folosind fie aceleasi enzimele metabolismului general, sau sintetaze speciale produse de celule in conditii nutritionale speciale. De exemplu, acizii grasi se sintetizeaza pe o cale comuna la toate celulele vii, iar anumite grupe taxonomice de microorganisme si plante sintetizeaza poliketide din aceiasi precursori, utilizand enzime asemanatoare.
Metabolitii secundari au fost denumiti idioliti, deoarece se sintetizeaza in idiofaza (faza de productie) culturii stationare. Metabolitii secundari au structuri chimice particulare, nu sunt esentiali pentru cresterea organismului producator, dar probabil au rol in asigurarea supravietuirii in mediile naturale. Diversitatea chimica si structurile neobisnuite ale metabolitilor secundari sunt ilustrate de numarul mare de clase carora le apartin: aminozaharuri, quinone, cumarine, epoxizi, alcaloizi ergot, glicozide, derivati indolici, lactone, macrolide, naftalene, nucleozide, peptide, poliacetilene, poliene, piroli, terpenoide, tetracicline etc.
Metabolitii secundari includ legaturi chimice neobisnuite: inele b-lactamice, peptide ciclice alcatuite din aminoacizi normali si modificati, legaturi nesaturate de poliacetilene si poliene, inelul macrolidelor.
Metabolitii secundari sunt produsi numai de unele specii ale unui gen, ca familii de compusi strans inruditi: cel putin 10 peniciline naturale, 10 bacitracine, 25 actinomicine etc. Proportia diferitelor componente in amestec depinde de factori genetici, de factorii de mediu si se datoreaza relativei lipse de specificitate a enzimelor implicate in metabolismul secundar. {n contrast, procesele de biosinteza ale metabolitilor primari sunt totdeauna catalizate de enzime cu specificitate inalta: enzima recunoaste un singur substrat si se formeaza un singur produs. Specificitatea actiunii enzimelor care catalizeaza sinteza metabolitilor primari se datoreaza faptului ca erorile de biosinteza ale componentelor celulare esentiale sunt, in general, letale, iar erorile care survin in metabolismul secundar nu au consecinte semnificative pentru celula producatoare, deoarece metabolitul secundar modificat isi pastreaza, de regula, activitatea biologica.
Metabolitii secundari se sintetizeaza pe o varietate mai mare de cai, decat cei primari. Desi au structuri chimice foarte diversificate si se sintetizeaza pe cai variate, metabolitii secundari se asambleaza dintr-un numar limitat de metaboliti intermediari.
Antibioticele sunt metaboliti secundari a caror sinteza incepe tarziu in timpul fazei de crestere, la intrarea in faza stationara. Experientele de autoradiografie cu aminoacizi marcati au evidentiat ca in perioada in care miceliul creste cu o rata inalta, aminoacizii se incorporeaza in proteinele celulare, dar nu se sintetizeaza actinomicina. Dupa ce microorganismul a incheiat faza de crestere, rata incorporarii aminoacizilor in proteine scade considerabil. Waksman (1961) a intuit ca proprietatea anumitor microorganisme de a sintetiza antibiotice nu este corelata cu nici un mecanism esential al nutritiei si cresterii celulei. {n general, sinteza metabolitilor secundari din categoria antibioticelor este supresata in timp ce celulele se gasesc in faza de multiplicare activa si este cea mai rapida dupa ce cultura intra in faza stationara. Comparativ cu metabolitii primari, antibioticele au specificitate redusa de biosinteza, deoarece acelasi organism sintetizeaza, de multe ori, un grup de molecule inrudite.
Cele doua faze, trofofaza si idiofaza, sunt bine separate la o cultura bacteriana producatoare de antibiotic, dar nu sunt clar delimitate pentru microorganismele filamentoase (actinomicete si fungi). Criteriul evaluarii cresterii masei celulare este determinarea greutatii uscate. {n numeroase procese de biosinteza industriala cu microorganisme filamentoase, greutatea uscata continua sa creasca semnificativ in idiofaza, dar cu o rata mai mica decat in trofofaza. Determinarea greutatii uscate nu este un criteriu optim pentru evaluarea cresterii. Masa celulara consta din totalitatea structurilor necesare diviziunii celulare (organitele celulare) si din materialele de rezerva (polioli, lipide, polifosfati si glucide nestructurale), care pot sa reprezinte 50-60% din greutatea uscata a celulei la sfarsitul procesului de biosinteza. Cresterea greutatii uscate in idiofaza este rezultatul acumularii substantelor de rezerva, o crestere cu caracter nereplicativ (nu este asociata cu diviziunea celulara),. De aceea, parametrul optim pentru masurarea cresterii masei replicative a celulei, este determinarea cantitativa a ADN. {n acest caz, cresterea celulei poate fi disociata de producerea de antibiotic. Sfarsitul fazei de crestere replicativa este marcat de alti parametrii: scaderea ratei activitatii respiratorii si scaderea ratei sintezei ARN.
Cele doua faze sunt bine delimitate in cazul fermentatiei antibioticelor (cloramfenicol, colistin, penicilina, bacitracina) in mediile organice complexe, care favorizeaza cresterea rapida a culturii discontinui*, dar se suprapun intr-un grad semnificativ, in mediile chimic definite (sintetice), care favorizeaza cresterea lenta.
Culturile bacteriene discontinui se obtin prin inocularea unui mediu nutritiv lichid sau solidificat, ce nu se reinoieste.
Factorul care controleaza declansarea biosintezei antibioticelor este deficienta unuia sau mai multor componente nutritionale care limiteaza cresterea. Epuizarea unui astfel de factor opreste cresterea si initiaza biosinteza idiolitilor. {n mediile definite chimic, favorizante ale cresterii lente, unul sau mai multi factori nutritionali pot fi limitanti ai cresterii chiar de la inceputul cultivarii, dar favorabili sintezei antibioticelor. Momentul sintezei produsului nu este un criteriu totdeauna valid pentru a defini metabolitul secundar.
Microorganismele par a fi programate sa produca antibiotice numai cand rata specifica de crestere scade sub un anumit nivel. Fenomenul s-a stabilizat in evolutie, ca raspuns la presiunile competitive. {n mediile bogate in substante nutritive, ca de exemplu intestinul mamiferelor, producerea antibioticelor nu este necesara, deoarece resursele satisfac necesitatile metabolice ale intregii asociatii. {n mediile naturale majore (sol, apa), nutrientii sunt totdeauna limitanti pentru cresterea diferitelor asociatii de microorganisme heterotrofe si sinteza antibioticelor devine avantajoasa pentru supravietuire.
Microorganismele evita efectul letal al antibioticelor pe care le produc (sinuciderea) prin urmatoarele mecanisme :
modificarea si detoxificarea antibioticelor de catre enzime sintetizate de organismele producatoare;
alterarea tintei antibioticului in celula producatoare;
scaderea permeabilitatii pe fata externa a membranei, dupa ce antibioticul a fost excretat.
Unele antibiotice au rol in dinamica proceselor de sporulare (de exemplu, polimixina, produsa de Bacillus polymyxa). Altele sunt produse secundare, rezultate din degradarea peretelui celular, corelata cu sporularea, deoarece peretele contine D-aminoacizi si glucide care se regasesc in compozitia chimica a unor antibiotice.
Producerea antibioticelor a evoluat ca un mecanism ecologic de inhibitie a cresterii altor microorganisme, cu care intra in competitie pentru resursele energetice. Fenomenul se numeste antibioza si are o semnificatie functionala opusa simbiozei. Dar microorganismele producatoare de antibiotice reprezinta o proportie foarte mica din totalul microorganismelor din sol. Faptul ca antibioticele se sintetizeaza la sfarsitul fazei de crestere, pare sa nu le confere un avantaj competitiv real.
Conditiile de mediu necesare sporularii si secretiei metabolitilor secundari sunt adeseori asemanatoare si chiar mai stringente decat acelea necesare cresterii vegetative. S-a crezut ca sinteza metabolitilor este obligatorie pentru sporulare, dar unele tulpini fungice sporuleaza chiar in absenta producerii metabolitilor secundari.
Cei mai multi metaboliti secundari sunt sintetizati de organisme cu crestere filamentoasa si cu morfologie relativ complexa.
Sinteza metabolitilor secundari, la microorganisme, este asociata cu procesele de sporulare. Se disting 4 categorii de metaboliti secundari a caror sinteza este declansata de procesul de sporulare:
metaboliti care activeaza sporularea (acidul linoleic, la Asp. nidulans);
pigmentii structurilor de sporulare (melaninele necesare formarii sau integritatii sporilor sexuati si asexuati). Melaninele sunt pigmenti de culoare inchisa care se formeaza prin polimerizarea oxidativa a compusilor fenolici, se sintetizeaza in timpul sporularii si sunt depozitati in peretele celular, avand rol protector fata de radiatiile UV, dar sunt si factori de virulenta;
metaboliti toxici secretati la timpul sporularii (micotoxinele);
antibiotice
Metabolitii secundari sunt substante neesentiale pentru organismul producator, carora li se atribuie urmatoarele activitati biologice:
inhibitia cresterii sau chiar efectul letal asupra altor organisme din mediu;
efecte toxice fata de organismele multicelulare (nevertebrate, plante) ;
stimuleaza diferentierea microorganismelor;
au rol in transportul ionilor metalici.
Metabolitii secundari au semnificatie adaptativa pentru microorganismele producatoare, deoarece sinteza lor este determinata genetic, iar pe de alta parte, multe clase de compusi prezinta o adaptare remarcabila de a interactiona cu tintele lor. Unii metaboliti au activitate biologica chiar la concentratiile mici produse in mediile naturale.
Antibioticele produse de Streptomyces se sintetizeaza in cantitati mici, in faza de tranzitie, cand cresterea miceliului vegetativ incetineste, ca rezultat al epuizarii nutrientilor si miceliul aerian este gata sa se dezvolte pe seama nutrientilor eliberati prin degradarea hifelor vegetative. Astfel de antibiotice ar avea rolul de a proteja organismul producator, de alte microorganisme care tind sa consume resursele nutritive din mediu.
Uneori, antibioticele produse de diferitele specii ale unui grup au actiune sinergica: de exemplu, antibioticele b-lactamice si acidul clavulanic (produs de Str. clavuligerus). Acidul clavulanic este un inhibitor natural al b-lactamazelor, care confera rezistenta la b-lactamice. Antibioticele b-lactamice si ale inhibitorilor b-lactamazei sunt eficiente fata de bacteriile rezistente la b-lactami. Efectul sinergic al asociatiei este reflectat de denumirea data combinatiei acidului clavulanic cu meticilina: augmentin.
Coproducerea cefamicinei (un antibiotic b-lactamic) si acidului clavulanic este constanta: nu exista prodcatori cunoscuti de acid clavulanic, care sa nu produca cefamicine (Challis, Hopwood, 2003).
Multe specii de Streptomyces produc doua sau mai multe antibiotice, cu actiune sinergica fata de un organism competitiv care domina numeric asociatia naturala. Astfel, Str. avermitilis sintetizeaza doi compusi antifungici cu structuri diferite: oligomicina si un macrolid polienic. Cele doua antibiotice au tinte moleculare distincte: oligomicina inhiba o sintaza mitocondriala, iar macrolidul polienic se leaga ireversibil de membrana celulelor fungice, alterand permeabilitatea lor. Oligomicina si macrolidele polienice pot actiona sinergic fata de fungi. Probabil ca un competitor fungic al lui Str. avermitilis, l-a selectat pe ultimul pentru sinteza acestor antibiotice.
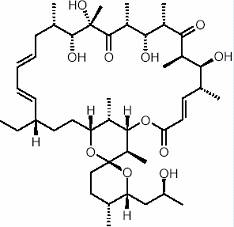
Oligomicina
Multe produse naturale de importanta medicala (antibiotice), alimentara, industriala sau agricola sunt metaboliti secundari.
Cresterea fungica si sinteza antibioticului sunt rezultatul interactiunii dintre miceliul fungic, substrat si conditiile de mediu. Sinteza este influentata de conditiile mediului de crestere al fungilor. Multe antibiotice sunt metaboliti secundari, produsi in conditii suboptimale de crestere sau in prezenta unor cantitati limitante de nutrienti. Temperatura, umiditatea, aeratia, pH-ul, rata de crestere influenteaza masa fungica si sinteza antibioticelor.
Sinteza proteinelor neribosomale*
Cele doua categorii de proteine - celulare si antibiotice polipeptidice - se sintetizeaza dupa mecanisme diferite. Dovezile experimentale au fost aduse utilizand inhibitori metabolici. De exemplu, cloramfenicolul si puromicina - inhibitori ai sintezei proteinelor celulare - stimuleaza incorporarea aminoacizilor in actinomicina. In abenta sintezei proteinelor celulare, rezerva de aminoacizi poate fi folosita exclusiv pentru sinteza antibioticelor.
Nu toate proteinele se sintetizeaza pe ribosomi. Unele polipeptide, cu mai putin de 50 de aminoacizi pot fi asamblate de peptid-sintetaze, ca si alti compusi, ca de exemplu acizii grasi, a caror sinteza este catalizata de alte sintetaze.
Produsele peptidice de sinteza neribosomala includ ciclosporina (cu actiune imunosupresoare) si antibiotice ca gramicidina S, tirocidina A si surfactinele. O structura modulara a peptid-sintetazelor determina alungirea secventiala a catenei peptidice, prin adausul de aminoacizi specifici.
Sinteza neribosomala a peptidelor are loc la procariote si la eucariotele inferioare si se bazeaza pe principiul matritei cu S (thiotemplate), catalizata de complexe enzimatice mari multifunctionale, denumite peptid-sintetaze, care sunt organizate in module (un modul de initiere a sintezei si mai multe module de alungire a catenei peptidice). Fiecare modul este alcatuit din mai multe domenii, care determina alungirea catenei polipeptidice prin adaugarea succesiva a aminoacizilor.
Modulele au un model comun de organizare care le permite activarea aminoacidului fixat si realizarea unei legaturi peptidice, ca si modificarea aminoacidului fixat prin reactii de epimerizare sau N-metilare.
S-a demonstrat experimental ca un modul de alungire trebuie sa posede cel putin 4 domenii:
un domeniu de adenilare (A) cu activitate de peptid-sintetaza care fixeaza aminoacidul si il activeaza printr-o reactie de adenilare;
un domeniu de tioesterificare (T sau PCP-peptidyl carrier protein) care mentine peptidul nascent asociat cu sintetaza, pe intreaga durata a sintezei prin intermediul unei legaturi tioesterice;
un domeniu de condensare (C) prin care sintetaza catalizeaza formarea legaturilor peptidice;
un domeniu specific (Te) cu activitate de tioesteraza care permite eliberarea peptidului de complexul sintetazei, dupa terminarea sintezei.
Spre deosebire de calea de sinteza proteica clasica (ribosomala) care utilizeaza doar 21 de aminoacizi (20 esentiali si selenocisteina), sinteza non-ribosomala poate utiliza peste 300 de aminoacizi (de exemplu, D-aminoacizi, aminoacizi N-metilati etc.), insa peptidele sintetizate nu pot depasi 48 de aminoacizi.
Peptid-sintetazele, ca si alte complexe enzimatice (de exemplu, poliketid-sintetazele) sunt interesante datorita posibilitatii utilizarii lor in biosinteza produselor nenaturale.
Majoritatea peptidelor neribosomale sintetizate de microorganisme sunt clasificate ca metaboliti secundari, adica rareori au rol in metabolismul primar, in crestere sau in reproducere, dar sinteza lor a evoluat cu un oarecare beneficiu pentru organismul producator.
Din punct de vedere chimic, antibioticele sunt un grup de substante foarte heterogene. Se disting urmatoarele categorii:
l. Antibioticele b-lactamice constituie unul dintre cele mai mari si importante grupe de antibiotice. Toate cuprind in structura lor, inelul β-lactamic si sunt foarte diverse: penicilinele, cefalosporinele si cefamicinele.
Penicilina este produsa de Penicillium chrysogenum. Molecula nativa (benzil-peniclina sau peniclina G) este alcatuita din inelul β-lactamic si inelul tiazolidinic. La C6 este atasat grupul fenil-acetamido.
La cefalosporine, inelul tiazolidinic are un atom de C suplimentar, cu o legatura nesaturata intre C3 si C4 si rezulta o structura denumita cefem.
Cefamicinele sunt similare ca structura chimica, dar inelul β-lactamic contine un grup metoxi, care-i confera stabilitate la multe enzime β-lactamazice.
Alte variante structurale ale compusilor β-lactamici utilizati in clinica sunt: carbapenem, carbacefem, oxacefem, clavam (acid clavulanic), sulfone, monobactam.
Penicilinele semisintetice se obtin din acidul 6-aminopenicilanic, care se condenseaza cu orice acid carboxilic. Rezulta astfel un numar mare de peniciline: oxacilina si derivatii sai, meticilina, ampicilina, amoxicilina, azlocilina, mezlocilina, piperacilina, ticarcilina.
Acidul 6-aminopenicilanic, pentru penicilinele semisintetice, se obtine prin tratamentul penicilinei cu o amidaza sau prin cultivarea organismului producator, intr-un mediu fara donorul gruparii acil.
Acidul 6-aminopenicilanic este un dipeptid ciclic, format prin condensarea L-cisteinei si D-valinei si de aceea penicilinele, cefalosporina si cloramfenicolul apartin grupului antibioticelor oligopeptidice.
Cloramfenicolul este un antibiotic simplu, sintetizat de Streptomyces, dar in cea mai mare parte se obtine prin sinteza chimica. Are un spectru larg de actiune: bacteriile Gram pozitive si Gram negative, dar si bacteriile parazite obligat intracelulare (chlamidii, rickettsii).
Cloramfenicolul contine o grupare nitro si un grup diclor-acetil. El se leaga de subunitatea ribosomala mare si blocheaza transferul peptidil, la ribosomii care alungesc catena.
2. Antibiotice polipeptidice: bacitracina (produsa de B. subtilis), gramicidina (sintetizata de B. brevis), cicloserina (produsa de Streptomyces), actinomicina, polimixina (sintetizata de B. polymyxa).
Bacitracina este un peptid ciclic ce impiedica defosforilarea purtatorului lipidic ce transfera noul peptidoglican, prin membrana celulei, in timpul sintezei peretelui celular. Bacitracina deriva dintr-o proteina a celulei vegetative, care este degradata partial in timpul sporularii. Este toxica pentru a fi aplicata sistemic, dar se gaseste in formulari pentru aplicatii locale.
Polimixinele sunt o familie de antibiotice produse de specii de Bacillus. O parte a polipeptidului are o configuratie ciclica, cu o "coada" hidrofoba de acid octanoic. In clinica se folosesc polimixina B si polimixina E (colistina), precum si derivatii lor sulfometilati. Polimixinele sulfometilate au activitate antibacteriana redusa, dar se cliveaza spontan si rezulta compusi mai activi.
Tyrocidina si gramicidina S sunt polipeptide ciclice. Ele produc dezorganizarea membranei, rezultatul fiind pierderea moleculelor mici si liza protoplastilor. Nu se folosesc pentru administrare sistemica, deoarece sunt toxice.
3. Antibioticele aminoglicozidice a caror denumire se termina cu "mycin" deriva direct sau indirect de la Streptomyces, iar cele care se termina cu "micin" deriva de la Micromonospora. Toate aminoglicozidele au un inel format din 6 unitati, cu grupari amino si de aici deriva denumirea de aminociclitol. Molecula lor polara, policationica, contine un aminociclitol, de care se leaga doua sau mai multe glucide, dintre care cel putin unul este aminat. La streptomicina, aminociclitolul este diguanidin-inozitolul (streptidina).
Majoritatea aminoglicozidelor au grupul aminociclitol reprezentat de deoxistreptamina. Ele se impart in derivati ai neomicinei, kanamicinei, gentamicinei.
Aminoglicozidele sunt active fata de numeroase bacterii infectioase Gram pozitive si Gram negative, dar si fata de M. tuberculosis. Legarea unei singure molecule este suficienta pentru inactivarea ribosomului bacterian. Aceste antibiotice nu traverseaza usor membranele celulare. Se absorb cu dificultate din intestin, dar pentru modificarea microbiotei intestinale, administrarea orala este calea optima. Sunt ineficiente fata de bacteriile cu localizare intracelulara. Anaerobia si prezenta cationilor bivalenti diminua eficienta aminoglicozidelor. Se administreaza numai in cazul infectiilor severe (tuberculoza, bruceloza, tularemie, plaga bubonica). Sunt sinergice cu antibioticele beta-lactamice si se folosesc in septicemiile cu bacterii Gram negative. Pentru a-si exercita efectul bactericid, aminoglicozidele necesita sinteza proteica.
4. Antibioticele polichetide (acetogenine) sunt substante naturale derivate din acizi poli-β-cetonici, care la randul lor se formeaza din acetil-CoA si mai multe molecule de malonil-CoA, dupa decarboxilare: griseofulvina (produsa de Penicillium patulum), tetraciclina (sintetizata de Streptomyces).
Tetraciclinele sunt un grup de substante naturale sau de semisinteza, a caror formula cuprinde un nucleu tetraciclic linear fuzionat, de care se ataseaza o varietate de grupari functionale: clor-tetraciclina (produsa de Streptomyces aureofaciens), oxitetraciclina (produsa de S. rimosus).
Tetraciclinele sunt agenti chelatori puternici si proprietatile lor farmacochinetice sunt influentate de chelarea ionilor de metal. Sunt cel mai important grup de antibiotice, datorita spectrului antibacterian foarte larg. Sunt active fata de bacteriile Gram pozitive si Gram negative, fata de protozoarele parazite (Entamoeba), fata de chlamidii, micoplasme si ricketsii. Actioneaza prin inhibitia sintezei proteinelor, deoarece inhiba atasarea aminoacil-ARNt la situsul acceptor ribosomal. Sunt larg utilizate in terapia antiinfectioasa umana si animala, deoarece nu produc colaterale majore. Se adauga ca supliment in furaje in doze subterapeutice, pentru stimularea cresterii.
5. Antibioticele macrolide
Denumirea de "macrolid" desemneaza o structura chimica caracterizata prin prezenta unui ciclu lactonic cu complexitate variabila, la care se ataseaza componenta glucidica. Ciclul lactonic rezulta prin inchiderea unui lant lung de acizi grasi hidroxilati. Antibioticele macrolide sunt foarte diverse, datorita atat variatiei inelului macrolidic, cat si a complexului glucidic. Cele mai cunoscute sunt eritromicina si oleandomicina.
6. Antibioticele steroidice au o structura chimica asemanatoare colesterolului. Acidul fusidic (fusidina) este produs de fungii filamentosi din g. Fusarium. Este activ prin legarea de factorul de elongatie G (EFG).
7. Antibioticele polienice se caracterizeaza prin prezenta, in molecula lor, a unui anumit numar de legaturi duble: nistatina, amfotericina B, candicidina (produse de membri ai g. Streptomyces), iar fumigalina este sintetizata de Aspergillus fumigatus.
8. Antibiotice glicopeptidice
In clinica se folosesc doua glicopeptide: vancomicina si teicoplanina. Vancomicina este o molecula mare, complexa, produsa de Streptomyces orientalis. Utilizarea ei este limitata, datorita toxicitatii asupra rinichiului.
Vancomicina este un heptapeptid rezultat din aminoacizi aromatici modificati si condensati intr-o structura triciclica, de care se ataseaza un dizaharid. Activitatea sa antimicrobiana se datoreaza legarii la catenele laterale de D-alanil-D-alanil ale peptidoglicanului, blocand formarea legaturilor incrucisate ale catenei polipeptidice si este limitata, in esenta, la bacteriile Gram pozitive, deoarece, la bacteriile Gram negative mureina acoperita de membrana externa, nu este accesibila antibioticelor glicopeptidice.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 2691
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved