| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Derivati functionali ai acizilor carboxilici
Provin prin modificarea grupei OH sau inlocuirea oxigenului carbonilic, ambele din structura grupei carboxilice. Rezulta derivati functionali care au proprietatea comuna ca prin hidroliza genereaza acidul din care au provenit.
1. Halogenuri ale acizilor carboxilici
Se formeaza prin inlocuirea grupei -OH din -COOH cu un atom de halogen. Acesti compusi sunt denumiti halogenuri de acil. Atomul de halogen din acesti compusi este foarte reactiv si poate fi substituit cu alti atomi sau grupe de atomi. Este motivul pentru care halogenurile acizilor carboxilici sunt utilizate ca agenti de acilare.
2. Anhidride ale acizilor carboxilici
Pot fi considerate derivati functionali rezultati prin eliminarea unei molecule de apa intre doua grupe carboxil. Cu alcoolii, fenolii si aminele reactioneaza mai putin energic decat clorurile acide. De asemenea se hidrolizeaza mai greu decat clorurile acide dar mai usor decat esterii.
Anhidridele sunt folosite drept agenti de acilare precum si in industria de medicamente.
Sunt derivati functionali rezultati prin inlocuirea grupei -OH din grupa -COOH cu grupa aminica. Atomii din grupa amidica pot fi inlocuiti cu radicali organici dand nastere amidelor substituite. Acestea, dupa numarul de substituenti de la atomul de azot, pot fi primare, secundare si tertiare.
Reactivitatea amidelor este legata de conjugarea electronilor p neparticipanti de la atomul de azot cu electronii ai dublei legaturi C=O. Ca urmare, reactia de hidroliza se petrece mai greu decat in cazul halogenurilor acide si numai in mediu acid sau bazic.
Amidele secundare ciclice se numesc imide.
4. Esteri
Sunt derivati functionali ai acizilor carboxilici in care gruparea -OH din -COOH este inlocuita cu o grupa alcoxil prin esterificare directa. Proprietatile esterilor depind de natura acidului si alcoolului din care provin.
Esterii acizilor inferiori sunt lichide cu miros placut de fructe sau flori. Sunt insolubili in apa si solubili in solventi organici. Moleculele esterilor nu sunt asociate prin legaturi de H si de aceea constantele fizice au valori mai mici decat ale acizilor din care provin.
Esterii participa la reactii de substitutie prin care se inlocuieste grupa alcoxil cu alte grupe functionale. Hidroliza esterilor are loc prin actiunea catalitica a acizilor sau bazelor. Hidroliza acida este o reactie reversibila care conduce la un acid si un alcool. Hidroliza bazica este o reactie ireversibila care conduce la saruri ale acizilor carboxilici si alcooli. Reactia se desfasoara cu viteza superioara hidrolizei acide. Reactia cu amoniacul conduce la amide iar reactia cu aminele conduce la amide substituite la atomul de azot
Lipidele constituie o grupa de substante bioorganice larg raspandite in organismele vii, unde au rol energetic, rol de substante de rezerva, rol plastic precum si rol de material izolant. Din punct de vedere structural, lipidele se clasifica in lipide simple (ceride, acilgliceroli, steride) si lipide complexe (fosfolipide, sfingolipide, glicolipide).
Ceridele sunt esteri ai acizilor grasi superiori (C14 - C34) cu alcooli monohidroxilici superiori si numar par de atomi de carbon. In natura, ceridele apar in amestec cu alcooli primar, acizi grasi liberi, rasini, gliceride, steride , amestecuri care poarta numele de ceruri.
Acilglicerolii, cele mai raspandite lipide in tesuturile plantelor (uleiuri) si animalelor (grasimi), sunt esteri ai acizilor grasi monocarboxilici saturati sau nesaturati cu numar par de atomi de carbon si catena normala cu glicerina. Intrucat glicerina este un alcool trihidroxilic, dupa gradul de acilare al grupelor OH se deosebesc monoacilgliceroli, diacilgliceroli si triacilgliceroli.
Ca esteri, acilglicerolii pot fi hidrolizati prin fierbere cu acizi sau baze. Hidroliza acilglicerolilor sub actiunea hidroxizilor alcalini se numeste saponificare. Ionii carboxilati eliberati in urma acestei reactii formeaza cu cationii sarurile corespunzatoare numite sapunuri. Cantitatea in mg de hidroxid de sodiu sau de potasiu necesara pentru saponificarea unui gram de triacilglicerol se numeste indice de saponificare.
Deosebit de importante sunt reactiile de aditie la dublele legaturi din moleculele acilglicerolilor. Prin hidrogenare, uleiurile vegetale se solidifica, proces folosit la prepararea margarinei. Cantitatea de I2 sau Br2, in grame, aditionata la dublele legaturi ale acizilor grasi din 100g acilglicerol se numeste indice de iod.
Sub actiunea oxigenului, umiditatii si luminii acilglicerolii naturali capata miros neplacut si gust iute. Procesul se numeste rincezire si are consecinte nedorite in industria alimentara. In conditii de umiditate lipazele naturale determina hidroliza partiala a acilglicerolilor conducand la eliberarea de acizi grasi care confera un gust specific. Acestia, sub actiunea oxigenului, se oxideaza la nivelul legaturilor duble rezultand peroxizi toxici care se pot scinda prin ruperea catenei hidrocarbonate rezultand compusi carbonilici ce confera produsului miros si gust neplacut.
Steridele sunt esteri ai acizilor grasi superiori cu alcooli tetraciclici monohidroxilici numiti steroli a caror unitate structurala de baza este steranul. Sterolii sunt raspanditi in tesuturile animale (zoosteroli), plante (fitosteroli) si ciuperci (micosteroli).
Lipidele complexe contin in molecula lor, pe langa componenta lipidica si o componenta de alta natura.
Fosfolipidele (fosfatide) sunt lipide complexe in care una din gruparile hidroxil primare ale glicerolului este esterificata cu acid fosforic.
Sfingolipidele sunt lipide complexe care contin in molecula sfingozina, un aminoalcool dihidroxilic nesaturat.
Glicolipidele sunt lipide complexe care contin in molecula, pe langa componenta lipidica si o componenta glucidica.
5. Acizi fenolici
Contin in molecula gruparile -OH si -COOH legate de un nucleu aromatic direct sau prin intermediul unei catene.
Acizii fenolici au proprietati ale acizilor carboxilici si fenolilor. Cand cele doua grupe sunt in pozitie orto se manifesta efectul inductiv negativ (-Is) al grupei -OH care conduce la formarea unei structuri inchise numite chelat. Aceasta structura influenteaza mobilitatea ionilor H+ care se desprind mai usor decat in cazul acidului benzoic.
6. Acizi carbonilici
Contin in molecula grupele -COOH si carbonil. In functie de tipul grupei carbonil acizii carbonilici pot fi acizi aldehidici sau acizi cetonici. Pozitia grupelor carbonil fata de grupa carboxil se noteaza cu litere ale alfabetului grecesc.
7. Aminoacizi
Sunt compusi organici care contin in molecula una sau mai multe grupe aminice precum si una sau mai multe grupe carboxil. Dupa natura radicalului de care se leaga grupele functionale aminoacizii sunt alifatici, aromatici si heterociclici. Dupa pozitia reciproca a celor doua grupe functionale aminoacizii pot fi α, β, γ, δ-aminoacizi.
Denumirea aminoacizilor se face: pozitia grupei aminice fata de gruparea COOH indicata prin litere grecesti la care se adauga numele acidului
Cu exceptia glicocolului care nu are in molecula atom de carbon asimetric, toti ceilalti aminoacizi au si ca urmare prezinta activitate optica. Izomerii optici sunt D, si L putand exista si sub forma de racemic. S-a constatat ca din cei 20 aminoacizi naturali cu raspandire universala care intra in structura proteinelor si care sunt metabolizati in organisme vii fac parte din seria L (numarul aminoacizilor este mai mare unii dintre ei gasindu-se rar in unele proteine sau liberi in plante)
Datorita prezentei in molecula a functiunilor acida si bazica, aminoacizii exista in solutie apoasa sub forma de ioni bipolari:
![]()
In mediu acid aminoacizii se comporta ca baze (accepta H+) iar in mediu bazic, ca acizi (cedeaza H+). Datorita acestei proprietati aminoacizii migreaza in camp electric. Daca in solutia unui aminoacid se adauga o mica cantitate de acid sau baza, aceasta va fi neutralizata fara a se modifica apreciabil pH-ul. Pe aceasta proprietate se bazeaza functia tampon a aminoacizilor in organismele vii.
Proprietatile aminoacizilor se datoreaza prezentei grupelor -NH2 sau -COOH precum si prezentei lor simultane.
Aminoacizii reactioneaza cu hidroxizii alcalini formand saruri:
![]()
Aminoacizii reactioneaza cu alcoolii, in cataliza acida, formand esteri:
![]()
Aminoacizii reactioneaza cu PCl5 rezultand cloruri acide, stabile sub forma de clorhidrati:
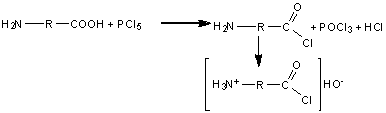
Decarboxilarea aminoacizilor conduce la obtinerea de amine fiziologic active. In organismele vii reactia se desfasoara enzimatic:
![]()
Reducerea aminoacizilor conduce la aminoalcooli
![]()
In prezenta amoniacului, aminoacizii conduc la formarea amidelor. Spre exemplu acidul -aminosuccinic (acid aspartic) in reactie cu amoniacul conduce la obtinerea amidei acidului aspartic, asparagina:
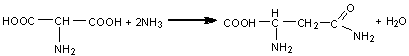
Reactia este foarte importanta pentru ca regleaza continutul de amoniac din organismele vegetale deoarece o concentratie prea mare de amoniac este toxica pentru plante. Prin formarea amidelor, plantele blocheaza amoniacul in exces care in caz de nevoie este eliberat prin reactia inversa.
Proprietati datorate prezentei grupei -NH2
Aminoacizii reactioneaza cu acizi minerali conducand la formarea de saruri.
Alchilarea aminoacizilor la gruparea aminica se realizeaza cu iodura sau sulfit de metil, in mediu alcalin, rezultand saruri cuaternare de amoniu numite betaine. Reprezentantul clasei este derivatul trimetilat al glicocolului, betaina propriu-zisa care se gaseste in sfecla de zahar:
![]()
Acilarea grupelor aminice se realizeaza cu cloruri acide sau anhidride rezultand aminoacizi acilati. De exemplu, glicocolul se acileaza cu clorura de benzil rezultand benzilglicocol:
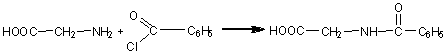
Daca reactia este condusa in prezenta clorurii unui aminoacid rezulta peptide
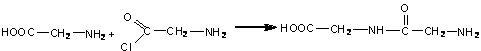
Reactia cu acidul azotos se petrece in mediu acid si determina dezaminarea aminoacidului conducand la hidroxiacizii corespunzatori cu degajare de azot. De exemplu, alanina se dezamineaza in prezenta acidului azotos rezultand acid lactic:
![]()
Reactia de transaminare se desfasoara intre un cetoacid si un aminoacid rezultand aminoacidul cetoacidului si cetoacidul aminoacidului. In organismul viu aceste reactii se petrec sub actiunea transaminazelor cand are loc transferul unei gruparii -NH2 de la un aminoacid la un cetoacid rezultand un nou aminoacid si un nou cetoacid:
Dezaminarea aminoacizilor se realizeaza oxidativ, hidrolitic sau reductiv, reactia fiind importanta in metabolismul organismelor vii.. Dezaminarea oxidativa conduce la α-aminoacizi:
![]()
Dezaminarea hidrolitica conduce la -hidroxiacizi:
![]()
Dezaminarea reductiva conduce la acizi carboxilici:
![]()
Proprietati determinate de prezenta simultana a celor doua grupe functionale
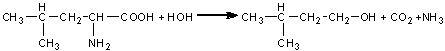
Reactia de dezaminare si decarboxilare are loc la obtinerea alcoolilor prin procese de fermentatie alcoolica ale cerealelor sau cartofilor sub actiunea enzimelor din drojdia de bere. Spre exemplu leucina din cartof prin fermentatie alcoolica conduce la alcool izoamilic:
Aminoacizii formeaza cu metalele grele (Ni, Pb, Cu) saruri complexe frumos colorate, proprietate utilizata in chimia analitica pentru identificarea cationilor respectivi.
Aminoacizii participa la reactii de condensare cu eliminare de apa intre grupele -NH2 si -COOH, rezultand peptide sau proteine, in functie de numarul de aminoacizi care participa la reactie. Legatura dintre aminoacizi se numeste legatura amidica sau peptidica. De exemplu, glicina si alanina se condenseaza formind o trpeptida numita glicil-alanil-glicina:
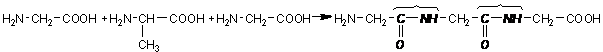
Aminoacizii se impart in mai multe grupe:
Aminoacizi monoamino monocarboxilici (acid -aminoacetic sau glicocol sau glicina; acid -aminopropionic sau -alanina; acid -aminoizovalerianic sau valina; acid -aminoizocapronic sau leucina);
Aminoacizi hidroxilati (acid -amino- -hidroxipropionic sau serina; acid -amino- -hidroxibutiric sau treonina);
Aminoacizi tiolici contin grupa tiolica (SH) sau tiolica substituita (acid -amino- -tiol propionic sau cisteina; acid -amino- -metil-tiobutiric sau metionina);
Aminoacizi monoamino dicarboxilici (acid -amino-succinic sau acid aspartic; acid -amino-glutaric sau acid glutamic);
Aminoacizi diamino monocarboxilici (acid -diaminovalerianic sau ornitina; acid -diamino-capronic sau lizina; acid -amino- -guanidin-valerianic sau arginina; acid -amino- -carbamid (ureid)-valerianic sau citrulina);
Aminoacizi aromatici (acid -amino, -fenil propionic sau fenilalanina; p-hidroxifenilalanina sau tirozina);
Aminoacizi heterociclici (acid -amino, -indol propionic sau triptofan; acid -amino, -imidazol propionic sau histidina.
8. Peptide
Sunt combinatii organice care pot fi considerate ca amide substituite ce rezulta prin eliminarea de apa intre doi sau mai multi aminoacizi (intre o grupa carboxil a unui aminoacid si o grupa amino a altuia). Resturile de aminoacizi din peptide sunt legate covalent prin legaturi peptidice:
![]()
Datele experimentale indica faptul ca legatura peptidica -CO-NH- constituie un sistem simplu conjugat, in care conjugarea se realizeaza intre perechea de electroni π a gruparii carbonilice si perechea de electroni neparticipanti de la atomul de N vecin. In urma delocalizarii electronilor, legatura peptidica manifesta un caracter pronuntat de legatura dubla.
Peptidele cu un numar mai mic de 10-20 resturi de aminoacizi in molecula sunt denumite oligopeptide. Peptidele cu numar mai mare de resturi de aminoacizi in molecula sunt numite polipeptide. Polipeptidele a caror secventa specifica este mai mare de 50 reziduuri sunt numite in mod obisnuit proteine dar cercetatorii au pareri diferite legate de numarul de reziduuri de aminoacizi de la care se foloseste acest termen. Cand doi sau mai multi aminoacizi se combina pentru a forma peptide, ceea ce ramane din fiecare aminoacid dupa indepartarea apei este denumit reziduu al aminoacidului. Reziduul care are o grupa amino libera se numeste N-terminal iar cel care are o grupare carboxil libera se numeste C-terminal. Reziduurile se denumesc dupa numele aminoacidului eliminandu-se cuvantul acid.
Pentru a denumi peptidele se incepe cu numele grupei acil reprezentand reziduul N-terminal urmat, in ordine, de numele grupelor acil reprezentand reziduurile interne. Numai reziduul C-terminal este denumit cu numele aminoacidului de la care provine si acesta reprezinta sfarsitul numelui peptidei.
Proteinele si acizii nucleici sunt cei mai importanti componenti chimici ai materiei vii. Proteinele indeplinesc multe functii importante in organismul viu:
rol structural impreuna cu lipidele si glucidele (reprezinta suportul chimic structural al tuturor formatiunilor morfologice evidentiate in celulele si organele plantelor, animalelor si microorganismelor);
rol de catalizatori ai reactiilor chimice in sistemele biologice (aceste proteine se numesc enzime);
rol in contractia musculara (actina si miozina din muschi);
rol de transport activ a unor substante micromoleculare si al ionilor anorganici;
rol de aparare a organismului, impotriva substantelor straine si celulelor provenite din alte organisme (sub forma de anticorpi; aceasta reactie de aparare a organismului viu se numeste imunitate - imunoglobuline);
rol hormonal participand la reglarea proceselor biochimice (unele proteine sau polipeptide pot actiona ca hormoni).
Proteinele se caracterizeaza prin patru nivele de organizare structurala care indica:
structura primara - numarul, natura si succesiunea resturilor de aminoacizi;
structura secundara - orientarea spatiala a catenei polipeptidice ( variante ale structurii secundare sunt structura α-helicoidala) si structura β-pliata);
structura tertiara - replierea si infasurarea segmentelor α-helicoidale si β-pliate intr-o organizare spatiala complexa sub forma de ghem sau globula;
structura cuaternara - nivelul de organizare structurala cel mai inalt, rezultat al asocierii a doua sau mai multe catene polipeptidice numite protomeri, fiecare cu structura sa primara, secundara si tertiara intr-un conglomerat spatial complex.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 6486
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2026 . All rights reserved