| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
HIDROCARBURI
Hidrocarburile sunt compusi organici in compozitia carora apar numai atomi de carbon si hidrogen.
Se cunosc azi peste 30.000 de hidrocarburi clasificate in mai multe clase, dupa principalele lor caracteristici (tabelul nr.1).
Tabelul nr.1
Clasificarea hidrocarburilor
|
Forma catenei |
Hibridizare la atom C |
Tipul de hidrocarburi |
Clasa de hidrocarburi |
|
liniara ramificata ciclica |
sp3 sp3 sp3 |
saturate saturate saturate |
alcalini izoalcalini cicloalcalini |
|
liniara liniara |
sp3 si sp2 sp3 si sp2 |
nesaturate nesaturate |
alchene alcadiene |
|
liniara |
sp3 si sp |
nesaturate |
alchine |
|
ciclica |
sp2 |
aromatice |
arene |
Hidrocarburile sunt combinatii de baza ; de la ele deriva toate clasele de compusi organici in mlecula carora, in locul unuia sau mai multor atomi de hidrogen, apar atomi sau grupari de atomi care contin si celelalte elemente organogene.
1.1. ALCANI
1.1.1. Definitie, nomenclatura, omologie. Se numesc alcani (parafine) hidrocarburile in care nu apar decat legaturi simple de tipul C-C si C-H si la care raportul numeric dintre cele doua tipuri de atomi care este exprimat prin formula :
CnH2n+2
in care n reprezinta numarul atomilor de carbon din molecula.
Alcanii sunt hidrocarburi saturate aciclice . Aceste hidrocarburi sunt saturate pentru ca datorita raportului numeric de mai sus, au un continut maxim posibil de atomi de hidrogen ; se numesc aciclice fiindca au catene de carbon deschise (liniare si ramificate).
Daca se inlocuieste in formula de mai sus n cu valori intregi si succesive (sirul natural al numerelor) vor rezulta formule moleculare corespunzatoare, fiecare in parte, cate unui alcan. Numele acestuia se va exprima dupa urmatoarea regula : la numeralul care arata numarul de atomi de caron din molecula, exprimat in limba graca, se adauga surfixul an exceptie facand primii patru termeni, care au denumiri specifice.
n = 1 CH4 metan CH4
n = 2 C2H6 etan CH3-CH3
n = 3 C3H8 propan CH3-CH2-CH3
n = 4 C4H10 butan CH3-CH2-CH2-CH3
n = 5 C5H12 pentan CH3-(CH2)3-CH3
n = 6 C6H14 hexan CH3-(CH2)4-CH3
n = 7 C7H16 heptan CH3-(CH2)5 -CH3
n = 8 C8H18 octan CH3-(CH2)6-CH3
n = 9 C9H20 nonan CH3-(CH2)7-CH3
n = 10 C10H22 decan CH3-(CH2)8-CH3
n = 11 C11H24 undecan CH3-(CH2)9-CH3
n = 12 C12H26 dodecan CH3-(CH2)10-CH3
: :
: :
n = 20 C20H42 eicosan CH3-(CH2)18-CH3
Toti alcanii de mai sus au catene liniare. La alcanii cu patru sau mai multi atomi de carbon in molecula poate aparea insa ramificarea lantului ; de aceea in denumirea alcanilor trebuie specificata si natura lantului. Acest lucru se realizeaza prin adaugarea la numele alcanului a prefixului normal pentru cei cu lantul liniar si izo pentru cei cu lantul ramificat.
Cicloalcanii (cicloparafine). Sund hiodrocarburi ciclice saturate care contin o catena de carbon inchisa sau ciclica si au formula generala CnH2n. Cateva exemple de cicloalcalini sunt :
CH2 CH2
![]()
![]()
![]() H2C CH2 H2C CH2 H2C CH2
H2C CH2 H2C CH2 H2C CH2
H2C CH2 H2C CH2
ciclopropan ciclobutan ciclopentan
Se observa ca fiecare termen al seriilor de alcani si cicloalcani prezentate mai inainte se deosebeste de vecinii sai imediati printr-o grupare metilen (-CH2-).
O astfel de serie se numeste serie omoloaga, iar membrii seriei sunt considerati omologi unul in raport cu celalalt. Deoarece intr-o serie omoloaga se conserva particularitatile structurale, temenii respectivi au prioritati asemanatoare.
1.1.2. Radicali. Daca din molecula unui alcan se indeparteaza un atom de hidrogen rezulta un rest de hidrocarbura cu o valenta nesatisfacuta la un atom de carbon. Aceasta poarta numele de radical hidrocarbonat alcanic, sau mai obisnuit radical alchil.
Numele radicalilor alchil cu o singura valenta libera (radicali monovalenti) se formeaza din numele hidrocarburii respective in care se inlocuieste surfixul an cu il. Surfixul ilen este folosit pentru radicalii divalenti, surfixul in pentru cei trivalenti, etc. Exemple :
CH4 CH3- -CH2- -CH
metan metil metilen metin
CH3-CH3 CH3-CH2- -CH2-CH2-
etan etil etilen
CH3-CH2-CH3 CH3-CH2-CH2- CH3-CH-CH3
propan propil izopropil
Din punct de vedere electronic un radical este o molecula care poarta la unul din atomii sai, in acest caz la carbon, un numar impar de electroni, deoarece unul din orbitali este ocupat de un singur electron.
Trebuie precizat ca radicalii alchil nu pot exista in stare libera ca substante stabile ; ei apar in anumite reactii chimice in care se si consuma, transformandu-se in substante stabile, cu toate valentele satisfacute. (Se cunosc si radicali liberi , cu o anumita durata de viata masurabila, dar cu structuri mult mai complicate decat ale radicalilor alchil.)
1.1.3. Izomerie. Atomii din metan, etan si propan nu se pot aranja decat in cate un anumit mod, adica :
H H H H H H
H - C - H H - C - C - H H - C - C - C - H Formule structurale desfasurate
H H H H H H
CH4 CH3-CH3 CH3-CH2-CH3 Formule structurale restranse
metan etan propan
Pentru butan exista doua posibilitati de aranjare a catenei :
CH3
CH3-CH2-CH2-CH3 H 3C - C - CH3
H
normal butan izobutan
p.f. = 0,50C p.f. = 11,70C
Cei doi termeni au aceeasi formula moleculara C4H10 dar structuri diferite, deci si proprietati diferite. Acesti doi compusi sunt izomeri. Pentru ca un acest caz izomeria se datoreste ramificarii catenei, ea poarta numele de izomerie de catena.
In continuare, in seria alcanilor, inmultirea numarului de atomi de carbon aduce dupa sine inmultirea numarului de izomeri de catena (de exemplu C6H14 are cinci izomeri, C10H22 are 75 izomeri, C20H42 are 366319 izomeri).
Pentru a nu se creea confuzii de nomenclatura, toti izomerii de catena ai alcanilor (izoalcanii) se denumesc dupa urmatoarea regula :
Se stabileste cea mai lunga catena liniara, se numeroteaza de la un capat la altul atomii de carbon, in asa fel incat catena laterala sa ocupe pozitia cu numrul cel mai mic, se denumesc ca radicali catenele laterale (ramificarile), se indica pozitia lor prin cifre si la sfarsit se adauga numele alcanului cu catena liniara stabilita.Cum se va denumi, de exemplu, izolcanul cu urmatoarea formula :
CH3 - CH - CH2 - CH2 - CH3
CH3
se numeste: 2-metil-pentan (si nu 4-metil-pentan). In cazul alcanilor cu mai multe ramificari numerotarea catenei de baza trebuie sa se faca astfel incat suma indicilor care arata pozitia ramificarilor sa fie minima. Citirea radicalilor se face in ordine alfabetica : astfel etilul va fi mentionat inaintea metilului. Prezenta mai multor radicali identici se indica prin prefixe : di, tri, etc. Care este, de pilda, denumirea corecta a izoalcanului cu formula :
CH3
CH3 - CH2 - CH - CH2 - C - CH3
CH2 CH3
CH3
Catena liniara cea mai lunga este cea alcatuita din sase atomi de carbon; deci baza denumirii o va constitui numele alcanului corespunzator - hexanul. Numerotarea atomilor de carbon se poate face inca in doua moduri si anume :
- C - - C -
- C1 C2 - C3 - C4 - C5 - C6 - - C6 C5 - C4 - C3 - C2 - C1 -
- C - - C - - C - - C -
- C - - C -
Pe baza regulei generale, substanta de mai sus poate fi denumita astfel :
3-etil-5,5-dimetil hexan sau 4-etil-2,2-dimetil hexan
Dintre cele doua denumiri posibile, este corecta ultima, suma indiciilor de pozitie (2+2+4=8) fiind mai mica decat in primul caz (5+5+3=13).
1.1.4. Structura. In molecula alcanilor toti atomii de carbon au starea de hibridizare sp3. In aceasta stare unghiurile dintre valentele atomului de carbon sunt de 109028' ; ele sunt orientate in spatiu dupa directiile celor patru varfuri ale unui tetraedu regulat. Modelele spatiale ale primilor doi termeni ai seriei alcanilor sunt redate in figura 9.
![]()
![]()
![]()
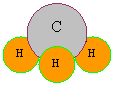
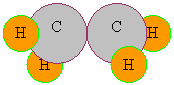
Pentru a reprezenta grafic structura alcanilor se folosesc cel mai des formule plane obisnuite (desfacute sau restranse, ca cele din pagina 22), renuntandu-se la formulele spatiale, dar subintelegandu-le.
Datorita orientarii tetraedice, in hidrocarburile cu doi si mai multi atomi de carbon, legatura C-C permite rotatia libera a celor doua grupe de atomi pe care le uneste. Hidrocarburile cu catene liniare au de fapt forma de linii frante, care din cauza rotatiei libere pot lua forme variabile. Cea mai stabila este insa forma in zig-zag, cu toti atomii de carbon in acelasi plan, ca in figura 10.
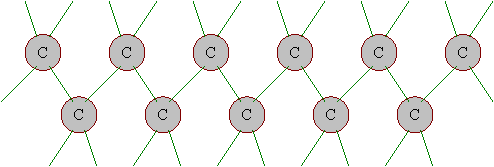
Fig Forma de zig-zag a lntului de atomi de carbon intr-un normal-alcan.
1.1.5. Stare naturala. Principalele surse de alcani sunt gazele naturale si petrolul.
Gazele naturale pot fi :
a) formate din metan (gazul metan) si
b) gaze de sonda sau gaze de petrol (continand alcani de la C1 la C5). Petrolul este un amestec de hirocarburi (vezi 2.5.
Tara noastra dispune de astfel de zacaminte : in Ardeal se afla gaz metan ; in Moldova, in partea sudica a Carpatilor, in zona Argesului si Olteniei sunt zacaminte de petrol.
O sursa naturala pentru obtinerea hidrocarburilor mai este carbunele si oxidul de carbon obtinut din acesta.
1.1.6. Proprietati fizice. La temperatura si presiunea obisnuita alcanii pot fi gazosi, lichizi sau solizi, in functie de atomii de carbon din molecula. Astfel termenii inferiori (pana la butan C4) sunt gazosi, termenii medii (pana la pentadecan C15) sunt lichizi, iar cei superiori (peste C16) sunt solizi.
Acesta modificare a starii de agregare se datoreste cresterii continue a puntelor de fierbere si de topire cu numarul atomilor de carbon.
In seriile omoloage, punctele de fierbere si de topire cresc cu cresterea masei moleculare. Aceasta regula generala se pastreaza si in cazul izoalcanilor, dar ramificarea micsoreaza punctul de fierbere al compusilor respectivi, de exemplu :
CH3 - CH2 - CH2 - CH2 - CH3 n-pentan p.f. = 360C
CH3 - CH - CH2 - CH3 izopentan p.f .= 27,80C
CH3
CH3
CH3- C-CH3 neopentan p.f. = 9,40C
CH3
Alcanii lichizi si solizi au densitatea mai mica decat unitatea (plutesc deasupra apei). Sunt substante insolubile in apa, dar solubile in solventi organici :
benzen, alcool, eter, cloroform etc. Alcanii lichizi sunt solventi pentru multe substante organice.
Alcanii gazosi nu au miros si de accea, pentru depistarea scaparilor de gaze din conducte sau butelii (aragaz), li se adauga substante urat mirositoare (compusi organici ai sulfului, numiti mercaptani), a caror prezenta este foarte usor de sesizat.
1.1.7. Proprietati chimice. Denumirea de parafine , care provine de la parum affinis = afinitate (chimica) mica, este folosita si astazi pentru alcani si izoalcani. Ea exprima reactivitatea scazuta a termenilor din aceasta clasa de hidrocarburi.
Reactiile chimice la care participa alcanii se pot grupa dupa natura legaturilor covalente care se desfac.
Legatura C-H se desface la substitutie, dehidrogenare, oxidare.
Legatura C-C se desface la descompunere termica, izomerizare, ardere.
Reactiile de substitutie sunt acele transformari chimice ale alcanilor in care, sub
actiunea unui anumit reactant, unul sau mai multi atomi de hidrogen din alcanul respectiv sunt inlocuiti cu atomi sau grupe de atomi proveniti din reactant.
Reactiile de substitutie sunt reactii caracteristice alcanilor (hidrocarburilor saturate) dar se intalnesc si la alte clase de hidrocarburi, precum si la substante cum sunt derivatii halogenati, alcoolii, acizii, etc.
Cea mai importanta reactie de substitutie este halogenarea.
Halogenarea alcanilor reprezinta reactia de substitutie a hidrogenului din alcan cu atomi de halogen, in care se obtin derivati halogenati :
R-H + X2 → R-X + HX
Alcan halogen derivat hidracid
halogenat
Alcanii reactioneaza direct cu clorul si cu bromul la lumina ( reactie fotochimica). Cu fluorul si iodul nu reactioneaza in acest mod. Clorurarea sau bromurarea alcanilor se poate efectua si in absenta luminii, dar la temperaturi ridicate, cuprinse intre 300-6000C. Clorurarea (reactia cu clorul) prezinta interes practic. In cazul alcanilor cu mai multi atomi de carbon, reactia conduce la un amestec de derivati halogenati, deoarece nu este selectiva.
Astfel, un ameste de metan si clor expus la o sursa de lumina sau incalzit la circa 5000C formeaza un amestec de derivati halogenati :
CH4 + Cl2 → CH3Cl + HCl
clorura de
metil
CH3Cl + Cl2 → CH2Cl2 + HCl
clorura de
metilen
CH2Cl2 +Cl2 → CHCl3 + HCl
cloroform
CHCl3 + Cl2 → CCl4 + HCl
tetraclorura
de carbon
2. Reactiile de izomerizare sunt acele transformari, in care normal alcanii, sub actiunea unor catalizatori, ca bromura sau clorura de aluminiu anhidra, la temperaturi de 50 - 1000 C, se transforma in izomeri cu structura ramificata, adica in izoalcani.
Astfel butanul trece in izobutan :
CH3 - CH2 - CH2 - CH3 = CH3 - CH - CH3
CH3
Reactiile de izomerizare au aplicatii practice in obtinerea benzinelor de calitate superioara, pentru ca izoalcanii ard mai bine in motoarele cu explozie ale automobilelor decat cei cu catene normale.
3. Reactiile de oxidare sunt transformarile suferite de alcani sub actiunea oxigenului. Acestea pot fi : oxidari incomplete sau oxidari si oxidari totale sau arderi.
a) Oxidarile sunt transformarile care conduc la produsi ce apartin altor clase de substante, ca alcooli, aldehide, acizi,etc., in functie de conditiile de lucru.
Importanta practica prezinta oxidarile metanului :
60 atm
![]() CH4 + O2 CH3OH
CH4 + O2 CH3OH
400C
alcool metilic ( metanol)
oxizi de azot
![]() CH4 + O2 CH2O + H2O
CH4 + O2 CH2O + H2O
400 - 600C
aldehida formica
![]() CH4 + O2 2 CO + 4 H2
CH4 + O2 2 CO + 4 H2
![]()
gaz de sinteza
c) Arderi. Oxidarea totala a alcanilor, numita si ardere, conduce la formarea
dioxidului de carbon si a apei.
Astfel, arderea metanului, butanului, etc. se poate exprima prin urmatoarele ecuatii chimice :
CH4 + 2 O2 → CO2 + 2 H2O + Q
C4H10 + 13/2 O2 → 4 CO2 + 5 H2O + Q
Aceste reactii sunt insotite de degajarea unei cantitati corespunzatoare de caldura (Q) si stau la baza folosirii alcanilor drept combustibili.
Alcanii cu numar mare de atomi de carbon ard progresiv si cu viteze controlabile ; termenii inferiori, gazosi sau lichizi in stare de vapori, formeaza cu oxigenul sau cu aerul amestecuri detonate, capabile sa produca explozii sub influenta unei scantei. Un exemplu il constituie detonatia metanului care se poate produce intre concentratiile limita ale acestuia in aer (5 - 15 %). Se impune de aceea sa se ia masuri de precautie deosebite ca sa nu existe pe conducte scapari de gaze naturale, ce pot provoca accidente.
4. Descompunerea termica a alcanilor. Datorita inertiei lor chimice alcanii prezinta o mare stabilitate termica, putand fi incalziti pana la 300 - 4000C fara a suferi vreo transformare. La temperaturi mai ridicate au loc ruperi ale legaturilor covalente
C - C si C - H in urma carora din moleculele mai mari, ale unor alcani superiori, rezulta molecule mai mici de hidrocarburi saturate si nesaturate.
Dupa temperatura la care are loc descompunerea termica aceasta poate fi :cracare, cand t < 6500C si piroliza, cand t > 6500C.
![]() Un exemplu il constituie
descompunerea termica a butanului, la 6000C, cand au loc urmatoarele
reactii :
Un exemplu il constituie
descompunerea termica a butanului, la 6000C, cand au loc urmatoarele
reactii :
![]() → CH4 + CH2 = CH - CH3 Reactii de cracare
→ CH4 + CH2 = CH - CH3 Reactii de cracare ![]()
metan propena
→ CH3 - CH3 + CH2 = CH2
etan etena
CH3 -CH2 - CH2 - CH3 →
![]() butan → CH2 = CH - CH2 - CH3 + H2
butan → CH2 = CH - CH2 - CH3 + H2
1- butena Reactii de dehidrogenare
→ CH3 - CH = CH - CH3 + H2
2- butena
Dupa cum se observa au loc doua tipuri de reactii :
reactii de rupere a unor legaturi C-C, numite reactii de cracare,
reactii de rupere a unor legaturi C-H, numite reactii de dehidrogenare.
La alcanii superiori, cu numar mare de atomi de carbon, posibilitatile de rupere a moleculei cresc foarte mult, astfel ca se obtin amestecuri de alcani si alchene cu molecule de diferite marimi.
Descompunerea termica a alcanilor isi gaseste aplicatii practice deosebit de importante in valorificarea rationala si superioara a petrolului.
1.1.8. Metanul CH4. A fost descoperit de A.Volta in 1778 in malul baltilor si a fost numit gaz de balta. In scoarta terestra formeaza zacaminte in care puritatea poate atinge 99%. Tara noastra poseda zacaminte de metan cu puritate ridicata (98 - 99%), cele mai importante fiind cele de la Sarmasel, Copsa Mica, Bazna, Nades, Sincai, Deleni, Bogota etc.
Metanul apare si in minele de carbuni unde, impreuna cu aerul, formeaza amestecul exploziv denumit gaz grizu ; mai apare in gazele de cocserie si in cele de cracare.
Metanul se extrage din zacamintele naturale cu ajutorul sondelor. De aici se transporta la consumatori (laboratoare, industrie, termocentrale, locuinte, etc.) cu ajutorul conductelor.
Metanul mai este utilizat drept combustibil dar azi se pune un accent deosebit pe pe transformarea lui intr-o serie de compusi chimici de o mare importanta practica. Aceasta prelucrare se numeste chimizarea metanului. Este suficient sa precizam ca prin chimizare valoarea unui metru cub de gaz metan creste de circa 30 de ori, ca sa ne dam seama de importanta economica a acesteia.
Principalele directii de chimizare a metanului sunt :
a) Chimizare prin clorurare (vezi 1.1.7.). Produsii obtinuti au diferite intrebuintari. Astfel, clorura de metil (CH3Cl) este un bun agent frigorific, clorura de metilen, (CH2Cl2) si tetraclorura de carbon (CCl4) se intrebuinteaza ca solventi. Tetraclorura de carbon se intrebuinteaza si la stingerea incendiilor.
b) Chimizare prin oxidare. Dupa cum s-a vazut in paginile anterioare, metanul, prin oxidare in diverse conditii, poate forma : alcool metilic, aldehida formica si gaz de sinteza. Prin oxidare, metanul mai poate forma si negru de fum, conform reactiei :
CH4 + O2 → C + 2 H2O
negru de fum
Randamentul de obtinere a negrului de fum prin acest procedeu este foarte mic si nerentabil. Astazi se fabrica negrul de fum mult mai rentabil din produse petroliere, de exemplu la noi in tara la Pitesti. Negrul de fum este utilizat la prelucrarea cauciucului, obtinerea crenelurilor de tipar, tusuri, etc.
Cand oxidarea metanului se face cu oxigen din aer, azotul existent ramane necombinat :
CH4 + aer (O2 + N2) → CO2 + 2 H2O + N2
procesul constituind o importanta sursa de azot.
c) Chimizare prin oxidare partiala cu vapori de apa. Prin oxidarea metanului cu vapori de apa se obtine gaz de sinteza :
Ni
![]() CH4 + H2O CO + 3H2
CH4 + H2O CO + 3H2
650 - 900 C gaz de sinteza
Gazul de sinteza obtinut este folosit la scara industriala in diverse sinteze de alcooli, aldehide, etc.
d) Amonoxidarea metanului. Este reactia metanului cu amoniac si aer, cu formare de acid cianhidric :
![]() CH4 + NH3 + 3/2
O2 Pt, 1000 C HCN + 3 H2O
CH4 + NH3 + 3/2
O2 Pt, 1000 C HCN + 3 H2O
acid cianhidric
e) Obtinerea din metan a acetilenei. Din metan se poate obtine acetilena cu largi utilizari practice.
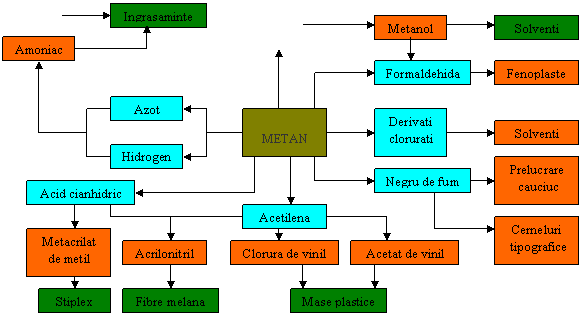
Produsele chimice obtinute prin reactiile descrise mai sus si-au gasit largi aplicatii industriale in marile combinate chimice ale tarii noastre, fiind prelucrate in continuare, prin alte procese chimice. Chimizarea metanului poate fi urmarita, in ansamblu pe schema:
Rasini sintetice Uree
Gaz de sinteza
![]()
![]()
![]()
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 11347
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2026 . All rights reserved