| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
DOCUMENTE SIMILARE |
||||||
|
||||||
Reactii de acilare
Introducere
Reactia de acilare Friedel-Crafts a compusilor aromatici substituiti si a compusilor heteroaromatici reprezinta o cale importanta pentru sinteza de cetone aromatice, utilizate ca intermediari in sintezele din chimia fina [1]. La nivel industrial reactia are loc intre un compus aromatic sau heteroaromatic si un agent de acilare precum un acid carboxilic sau un derivat al acestuia (de ex. anhidrida acetica) in prezenta unui catalizator acid. In general, conditiile de reactie utilizate sunt severe si se utilizeaza catalizatori in faza omogena, precum baze organice (piridina cu 4-dimetilamina) [2], catalizatori de tip acid Lewis (AlCl3, BF3, TaCl5) [3-5] sau acizi anorganici [6] care genereaza deseuri corozive si toxice (mai mult de 4 moli de Cl- per mol de cetona produsa). Un mare neajuns in procesele care folosesc acizi Lewis este faptul ca nu este posibila regenerarea si recuperarea catalizatorului. Deasemenea, astfel de reactii decurg in prezenta solventilor clorurati care sunt daunatori mediului inconjurator (de ex. diclorometanul).
Intrucat aceste sisteme sunt foarte departe de principiile chimiei 'verzi', au fost cautate alte sisteme catalitice care sa raspunda acestor exigente. Astfel, multe studii recente s-au centrat pe utilizarea catalizatorilor omogeni, stabili la umiditate si a catalizatorilor heterogeni. De exemplu, s-a aratat ca, spre deosebire de AlCl3 care este un compus extrem de sensibil fata de apa, triflatii diferitelor metale sunt catalizatori acizi Lewis extrem de eficienti si stabili fata de umiditate [7, 8]. Ca atare, multe dintre reactiile clasice, catalizate de clorura de aluminiu, s-au inlocuit cu reactii similare, catalizate de astfel de triflati. La fel ca si in cazul reactiilor catalizate de AlCl3, alte reactii catalizate de acizi Brønsted (H2SO4, H3PO4, CF3SO3H, s.a) sau acizi Lewis BF3, TiCl4 sau SnCl4 vor trebui reconsiderate pentru identificarea unor sisteme catalitice "verzi". Pe de alta parte, utilizarea catalizatorilor acizi solizi reprezinta o alternativa atractiva a sistemelor omogene, cu avantaje economice atat pentru industrie cat si pentru mediul inconjurator. Zeolitii Beta, de exemplu, s-au dovedit a fi extrem de eficienti in reactia de acilare in faza gazoasa a inelelor aromatice, cu agent de acilare - anhidrida acetica [9]. Datorita aciditatii slabe a zeolitilor, comparativ cu cea a clorurii de aluminiu sau a acizilor minerali lichizi, acestia sunt mult mai indicati pentru acilarea compusilor aromatici activati, precum toluenul, xilenul, anisolul, veratrolul sau 2-metoxinaftalina.
Inlocuirea catalizatorilor lichizi cu solide acide poate aduce numeroase avantaje precum: reducerea coroziunii, o separare mai simpla a catalizatorului, reutilizarea catalizatorilor si posibilitatea obtinerii de conversii si selectivitati ridicate. In literatura sunt numeroase exemple pentru reactia de acilare a 2-metoxinaftalinei (in urma careia rezulta intermediarul Naproxenului) in prezenta de anhidride si solventi clorurati cu numerosi zeoliti: HEU-1, Beta , ZSM-12 [10, 11-13]. Un neajuns a acestor reactii este faptul ca au loc in faza gazoasa. S-au mai investigat si zeoliti precum: faujasite sau mordenit, insa rezultatele obtinute nu au fost cele dorite [11].
Asa cum s-a mentionat, alte sisteme cu aciditate si stabilitate ridicata, studiate pentru aceast tip de reactie, au fost triflatii metalici. Literatura prezinta mai multe rapoarte despre utilizarea triflatilor in reactiile de acilare in faza omogena [14]. Acidul triflic s-a dovedit activ in acilarea hidrocarburilor aromatice cu b-lactame, iar triflatii lantanidelor au condus, deasemenea, la rezultate bune in acilarea acelorasi substraturi utilizand anhidrida acetica ca si agent de acilare [15]. Deasemenea, inlocuirea anhidridei acetice sau a clorurii acide cu acid acetic, reprezinta un avantaj pentru mediul inconjurator, deoarece substantele folosite in sintezele chimice conduc la formarea de produsi secundari de reactie netoxici. Microundele reprezinta o sursa de incalzire alternativa celei conventionale, in multe cazuri mult mai eficienta in vederea obtinerii de conversii si selectivitati mai ridicate [16-22]. Un alt avantaj al acestei tehnici este ca reactiile pot decurge cu eficienta marita atat in apa cat si in conditii de '' free solvent''. Aceasta din urma este considerata un atu foarte important al chimiei cu microunde, deoarece are un avantaj ''verde'', problema eliminarii solventului dupa reactie rezolvandu-se de la sine. Ca atare, pentru rectiile organice iradierea cu microunde incepe sa capete o dezvoltarea tot mai larga [17, 18, 21].
In urma acilarii compusilor aromatici substituiti cat si a compusilor heteroaromatici se obtin produsi cu importanta comerciala majora in industria chimica, precum produsi farmaceutici, aditivi pentru industria vopselelor, parfumuri si coloranti [1].
Obiective
Asa cum s-a aratat, la ora actuala, datorita problemelor de poluare din ce in ce mai mari, exista o tendinta, din ce in ce mai stringenta de a inlocui procesele poluante si puternic energofage cu unele mai blande, in acord cu principiile chimiei verzi si a dezvoltarii durabile. Una dintre cele mai frecvent utilizate reactii la nivel industrial, atat pentru obtinerea de produsi valorosi in diverse sectoare de consum, cat si pentru protectia anumitor grupari functionale in timpul unei sinteze, este reactia de acilare. Din pacate, aceasta reactie este inca realizata in maniera in care, pe langa produsul de reactie, se formeaza si multipli produsi secundari extrem de nocivi mediului. Ca atare, studiul de fata a avut ca obiectiv principal realizarea unor serii de reactii de acilare ale compusilor aromatici si heteroaromatici in prezenta unor catalizatori pe baza de triflat de Sn si Al in silice mezoporoasa. Ca agent de acilare s-a utilizat anhidrida acetica si acidul acetic, iar ca sursa de energie s-a utilizat atat incalzirea "conventionala" termica cat si iradierea cu microunde. Catalizatorii utilizati sunt importanti prin faptul ca combina un sistem mezoporos cu suprafata puternic hidrofila cu specii de triflat de Sn sau Al dispersate pe suprafata. Aceste specii actioneaza ca si centri catalitici cu caracter de acid Lewis. Catalizatorii pe baza de triflat de Sn, utilizati in aceasta lucrare, au fost aplicati cu succes in reactiile de acilare a sulfonamidelor aromatice cu acid acetic ca si agent de acilare, precum si in sinteza (dl)- -tocoferolului [23]. Spre deosebire de acestia, triflatii de Al utilizati in lucrare n-au mai fost testati in alte reactii.
Experimental
3.1. Prepararea catalizatorilor
Catalizatorii SnOTf-MCM-41 si SnOTf-UVM-7, cu structura mezoporoasa mono- si bimodala, s-au preparat in doua etape, in care acidul triflic s-a incorporat in silice mezoporoasa cu staniu. Incorporarea staniului in peretii mezoporosi s-a realizat prin metoda Atrane [24]. Probele de silice dopate cu staniu s-au abreviat cu Sn-MCM-41 si Sn-UVM-7, iar probele catalitice finale cu SnTf(22)-MCM-41 (Si/Sn = 21.81), SnTf(47)-MCM-41 (Si/Sn = 47.32), SnTf(51)-MCM-41 (Si/Sn = 50.84), si SnTf(18)-UVM-7 (Si/Sn = 18.40).
O alta serie de catalizatori utilizati in studiul de fata au fost cei pe baza de triflat de aluminiu. Catalizatorii cu pori bimodali (AlTf-UVM-7 cu continutul de Si/Al= 71, 52, 38, 25) au fost preparati in doua etape, acidul triflic fiind incorporat in silicea poroasa cu continut de Al, sintetizata anterior (matreiale de Al-UVM-7 cu continutul de Si/Al= 17, 25, 32 si 50).
Teste catalitice
a) Reactii de acilare cu incalzire termica "conventionala"
In conditii standard, intr-un vas de reactie cu capacitate de 10 ml, s-au dizolvat 1.25 mmoli de substrat (2-metoxinaftalina, toluen, fenol, furan si tiofen) in 4ml de solvent (acetonitril, THF, heptan, diclorometan), la care s-au adaugat 3,75 mmoli de agent de acilare (anhidrida acetica sau acid acetic) si 15 mg de catalizator (raport agent de acilare: substrat = 3:1). In paralel s-au realizat si reactii "free solvent", in aceleasi conditii. Masa de reactie s-a mentinut sub agitare, la temperatura camerei, 80ºC si 140ºC, pentru 2-18h. Dupa reactie, catalizatorul s-a separat prin filtrare iar produsii de reactie s-au analizat prin cromatografie de gaze (GC Schimadzu) cu detectie: FID, coloana(TR-WAX+TR1MS) cu lungimea de 60m in urmatoarele conditii: i) pentru reactiile cu 2-metoxinaftalina, temperatura: 40-190ºC (panta de incalzire 10ºC/min); ii) pentru reactiile de acilare a furanului, tiofenului, fenolului si toluenului: temperatura: 40-230ºC (panta de incalzire 10ºC/min). Produsii de reactie au fost identificati prin cromatografie de gaze cuplata cu spectrometrie de masa (GC-MS).
b) Reactii de acilare cu incalzire prin iradiere cu microunde
Pentru aceste reactii s-a utilizat un reactor cu microunde, START S (Milestone Italy). Reactiile s-au realizat sub agitare, la o temperatura de 117ºC sau 180ºC si o putere de iradiere de 600 W si timpi de reactie de 1-6 h. Intr-un experiment standard s-au utilizat 3,75 mmoli de substrat (fenol si tiofen), 11,25 mmoli agent de acilare (anhidrida acetica sau acid acetic) si 45mg de catalizator (raport molar agent de acilare: substrat= 3:1). Reactiile s-au realizat in conditii "free solvent". Dupa reactie, amestecul s-a racit la temperatura camerei, catalizatorul s-a filtrat iar produsii de reactie s-au analizat prin cromatografie de gaze (GC) si s-au identificat prin cromatografie de gaze cuplata cu spectrometrie de masa (GC-MS).
c) Formule de calcul pentru exprimarea performantelor catalitice :
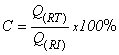
ØConversia (C%) s-a calculat ca raport intre cantitatea de reactiv
transformat (RT) si cantitatea de reactiv introdus (RI) in reactie :
ØSelectivitatea (S%)- raport intre cantitatea de produs format (PF) si cantitatea de reactiv transformat (RT) :
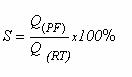
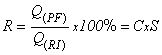
ØRandamentul
(R%)- raport intre cantitatea de produs format
(PF) si cantitatea de reactiv introdus (RI) :
Rezultate si discutii
Selectarea conditiilor de pH in prima etapa a sintezei catalizatorilor a permis prepararea a doua tipuri de materiale: sisteme poroase unimodale si bimodale. Astfel, la valori ridicate de pH s-a obtinut Sn-MCM-41, format din particule micrometrice largi, insa lucrandu-se in conditii bazice moderate, a fost izolat Sn-UVM-7 (o versiune nanometrica a materialului de M41). Al doilea catalizator reprezinta, in fapt, o asamblare a particulelor mezoporoase nanometrice definind un sistem poros aditional de tip - textura ierarhica (materialele de tip UVM-7). Natura unimodala si bimodala a porilor din materialele de MCM-41 si UVM-7 a fost confirmata de izotermele de adsorbtie-desorbtie a N2 (Figura 1A, B).
B A
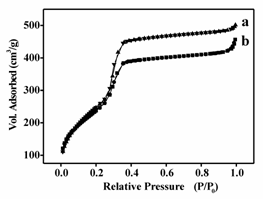
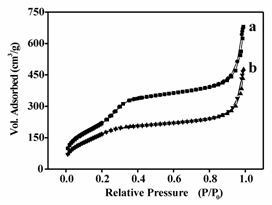
Figura 1. A: izoterme de adsorbtie-desorbtie a N2 pentru catalizatorii (a) Sn-MCM-41 si (b) SnTf-MCM-41 si B: izoterme de adsorbtie-desorbtie a N2 pentru catalizatorii (a) Sn-UVM-7 si (b) SnTf-UVM-7.
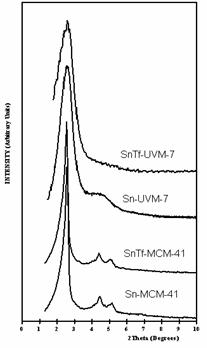
Figura 2. Difractogramele XRD caracteristice probelor pe baza de Sn si SnTf.
In cazul materialului MCM-41, pe langa linia intensa, difractograma prezinta alte doua semnale de intensitate mica, reflectiilor (110) si (200). Aceste trasaturi indica faptul ca simetria ordonata mezoporoasa hexagonala, tipica silicei mezoporoase MCM-41 a fost mentinuta atat dupa incorporarea Sn (prima etapa a sintezei) cat si dupa reactia cu acidul triflic (etapa a doua a sintezei). Pe de alta parte, semnalul larg cu intensitate relativ scazuta poate fi atribuit unei suprapuneri a reflectiilor (110) si (200), tipica celulelor hexagonale in cazul Sn-UVM-7 (prima etapa), semnal care dispare dupa reactia cu acidul triflic (etapa a doua). Pentru ambele serii (MCM-41 si UVM-7), pozitia liniei de difractie ramane practic neschimbata. Aceasta confirma ca mezostructura nu a fost afectata dupa reactia cu acidul triflic. Pe de alta parte, a doua etapa a reactiei afecteaza putin intensitatea semnalului. Pierderea in intensitate a liniilor de difractie, observata in XRD, corespunzatoare SnTf-MCM-41 si SnTf-UVM-7 (in comparatie cu Sn-MCM-41 si Sn-UVM-7), trebuie atribuita aceluiasi fenomen de anulare de faze asociat cu introducerea anionilor de triflat in interiorul porilor, desi nu trebuie pierduta din vedere nici posibilitatea pierderii, intr-o anumita masura, a simetriei. In toate probele, absenta liniilor de difractie in difractograma XRD la valori ridicate a unghiurilor, indica absenta segregarii de faza care sa conduca la formarea oxizilor SnO sau SnO2.
 Microscopia cu transmisie de electroni (TEM, Figura 3)
confirma datele obtinute atat din XRD cat si din izotermele de
adsorbtie-desorbtie de N2. Observarea, in ambele cazuri, a unei
morfologii de particula dominante, sustine natura monofazica a catalizatorilor.
Microscopia cu transmisie de electroni (TEM, Figura 3)
confirma datele obtinute atat din XRD cat si din izotermele de
adsorbtie-desorbtie de N2. Observarea, in ambele cazuri, a unei
morfologii de particula dominante, sustine natura monofazica a catalizatorilor.
Figura 3. Imaginea TEM a (a) SnTf- MCM-41 [inserarea prezina imaginea TEM marita (x5) a porilor ordonati si domeniile bogate in Sn(x3)] si (b) catalizatorul de SnTf-UVM-7[imaginea inserata reprezinta o imagine TEM marita (x 3)].
Pentru catalizatorii SnTf-MCM-41 si SnTf-UVM-7 s-au determinat morfologii tipice - particule largi cu structura hexagonala si agregate dezordonate de nanoparticule. Mai mult, imaginile TEM prezinta si pete mici de culoare neagra (de dimensiuni de cca 2nm) care corespund domeniilor imbogatite in Sn, pentru ambii catalizatori.
Sumarul caracteristicilor texturale a catalizatorilor preparati sunt prezentate in Tabelul1.
Tabelul 1. Caracteristicile fizice ale catalizatorilor preparati.
|
Proba |
d100 (nm) |
SBET (m2/g) |
Pori mici (nm) |
Pori mari (nm) |
|
Sn-MCM-41 | ||||
|
SnTf(51)-MCM-41 | ||||
|
SnTf(47)-MCM-41 | ||||
|
SnTf(22)-MCM-41 | ||||
|
Sn-UVM-7 | ||||
|
SnTf(18)-UVM-7 |
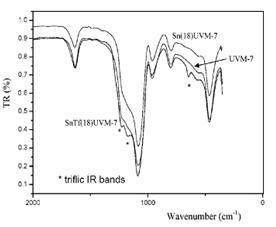 In figura 4, este prezentata formarea
speciilor de triflat de Sn. Spectrul FTIR indica ca nici unul dintre suporturi,
MCM-41 si UVM-7, nu retine triflatul, nici macar in urme. Din contra, pe
probele de Sn suportate pe silice, acidul triflic a fost incorporat intr-o
cantitate ce creste odata cu cresterea continutului de Sn. Nu s-a observat nici o fixare a sa pe peretii silicei, ci doar pe atomii de Sn si Sn-SiO2.
In figura 4, este prezentata formarea
speciilor de triflat de Sn. Spectrul FTIR indica ca nici unul dintre suporturi,
MCM-41 si UVM-7, nu retine triflatul, nici macar in urme. Din contra, pe
probele de Sn suportate pe silice, acidul triflic a fost incorporat intr-o
cantitate ce creste odata cu cresterea continutului de Sn. Nu s-a observat nici o fixare a sa pe peretii silicei, ci doar pe atomii de Sn si Sn-SiO2.
Figura 4. Studiul comparativ al spectrelor FTIR a UVM-7, Sn(18)-UVM-7 si SnTf(18)-UVM-7.
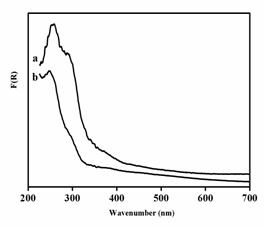 Examinarea UV-Vis a materialelor MCM-41 si UVM-7,
sugereaza prezenta speciilor tetraedrice Sn+4
cu o dispersie ridicata, caracterizate de banda de absorbtie de la 250nm,
caracteristica tranzitiei de sarcina de la O2- la Sn4+ in
coordinarea tetraedrica [25]. Pentru catalizatorul SnTf(18)-UVM-7, centrii de
Sn par a fi speciile Sn4+, cu preponderenta. In cazul probelor
SnTf-MCM-41, banda aditionala observata (centrata la 289nm, caracteristica
tranzitiei de sarcina de la O2− la
Sn4+ in coordinare octaedrica cu un anumit grad de polimerizare[26]
) poate fi asociata existentei unor nanodomenii de tip casiterite (Figura 5) cu
o scadere a centrilor activi de la 30% la 50% pentru probele cu continut scazut
si ridicat de Sn.
Examinarea UV-Vis a materialelor MCM-41 si UVM-7,
sugereaza prezenta speciilor tetraedrice Sn+4
cu o dispersie ridicata, caracterizate de banda de absorbtie de la 250nm,
caracteristica tranzitiei de sarcina de la O2- la Sn4+ in
coordinarea tetraedrica [25]. Pentru catalizatorul SnTf(18)-UVM-7, centrii de
Sn par a fi speciile Sn4+, cu preponderenta. In cazul probelor
SnTf-MCM-41, banda aditionala observata (centrata la 289nm, caracteristica
tranzitiei de sarcina de la O2− la
Sn4+ in coordinare octaedrica cu un anumit grad de polimerizare[26]
) poate fi asociata existentei unor nanodomenii de tip casiterite (Figura 5) cu
o scadere a centrilor activi de la 30% la 50% pentru probele cu continut scazut
si ridicat de Sn.
Tendinta de a forma legaturi de Sn-O-Sn este datorata valorilor de pH ridicate folosite la prepararea MCM-41 in comparatie cu cele folosite pentru prepararea UVM-7.
Figura 5. Spectrele UV-vis cu reflectie difuza a catalizatorilor de (a) SnTf- MCM-41 si (b) SnTf-UVM-7.
Chemosorbtia de NH3 arata ca precursorul mezoporos de staniu nu chemosoarbe amoniacul, ceea ce sugereaza absenta aciditatii. Pe baza chemosorbtiei de NH3 (cm3(STM)/g), pentru catalizatorii de SnTf(22)-MCM-41 si SnTf(18)-UMV-7 s-a determinat un numar ridicat de centri acizi in cazul probelor cu o dispersie mare a Sn (tabelul 2). Astfel, pe baza acestor rezultate, se poate spune ca centrii activi corespund intr-adevar speciilor de triflat de Sn cu dispersie ridicata.
In Tabelul 2 sunt prezentate principalele caracteristici texturale si chimice ale celor doua tipuri de catalizatori.
Tabelul 2. Parametri fizico-chimici [Coman S. M., Pop G., Stere C., Parvulescu V. I., Haskouri J. El, Beltran D., Amoros P. (2007) J. Catal. 251, p.388] ai probelor catalitice pe baza de triflat de Sn
|
Proba |
Si/Sn |
Sn/S |
Numarul centrilor/m2* |
Sny(O,OH)z (% moli) |
Sn(OTf)x (% moli) |
|
|
SnTf(22)-MCM-41 |
2.31 x 1020 | |||||
|
SnTf(47)-MCM-41 |
1.29 x 1020 | |||||
|
SnTf(51)-MCM-41 |
1.22 x 1020 | |||||
|
SnTf(18)-UMV-7 |
2.66 x 1020 | |||||
*-bazate pe masurarile de chemosorbtie de NH3.
Aplicand metoda Atrane de preparare, catalizatorii obtinuti poseda atomi de Sn cu o dispersie foarte mare pe suprafata mezoporoasa. In ceea ce priveste textura, daca probele pe baza de MCM-41 constau in particule micrometrice cu pori unimodali, cele pe baza de UVM-7 sunt formate din agregate de nanoparticule cu pori bimodale. Caracterizarea prin UV-Vis sugereaza prezenta Sn+4 dispersat cu structura de tetraedru, (banda de absorbtie la 250nm - caracteristica tranzitiei de sarcina de la O2- la Sn4+ pentru coordinarea tetraedrica).
Acilarea compusilor aromatici
a) Acilarea 2-metoxinaftalinei
Studiile din literatura au demonstrat ca acilarea 2-metoxinaftalinei (2-MN) decurge cu formarea de doi produsi, si anume 2-acetil-6-metoxinaftalina (2-AMN sau 2,6-AMN), care este intermediarul pentru obtinerea Naproxenului (acidul S-(+)-6-metoxi-α-metil-2-naftalenacetic) si 1-acetil-2-metoxinaftalina (1,2-AMN) (produs secundar). Chiar daca acilarea 2-MN are loc preferential in pozitia 1, care este pozitia controlata cinetic, rezultand 1,2-AMN, s-a ratat ca prin efecte de selectivitate de conformatie moleculara controlata, se poate modifica raportul dintre produsii de reactie cu obtinerea preponderenta de 2,6-AMN [27]. Produsii formati in urma reactiei de acilare a 2-MN sunt prezentati in Schema 1.

Schema 1. Produsii obtinuti in urma acilarii 2-MN cu Ac2O.
Rezultatele obtinute in acilarea 2-MN cu anhidrida acetica, in prezenta catalizatorilor pe baza de triflat de aluminiu, sunt reprezentate in Tabelul 2. Izomerul II, poate suferi o transacilare intramoleculara cu obtinerea de noi derivati acetilati ai metoxinaftalinei (1-acetil-7-metoxinaftalina, III), in timp ce acilarea consecutiva a produsilor monoacilati este si ea posibila cu obtinerea derivatilor diacetilati (IV). Trebuie subliniat si faptul ca in unele cazuri se pot obtine si produsi de hidroliza ai 2-MN si anume 2-naftolul (V), precum si noi derivati acetilati (acetil-naftoli, VI). Hidroliza legaturii terminale C-O in aril eteri a fost raportata pe zeoliti ce contin foarte mult Al extra retelar [28]. Prezenta urmelor de apa pe catalizator, chiar si dupa ce au fost supusi procesului de activare la temperaturi ridicate, poate produce hidroliza centrilor acizi Lewis cu formarea de centri Bronsted puternici. Acesti centri sunt capabili sa demetileze 2-MN la 2-naftol. Astfel de demetilari genereaza radicali metil in mediul de reactie, care pot fi neutralizati fie ca metanol fie ca si compusi metilati ai 2-MN printr-un mecanism de transalchilare. Astfel, se poate explica obtinerea unui izomer metilic al 2-MN (VII) in amestecul de reactie. Cateva rezultate pentru acilarea 2-MN cu anhidrida acetica sunt prezentate mai jos (Tabel 3).
Tabelul 3. Acilarea 2-MN cu anhidrida acetica in prezenta de triflati de Al
|
Nr |
Catalizator |
C, % |
S2,6- , % |
S1,2- , % |
|
AlCTf (Si/Al=15) | ||||
|
AlCTf (Si/Al=30) | ||||
|
AlCTf (Si/Al=45) | ||||
|
AlCTf (Si/Al=60) | ||||
|
AlETf (Si/Al=15) | ||||
|
AlETf (Si/Al=30) | ||||
|
AlETf (Si/Al=45) | ||||
|
AlETf (Si/Al=60) |
Conditii de reactie: 2-MN/Ac2O=1/3, 30 mg de catalizator, 80ºC, 4h, fara solvent
Selectivitatea extrem de scazuta in produsul de interes (Tabel 3) nu a putut fi, din pacate, imbunatatita nici prin cresterea temperaturii de reactie (la 110ºC) sau a timpului de reactie (la 18h). Pe de alta parte, utilizarea unui solvent in mediul de reactie (dioxan si nitrobenzen) a avut ca efect o scadere a conversiei 2-MN in timp ce selectivitatea la 2,6-AMN a crescut cu doar o unitate.
b) Acilarea toluenului
Acilarea toluenului cu anhidrida acetica sau cloruri acide conduce la 4-metilacetofenona (4-MACF), compus utilizat ca intermediar cosmetic (Schema 2) [29]. Ca si catalizatori, literatura mentioneaza hafniu trifluorometan sulfonat, ZrO2-SO42- [30] si acetati ai unor metale precum Cu(II) si Pd(II) [31].

Schema 2. Acilarea toluenului cu anhidrida acetica
Rezultatele experimentale obtinute in acilarea toluenului, in prezenta catalizatorilor pe baza de triflat de staniu sunt reprezentate in Tabelul 4.
Tabelul 4 Acilarea toluenului cu anhidrida acetica in prezenta de triflati de staniu
|
Nr. |
Catalizator |
S , % |
|
|
SnTf(22)-MCM-41 | |||
|
SnTf(18)-UVM-7 | |||
|
SnTf(18)-UVM-7 | |||
|
SnTf(18)-UVM-7* |
Conditii de reactie: raport molar Toluen/Ac2O=1/3, 15mg catalizator, T=80C, timp= 6h si 18h*, solvent=4ml AcCN.
Rezultatele obtinute arata ca acilarea toluenului nu decurge in prezenta acestor catalizatori.
c) Acilarea fenolului
Studiile anterioare au aratat ca in prezenta de zeoliti ca si catalizatori, solventii nepolari determina o inhibitie puternica a acilarii, datorita produsilor de reactie formati foarte polari (acidul acetic, produsii acilati) care se adsorb pe centri acizi, blocandu-i. Pe de alta parte, solventii polari se adsorb competitiv cu moleculele reactante la centri acizi. Pe baza acestor observatii, pentru a clarifica efectul solventului utilizat, intr-o prima etapa s-a studiat acilarea toluenului la o-hidroxiacetofenona, cu anhidrida acetica, in diferiti solventi. Produsii posibili pentru aceasta reactie sunt reprezentati in Schema 3

Schema 3. Acilarea fenolului cu anhidrida acetica
Rezultatele obtinute in urma acilarii fenolului cu anhidrida acetica sunt prezentate in tabelul 5.
Tabelul 5. Rezultatele acilarii fenolului cu anhidrida acetica, in prezenta catalizatorilor pe baza de triflat de staniu, in prezenta de diferiti solventi
|
Nr. |
Catalizator |
Solvent |
C, % |
S2 , % |
S3 , % |
|
SnTf(47)-MCM-41 |
AcCN | ||||
|
THF | |||||
|
Heptan | |||||
|
CH2Cl2 | |||||
|
SnTf(51)-MCM-41 |
AcCN | ||||
|
THF | |||||
|
Heptan | |||||
|
CH2Cl2 |
Conditii de reactie: raportul molar substrat/agent de acilare= 1/3, 15 mg catalizator, 80C, 2 h, 4 ml de solvent, S2 - selectivitatea la fenilacetat, S3 - selectivitatea la o-hidroxiacetofenona, C -conversia.
Analizand rezultatele obtinute din Tabelul 5, se observa ca, cu exceptia THF, conversia fenolului este de circa 99%, indiferent de catalizatorul sau solventul utilizat. Mai mult, nici selectivitatea in fenilacetat nu depinde de natura solventului sau a catalizatorului, aceasta ramanand practic neschimbata (99%). Cu alte cuvinte, compozitia si structura catalizatorului au o influenta foarte mica in aceasta reactie. Din pacate, nici natura solventului nu are o influenta importanta, selectivitate in produsul dorit nefiind mai mare de 2%. Pentru aceasta reactie s-a studiat si efectul iradierii cu microunde, folosind ca agent de acilare acid acetic. Rezultatele obtinute sunt prezentate in Tabelul 6.
Tabelul 6 Acilarea fenolului cu acid acetic in prezenta microundelor
|
Nr |
Catalizator |
C, % |
S2 , % |
S3 , % |
|
SnTf(18)-UVM-7* | ||||
|
SnTf(18)-UVM-7** |
Conditii de reactie: raportul molar substrat/agent de acilare= 1/3, 15 mg catalizator, 117 si 3h*; 180C si 1h**, 4 ml de AcCN, S2 - selectivitate in fenilacetat, S3 - selectivitate in o-hidroxiacetofenona, C - conversia.
Cresterea conversiei fenolului de la 4,7% la 98,2% in conditiile de reactie prezentate in Tabelul 6, reprezinta un rezultat foarte bun. Pe de alta parte, cresterea temperaturii de la 117ºC la 180ºC determina o crestere a selectivitatii in produsul de interes de la 1,8% la 7%.
Rezultatele obtinute sunt foarte importante pentru chimia "verde", atat datorita agentului de acilare utilizat (acid acetic) cat si al tehnicii de incalzire a masei de reactie (iradiere cu microunde).
Acilarea compusilor heteroaromatici
In general, pentru compusii heteroaromatici precum furanul, tiofenul sau pirolul, substitutia electrofilica decurge mai rapid in comparatie cu benzenul. In cataliza omogena sunt cunoscute numeroase exemple de acilare a acestor compusi, in prezenta catalizatorilor de tip acid Lewis sau Bronsted [32], dar si in cataliza heterogena. Aceste reactii sunt foarte selective, de aceea problema formarii diferitor izomeri ca produsi secundari este exclusa. Astfel, pozitia 2 este mai favorizata atacului electrofil (E = ion acil) fata de pozitia 3, posibil datorita delocalizarii sarcinii pozitive mai avansate in aceasta pozitie. In mod similar decurge si acilarea furanului (Schema 4).
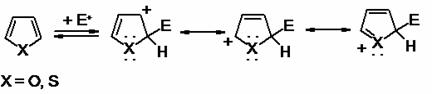
Atacul electrofil (E=ionul acil) in pozitia 2
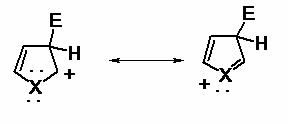
Atacul electrofilic in pozitia 3
Schema 4. Formele intermediare ale carbocationilor de tiofen (X=S) si furan (X=O), (E=electrofil-ionul acil)
a) Acilarea tiofenului
Spre deosebire de reactiile de acilare a benzenului, reactiile de acilare ale compusilor heteroaromatici precum furanul, tiofenul, pirolul si derivatii indolului sunt insuficient studiate, desi produsii de reactie obtinuti sunt compusi importanti in industria cosmetica si farmaceutica [33]. In cazul acilarii tiofenului cu anhidrida acetica, reactia decurge conform Schemei 5.

Schema 5. Acilarea tiofenului cu anhidrida acetica.
Rezultatele obtinute in urma acestei reactii sunt prezentate in tabelul 7.
Tabelul 7 Acilarea tiofenului cu anhidrida acetica in prezenta catalizatorilor de triflat de Sn.
|
Nr. |
Catalizator |
C, % |
S2 , % |
S3 , % |
|
SnTf(22)-MCM-41 | ||||
|
SnTf(47)-MCM-41 | ||||
|
SnTf(51)-MCM-41 | ||||
|
SnTf(18)-UVM-7 | ||||
|
SnTf(22)-MCM-41 | ||||
|
SnTf(47)-MCM-41 | ||||
|
SnTf(51)-MCM-41 | ||||
|
SnTf(18)-UVM-7 |
Conditii de reactie: raport molar substrat/agent de acilare= 1/3, 15 mg catalizator, 2h, 1-4=temperatura camerei, 1-4*-temperatura 80ºC, 4 ml de AcCN, S2 - selectivitatea in 2-acetiltiofen, S3 - selectivitatea in 3-acetiltiofen, C - conversia.
Asa cum se observa din Tabelul 7, cele mai ridicate conversii (85-99%) la temperatura camerei s-au obtinut in prezenta probelor SnTf(22)-MCM-41 si SnTf(18)-UVM-7, ambele caracterizate de un raport Si/Sn scazut. In acelasi timp selectivitatea la produsul de interes 2 (Schema 5) a fost foarte ridicata (99%) indiferent de natura catalizatorului. Acest nivel ridicat de selectivitate a fost inregistrat si la 80C, conversiile pentru cei doi catalizatori SnTf(47)-MCM-41 si SnTf(51)-MCM-41 ridicandu-se la valori de 52-75%. Optimizarea conditiilor de reactie pentru aceste probe a facut posibila cresterea conversiei tiofenului la 83.5% in cazul utilizarii probei SnTf(47)-MCM-41, in solvent nepolar de tipul heptanului (Tabel 8).
Tabelul 8 Efectul solventului asupra performantelor catalitice in acilarea tiofenului cu anhidrida acetica
|
Nr. |
Catalizator |
Solvent |
C, % |
S2 , % |
S3 , % |
|
SnTf(47)-MCM-41 |
AcCN | ||||
|
THF | |||||
|
Heptan | |||||
|
CH2Cl2 | |||||
|
SnTf(51)-MCM-41 |
AcCN | ||||
|
THF | |||||
|
Heptan | |||||
|
CH2Cl2 |
Conditii de reactie: raport molar substrat/agent de acilare= 1/3, 15 mg catalizator, 80C, 2h, 4 ml de AcCN, tetrahidrofuran (THF), heptan si diclorometan (CH2Cl2) S2 - selectivitatea in 2-acetiltiofen, S3 - selectivitatea in 3-acetiltiofen, C - conversia.
Utilizarea tetrahidrofuranului face ca reactia sa nu aiba loc (sub 1%).
Datorita stabilitatii mult mai ridicate a acidului acetic fata de anhidrida acetica, reactiile de acilare realizate utilizand acest agent de acilare au necesitat conditii de reactie mai severe, precum temperaturi de reactie mai ridicate sau timpi de reactie mai indelungati (Tabel 9).
Tabelul 9. Acilarea tiofenului cu acidul acetic, in prezenta SnTf(22)-MCM-41
|
Nr. |
Catalizator |
C, % |
S2 , % |
S3 , % |
|
SnTf(22)-MCM-41* | ||||
|
SnTf(22)-MCM-41** | ||||
|
SnTf(22)-MCM-41*** | ||||
|
SnTf(22)-MCM-41**** |
Conditii de reactie: raport molar substrat/agent de acilare= 1/3, 15 mg catalizator, 2h la 120C*, 2h la 140C**, 4h la 140C***, 7h la 140C****, 4 ml de AcCN, reactiile s-au realizat in autoclava, S2 - selectivitatea in 2-acetiltiofen, S3 - selectivitatea in 3-acetiltiofen, C - conversia.
Asa cum se observa din Tabelul 9, in prezenta catalizatorului SnTf(22)-MCM-41, o crestere a temperaturii de la 120 la 140C determina cresterea conversiei de la 1 la 9.3% in timp ce selectivitatea la compusul de interes scade nesemnificativ (de la 100% la 99.1%). Pentru aceeasi temperatura de reactie (140C), cresterea timpului de reactie de la 2h la 7h duce la o crestere a conversiei pana la 96.4% in timp ce selectivitatea ramane la acelasi nivel (98.4%). Spre deosebire de fenol, reactia de acilare a tiofenului realizata la iradiere cu microunde, la 117ºC, nu a dus la nici un rezultat.
b) Acilarea furanului
Acilarea furanului decurge la fel de usor ca si acilarea tiofenului, atat la temperatura camerei cat si la 80ºC (Schema 6), cu agent de acilare - anhidrida acetica si in prezenta de catalizatori pe baza de triflat de staniu. Rezultatele obtinute sunt prezentate in Tabelul 10.
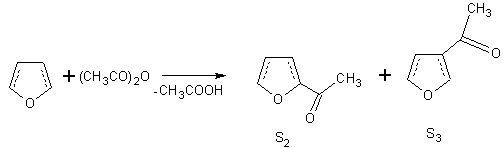
Schema 6. Acilarea furanului cu anhidrida acetica
Tabelul 10 Acilarea furanului cu anhidrida acetica, in prezenta catalizatorilor de triflat de staniu la temperatura camerei.
|
Nr. |
Catalizator |
C, % |
S2 , % |
S3 , % |
|
SnTf(22)-MCM-41 | ||||
|
SnTf(47)-MCM-41 | ||||
|
SnTf(51)-MCM-41 | ||||
|
SnTf(18)-UVM-7 |
Conditii de reactie: raport molar substrat/agent de acilare= 1/3, 15 mg catalizator, 2h, 4 ml de AcCN, S2 - selectivitatea in 2-acetilfuran, S3 - selectivitatea in 3-acetifuran, C - conversia.
Asa cum se observa din Tabelul 10, in prezenta catalizatorului cu structura bimodala SnTf(18)-UVM-7, reactia decurge cu conversie aproape totala (99.9%), in timp ce in prezenta probelor cu structura unimodala si continut scazut de triflat de staniu reactia decurge cu conversii de doar 45-50%. In acelasi timp, ca si in cazul acilarii tiofenului, selectivitatea in produsul principal de reactie este foarte ridicata (98-100%), indiferent de natura catalizatorului (cantitate de triflat de staniu sau structura poroasa).
Ca si in cazul acilarii tiofenului, solventul utilizat influenteaza performantele catalitice (Tabel 11).
Tabelul 11. Influenta solventului asupra performantelor catalitice, in acilarea furanului cu anhidrida acetica, la temperatura camerei
|
Nr. |
Catalizator |
Solvent |
C, % |
S2 , % |
S3 , % |
|
SnTf(47)-MCM-41 |
AcCN | ||||
|
THF | |||||
|
Heptan | |||||
|
CH2Cl2 | |||||
|
SnTf(51)-MCM-41 |
AcCN | ||||
|
THF | |||||
|
Heptan | |||||
|
CH2Cl2 |
Conditii de reactie: raport molar substrat/agent de acilare= 1/3, 15 mg catalizator, 2h, 4 ml de solven (tetrahidrofuran, acetonitril, heptan, diclorometan); S2 - selectivitatea in 2-acetilfuran, S3 - selectivitatea in 3-acetifuran, C - conversia.
Asa cum arata Tabelul 11, cel mai indicat solvent pentru aceasta reactie pare sa fie unul de natura nepolara, precum heptanul. Astfel, reactiile realizate in acest solvent determina obtinerea unor conversii de 51-71%, cu selectivitati la compusul acilat urmarit de 100%, indiferent de natura catalizatorului. Ca si in cazul acilarii tiofenului inlocuirea acestui solvent cu unul puternic polar de tipul tetrahidrofuranului(THF), determina o scadere drastica a celor doua performante catalitice. Cu alte cuvinte, in prezenta acestui solvent conversia nu a depasit 3% in timp ce selectivitatea la compusul acilat in pozitia 2 nu depaseste 35%.
Concluzii
Studiul catalitic realizat arata ca intre cele doua clase de catalizatori exista diferente majore din punct de vedere a performantelor catalitice in reactiile de acilare. Astfel, daca probele pe baza de triflat de aluminiu nu sunt active si selective in astfel de reactii, triflatii de staniu sunt activi si selectivi in multe din astfel de reactii. Optimizarea conditiilor de reactie determina obtinerea unor conversii si selectivitati extrem de ridicate in prezenta acestor catalizatori. Astfel, chiar in acilarea cu agent de acilare - acid acetic, reactia poate decurge cu conversii si selectivitati de 98-100%.
Rezultatele obtinute au fost acceptate pentru publicare in Topics in Catalysis:
- Natalia Candu, Simona Coman, Vasile I. Parvulescu, Jamal El Haskouri, Pedro Amoros, Daniel Beltran, "Metal Triflates Incorporated in Mesoporous Catalysts for Green Synthesis of Fine Chemicals", acceptat in Topics in Catalysis (2008).
BIBLIOGRAFIE
Bauer K., Garbe D. Common Fragrance and Flavor Materials, VCH Publishers, Weinheim, p.73, 1985.
Chaudhari R.V., B.M. Bhanage, R.M. Desplande, H. Delmas, Nature 373, p. 501, 1995.
Olah, G.A, ²Friedel-Crafts and Related Reactions² , Willey, New York , 1964.
Kouvenhoven, H.W, and Van Bekkum, H., in ²Handbook of Heterogeneous Catalysis² , G.Ertl, Knozinger, and J. Weitkamp Eds., vol. 5, p.2358, Willey, New York , 1997.
Van Bekkum, H. Hoefnagel, A.J., van Koten, M.A. Gunnewegh, E.A. Vogt, A.H., A.H.G and Kouwenhoven, H.W, in ²Zeolites and Micropourous Crystals ² (T.Hattori and T.Yashima Eds.), Studies Surface Science Catalysis, vol.83, p. 379. Elsevier, Amsterdam 1994.
Kobayashi S., Synletters, p. 689, 1994
Nishioka T., S. Tanaka, O. Yamashita, T. Ozawa, M. Kohama, US Patent 5,907,048 to Kao, CA: 128-257332n, 1999.
Kobayashi O., N. Hashizume, Japanese Patent 98,087549 to Kao, CA: 128-257234g, 1998.
S. Ratton, "Heterogeneous catalysis in the fine chemicals industry", Chem. Today 3/4 p. 33-37, 1998.
Harvey, G., and Mader, G., ²Collect. Czech. Chem. Commun. ² , p. 862, 1992.
Yadav, G. D., and Krishnan, M. S., ²Chem. Eng. Sci. ² , p.4189, 1999.
Harvey, G., Binder, G., and Prins, R., ²Stud. Surf. Sci. Catalysis ² , p.397, 1995.
Heinichen, H. K., and Holderich, W. F., J. Catal. 185, p. 408, 1999.
Anderson K.W. and J.J. Tepe, Tetrahedron Lett., , 58, p. 8475, 2002.
Kobazashi S., M. Sugiura, H. Kitagawaand W.W.L. Lam, Chem. Revue, 102, p. 227, 2002.
Bose A. K., Banik B. K., Lavlinskaia N., Jayaraman M., Manhas M. S. Chemtech. 27:18, 1997.
Loupy A. Microwaves in Organic Synthesis, Wiley-VCH, Weinheim, 2002.
Lidstrom P., Tierney J. P. Microwave Assisted Organic Synthesis, Blackwell. 2005.
Kappe C. O. Angew. Chem., Int. Ed. 43:6250, 2004.
Bogdal D., Lukasiewicz M., Pielichowski J. Green Chem. 6:110, 2004.
Loones K. T. J., Maes B. U. W., Rombouts G., Hostyn S., Diels G. Tetrahedron 61:10338, 2005.
Burczyk A., Loupy A., Bogdal D., Petit A. Tetrahedron 61:179, 2005.
Coman S. M., Pop G., Stere C., Parvulescu V. I., Haskouri J. El, Beltran D., Amoros P. J. Catal. 251:388, 2007.
S. Cabrera, J. El Haskouri, C. Guillem, J. Latorre, A. Beltrn, D. Beltrn, M.D. Marcos, P. Amors, Solid State Sci. 2 405, 2000.
S. Samanta, N.K. Mal, A. Manna, A. Bhaumik, Appl. Catal. A Gen. 273, 157, 2004.
Z.C. Liu, H.R. Chen, W.M. Huang, J.L. Gu, W.B. Bu, Z.L. Hua, J.L. Shi, Microporous Mesoporous Mater. 89, 270, 2006.
Das D., S. Cheng, Appl. Catalysis A: General 201, p.159, 2000.
Sheldon R.A., H. van Bekkum, in: ²Fine Chemicals through Heterogeneous Catalysis², Eds., Wiley-VCH, p. 1, 2001.
(a) Hachiya, I.; Moriwaki, M.; Kobayashi, S. Tetrahedron Lett., 36, p.409-412, 1995. (b) Hachiya, I.; Moriwaki, M.; Kobayashi, S. Bull. Chem. Soc. Jpn, 68, p. 2053-2060, 1995.
T. Yamaguchi, K. Tanabe, in: Proceedings of the 7th Sov.Yaponskii Seminar, Katal. Sb. Dokal, p. 22; Chem. Abstr. 102, 61886, 1983.
T.N. Shakhtakhtinski, A.M. Aliev, N.V. Biramov, R.Yu. Agaeva, R.M. Babaer, Azerb. Khim. ZR. 6 259; Chem.Abstr. 102, 61891, 1983.
Ertl G., Knozinger H., Schuth F., Weitkamp J. Handbook of Heterogeneous Catalysis, Vol. 7, WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim, 2008.
Kobayashi S., I. Hachiya, M. Araki and H. Ishitani, Tetrahedron Lett. 34, 1993, p. 3755; Kobayashi S., Synlett., 1994, p. 689; S. Kobayashi, Eur. J. Org. Chem., p.15, 1999.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 12579
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved