| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Coroziunea electrochimica
Datorita reactivitatii lor mari fata de componentii mediului ambiant, metalele pot trece relativ usor in alti compusi cu proprietati diferite, de cele mai multe ori inferioare din punct de vedere practic. Cand procesul are loc in mediu uscat intre metal si diferiti oxidanti in stare gazoasa, este numit coroziune chimica. Prezenta unei solutii de electrolit care contine componenti capabili de reactii de reducere, conduce la cuplarea reactiei de oxidare a metalului cu cea de reducere, prin formarea unei pile electrochimice. Se produce in acest caz o coroziune electrochimica. Coroziunea electrochimica reprezinta un ansamblu de procese fizico - chimice in urma carora metalele si aliajele acestora trec sub forma unor compusi metalici (oxizi, hidroxizi, saruri) ca urmare a formarii unor micropile in care metalul este supus oxidarii anodice in timp ce un component din solutie, numit depolarizant, sufera reactia complementara de reducere. Metalul trece in solutie sub forma de ioni cedand electronii retelei metalice pe care ii consuma depolarizantul.
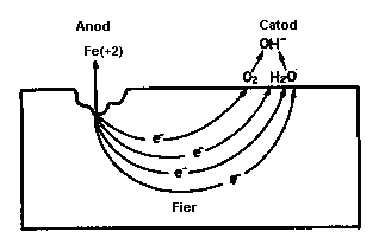
Figura 13. Micropila de coroziune a fierului
Avand in vedere caracterul neintentionat al formarii unor astfel de pile pe suprafata metalului, este firesc sa ne intrebam care este natura "electrozilor" responsabili de procesul electrochimic. In timp ce pentru o suprafata metalica ideala proprietatile locale trebuie sa fie identice in oricare punct, pe suprafetele reale exista o multitudine de neuniformitati determinate de prezenta unor impuritati, a unor neomogenitati de natura mecanica (adancituri, santuri, tensiuni diferite), a unor regiuni neechivalente (suprafata, muchie varf etc.), a unor diferente de compozitie sau de temperatura (rezultate ca urmare a unor fluctuatii locale). Un cuplu format din doua zone vecine cu proprietati diferite, poate deveni o micropila in prezenta unei solutii de electrolit. Deoarece metalul ramane in ansamblu neutru din punct de vedere electric, rezulta ca procesul anodic (de oxidare) si cel catodic (de reducere) au loc cu aceeasi viteza. Procesul global se desfasoara la un potential caracteristic fiecarui sistem, numit potential stationar, es, sau potential mixt. O reducere a vitezei unuia dintre procesele electrochimice (reducerea densitatii de curent) conduce la reducerea identica si a vitezei celuilalt proces. Rezulta ca procesul de coroziune poate fi franat fie de procesele anodice, fie de cele catodice.
O reprezentare simplificata a curbei de polarizare caracteristica procesului de coroziune electrochimica este redata in Figura 13.
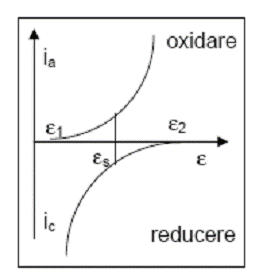
Figura 13. Diagrama de polarizare pentru coroziunea unui metal
Intelegerea mecanismului de coroziune electrochimica da posibilitatea proiectarii sistemelor de protectie anticoroziva. Dintre acestea cele mai utilizate sunt urmatoarele:
Acoperirea suprafetei metalice cu o pelicula de metal mai rezistent la coroziune (Cu, Zn, Ni, Cr, Ag etc.)
Acoperirea suprafetei metalice cu pelicule nemetalice izolante (polimerice, de oxizi cu structura compacta etc.)
Adaosul unor inhibitori de coroziune, substante cu proprietatea de a se adsorbi preferential fie pe centrii catodici, fie pe cei anodici. Consumul acestora este cu mult mai redus decat in cazul acoperirii cu pelicule compacte. Blocarea unui anumit fel de centrii reduce sau anuleaza valoarea curentului de coroziune.
Protectia catodica, prin care se leaga metalul intr-un circuit electric extern la o sursa de curent continuu. Cand metalul este catod, pe el nu mai pot avea loc reactii de oxidare. Anodul este un electrod inert cum ar fi de exemplu grafitul. Protectia catodica poate fi realizata si cu ajutorul "anozilor de sacrificiu". Anozii de sacrificiu (de exemplu Zn) sunt metale care se oxideaza mai usor decat metalul care trebuie protejat (de exemplu Fe), formand o pila in care se consuma anodul, atunci cand cele doua metale sunt legate direct si ambele vin in contact cu electrolitul. Pe catod au loc reactii de reducere ale depolarizantilor existenti in mediul coroziv.
Protectie anodica, prin care metalul de protejat este mentinut intr-o pila sub forma de anod, cand curentul conduce la formarea unei pelicule protectoare (pasivare). Procedeul implica riscuri mai mari intrucat deteriorarea locala a peliculei protectoare poate conduce la o coroziune accelerata datorata functiei sale de anod.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 2072
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2026 . All rights reserved