| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
In acest capitol vom aborda echilibrele sistemelor Me - S - O - C - H, pentru a intelege procesele fizico-chimice prin care metalele grele, existente sub forma de minerale (sulfuri), ajung sa intre in ecosistem, si sa produca poluarea acestuia.
Asadar, vom discuta posibilitatile de dizolvare a sulfurilor de Fe, Cu, Pb, Zn in conditii exogene, adica temperaturi de 25oC si 1 atm, si ce este mai important conditii de Eh > 0 si pH acid.
Numarul elementelor chimice care formeaza combinatii cu sulful este destul de mare, circa 40, dintre care sunt de mentionat Fe, Zn, Cu, Pb, Sb, Bi, Hg, Co, Ni, Co, Mo, s.a. Mai mult de 50% sulf este legat de Fe, pirita si pirotina fiind sulfurile cele mai raspandite in scoarta.
Sulfurile reprezinta minerale cu capacitate mare de alterare si deci cu implicatii majore in fenomenele generale de poluare in zonele miniere, respectiv in generarea mediilor acide. Compusii secundari formati prin alterarea acestor minerale vor influenta puternic migrarea elementelor metalice si a altor ioni. Dintre sulfurile de fier - pirita, marcasita si pirotina - sunt cele mai importante.

Diagrama Pourbaix Eh - pH pentru sulfurile de fier
Oxidarea ionului de fier bivalent la ionul trivalent este o reactie care se produce foarte incet la un pH mai mic de 4, in timp ce reactia de oxidare a Fe2+ de catre Fe3+ are loc mai rapid. Datorita reactiei lente de trecere a Fe2+ la o presiune partiala a oxigenului de 0,2 atm, raportul Fe2+ / Fe3+ este foarte ridicat desi mediul este puternic oxidant. Acest raport este controlat nu numai de oxigenul dizolvat, ci si de cinetica reactiilor si de activitatea bacteriilor.
Din diagrama Fe-S-O-H, la 25OC si 1 atm, observam comportarea si domeniile de stabilitate ale celor doua sulfuri de Fe: pirita si pirotina. Astfel, pirita se caracterizeaza printr-un domeniu de stabilitate foarte mare, pe un interval pH foarte larg ; contrar ei se comporta pirotina, al carei interval de stabilitate este restrans si la un pH mai mic de 10, caz destul de rar pentru mediile naturale exogene.
Diagrama Pourbaix, pentru sistemul Fe-C-O-H, indica un camp foarte larg de stabilitate a Fe(OH)3 care in prezenta sulfului din sistem este transformat in hematit, (Fe2O3). Prezenta sulfului in sistem va determina inlocuirea campului Fe2+ in cea mai mare parte, si a FeCO3 cu pirita.
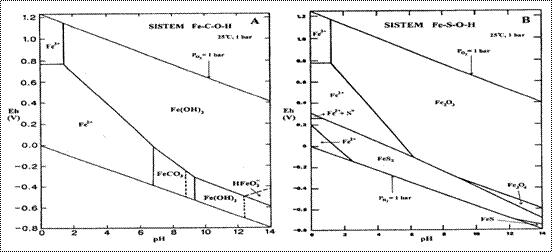
Diagrame Pourbaix la t, p
normale pentru sist. (A) Fe-C-O-H, (B) Fe-S-O-H,
(dupa Brookins, 1998)
Fierul trivalent este un oxidant puternic care determina oxidarea piritei intr-un ritm de zece ori mai rapid decat oxigenul; solubilitatea ionului feric creste cu descresterea pH-ului, de aici rezulta ca oxidarea sulfurilor de catre fierul trivalent devine importanta la pH acid. Studiul a relevat ca la un pH mai mic de 6, activitatea ionului feric este controlata de fazele sulfatice.

Diagrama Pourbaix Eh - pH pentru calcopirita
Diagrama Eh-pH la tempe-ratura de 25ºC indica prezenta ionului Cu2+ in domeniul acid pana la un pH de aproximativ 6,3. Peste aceasta valoare se formeaza malachit pana aproape de pH = 11 (Garrels si Christ, 1965).
Solutiile rezultate din alterarea calcopiritei contin concentratii ridicate de sulfat de cupru, care prin evaporare duc la cristalizarea calcantitului (CuSO4*5H2O), formandu-se mase compacte pamantoase sau cristale foarte fine, cu habitus tabular.
Extrem de rar, asociat cu produsii de alterare ai calcopiritei, se poate intalni sulful nativ. Acest fenomen apare in cazul in care procesul de alterare nu se desfasoara complet.
Diagrama Eh-pH, c.n., pentru sistemul Cu-S-O-H2O
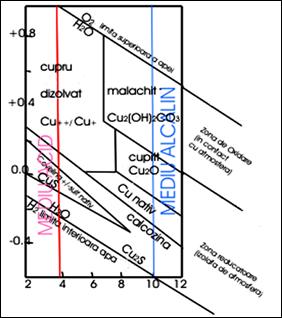
(dupa Garrels si Christ, 1965, cu completari).
Compusii comuni care se gasesc in efluentii proveniti de la haldele si iazurile de decantare - goethit FeO(OH), jarosit, etc. - pot reduce activitatea ionilor de cupru din solutie prin fenomene de adsorbtie; astfel la un pH neutru ionii de cupru sunt adsorbiti 100% pe suprafata acestuia. Cuprul, de asemenea poate coprecipita sau poate fi adsorbit de jarosit si goethit.

Diagrama Pourbaix Eh - pH pentru blenda
Alterarea sulfurilor cu apa oxigenata,
experienta realizata de
![]()
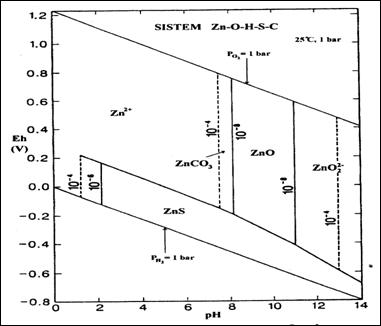
Diagrama
Pourbaix pentru sistemul Zn-O-H-S-C, c.n. (dupa Brookins, 1998).
Pentru reactia formata in conditii naturale ei au propus urmatoarea ecuatie:
![]()
In ambele cazuri Jennings et al.(2000) considera ca hidroliza Zn2+ este ras-punzatoare pentru producerea ionului H+.
Diagrama Pourbaix creata de Brookins, (1998), pentru o solutie cu Zn, O, H, S si C confirma prezenta ionului de zinc in solutie in conditii de pH si Eh variate. Radicalul Zn(OH)+ se formeaza la un pH cuprins intre 7 si 10. In acest interval, din concentratia totala de zinc, doar aproximativ 13% formeaza ionul Zn(OH)+ la pH = 8,5.

Diagrama Pourbaix Eh - pH pentru galena
Particulele aflate in suspensie in apa raurilor vor avea un rol important pentru transportul plumbului pe o distanta mai mare fata de sursa primara. In afara de adsortia pe suprafata particulelor aflate in suspensie, migrarea plumbului poate fi influentata si de substante organice cu rol de liganzi cu care acesta realizeaza complecsi solubili.
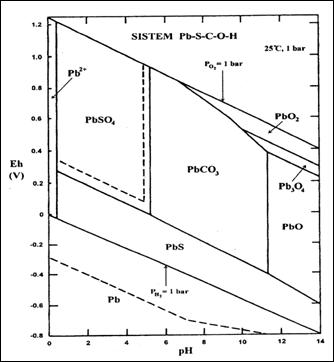
Diagrama Pourbaix pentru sistemul Pb-S-C-O-H, c.n.(dupa Brookins, 1998).
Migrarea pe distanta redusa a ionului liber Pb2+ este ilustrata si de diagrama Eh-pH, pentru o sistemul Pb-S-C-O-H Din diagrama prezentata se observa ca la un pH mai mic de 0,4 in solutie este prezent ionul de Pb2+, urmat de formarea anglezitului (PbSO4), care are solubilitate scazuta si conduce la precipitarea acestuia, la un pH cuprins intre 0,4 - 5, conform reactiei:
![]()
In intervalul de pH= 5 - 11, se formeaza carbonatul de plumb PbCO3 (ceruzit), dupa urmatoarea ecuatie:
![]()
In conditiile in care concentratia ionilor CO32- si SO42- este scazuta, domeniul de stabilitate a Pb2+ este mai mare (Brookins, 1998). Calculele termodinamice pentru o solutie apoasa, avand o concentratie a Pb2+ de 1mg/l, in absenta ionilor SO42- si CO32-, confirma activitatea ridicata a ionului liber de plumb, pana in apropierea pH-ului neutru. In domeniul acid, prin alterarea galenei, se formeaza anglezit. Acest mineral are produsul de solubilitate (Ksp) de valoarea 10-7,79, ceea ce indica o solubilitate scazuta. Formarea PbSO4 va impiedica hidroliza ionului Pb2+, in urma careia s-ar produce mediu acid, conform ecuatiei (Jennings et al., 2000):
![]()
Formarea PbSO4 va reduce activitatea ionului de plumb astfel incat, in apropierea domeniului bazic (peste valoarea pH-ului de 7,5), va exista o cantitate mica de plumb liber pentru a forma Pb(OH)2, si astfel nu se genereaza ioni de hidrogen, conform reactiei de mai sus.
Conform datelor lui Jennings et al.,( 2000) reactia de alterare a galenei in medii naturale se desfasoara dupa ecuatia:
![]()
Reactiile chimice care se desfasoara in decursul alterarii sulfurilor sunt mult mai complexe decat rezulta din reactiile chimice prezentate depind, in mare masura, de conditiile de mediu, de prezenta diferitilor ioni in solutie, precum si a diferitelor minerale care pot juca un rol tampon pentru solutiile acide.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 2475
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved