| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Polarizarea electrozilor
Potentialul de echilibru (sau reversibil) al unui
electrod, ca si tensiunea electromotoare a unei pile formate din astfel de
electrozi, sunt masurate in conditiile in care reactiile de electrod, de
oxidare si de reducere, au viteze egale. La fiecare electrod, curentul anodic este
egal cu cel catodic (in valoare absoluta), iar suma lor algebrica (curentul
net) este nula. Electrodul, ca si pila, nu este traversat de un curent electric
semnificativ. S-a observat ca trecerea unui curent electric prin sistem conduce
la modificarea potentialelor de electrod si, in consecinta, si a tensiunii
electromotoare a unei pile. Pentru a diferentia cele doua situatii, vom nota cu
indicele "r" starea de reversibilitate si cu indicele "I" starea in care
electrodul este traversat de curentul I: er si eI , sau Er si EI . Fenomenul apare atat in cazul generarii chimice a
curentului electric intr-o pila, cat si in cazul electrolizei, cand trecerea
curentului electric induce transformari chimice si poate fi exprimat in forma
concisa: ![]() si
si ![]() . Mai mult, s-a gasit ca
pentru debitare de curent EI < Er , iar pentru electroliza EI > Er . Aceste rezultate nu pot fi explicate pe baza
proprietatilor termodinamice ale sistemului. O explicatie satisfacatoare a fost
oferita pe baza analizei cineticii proceselor de electrod. Totalitatea
proceselor care contribuie la aparitia diferentelor mentionate a fost numita
polarizarea electrozilor, iar diferenta dintre cele doua potentiale este numita
supratensiune.
. Mai mult, s-a gasit ca
pentru debitare de curent EI < Er , iar pentru electroliza EI > Er . Aceste rezultate nu pot fi explicate pe baza
proprietatilor termodinamice ale sistemului. O explicatie satisfacatoare a fost
oferita pe baza analizei cineticii proceselor de electrod. Totalitatea
proceselor care contribuie la aparitia diferentelor mentionate a fost numita
polarizarea electrozilor, iar diferenta dintre cele doua potentiale este numita
supratensiune.
Cand zona de separatie conductor electronic/conductor ionic este traversata de un curent electric, procesul global este rezultatul unei serii de etape consecutive dintre care cele mai importante sunt:
o transportul ionilor (sau al moleculelor neutre) intre cele doua faze prin migratia in campul electric sau/si prin difuzie
o adsorbtia/desorbtia speciilor chimice pe suprafata electrodului, insotite de fenomene de desolvatare/solvatare
o transferul de electroni (procesul redox)
o reactiile chimice secundare care preced sau urmeaza transferul de electroni
o formarea unor faze noi (cristaline, gazoase) care necesita un aport suplimentar de energie.
Dupa cum s-a vazut la studiul vitezei proceselor consecutive, intr-o succesiune de etape, una poate deveni limitativa, franand viteza procesului global. Pentru a asigura viteza dorita a procesului global este necesar consumul unei energii suplimentare. Fenomenele cele mai cunoscute care conduc la aparitia supratensiunii la electrozii strabatuti de un curent electric sunt pierderile ohmice (datorate caderilor de tensiune pe rezistentele celor doua tipuri de conductori) si polarizarea. Pentru procesul de generare chimica a curentului electric tensiunea pilei la curentul nominal I este: EI Ereversibil Eohmic Epolarizare , iar pentru electroliza: EI Ereversibil Eohmic Epolarizare
Pentru un acumulator, care poate functiona in ambele regimuri (electroliza la incarcare si generator de curent la descarcare), curba curent - tensiune arata (calitativ) ca in Figura 8.
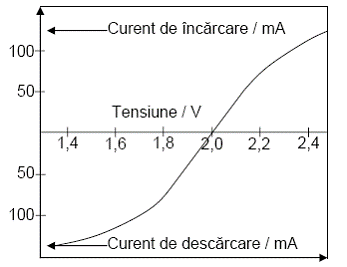
Figura 8. Curba de polarizare a unui acumulator cu plumb
Se observa ca, pentru curent zero, tensiunea reversibila este ≈ 2 V. La incarcare, pentru a creste curentul, este necesara o crestere a tensiunii externe aplicate. La descarcare, cu cat curentul debitat este mai mare, cu atat tensiunea pilei este mai mica.
O analiza stiintifica a acestor fenomene se bazeaza pe studiul curbelor densitate de curent - tensiune. Densitatea de curent reprezinta intensitatea curentului raportata la suprafata electrodului (i I S) si este o masura a vitezei globale a proceselor de electrod: i zF vR S , unde vR S este viteza reactiei raportata la suprafata electrodului.
Curba de polarizare, reprezentand densitatea de curent in functie de potentialul electrodului, este ilustrata detaliat in Figura 9. In ceea ce priveste alegerea semnului curentului electric exista doua posibilitati, egal folosite in literatura de specialitate. In exemplul prezentat s-a considerat, in mod conventional, ca sensul curentului anodic este cel pozitiv, iar cel al curentului catodic este cel negativ. Valoarea potentialului pentru care cei doi curenti, anodic si catodic, sunt egali si de semn contrar (avand valoarea comuna i0), este egala cu valoarea potentialului reversibil de electrod, er . Pentru o valoare oarecare e > er, curentul anodic este mai mare decat cel catodic si electrodul este strabatut de un curent net anodic, cand reactia de oxidare este preponderenta. Supratensiunea anodica este data de
ha =e -er >
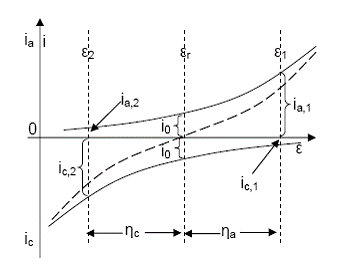
Figura 4.9. Curba de polarizare a unui electrod
Pentru o valoare a potentialului e > er, curentul catodic este mai mare (in valoare absoluta) decat cel catodic si electrodul este strabatut de un curent net catodic, cand reactia de reducere este preponderenta. Supratensiunea catodica este data in acest caz de ha =e -er <
Pentru o pila electrochimica, in care un electrod este anod iar celalalt catod, tensiunea electromotoare in regim de debitare a curentului I este data de:
![]()
Deoarece hc < si ha > , rezulta ca EI < Er , asa cum s-a gasit si pe cale experimentala.
Polarizarea electrozilor poate fi datorata existentei unei etape limitative, sau actiunii combinate a catorva mecanisme posibile. Cele mai cunoscute mecanisme de polarizare sunt:
![]() polarizarea de concentratie, datorata aparitiei unui
gradient local de concentratie (concentratia de langa electrod este mai mica
decat cea din restul solutiei)
polarizarea de concentratie, datorata aparitiei unui
gradient local de concentratie (concentratia de langa electrod este mai mica
decat cea din restul solutiei)
![]() polarizarea electrochimica, datorata franarii procesului
cu transfer de electron
polarizarea electrochimica, datorata franarii procesului
cu transfer de electron
![]() polarizare la schimbarea de faza, datorata aportului
suplimentar de energie necesar la formarea unei faze noi (cristalizarea unui
metal, formarea unui gaz etc.)
polarizare la schimbarea de faza, datorata aportului
suplimentar de energie necesar la formarea unei faze noi (cristalizarea unui
metal, formarea unui gaz etc.)
![]() polarizarea de reactie, datorata vitezei reduse cu care
are loc o reactie care este implicata in procesele de electrod.
polarizarea de reactie, datorata vitezei reduse cu care
are loc o reactie care este implicata in procesele de electrod.
Componentii care reduc polarizarea sunt numiti depolarizanti si sunt utilizati la obtinerea unor curenti mai mari fara reducerea tensiunii electromotoare a pilei.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 2753
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2026 . All rights reserved