| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Racirea progresiva a solutiilor se soldeaza cu aparitia fazei solide care poate fi constituita din cristalele solventului pur, ale solvatului pur, din cristalele unui compus stoechiometric al solvatului cu solventul sau un amestec nestoechiometric de solvent solid si solvat.
Se considera cazul cand solventul pur in stare solida se
afla in echilibru cu solutia lichida. Cercetarile experimentale au aratat ca
solventul din solutie cristalizeaza la o temperatura mai mica Ts
decat solventul pur ![]() .
.
Scaderea temperaturii de solidificare a solutiei este proportionala cu concentratia molala a acesteia b2:
![]() (5.60)
(5.60)
unde: ![]() = temperatura de solidificare (topire) a solventului pur;
= temperatura de solidificare (topire) a solventului pur;
Ts = temperatura de solidificare (topire) a solutiei;
Ks = constanta crioscopica (scaderea crioscopica molala);
b2 = concentratia molala a solutiei.
Relatia (5.60) se numeste ecuatie crioscopica.
Ecuatia (5.60) se fundamenteaza termodinamic plecand de la conditia de echilibru dintre potentialul chimic al solventului solid pur ( 1p) si potentialul chimic al solutiei (solventului in solutie) ( 1s
1p 1s (5.61)
respectiv
![]() (5.62)
(5.62)
deoarece in stare
solida pura ![]() .
.
Deci:
![]() (5.63)
(5.63)
Introducand in ecuatia Gibbs-Helmholtz (5.24) pe ![]() din relatia (5.63), se obtine:
din relatia (5.63), se obtine:
![]() (5.64)
(5.64)
unde: Ht = caldura latenta molara de topire; Ht > 0;
Hs = caldura latenta molara de solidificare;
Hs = - Ht; Hs < 0.
Considerand Ht constant, separand variabilele si integrand ecuatia (5.64):
![]() (5.65)
(5.65)
se obtine:
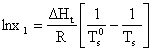 (5.66)
(5.66)
respectiv
![]() (5.67)
(5.67)
considerand ca ![]() ≈ Ts.
≈ Ts.
Inlocuind ln(1 - x2) cu -x2, relatia (5.67) devine:
![]() (5.68)
(5.68)
Din ecuatia (5.68) rezulta:
![]() (5.69)
(5.69)
Tinand cont de relatiile (5.53) si (5.55), ecuatia (5.69) devine:
![]() (5.70)
(5.70)
unde:
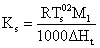 (5.71)
(5.71)
Ks depinde numai de natura solventului. Relatia (5.70) coincide cu ecuatia crioscopica (5.60).
Relatia (5.70) permite calcularea masei moleculare a solvatului M2 daca se cunosc Ks si Ts:
![]() (5.72)
(5.72)
Dispozitivul experimental folosit pentru masurarea diferentei Ts se numeste crioscop.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 2789
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved