| CATEGORII DOCUMENTE |
| Aeronautica | Comunicatii | Electronica electricitate | Merceologie | Tehnica mecanica |
PREPARATE ENZIMATICE SI ENZIME IMOBILIZATE
Preparatele enzimatice si de enzime imobilizate folosite in realizarea diferitelor procese biotehnologice din industria alimentara sunt considerate ca adjuvanti de transformare. In anul 1982, Comitetul mixt FAO/OMS de experti in aditivi alimentari a stabilit o serie de "norme generale pentru preparatele enzimatice utilizate in prepararea alimentelor'. Conform acestui comitet, preparatele enzimatice, folosite ca aditivi in industria alimentara, sunt obtinute din materii prime de origine animala, vegetala sau microbiana, fiind constituite din celule intregi, din parti de celule sau extracte complet lipsite de celule. Pot contine una sau mai multe componente enzimatice active, suporturi, solventi, agenti de conservare, antioxidanti si alte substante necesare si conforme unei bune practici de fabricare. Ele se pot prezenta sub forma lichida, semilichida, uscate sau imobilizate, avind o culoare care poate sa varieze de la qvasi incolor la brun inchis.
In ceea ce priveste materiile prime din care sint obtinute preparatele enzimatice, normele Comitetului mixt FAO/OMS prevad ca:
- tesuturile de origine animala sa raspunda normelor veterinare aplicate carnii si manipularea lor sa satisfaca exigentele unei bune practici igienice;
- materialele de origine vegetala, folosite ca surse de enzime sau ca ingrediente in prepararea mediilor de cultura pentru microorganismele producatoare de enzime, trebuie sa nu elibereze nici un reziduu nociv pentru sanatate, in conditii normale de utilizare;
- preparatele enzimatice de origine microbiana trebuie produse prin folosirea controlata fara penetrare de microorganisme susceptibile de a conduce la aparitia de substante toxice sau alte produse nedorite.
In cazul preparatelor de enzime imobilizate, in care insolubilizarea enzimei se realizeaza prin procedee fizice si/sau chimice, suportul si in special agentul de imobilizare folosit trebuie sa fie inert sau admis de a fi utilizat in produsele alimentare, iar orice eliberare de enzima de pe suport, si mai ales eliberarea de agent de imobilizare, trebuie sa ramina in limitele acceptabile care vor fi precizate pentru fiecare preparat enzimatic imobilizat.
Aditivii (inclusiv adjuvantii de transformare) si ingredientele care intervin in producerea preparatelor enzimatice trebuie sa fie substante acceptate pentru a fi utilizate in produsele alimentare ca: apa, substante insolubile care pot fi indepartate o data ce s-a produs procesul de transformare.
Limitele si metodele de determinare a componentelor contaminante ale preparatelor enzimatice folosite in industria alimentara sint aratate in tabelul
Limite si metode de determinare pentru componentele contaminante,
recomandate de Comitetul mixt FAO/OMS (Etude FAO: Alimentations et Nutrion, 19/1982)
|
Componente contaminante ale preparatelor enzimatice |
Limite admisibile |
Metodele de determinare recomandate sint publicate in: |
|
Arsen Plumb Metale grele |
Maximum 3 mg/kg Maximum 10 mg/kg Maximum 40 mg/kg (exprimate ca plumb) |
Me'thodes Generales (Directives Generales pour l'usage des normes IECFA d'identite et de purete) |
|
Numar total de germeni viabili Coliformi |
Maximum 5. 1O4 /g Maximum 30/g |
Microbiologic - Directives generales pour le denombrement de microorganisme Directives generales pour le denombrement des coliformes Methode par le comptage de colonies obtenues à 30C. ISO. Norme internationale Ref. nr. ISO 4833, Premier Edition (1978-02-01) |
|
Escherichia coli Salmonclla |
Absent pe o proba de 25 g Absent pe o proba de 25 g |
FDA - Bacteriogical Analvtical Manual - Fifth Edition ( 1978) Cap. X. Enteropathogenic Escherichia coli ; Cap. XII. Isolaion and identification of Salmonella |
|
Activitatea antibiotica de origine bacteriana |
Absenta |
Etude FAO: Alimentation et Nutrition, 19/1982; Appendice A |
Preparate enzimatice
Preparatele enzimatice folosite in industria alimentara trebuie produse in conditii similare unei bune practici de fabricare a produselor alimentare, iar prin utilizarea lor sa nu se ajunga la o crestere a numarului total de germeni (NTG) si la cresterea continutului in saruri peste limitele admise pentru un anumit produs alimentar luat in considerare.
Pentru obtinerea preparatelor enzimatice sunt folosite de obicei surse bogate in enzimele dorite, care sunt ieftine, usor accesibile si care se prelucreaza usor. Aceste surse pot fi de origine vegetala, animala sau microbiana. In plante, concentratii mari de enzime se pot intalni in seminte, cereale germinate sau negerminate, radacini, seva si latexuri, frunze si in unele cazuri chiar in coaja.
La animale, concentratii mari de enzime se gasesc in special in ficat, pancreas, mucoasa stomacala sau intestinala, inima, rinichi, creier etc. In scopuri practice sunt folosite mai ales pancreasul, mucoasa stomacala si intestinala.
O sursa foarte importanta de enzime, pentru producerea preparatelor enzimatice, o constituie diferitele microorganisme ca: bacteriile, drojdiile si microciupercile (mucegaiurile). Fata de sursele de enzime de origine vegetala sau animala, culturile diferitelor microorganisme prezinta o serie de avantaje care explica in mare masura tendinta manifestata in ultimele 2-3 decenii de a fi folosite din ce in ce mai mult pentru obtinerea de preparate enzimatice. Microorganismele pot fi obtinute in cantitati mari, prin inmultire in instalatii speciale, pe medii de cultura ieftine (de obicei subproduse ale industriei alimentare ca: tarite de griu, extract de porumb obtinut prin concentrarea apelor de inmuiere de la fabricarea amidonului, melasa, sroturi de soia si de floarea-soarelui etc.).
Ciclul de crestere si dezvoltare al microorganismelor este foarte scurt fata de cel al plantelor si animalelor, iar obtinerea microorganismelor in cantitati mari nu necesita angajarea de terenuri cultivabile, cum este cazul la materiile prime vegetale. In plus, microorganismele prezinta si avantajul ca productia lor de enzime poate fi mult marita prin selectarea si utilizarea de tulpini si mutante inalt productive precum si prin stabilirea conditiilor fizice si chimice optime (medii de cultura si conditii optime de cultivare) pentru producerea de enzime.
In cazul utilizarii microorganismelor ca surse de enzime pentru industria alimentara, selectarea acestora se va face luindu-se in considerare o serie de criterii cum sint urmatoarele: sa nu manifeste putere patogena si sa nu produca toxine (endo-, exotoxine sau micotoxine), sa nu manifeste activitate antibiotica sau potential alergen si sa produca cu precadere si in cantitati mari enzima sau complexul enzimatic dorit, pe medii de cultura ieftine si in conditii avantajoase.
Indiferent de sursa de materii prime, prelucrarea lor pentru obtinerea de preparate enzimatice de uz alimentar este in linii generale aceeasi (fig. 4).
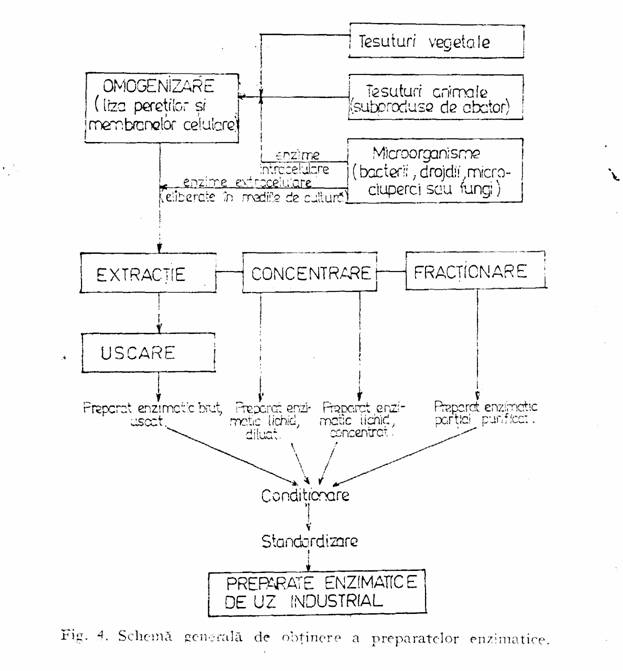
Enzimele obtinute ca preparate brute sau partial purificate, sub forma lichida, semilichida sau uscata sunt utilizate in industria alimentara ca atare, fiind adaugate si actionind in mediile pe care urmeaza sa le transforme ca enzime "libere', respectiv solubilizate in medii apoase si fara a mai putea fi ulterior recuperate. Activitatea lor, dupa ce au realizat transformarile dorite, este de obicei oprita prin diferite tratamente, mai ales pe cale termica, prin acidulare sau alcalinizare. In unele cazuri ele mai ramin active si in produsul finit.
Preparate enzimatice imobilizate
Principiul general al procedeelor de imobilizare a enzimelor consta in legarea sau fixarea unei enzime sau a unui sistem multienzimatic de suportul insolubil in apa, in conditiile pastrarii proprietatilor catalitice, respectiv specificitatea de actiune si posibilitatea de a actiona la pH si temperatura asemanatoare enzimelor libere (neimobilizate).
Suporturile sau matricile utilizate in imobilizarea enzimelor pot fi de natura anorganica: silicea coloidala, caolinita, particule sau perle de sticla cu grad de porozitate controlat, oxizi metalici (alumina, oxid de zirconiu, oxid de titan, carbune etc.), si de natura organica: celuloza si derivatii acesteia, agaroza, amidon, dextran, colagen, polimeri obtinuti prin polimerizarea unor monomeri de tipul acrilamida, acid metacrilic s.a., rasini formaldehidice etc.
In functie de natura legaturilor care se stabilesc intre enzime si suportul de imobilizare, procedeul sau metodele de imobilizare pot fi fizice sau chimice.
Procedeele fizice se bazeaza pe imobilizarea enzimelor prin intermediul legaturilor fizice ca de exemplu, interactiuni electrostatice, formarea de legaturi ionice, formarea de legaturi de hidrogen, interactiuni proteina-proteina etc., diferentiindu-se in acest sens (fig. 5.):
- adsorbtia pe suporturi insolubile in apa (carbune, clei, rasini schimbatoare de ioni, celuloza, sticla etc.) ;
- includerea in structuri macromoleculare (aceasta incluziune se realizeaza prin polimerizarea unor materiale ca poliacrilamida in silicagel, amidon, in prezenta moleculelor de enzima, astfel incit se formeaza o matrice de polimer in care sint incluse moleculele de enzima si in care atit substratul cit si produsul poate sa difuzeze) ;
- microincapsulare in membrane semipermeabile ;
- imobilizarea in celule de ultrafiltrare.
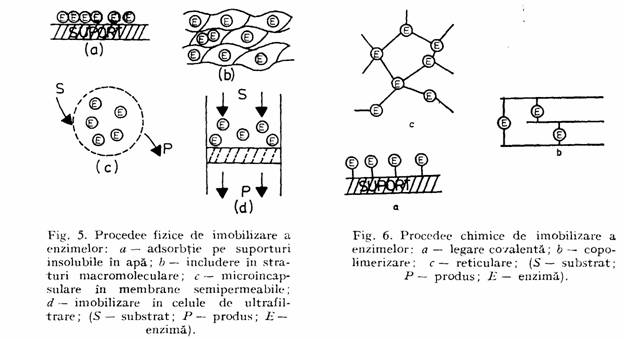
Procedeele chimice de imobilizare a enzimelor se refera la cele care conduc la formarea de legaturi covalente sau partial covalente, intre gruparile functionale, care insa nu sint esentiale pentru manifestarea activitatii catalitice (nu sint implicate in situsul catalitic al enzimei), si un suport activat chimic, insolubil in apa. In cadrul acestor procedee se pot evidentia (fig. 6):
- legarea covalenta a enzimelor de suporturi insolubile, care poseda grupari reactive sau care pot fi activate prin diferite reactii chimice;
- copolimerizarea enzimelor cu un monomer reactiv si legarea incrucisata (cross-linking) sau reticulara intra- si intermoleculara a enzimelor legate de un suport cu un reactiv multifunctional. La imobilizarea enzimelor trebuie sa se aiba in vedere urmatoarele: conformatia spatiala a moleculelor de enzima in sistemul imobilizat este diferita de cea a mediului natural din care s-a extras enzima. Pe de alta parte, structura tridimensionala a moleculei de enzima este distorsionata de legaturile sale cu suportul; micromediul moleculei de enzima imobilizat este diferit de cel al enzimei aflate in solutie, afectindu-se viteza de difuzie a substratului si a produsilor de reactie. Inhibitia de substrat si de produs poate, de asemenea juca un rol important; procesul de transport al substantelor este un proces pasiv, in comparatie cu situatia enzimei din celula vie, iar aceasta va avea desigur influenta si asupra vitezei de reactie.
Imobilizarea enzimelor pe un suport anorganic sau organic provoaca schimbari in comportamentul acestora si in cinetica reactiilor: se mareste stabilitatea enzimei (stabilitatea enzimei atit in stare statica cit si in stare dinamica fiind influentata de procedeul de imobilizare, masura acestei stabilitati fiind 1/2 din durata de viata a enzimei); se schimba afinitatea enzimei fata de substrat, aceasta fiind influentata de durata lor de contact care, la rindul ei, este determinata de viteza fluxului sau viteza de agitare a substratului in contact cu sistemul suport-enzima, de viteza de difuzie a substratului la enzima imobilizata; se modifica caracterul catalizei prin trecere de la cataliza omogena la cea eterogena.
La folosirea enzimelor imobilizate poate avea loc o variatie a pH-ului optim iar randamentul in produsul de transformare este micsorat. De exemplu, prin folosirea amiloglucozidazei in solutie, plecind de la o suspensie de amidon cu 33% s.u., se ajunge la un randament de transformare in glucoza de 95,5- 96%, in timp ce la folosirea amiloglucozidazei imobilizate, randamentul este de 92-93%.
In orice caz, preparatele de enzime imobilizate, fata de cele libere sau solubile, prezinta o serie de avantaje printre care se amintesc urmatoarele:
- refolosirea repetata a enzimei, cu aceeasi cantitate de enzima putandu-se transforma cantitati mai mari de substrat;
- se poate lucra in sistem semicontinuu sau continuu, cu automatizarea procesului, ceea ce asigura un control precis al parametrilor de lucru ;
- are loc o crestere a vitezei de lucru, prin controlul riguros al vitezei fluxului de substrat si al concentratiei acestuia;
- se poate stopa reactia enzimatica la momentul dorit si se evita trecerea enzimei in produsul transformat ;
- costurile globale de productie sunt mai mici in comparatie cu procedeele de folosire a enzimelor libere ;
- se pot utiliza si enzime care nu sunt trecute pe lista GRAS (Generally Recognised as Safe).
Factorii critici ce trebuie luati in considerare la folosirea enzimelor imobilizate sint urmatorii:
- eficienta economica a imobilizarii determinata de costul enzimei, suportului si metoda de imobilizare;
- activitatea enzimei imobilizata care este in functie de tehnica de imobilizare, caracteristicile materialului de suport, viteza de difuzie a substratului la enzima si a produsului de transformare.
- caracteristicile substratului ce trebuie transformat ;
- stabilitatea enzimei care trebuie mentinuta un timp cat mai indelungat ;
-contaminarea microbiologica a sistemului enzima-suport in timpul utilizarii reactorului respectiv.
Cu toate avantajele pe care le prezinta enzimele imobilizate, pina in prezent, industria alimentara utilizeaza la nivel industrial numai glucozizomeraza imobilizata pentru izomerizarea glucozei in fructoza si lactaza imobilizata pentru hidroliza lactozei din lapte sau zer. Sunt efectuate insa o serie de cercetari la nivel de laborator si chiar la nivel pilot, care permit sa se intrevada in viitor extinderea folosirii preparatelor de enzime imobilizate si in alte sectoare ale industriei alimentare; in acest sens, sunt insa necesare cercetari care sa conduca, probabil, la modificarea sau adoptarea unor tehnologii "clasice' de obtinere a diferitelor produse alimentare, la utilizarea preparatelor de enzime imobilizate sau la stabilirea de noi tipuri de bioreactoare si eventual noi moduri de folosire a enzimelor imobilizate in medii eterogene, consistente si viscoase de felul celor prelucrate intr-o serie de sectoare ale industriei alimentare.
3 Enzime de fermentatie
Cea mai importanta problema care trebuie rezolvata la obtinerea de preparate enzimatice cu ajutorul microorganismelor este gasirea unui microorganism care sa produca in cantitate mare enzima sau sistemul enzimatic dorit. In acest caz un interes practic il reprezinta microorganismele heterotrofe.
Pentru ca un organism sa poata ataca un substrat si sa-l metabolizeze, el trebuie sa posede enzimele necesare care sa catabolizeze reactiile de metabolism in conditiile de mediu proprii pentru dezvoltare.
Totalitatea enzimelor pe care un organism le poseda in permanenta sau pe care poate sa le elaboreze la nevoie formeaza echipamentul enzimatic potential al microorganismului. Echipamentul enzimatic este determinat la randul lui de genetica microorganismului. Zestrea ereditara constituita din gene care sintetizeza enzimele microorganismelor variaza de la o specie la alta.
Majoritatea enzimelor care alcatuiesc echipamentul enzimatic sunt enzime intracelulare. Aceasta inseamna ca enzimele sintetizate de gene, dupa formare, raman in celula, nefiind secretate in mediul inconjurator in care microorganismele se dezvolta. Activitatea lor se desfasoara in interiorul celulei. Unele microorganisme cum sunt drojdiile, bacteriile lactice, nu contin decat enzime intracelulare. La astfel de microorganisme eliberarea enzimelor in mediul inconjurator are loc dupa moartea celulelor, in urma proceselor de autoliza. Din acesta cauza, astfel de microorganisme nu metabolizeaza decat substraturi nutritive solubile si permeabile prin membranele lor celulare.
Alte microorganisme, asa cum sunt bacteriile din genul Baccillus sau fungii din genul Aspergillus, elaboreaza pe langa un mare numar de enzime intracelulare si enzime extracelulare, pe care le secreta in mediul inconjurator. Enzimele extracelulare sunt, in general hidrolaze si sunt secretate de microorganisme cu scopul de a degrada substraturile insolubile si solubile cu molecule mari la compusi solubili usor asimilabili.
Enzime intracelulare de fermentatie
In categoria enzimelor intracelulare sunt incluse toate enzimele care raman cu biomasa dupa separarea lichidului de fermentatie. Unele enzime se acumuleaza probabil in periplasma, astfel incat in mediul de cultura se afla cantitati mici de enzime rezultate din ruperea peretilor unui numar mic de celule. Principalele tipuri de enzime intracelulare sunt prezentate in tabelul urmator:
|
Enzima |
Microorganismul producator |
Durata Fermentatiei, h |
Nivelul de productie |
|
Penicillinacilaza |
Escherichia coli |
Laborator 100 l |
|
|
α - Galactozidaza |
Mortierella vinacea Saccaromyces cerevisiae |
Laborator Laborator |
|
|
Glucozizomeraza |
Streptomyces albus Streptomyces sp. |
Laborator Laborator |
|
|
Glucozoxidaza |
Pergillus niger |
500l |
|
|
Pullulanaza |
Klebsiella aerogenes |
15 l |
|
|
Lactaza |
Candida pseudotropicalis |
Laborator |
Majoritatea acestor enzime actioneaza asupra unor substraturi cu masa moleculara mica. Aceasta se explica prin faptul ca substraturile mici pot patrunde in celule si functioneaza astfel ca inductori ai enzimelor care le degradeaza. Spre deosebire de acestea, enzimele extracelulare actioneaza asupra substraturilor cu masa moleculara mare.
Enzimele intracelulare se impart in doua mari categorii: unele au o pozitie centrala in metabolismul organismului in crestere si se produc in cantitati mari in biomasa, altele au un rol secundar, minor si se produc in cantitati mici. Pentru utilizarea acestora din urma in scopuri industriale este necesara imobilizarea lor, astfel incat sa fie economica si justificata folosirea lor.
In ceea ce priveste activitatea enzimatica a acestor preparate, de cele mai multe ori constituie un secret de serviciu, deoarece poate face oricand obiectul unui brevet de inventie. Pentru ca o enzima sa fie economica, ea trebuie sa aiba o activitate enzimatica minima( 100 UE/ml). De aceea majoritatea enzimelor intracelulare la care nu se atinge acesta valoare se imobilizeaza. Alteori, aceste enzime se utilizeaza pentru atacul unor impuritati care incomodeaza procesul principal, dar fara atacul componentului principal. De exemplu, hidroliza enzimatica completa a amidonului presupune si hidroliza legaturilor α - 1,6 glucozidice, aflate in numar mic in structura amilopectinei.
Pullulanaza este folosita in acest caz pentru hidroliza legaturilor α - 1,6 facilitand in acest fel actiunea amiloglucozidazei si β- amilazei.
Glucozoxidaza este folosita pentru indepartarea urmelor de glucoza din praful de oua folosit la obtinerea maionezei si in acest caz nu trebuie sa aiba o activitate enzimatica mare.
Producerea enzimelor intracelulare ridica probleme specifice. Bioprocesul trebuie astfel condus incat pe parcursul biosintezei sa se evite spargerea celulelor. Un alt aspect se refera la stabilitatea enzimelor; unele enzime sunt stabile in mediul intracelular si devin instabile in afara celulei.
Unul dintre dezavantajele procedeelor de obtinere prin biosinteza a enzimelor intracelulare il constituie necesitatea eliberarii acestora din celule, prin distrugerea membranei celulare, extractie si ulterior separarea extractului de resturile celulare. In plus enzimele sunt impurificate cu toate proteinele intracelulare, chiar daca enzime dorita se afla in propertie mare in totalul proteinelor extrase din celule.
Un avantaj tehnologic al enzimelor intracelulare il constituie faptul ca extractia se poate efectua cu un volum mic de solutie tampon, ceea ce conduce la obtinerea unui extract brut cu continut mare de enzima si nu mai este necesara concentrarea ulterioara a acestuia.
Enzime extracelulare de fermentatie
Cele mai importante enzime microbiene extracelulare sunt, in general, hidrolazele( proteinaze, amilaze, celulaze) care actioneaza asupra substraturilor cu masa moleculara mare. Pentru microorganisme, este normal, din punct de vedere fziologic, sa produca nutrienti din polimeri biologici disponibili in mediul inconjurator celular.
Pentru a ataca mai usor substraturile, microorganismele isi produc singure enzimele necesare hidrolizei acestora si uneori aceasta productie de enzima este optima chiar la tulpinile salbatice.
Enzimele hidrolitice produse prin fermentatie si utilizate in cantitati mari in industrie sunt proteazele, amilazele, celulazele. Acestea sunt comercializate si utilizate in industria alimentara, textila, detergentilor.
Pentru ca productia unei enzime extracelulare utilizeaza in cea mai mare parte resursele diponibile ale celulei, biosinteza si secretia unei astfel de enzime sunt supuse unui complex de factori regulatori. In general, productia acestor enzime este indusa de niveluri reduse ale polimerilor, iar uneori polimerii insisi functioneaza ca inductori. Alteori, compusii care nu sunt substraturi pentru enzime, dar sunt inruditi ca structura cu acestea, pot functiona ca inductori. De exemplu, productia de celulaze este indusa atat de lactoza, cat si de celobioza. Productia acestor enzime este de asemenea supusa represiei prin cataboliti. Atata timp cat nutrientii cu masa moleculara mica sunt diponibili, celulele cresc fara sa produca hidrolaze si abia la epuizarea nutrientilor incepe biosinteza enzimelor hidrolitice extracelulare. Astfel, inductia si represia biosintezei enzimelor sunt fenomene complexe ce au loc in concordanta cu conditiile de mediu in care se gasesc celulele.
Trebuie retinut faptul ca factorii care determina inmultire si dezvoltarea celulei vor determina si declansarea biosintezei enzimelor. Un rol important in formarea enzimei il are existenta in mediul de cultura a substratului care induce formarea enzimei specifice degradarii respectivului substrat. El constituie inductorul operonului enzimei.
Primul studiu sistematic efectuat in aceasta directie a fost efectuat de Karstrm, care imparte enzimele in doua grupe: enzimele constitutive si enzimele adaptative.
Enzimele constitutive se sintetizeaza in celule in mod permanent. Concentratia lor este insa influentata de prezenta sau absenta in mediul de cultura a substraturilor pe care ele le metabilizeaza. Concentratia aceastor enzime poate sa varieze si sub influenta altor factori: sursa de azot, sursa de carbon, factorii de crestere, sarurile minerale, temperatura, pH-ul.
In schimb, sinteza enzimelor adaptative este declansata numai de prezenta substraturilor specifice in mediul de cultura sau atunci cand este nevoie de prezenta lor in procesele metabolice.
Pe baza unor studii indelungate si de profunzime cu privire la biosinteza enzimelor induse de substrat s-a ajuns la urmatoarele concluzii:
Elaborarea de catre un organism a unei enzime induse are loc numai in prezenta inductorului; ca inductor functioneza, de obicei, substratul care trebuie metabolizat; functia de inductor poate sa o indeplinesca si substantele inrudite structural cu acesta, dar care nu poate indeplini functia de substrat;
Biosinteza are loc pornind intotdeauna de la substante cu structura simpla;
Procesul de biosinteza decurge cu consum de energie si din acest motiv, pe langa substantele necesare sintezei(aminoacizi, vitamine, diferiti cationi) este nevoie in mediu si de o sursa de carbon, de obicei un glucid;
Sinteza enzimelor induse are loc, de regula, in timpul inmultirii microorganismului; ea poate sa aiba loc in faza stationara, daca sunt prezente inductorul si substraturile de sinteza;
Procesul de biosinteza al enzimelor este inhibat de toate substantele care inhiba biosinteza substantelor proteice, de exemplu cloramfenicolul;
Biosinteza enzimelor induse este inhibata ori de cate ori in mediul de cultura este prezent un substrat usor metabolizabil de catre enzimele constitutive ale microorgamismului;
Biosinteza unei enzime induse este inhibata selectiv si de metabolitii rezultati din reactiile de transformare ale inductorului, datorita activitatii acestuia; fenomenul se numeste represie;
4 Enzime microbiene cu aplicatii industriale. Domenii de utilizare
Principalele aplicatii ale enzimelor utilizate pe scara larga in ultimele 2 decenii sunt prezentate in tabelul urmator(Frost si Moss,1985):
|
Denumirea enzimei |
Industriile utilizatoare |
Tipul de fermentatie |
I Felul enzimei |
Forma de conditionare |
|
1.Enzime proteolitice |
||||
|
Enzime proteolitice alcaline bacteriene |
Detergenti Procese alimentare Pielarie |
Submers |
Extracelulare(Ex) |
Lichid(L) Solid(S) |
|
Enzime proteolitice bacteriene neutre |
Industria alimentara |
Submers |
Extracelulare(Ex) |
Lichid(L) |
|
Enzime proteolitice fungice |
Panificatie Industria branzeturilor |
Submers Submers in culturi de suprafata |
Extracelulare(Ex) |
Lichid(L) Solid(S) |
|
Enzime amilolitice |
||||
|
α -amilaze bacteriene |
Amidon, bere Detergenti, textile |
Submers |
Extracelulare(Ex) |
Lichid(L) Solid(S) |
|
α -amilaze fungice |
Amidon Panificatie |
Submers |
Extracelulare(Ex) |
Lichid(L) Solid(S) |
|
Amiloglucozidaze |
Amidon Bere |
Submers |
Extracelulare(Ex) |
Lichid(L) Solid(S) |
|
Pullulanaze |
Amidon |
Submers in culturi de suprafata |
Extracelulare(Ex) Intracelulare(In) |
Lichid(L) Solid(S) |
|
3. Alte glucozidaze |
||||
|
Lactaza(β-galactozidaza) |
Industria laptelui |
Submers in culturi de suprafata |
Extracelulare(Ex) Intracelulare(In) |
Lichid(L) Solid(S) |
|
Invertaza |
Industria textila |
Submers |
Intracelulare(In) |
Lichid(L) Solid(S) |
|
Rafinaza(α -galactozidaza) |
Rafinarea zaharului |
Submers |
Intracelulare(In) |
Imobilizata(Im) |
|
Celulaze |
Industria alimentara(sucuri) |
Submers |
Extracelular(Ex) |
Lichid(L) Solid(S) |
|
Β-1,3(4)-Glucanaze |
Industria berii |
Submers |
Extracelular(Ex) |
Lichid(L) |
|
Lipaze |
Industria alimentara Teste de diagnostic |
Submers |
Extracelular(Ex) |
Solid(S) |
|
Pectinaze |
Industria sucurilor si bauturilor alcoolice |
Submers in culturi de suprafata |
Extracelular(Ex) |
Lichid(L) Solid(S) |
|
4. Alte enzime |
||||
|
Glucozizomeraza |
Amidon |
Submers |
Intracelulare(In) |
Imobilizata(Im) |
|
Glucozoxidaza |
Industria sucurilor si bauturilor alcoolice Teste de diagnostic |
Submers |
Intracelulare(In) |
Lichid(L) Solid(S) |
|
Catalaza |
Industria sucurilor |
Submers |
Intracelulare(In) |
Lichid(L) Solid(S) |
|
Penicilinacilaza |
Antibiotice |
Submers |
Intracelulare(In) |
Imobilizata(Im) |
O analiza a pietei comerciale arata ca enzimele obtinute prin procese fermentative microbiene reprezinta aproximativ 80% din totalul productiei de enzime produse astazi in lume. Dintre celelelte enzime, obtinute prin extractie, necesitatile sunt acoperite de urmatoarele preparate: cheag de vitel, β-amilaza din orz, proteinaza pancreatica, etc.
Dintre enzimele de fermentatie cea mai mare cantitate o reprezinta proteinazele alcaline bacteriene utilizate in industria detergentilor.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 5683
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved