| CATEGORII DOCUMENTE |
| Alimentatie nutritie | Asistenta sociala | Cosmetica frumusete | Logopedie | Retete culinare | Sport |
Universitatea din
Facultatea de Stiinte
Master: Fizica Explorarilor si Terapiilor Biomedicale
PET
PET - CT
Capitolul I
Introducere
Tomografia pe baza de emisie pozitronica (PET) este una dintre cele mai moderne metode de obtinere a imaginii functionale in scop medical. Investigatiile PET combinate cu CT reprezinta, in zilele noastre, culmea tehnologiei de diagnostic, in tarile dezvoltate fiind considerate deja investigatii de rutina. Din pacate insa, investigatiile PET-CT nu sunt accesibile in Romania.
Descoperirea unei metode imagistice in vivo care sa permita "vizualizarea"
metabolismelor din organism a reprezentat o revolutie atat in medicina nucleara cat si in imagistica moleculara. Aceasta in conditiile in care cele patru elemente fundamentale ale materiei vii (C, H, O, N) nu poseda izotopi radioactivi ale caror proprietati fizice sa fie adaptate detectiei scintigrafice conventionale. In cazul a trei dintre aceste elemente exista,insa, radioizotopi care emit pozitroni (11C, 15O si 13N). Radioelementele mentionate au un timp de injumatatire foarte scurt (20 minute, 123 secunde si, respectiv, 10 minute) si se obtin cu ajutorul ciclotronului. Un alt element emitator de pozitroni, 18F (timp de injumatatire 120 minute), desi nu exista in organism, poate marca molecula de glucoza, al carei metabolism il poate face, astfel, "vizibil", detectabil cu ajutorul gamma camerei. Acestea sunt, de altfel, si principalele elemente radioactive utilizate de tomografia prin emisie de pozitroni (Positron emission tomography - PET).
Tomografia cu Emisie de Pozitroni / PET scan - este o metoda de Imagistica Medicala de ultima generatie, constituind modalitatea cea mai moderna de diagnostic. PET scan permite medicului sa examineze complet si dintr-o data corpul pacientului, prin producerea unor imagini ale fiziologiei, deci functionarii organismului, imagini imposibil de obtinut cu alte metode.
Acest mod de vizualizare infatiseaza metabolismul precum si alte functii importante, nu doar simpla structura anatomica a anumitor organe asa cum este revelata de clasicele examene radiologice .
Scanarea de tip PET este frecvent folosita pentru supravegherea periodica a posibilelor degenerari de tip malign; este un procedeu prin care se identifica celulele tumorale din organism. Este injectata intravenos o mica cantitate de glucoza (zahar) marcata radioactiv. Scaner-ul PET se va roti in jurul corpului si va capta imagini ale zonelor din organism unde glucoza este consumata. Celulele maligne vor aparea mai luminoase deoarece sunt mai active metabolic si folosesc mai multa glucoza .
Scanarea PET poate :
-diferentia tumorile maligne de cele benigne
-diferentia intre un nodul limfatic malign si unul benign
-detecta degenerarea maligna intr-un tesut cu aparenta anatomica normala
-evalua raspunsul la tratamentul anti canceros
-poate fi folosita pentru masurarea metabolismului cerebral.
Studiile stiintifice au aratat ca degenerarea senila de tip Alzheimer poate fi identificata prin scanare PET inainte de aparitia simptomelor clinice: pierdere de memorie sau tuburari comportamentale. Detectarea senilitatii de tip Alzheimer cat mai devreme este extrem de importanta pentru a da posibilitatea noilor optiuni de tratament sa fie cat mai efective.
Indicatiile PET sunt: complement al mamografiei in detectarea cancerului mamar, diagnosticul diferential benign-malign al tumorilor mamare, stadializarea cazurilor noi de cancer mamar, detectarea metastazelor la distanta si evaluarea raspunsului la terapia neoadjuvanta.
Deocamdata, PET ramane o investigatie mai scumpa decat tehnicile imagistice clasice, de aceea PET este utilizata in evaluarea tumorilor mamare doar in situatii speciale: la pacientele cu risc inalt, boala fibrochistica sau implantele mamare.
Dementa poate fi vindecata. Cinci oameni dintr-o suta vor suferi de o forma de dementa, dintre care cea mai frecventa este Alzheimer, care nu poate fi detectata prin CT sau RMN. Cu ajutorul PET/CT, maladia Alzheimer poate fi identificata si diagnosticata cu patru-cinci ani inainte de a se manifesta, iar tratata in acel moment, nu mai progreseaza.
Ministerul
Sanatatii a autorizat folosirea scannerului la anumite tipuri de cancer:
pulmonar, de colon, tiroidian, esofagian, cerebral etc. Echipamentele de acest
gen pot fi folosite si la scanarea inimii si a creierului. In
Capitolul II
Descrirea si functionarea PET-ului
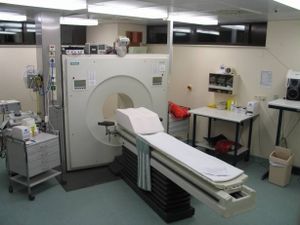
Figura 1 - Imaginea unui PET
PET-ul este o tehnica imagistica medicala din medicina nucleara, care produce o imagine tri-dimensionala sau o harta cu procesele functionale din corp. PET permite detectia distributiei in organism a unor radiofarmaceutice care include radioizotopi emitatori de pozitroni.
Cei patru radioizotopi mentionati anterior sunt folositi la marcarea unei varietati de molecule obtinandu-se, astfel, radiotrasori utilizabili in investigarea atat a diferitelor tipuri de metabolism cat si a altor procese biologice.
Pozitronul, anti-particula a electronului de aceeasi masa si cu sarcina electrica egala dar pozitiva, are un parcurs scurt (circa 1 mm) si o durata de viata limitata in tesuturile organismului, deoarece interactioneaza cu electronii existenti in tesuturi, ceea ce conduce la anihilarea sau dematerializarea celor doua particule (Fig. 2).
Aceasta anihilare se insoteste de aparitia cvasisimultana a doi fotoni gamma, fiecare cu o energie de 511 keV, emisi la 180 unul de altul, care vor traversa tesuturile, parasind organismul si fiind detectati cu ajutorul gamma camerei . Acest fenomen fizic face posibila detectia distributiei izotopului emitator de pozitroni din radiofarmaceuticul administrat intravenos pacientului.
|
RADIOIZOTOP EMITATOR DE POZITRONI 18F, 11C, 15O si 13N |
|
POZITRON | ||
|
din tesuturi |
||
 ANIHILARE
ANIHILARE
|
2 fotoni gamma, 511 keV |
![]()
|
detectie in coincidenta (interval de ordinul a 10-9 sec | ||
|
Modificari esentiale ale detectorului: - cristal de germanat de bismut - tuburi fotomultiplicatoare situate in directii opuse (dispuse circular sau nu) |
||
Figura 2 - Principiul tomografiei prin emisie de pozitroni
2.1. Gamma camera PET
Desi PET se bazeaza, in esenta, pe acelasi principiu fizic de detectie a scintilatiilor ca si gamma camera "conventionala" sistemele de detectie PET prezinta doua modificari esentiale: tuburile fotomultiplicatoare trebuie astfel plasate incat sa permita detectia in coincidenta, de jur imprejurul organismului a fotonilor gamma rezultati, iar cristalul de scintilatie trebuie sa fie dintr-un material care sa permita conversia fotonilor gamma cu energie mai mare decat in cazul scintigrafiei conventionale (511 keV, in cazul PET, fata de intervalul 100 - 400 keV, in scintigrafia conventionala) in fotoni in domeniul vizibil.
Ca urmare, camera PET este formata din fotomultiplicatoare dispuse circular, in mai multe coroane de blocuri detectoare (intre 2 si 8), iar cristalul de scintilatie este de germanat de bismut (BGO), cel mai frecvent, sau fluorura de bariu (BaF2) spre deosebire de gammacamera "conventionala" al carei cristal este alcatuit din iodura de sodiu (NaI).
In ultimii ani a fost propusa detectia in coincidenta utilizand gamma camere adaptate, cu dublu cap (doua detectoare), acestea ramanand totodata utile pentru realizarea scintigrafiilor "traditionale". Cele doua capuri detectoare sunt plasate de o parte si de alta a pacientului. Diferenta fata de gamma-camera "traditionala" apare la nivelul cristalului de scintilatie: acesta este inlocuit cu unul de dimensiuni duble (19 mm in loc de 9,5 mm).
Spre deosebire de PET unde doza injectata este in jur de 500 MBq, utilizand o gamma-camera cu sistem de detectie in coincidenta doza optima este de 100-200 MBq (pentru eliminarea artefactelor). Imaginea tomoscintigrafica se obtine prin rotirea extrem de lenta a celor 2 detectoare in jurul pacientului. Sectiunile pot fi apoi reconstruite in 3D. Se incearca chiar constructia unei gamma-camere cu 3 detectoare, crescand astfel sensibilitatea detectiei si, deci, calitatea imaginii.
2.2. Radiofarmaceutice PET
18F- Fluorodeoxiglucoza
Utilizarea 18F FDG (Fig. 2) pentru vizualizarea tesuturilor mari consumatoare de glucoza a transformat, neindoielnic, oncologia nucleara in cea mai inportanta metoda pentru depistarea si evaluarea evolutiva a tesutului tumoral.
(FDG) este un analog al glucozei, si, deci, patrunde in celula in acelasi mod ca si glucoza. Odata ajunsa in celula, FDG este fosforilata si se acumuleaza intracelular, nefiind catabolizata. Absenta gruparii OH in pozitia 2 determina o blocare enzimatica cu acumulare de 18F FDG intracelular (sub forma de FDG-6-PO4), in platou (proportional cu intensitatea glicolizei) - fenomen cunoscut sub numele de trapping. Regiunile in care exista o captare crescuta a radiofarmaceuticului corespund, deci, zonelor cu metabolism glucidic ridicat.
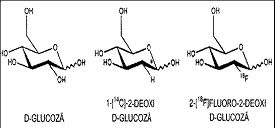
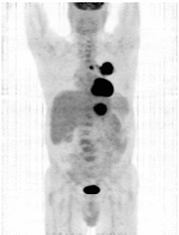
Fig. 3. Structura 18F-FDG, in comparatie cu Fig. 4. Imagine PET cu F FDG:
D-glucoza si 2-deoxi-D-glucoza neoplasm pulmonar primar (lob superior stang) cu
metastaze (paratraheal si in lobul hepatic stang)
Celulele canceroase au un metabolism crescut si particular al glucozei prin: cresterea glicolizei anaerobe, cresterea activitatii hexokinazei (HK) si piruvatkinazei (PK), alterarea numarului, formei si functiei mitocondriilor, cresterea transportului membranar al glucozei (prin cresterea numarului transportorilor, in special GLUT-1 si GLUT-3). Prin urmare, aceste celule vor acumula 18F FDG in cantitate mare.
Factorii care au impus utilizarea 18F-FDG ca radiotrasor PET principal (alti
radiotrasori PET sunt utilizati in procent de 10% din frecventa de utilizare a FDG) sunt:
- captarea 18F-FDG de catre celulele tumorale cu activitate glicolitica crescuta; majoritatea tumorilor maligne (pulmonare, mamare, de colon, limfoame, melanoame) pot fi detectate
cu 18F-FDG;
- timpul relativ lung de injumatatire al radionuclidului (18F) - 110 min;
- obtinerea 18F in cantitati suficiente in ciclotroane de mici dimensiuni.
2.2.2. Trasori PET pentru imagistica tumorala, altii decat 18F FDG
Alaturi de evaluarea metabolismului glucidic, PET permite evaluarea si a altor tipuri
de metabolism, folosindu-se alti radiotrasori (Tabelul I).
|
Radiotrasor |
Analog biologic |
Activitate investigata |
|
18F-FDG |
Glucoza |
metabolismul glucozei fosforilarea prin hexokinaza |
|
18F-fluoro-DOPA |
Dopamina |
metabolismul aminoacizilor |
|
18F-fluoro-metiltirozina |
Tirozina |
metabolismul aminoacizilor |
|
18F-fluoro-2-deoxiuridina |
Fluorodeoxiuridina |
metabolismul acizilor nucleici |
|
18F-fluoro-aciclovir |
Acyclovir |
fosforilarea prin timidinkinaza |
|
11C-acetat |
Acetate |
metabolismul acizilor grasi |
|
13N-amoniac |
perfuzia tisulara |
|
|
15O-apa |
Apa |
perfuzia tisulara |
Tabel nr. 1 Radiotrasori uzuali in PET
11C-metionina si analogii marcati de aminoacizi
Utilizarea 11C-L-metioninei in imagistica tumorala se bazeaza pe observarea transportului si utilizarii crescute a aminoacizilor in cancere, a activitatii crescute a cailor de transmetilare in unele cancere. In mod normal exista o captare substantiala a acestui trasor in pancreas, glande salivare, ficat si rinichi. Ca aminoacid natural, exista un anumit grad de metabolizare a L-metioninei in sange.
Trasorul a fost folosit in imagistica tumorilor cerebrale, a cancerelor de cap si gat, a limfoamelor si cancerelor pulmonare. S-a demonstrate stereospecificitatea captarii tumorale, cu o captare a L-metioninei mult mai mare decat cea a D-metioninei in tumori cerebrale cu bariera hemato-encefalica intacta.
Alti aminoacizi utilizati in PET sunt L-tirozina si aminoacizi artificiali care nu sunt metabolizati semnificativ in vivo si reprezinta, astfel, o alternativa buna de examinare a transportului aminoacizilor in tumori.
11C-timidina si alti precursori ADN
Rate crescute ale sintezei de ADN caracterizeaza multe tumori cu crestere rapida si tesuturi care prolifereaza rapid in mod normal. Din acest motiv, unele tumori pot fi investigate cu 11C-timidina si analogi structurali ai acesteia, deoarece timidina se fixeaza numai in tesuturi cu sinteza ADN in curs de desfasurare.
Insa, utilizarea sa este complicata de faptul ca este rapid metabolizata in sange, ceea ce inseamna ca doar o mica fractiune din materialul marcat din sange este 11C-timidina. Localizarea markerului radioactiv este importanta in utilizarea 11C-timidinei. De exemplu, daca este marcat pe inel in partea opusa pozitiei C-1, vor aparea mai multi metaboliti, cuantificarea devenind mai dificila.
Alti compusi, ca 18F-fluoro-deoxiuridina, reprezinta de asemenea potentiali agenti imagistici. Analogi structurali ai timidinei marcati cu 18F sunt in curs de investigare in vivo, pe pacienti.
Agenti chemoterapeutici radiomarcati
O serie de agenti chemoterapeutici marcati pentru PET au fost sintetizati si aplicati deja intr-o masura restransa la pacienti, pentru a urmari livrarea si acumularea agentului terapeutic in cancer. De exemplu, 18F-fluoro-deoxiuridina a fost folosita in terapia cancerelor colorectale si a altor tipuri, iar studiile preliminare au aratat ca are potential de predictie a raspunsului la terapie, pe baza unei investigari PET initiale.
Radiotrasori pentru studiul fluxului sanguin tumoral
Prin PET pot fi investigati si o serie de alti parametri tumorali. Fluxul sanguin tumoral poate fi masurat cu ajutorul 15O-H2O sau prin inhalarea de 15O-CO2 urmate de cuantificarea imaginilor. Volumul de distributie al tumorii (portiunea din tumora care comunica liber cu sangele) poate fi studiat folosind 15O-H2O.
Acesti parametri pot fi determinati cantitativ folosind tehnici de modelare matematica.
Radiotrasori pentru studiul statusului receptorilor tumorali
Tumorile pot exprima o varietate de markeri
pe suprafata lor, inclusiv receptori sauantigeni asociati cu tumora, cum ar fi
receptorii la estrogen sau progesteron. Au fost sintetizati liganzi specifici
pentru acesti receptori, dintre care cel mai cunoscut este
18F-17β-estradiol (
Oligonucleotide radiomarcate
Reprezinta o clasa de radiofarmaceutice inca in studiu, domeniu care s-a dezvoltat prin disponibilitatea oligonucleotidelor sintetice. Se deosebesc doua categorii: oligonucleotide antisens si oligonucleotide aptamer.
Oligonucleotidele antisens sunt oligonucleotide cu lant scurt, de cateva nucleotide, a caror secventa este complementara si permite legarea la ARN tinta (mARN sau ARNviral) inhiband translarea, si, in final, sinteza unor proteine.
Oligonucleotidele aptamer sunt fragmente de ARN sintetizate in vitro, asemanatoare oligonucleotidelor antisens, de care se deosebesc esential deoarece se pot lega si la alte molecule mici, proteice, din organism (molecule celulare de suprafata etc.), nu doar la acizii nucleici. Au afinitate si specificitate mai mare decat anticorpii.
Principiul imagisticii cu oligonucleotide radiomarcate este urmatorul:
oligonucleotidele radiomarcate (doze mici) administrate i.v. pacientului difuzeaza in organism fara a fi degradate, patrund in anumite celule, se hibrideaza specific cu o secventa complementara (tinta) de ARNm (in celulele care exprima acest ARN); se pot observa, scintigrafic, focare de acumulare de radioactivitate, corespunzand supraexpresiei unei anumite gene (care codeaza o anume disfunctie), in regiuni bine delimitate din organism.
Utilizand diferitele radiofarmaceutice PET mentionate, dar indeosebi 18F FDG, pana in prezent, principalele aplicatii ale PET sunt in oncologie si anume: tumori cerebrale (glioame), cancer pulmonar, cancer colo-rectal, hepatic, pancreatic, cancer mamar, cancer de ovar, limfom Hodgkin si non-Hodgkin, melanoame si sarcoame, cancere din sfera ORL.
Capitolul III
PET - CT Principiu fizic si utilitate
Principala limita a metodei PET consta in rezolutia mica in comparatie cu CT si RMN, ceea ce determina imposibilitatea localizarii precise a detaliilor anatomice si, implicit, a leziunilor in intregime sau a regiunilor metabolic active in ansamblul unor leziuni de constitutie eterogena, necesar a fi biopsiate, de exemplu.
Pe de alta parte, CT este o metoda imagistica care poate pune in evidenta detalii anatomice, structurale, cu o rezolutie foarte buna dar nu si diferente in fiziologia tesutului respectiv, pe care PET le poate vizualiza. Ani de zile pentru a localiza cu precizie modificarile functionale observate prin PET s-au propus doua variante: fuziunea imaginilor PET si CT folosind repere anatomice pentru a achizitiona imagini din regiuni identice si dupa realinierea seturilor de imagini obtinute prin cele doua metode, folosind soft-uri specializate in acest sens. Dar acest lucru era dificil din mai multe puncte de vedere, cum ar fi: diferente legate de
respiratie, de distanta la care se gaseste detectorul in timpul achizitiei, de pozitionarea pacientului etc. Aceste inconveniente au fost rezolvate prin asezarea celor doua detectoare pe acelasi suport (Fig. 5), prin metoda PET-CT, initiata de D. Townsend in anul 2000.
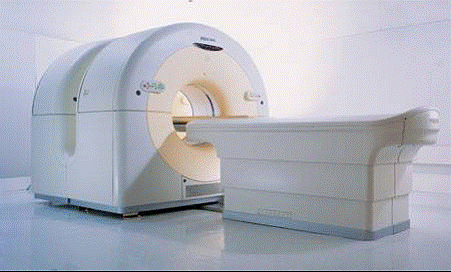
Figura nr. 5 - Dispozitiv PET - CT
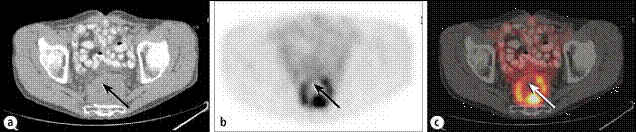
Fig. 6- Carcinom rectal - recidiva:
a) CT: formatiune presacrata de dimensiuni mari, omogena; sageata indica directia acului de biopsie, rezultatul biopsiei fiind negativ;
b) Imagine PET (18FFDG), cu fixare eterogena, demonstrand o zona tumorala activa, periferic;
c) imaginea fuzionata PET-CT demonstreaza prezenta unui inel tumoral discontinuu care inconjoara un centru necrotic; repetarea biopsiei in zona functionala a tumorii demonstreaza recidiva tumorala.
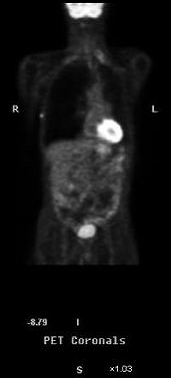
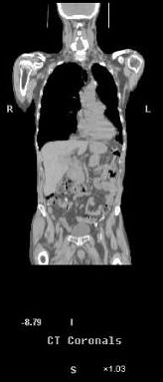
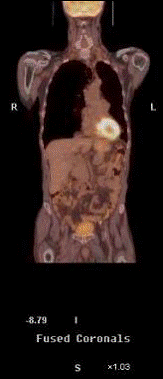
Fig. 7.
Rezulta ca PET si CT prezinta avantaje complementare, iar combinarea acestora crestepotentialul de localizare a leziunilor si reduce dificultatile de interpretare a imaginilor obtinute prin PET.
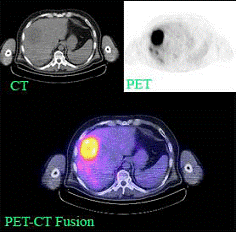
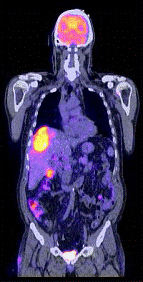
Fig. 8- Metastaze intrahepatice: imagini PET (18FFDG), CT si PET-CT.
sectiuni transversale (stanga) si sectiuni coronale (dreapta)
Indicatiile clinice ale PET-CT sunt, de fapt, identice cu acelea ale PET, referindu-se indeosebi la domeniul oncologiei nucleare: diagnostic tumoral (Fig. 6, 8,) stadializare (Fig.9) si evaluare evolutiva (Fig. 10), pre- si post- terapie . Evident, metoda PET-CT prezinta o serie de avantaje fata de fiecare dintre cele doua metode utilizate separat:
a) se pot obtine imagini metabolice si anatomice intr-un timp redus fata de utilizarea separata a celor doua metode (Fig.7);
b) o singura explorare imagistica permite atat diagnosticul tumorii primare cat si al metastazelor, dand si posibilitatea stadializarii tumorale;
c) tesutul tumoral este diagnosticat imagistic cu mare sensibilitate si specificitate (prin PET) dar si localizat anatomic cu mare precizie si rezolutie (prin CT);
d) faptul ca pacientul nu se deplaseaza intre achizitia celor doua tipuri de imagini face ca fuziunea imaginilor sa fie aproape perfecta (doar miscarile respiratorii mai pot interveni);
e) regiuni dificil de evaluat imagistic (cum ar fi regiunea cervicala, capul, mediastinul, abdomenul postchirurgical) pot fi examinate cu mare acuratete;
f) imaginile fuzionate PET-CT pot fi folosite atat pentru stabilirea cu precizie a regiunilor pentru radioterapie cat si pentru evaluarea post tratament chirurgical, chimioterapie sau/si radioterapie
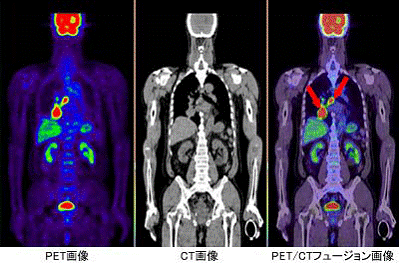
Fig. 9- Neoplasm pulmonar drept cu metastaza ganglionara (sagetile rosii)
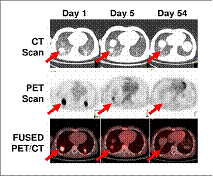
Fig. 10. Urmarire evolutiva a unui sarcom aflat sub tratament tintit, intratumoral, (ziua5 si 54) comparativ cu imagini anterior tratamentului (ziua 1).
comparativ cu imaginile PET (18FFDG), care arata o reducere evidenta a metabolismului glucidic tumoral, demonstrand eficienta terapiei.
In prezent, aplicatiile clinice ale PET cu 18F FDG-CT in oncologie includ diagnosticul diferential intre tesutul benign si malign, stadializarea cancerului inainte de terapie, evaluarea rezultatului terapiei neoplaziilor, depistarea recurentelor tumorale post terapeutice in numeroase tipuri de neoplazii, incluzand: cancerul pulmonar, gastrointestinal, mamar, limfomul malign.
In viitorul apropiat MN va deschide
posibilitatea obtinerii unor imagini moleculare, in acord cu evolutia medicinii
moleculare, indeosebi prin tehnici PET si PET-CT. Aceasta ca o consecinta a
cercetarilor de genomica si proteomica. Ramane un imperativ ca aceste progrese
sa devina accesibile si la noi in
BIBLIOGRAFIE
1. Green MA, Welch MJ. Radiopharmaceuticals for Positron Emission Tomography (PET). In: Early PJ,
Sodee DB, editors.
Principles and Practice of Nuclear Medicine.
2. Phelps M.E. The Merging of Biology and Imaging into Molecular Imaging. J Nucl Med 2000; 41(4):
3. Elgazzar A. The Pathophysiologic Basis of Nuclear Medecine. Abdelhamid H. Elgazzar editors.
Springer-Verlag; 2001. p. 179-188.
4. Beyer T, Townsend DW, Brun T, Kinahan PE, Charron M, Roddy R, Jerin J, Young J, Byars L, Nutt R.
A combined PET/CT Scanner for Clinical Oncology. J Nucl Med, 2000, 41(3): 1369-1379.
5. Delbeke D, Sandler MP. The role of Hybrid Cameras in Oncology. Semin Nucl Med. 2000; 30(4): 268-
6. Stoot JHMB, Ribeiro MJS, McCready VR, van Santen WHC, Bourguignon M, Mazière B, Pauwels
EKJ. 18F-FDG et physiopathologie tumorale. Mdecine Nuclaire. 1999; 23(4); 239-247.
7. Gjedde A. Glucose Metabolism. In: Wagner HN, Szabo Z, Buchanan JW editors. Principles of Nuclear
Medicine.
8. Brunet-Desruet MD, Morin C, Ghezzi C, Comet M, Fagret D. Quantification in vivo des transporteurs
du glucose: intrêt du dveloppement d'un radioligand en mdecine nuclaire. Mdecine Nuclaire.
9. Maublant J, Lagrange JL. Applications du fluor-18-fluoro-2-dsoxyglucose en cancrologie. Mdecine
Nuclaire. 1995; 19: 64-72.
10. Schiepers C
(editor). Diagnostic Nuclear Medicine. 2nd Revised Edition.
Springer-Verlag. 2006.
11. Bar-Shalom R,
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 6003
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved