| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Multiplicarea virusurilor
Multiplicarea este procesul complex in cursul caruia are loc transcrierea si traducerea informatiei genetice in proteine, replicarea genomului si asamblarea virionilor progeni.
Procesul multiplicarii virale prezinta particularitati care decurg din parazitismul absolut, de nivel genetic, al acestor entitati. Replicarea are loc exclusiv in celulele vii, care furnizeaza nu numai precursorii monomerici ai macromoleculelor, ci si intregul dispozitiv celular efector (ribosomi, enzime activatoare ale aminoacizilor, ARNt, diferiti factori solubili, sistemele generatoare de energie etc.).
Celula infectata cu un virus constituie un complex viu - complexul virus-celula - in care se desfasoara doua categorii de procese:
sintezele moleculare specific virale
diataxia virala. Termenul de "diataxie"(Lwoff, l98l) semnifica "punerea in ordine" sau asamblarea moleculelor specific virale, in structuri virale.
Multiplicarea virala este, in esenta, rezultatul exprimarii programului genetic viral, datorita caruia, ordinea celulara normala este inlocuita de ordinea virala. Informatia genetica virala deviaza metabolismul celulei.
Desi celula poate asigura majoritatea functiilor replicarii virale, adeseori este necesara actiunea unor enzime virale existente in virion sau codificate timpuriu de genomul viral.
Numarul genelor virale difera considerabil. Ele codifica sinteza urmatoarelor categorii de proteine:
enzime pentru replicarea genomului viral (replicaze). Ele pot fi componente ale virionului matur (infectios) sau se sintetizeaza in celula, dupa infectie;
proteine structurale, componente ale capsidei si peplosului;
proteine reglatoare, de doua categorii: a) cele care modifica specificitatea aparatului de biosinteza al celulei in sensul specificitatii virale; b) proteine reglatoare ale morfogenezei virale.
Multiplicarea virala (producerea particulelor virale progene) este conditionata de infectia fiecarei celule, in vivo sau in vitro, cu cel putin o particula virala. Practic insa, pentru a asigura infectia fiecarei celule a unei culturi si un grad foarte inalt de sincronizare a etapelor replicarii sunt necesare l0-l00 particule virale pentru fiecare celula.
Calitatea unei celule sau a unui organism de a fi gazda pentru multiplicarea unui virus poarta denumirea de sensibilitate.
Pentru ca o celula sa fie sensibila la infectie sunt necesare doua conditii:
virionul sa se fixeze stabil de componente moleculare ale suprafetei celulei;
celula sa permita desfasurarea ciclului de replicare (sa fie permisiva). Particularitatile functionale ale celulelor care conditioneaza desfasurarea ciclului de multiplicare virala, au fost echivalate, prin analogie, cu factorii de crestere ai celulei bacteriene.
Tipurile de celule si speciile de organisme pe care le poate infecta si in care se poate multiplica un virus, definesc spectrul sau de gazda. Unele virusuri au spectrul de gazda foarte larg si se pot multiplica in celulele unor specii foarte diverse. De exemplu, arbovirusurile se multiplica in tesuturile insectelor hematofage si sunt transmise vertebratelor, la care produc infectii. Unele rhabdovirusuri infectioase pentru vertebrate se multiplica in tesuturile insectelor, dar si ale unor plante. Alte virusuri sunt foarte specializate si infecteaza cateva tipuri de celule ale unei specii.
Multiplicarea virala se desfasoara intr-o serie de etape succesive, mai mult sau mai putin secventiale, desi o anumita faza se continua in faza urmatoare, astfel incat dupa cateva ore de la infectie, intr-o singura celula se pot intalni majoritatea fazelor replicarii unui virus cu genom ADN. Multiplicarea virala propriu-zisa este precedata de interactiunea virionilor cu substratul celular.
Initierea procesului infectios
Evenimentul preliminar al multiplicarii este adsorbtia particulei virale, ca o consecinta a ciocnirilor intamplatoare a virionilor aflati in suspensie, cu suprafata celulei. Procesul adsorbtiei este ineficient, uneori fiind necesare milioane de ciocniri favorizate de miscarile browniene ale moleculelor din suspensie. Fortele electrostatice au rol important in realizarea adsorbtiei. Densitatea virionilor si a celulelor influenteaza decisiv eficienta acestui proces, care este reversibil.
Fixarea ireversibila(atasarea) a virusului pe suprafata celulei, presupune actiunea unui mecanism care stabilizeaza interactiunea, pana in momentul inglobarii virionului. Una din particularitatile virusurilor si anume specificitatea lor pentru o anumita categorie de celule este in primul rand o specificitate de fixare, conditionata de interactiunea unei proteine virale(ligand* sau antireceptor), cu un constituient normal al suprafetei celulare, care are rolul de receptor de virus.
Ligandul este orice molecula sau structura care mediaza interactiunea specifica sau nespecifica dintre un virus si celula sau dintre doua celule.
Rolul interactiunii specifice este demonstrat de faptul ca acidul nucleic viral purificat este infectios pentru un spectru mai larg de celule.
Gradul de specificitate al interactiunii virus-celula este diferit. Suprafata celulelor vegetale este acoperita cu ceara, pectina, dar mai ales cu un perete gros celulozic si nu are receptori de virus. Nu se cunoaste nici un virus care sa utilizeze receptori celulari specifici. Infectia celulei vegetale este conditionata de lezarea peretelui celulozic: virusurile sunt inoculate de vectori (artropode, nematode)care transmit virusul sau prin leziunea mecanica a celulei.
Infectia virala n-are consecinte patologice daca virusul nu se disemineaza de la celula infectata initial (adeseori in frunze), la celulele invecinate. Trecerea virusului de la o celula la alta este impiedicata de peretii celulari. Dar celulele contin canale in peretele despartitor (plasmodesmata), ceea ce produce un continuum intercelular.
Diseminarea virusurilor la distanta in tesuturile plantei se face prin celulele perforate ale floemului.
Interactiunea fag-bacterie este caracterizata printr-un grad inalt de specificitate (utilizata in scop practic pentru tipizarea fagica a tulpinilor bacteriene), iar aceea dintre virus si celula animala are un nivel intermediar. Uneori, atasarea virusului de celula animala este mediata de receptori foarte specifici, de aici decurgand citotropismul, cu consecinte majore asupra patogenitatii virale. De exemplu, poliovirusul (un enterovirus) are specificitate de legare pentru celulele mucoasei intestinale si pentru motoneuronii din coloanele anterioare ale maduvei spinarii. In mod obisnuit, ciclul se desfasoara in celulele mucoasei intestinale, fara manifestari clinice, dar dupa infectia motoneuronilor survine paralizia musculara.
Se cunosc mai bine liganzii virali, decat receptorii celulari. Virionii inveliti se leaga de receptorii celulari prin glicoproteinele peplosului, care adesea proemina sub forma spiculelor.
Structurile de legare a virusurilor nude cu simetrie icozaedrica sunt situate la varfurile icozaedrului. Ele sunt polipeptide ale capsidei sau sunt proteine fibrilare proeminente la varfuri (de exemplu, fibra pentonica a adenovirusurilor).
Definirea receptorului celular de virus este dificila, deoarece particula virala este un ligand de dimensiuni mari, ce interactioneaza cu o suprafata mare a celulei, la nivelul careia se gasesc molecule de legare specifica si nespecifica. Pentru ca o molecula membranara sa aiba rolul de receptor pentru virus, in primul rand, trebuie sa aiba o densitate suficient de mare pentru a asigura interactiuni multiple cu ligandul viral. Pe de alta parte, virusul se poate lega de receptori diferiti pe diferite tipuri de celule. Totusi, s-au identificat receptorii celulari pentru cateva virusuri.
Din punct de vedere biochimic, receptorii celulari pentru virusuri sunt glicoproteine, glicolipide sau glucide. Specificitatea de legare este conferita de o parte a unei macromolecule sau de catenele glucidice ale conjugatelor glicoproteice.
Astfel, ligandul virusului influenza - hemaglutinina (o glicoproteina a peplosului) se leaga specific de resturile de acid sialic ale glicoproteinelor membranei citoplasmatice.
Receptorul pentru acetilcolina, de la nivelul sinapselor neuroefectoare poate avea rol de receptor si pentru virusul rabic.
Invelisul HSV1 contine cel putin 9 glicoproteine. Cateva (B, C, D, H, L) mediaza legarea virionului de heparan-sulfat*, cu rol de receptor celular. Glicoproteinele B si D mediaza tropismul HSV1 pentru neuronii SNC.
Heparan-sulfatul este un proteoglican, o macromolecula alcatuita dintr-o regiune centrala proteica, pe care se leaga covalent catene laterale de glicozaminoglicani, formand un monomer proteoglicanic. Mai multi monomeri se leaga prin intermediul componentei proteice, de o molecula lunga de acid hialuronic.
Glicozaminoglicanii (MPZ acide) sunt polizaharide ce contin unitati dizaharidice inalt repetitive.
EBV produce mononucleoza infectioasa, o maladie limfoproliferativa benigna. Este singurul virus al familiei pentru care s-a identificat un receptor de mare afinitate: este glicoproteina membranara CD21 (sau CR2, adica receptorul pentru complement de tip 2, ce leaga C3d). Receptorul CD21 are rol in activarea normala a limfocitelor B. In timpul activarii cascadei C, C3 este clivat in C3b, care se leaga de complexele Ag-Ac. C3b este prelucrat proteolitic si rezulta C3d. C3d atasat de complexul Ag-Ac, se fixeaza la limfocitul B, pe calea CR2. C3d este ligandul natural pentru CR2.
Receptorul pentru HCMV pare a fi molecula CMH I.
Receptorii celulari pentru virusurile nude cu simetrie icozaedrica sunt mai putin cunoscuti.
Adenovirusurile se fixeaza prin intermediul fibrei pentonice, la o varietate de receptori celulari, inclusiv moleculele CMH I.
Receptorii pentru Rhinovirusuri sunt moleculele intercelulare de aderenta (ICAM-1). ICAM-1 se gaseste pe celulele epiteliului cavitatii nazale si pe multe alte tipuri de celule din organism. Are 5 domenii extracelulare omologe domeniilor Ig (D1-D5), un domeniu transmembranar si un domeniu citosolic si face parte din suprafamilia Ig. Cele 5 domenii sunt asezate linear. Functia normala este de a lega integrina LFA-1 de pe suprafata limfocitelor. Interactiunea LFA-1-ICAM-1 mediaza aderenta dintre celulele epiteliale si limfocitele T care lizeaza celulele epiteliale infectate cu virus.
Expresia ICAM-1 pe celulele epiteliale ale cavitatii nazale este restrictiva in conditii normale, dar este indusa de mediatorii inflamatiei (IL-1, IFN g, TNF) eliberati dupa infectia cu rinovirus, ceea ce usureaza diseminarea infectiei. Pe de alta parte, inductia expresiei ICAM-1 este importanta pentru localizarea limfocitelor la situsul inflamatiei.
Receptori pentru HIV1. Molecula CD4 are rol de coreceptor pentru recunoasterea Ag, in asociatie cu moleculele CMH II, dar transmite si semnalul activator al celulei T. Celulele CD4 secreta limfochine activatoare pentru limfocitele B si macrofage. CD4 se gaseste si pe membrana celulelor liniei monocit-macrofag.
Proteina CD4 este un polipeptid de 55 kDa al membranei. Regiunea extracelulara contine 372 aminoacizi, ce formeaza 4 domenii, omologe cu ale moleculei de Ig.
HIV infecteaza si celule CD4- : neuroni, astrocite.
Utilizarea AMC specifici fata de diferite componente membranare a dus la identificarea sfingolipidului* galactozil ceramid (Gal C), ca un posibil receptor pentru HIV pe membrana neuronala.
Sfingolipidele sunt formate dintr-un aminoalcool cu 18 atomi de C(sfingozina). La gruparea -NH2 a sfingozinei este legat un acid gras, majoritatea cu 24 atomi de C). Cele care contin o grupare glucidica se numesc sfingoglicolipide.
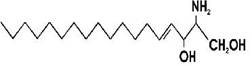
Sfingozina
Celulele organismelor uman si animal au receptori pentru un numar mare de agenti infectiosi. Teleonomic insa, moleculele cu rol de receptori nu sunt destinate legarii virionilor, ci indeplinesc diferite functii normale: de exemplu, unele au rol de receptori de hormoni. Moleculele care au rol de receptori de virus sunt polifunctionale. Virusurile imprumuta diferite molecule ale suprafetei celulare, prin intermediul carora dobandesc accesul in celula. Numarul receptorilor de virus, pe suprafata unei celule este cuprins intre l0 000 si l00 000.
Tropismul unor virusuri pentru anumite celule sau tesuturi este determinat de specificitatea interactiunii cu receptorul: de exemplu, tropismul HIV-1 pentru limfocitele T si pentru macrofagele care prezinta receptorul CD4 ; tropismul EBV pentru limfocitele B care contin receptorul CD21. Dar specificitatea si distributia tisulara a receptorilor nu poate explica tropismul celor mai multe ribovirusuri, deoarece adeseori infectia este abortiva: virionul este internalizat si genomul este dezvelit, dar multiplicarea este stopata intr-o etapa ulterioara, ceea ce sugereaza existenta unor factori celulari, care conditioneaza sinteza macromoleculelor esentiale ale ciclului de multiplicare virala (ARN, proteine). De exemplu, virusul influenza se fixeaza de resturile de acid sialic ale glicoproteinelor si glicolipidelor, care au o distributie ubicvitara in cele mai multe tesuturi. Totusi, infectia cu virusul influenza este limitata exclusiv la celulele epiteliale ale tractului respirator al omului si la modelele animale ale infectiei. Pentru aceste virusuri, tropismul viral este conditionat de existenta receptorilor celulari si de starea de permisivitate a celulei. Virusurile se multiplica in celulele care nu pot sa declanseze un raspuns antiviral mediat de IFN α/β.
Atasarea de receptorii celulari este un proces reversibil. Daca nu se produce internalizarea, virusul poate sa se detaseze (fenomen denumit elutie), de pe suprafata celulei. Unele virusuri au mecanisme speciale de elutie. Detasarea virionilor ortho- si paramyxo- este mediata de neuraminidaza (NA), o esteraza care cliveaza resturile de acid sialic din catenele glucidice ale glicoproteinelor. Resturile de acid sialic raman legate de HA si previn legarea de alt receptor. De aceea, se admite ca rolul NA este de a desializa glicoproteinele pe masura ce ele sunt inserate in invelisul viral nascent.
De cele mai multe ori, atasarea virusului determina modificari ireversibile in structura receptorului si in mod obligatoriu urmeaza internalizarea (inglobarea virusului in celula). Uneori insa, dupa fixare, virionul se poate detasa si se reabsoarbe pe alta celula.
Dupa legarea virusului, receptorii celulari se modifica. Astfel, glicoproteina CD4, dupa interactiunea cu HIV se fosforileaza, o modificare esentiala pentru inglobarea virionului. Inhibitia fosforilarii cu inhibitori ai protein-kinazei blocheaza inglobarea si virionii raman la suprafata celulei. Fosforilarea declanseaza semnalul reorganizarii citoscheletului.
Chiar daca virusul nu patrunde in celula, legarea sa de membrana citoplasmatica influenteaza activitatea celulei. De exemplu, legarea VEB de suprafata limfocitului B poate initia activarea acestuia.
Patrunderea virusului in celula(infectia propriu-zisa)
Faza de patrundere sau de inglobare a virusurilor in celulele sensibile se desfasoara dupa mecanisme diferite, derivate din complexitatea structurilor de suprafata ale celulei si ale virionului (fig. 85).
Peretele mureinic al bacteriilor Gram pozitive, complexitatea structurala a peretelui bacteriilor Gram negative, precum si natura celulozica a peretelui vegetal constituie bariere foarte eficiente fata de infectia virala. Celulele vegetale sunt infectate numai dupa leziunea mecanica a peretelui celulozic, iar fagii din seria T-par au un aparat complex, foarte specializat, prin intermediul caruia genomul viral este injectat in celula bacteriana.
Virusurile infectioase pentru celulele animale sunt inglobate in intregime in celula sensibila, consecinta directa a absentei peretelui celular.
Patrunderea virusurilor in celula animala, dupa fixarea ireversibila se poate produce prin doua mecanisme fundamentale: endocitoza si fuziunea.
Mecanismul predominant prin care virusurile patrund in celula animala este endocitoza (denumita si viropexie), un proces analog celui de pinocitoza, caracteristic virusurilor nude (adeno-, reovirusuri), dar si unor virusuri invelite (influenza, rhabdo-, poxvirusuri).
Interactiunea initiala a virionului cu receptorii din membrana celulara nu este suficienta pentru a declansa endocitoza particulei legate, ci reprezinta semnalul* pentru initierea agregarii proteinelor contractile ale celulei si pentru formarea unor pseudopode.
Celulele (cu exceptia fagocitelor profesioniste) au capacitati endocitare foarte limitate. Dupa fixarea virionului de receptor este indusa endocitoza, ce consta in reorganizarea unor componente ale citoscheletului.
Formarea pseudopodelor usureaza interactiunile multiple ale suprafetei virionului cu receptorii celulei. Proteinele contractile ale citoplasmei se activeaza si realizeaza inchiderea particulei virale, intr-o vacuola de endocitoza, denumita microvezicula sau pinosom tapetat cu clatrina*, printr-un mecanism similar inchiderii unui fermoar.
Clatrina este o proteina mare, oligomerica, ce formeaza o retea pe suprafata interna a membranei plasmatice, favorizand intruzia membranei si formarea unei vezicule tapetata cu reteaua moleculara, care ulterior poate fuziona cu alte organite celulare.
Marginile libere ale membranei celulare intruzate, fuzioneaza si restabilesc integritatea suprafetei celulare, astfel incat virusul ramane inclus intr-o vezicula de endocitoza. Vezicula pierde invelisul de clatrina si fuzioneaza repede cu mici cisterne de reticul endoplasmic neted si cu lizosomi. Se formeaza un endosom al carui pH se acidifica sub actiunea unei pompe protonice din membrana. Pe masura ce pH scade, proteinele capsidei sufera modificari de conformatie si expun un domeniu hidrofob ce determina fuziunea cu membrana endosomului. Acesta este mecanismul de patrundere a virionilor nuzi, prin liza endosomului. Virusul eliberat din endosom este fie sub forma nucleocapsidei (adeno, herpes), fie sub forma nucleoproteinelor (enterovirusuri).
Pentru virusurile invelite, la pH acid al endosomului, invelisul viral fuzioneaza cu membrana endosomului, ceea ce favorizeaza eliberarea nucleocapsidei in citoplasma.
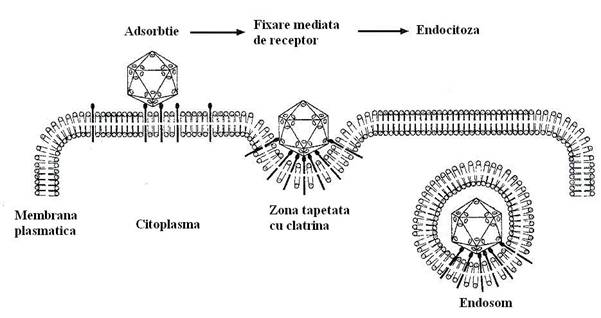
Fig. 85. Inglobarea unei particule virale nude prin mecanismul endocitozei mediata de receptori.
Al II-lea mecanism de patrundere, pentru unele virusuri invelite, consta intr-un proces de fuziune a invelisului viral cu membrana citoplasmatica. Peplosul, la contactul cu membrana celulara, se dizolva si ramane incorporat in membrana. La locul coalescentei celor doua structuri, se formeaza un "canal", care permite trecerea virionului in citoplasma.
Fuziunea invelisului viral, cu membrana plasmatica necesita interactiunea proteinelor virale "de fuziune" ale peplosului, cu constituientii specifici ai membranei celulare. Fuziunea este modalitatea de patrundere in celula, caracteristica virusurilor invelite. Astfel patrund in celula unele paramixo- si poxvirusuri.
Paramixovirusurile contin, inclavata in peplos, o proteina de fuziune (F), care mediaza fuziunea invelisului viral cu membrana celulei sensibile. Proteina F mediaza fuziunea celor doua structuri, numai daca este inclavata in invelisul fosfolipidic viral si daca este tinuta in contact strans cu membrana celulara, prin intermediul hemaglutininelor.
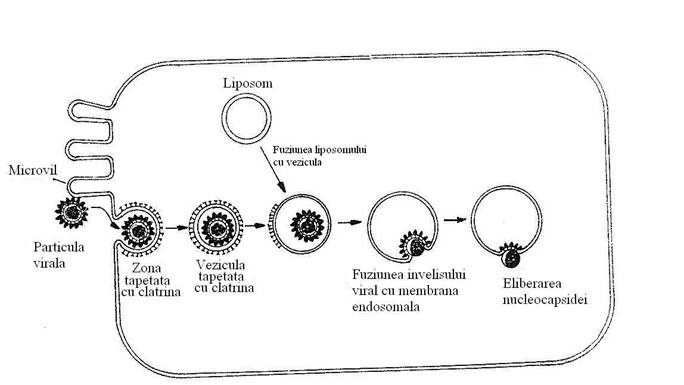
Fig. 86. Unele virusuri animale invelite intra in celula, fiind endocitate in vezicule tapetate cu clatrina. Vezicula de fagocitoza isi pierde invelisul de clatrina si fuzioneaza cu lizosomii. Scaderea pH-ului in vezicula determina un proces de fuziune a invelisului viral cu embrana veziculei endosomale si eliberarea nucleocapsidei in citoplasma.
Cele doua mecanisme de inglobare (endocitoza si fuziunea) nu se exclud reciproc. Acelasi virus invelit poate fi inglobat pe o cale sau alta, in functie de substratul celular. Mai mult, cele doua mecanisme pot coexista frecvent pentru un virus dat, in raporturile sale cu o linie celulara.
Rareori, virionul patrunde in celula, prin modalitati particulare, ce constau in liza locala a membranei plasmatice, la contactul cu virionul. Se produce liza peplosului viral si a membranei celulare sau virionul trece intact prin bresa membranara ;
Decapsidarea este procesul de conversie treptata a virusului, din starea de virion complet, la starea de virus vegetativ (genomul liber in celula infectata), prin pierderea capsidei si, cand este cazul, a invelisului viral.
Dezagregarea capsidei este un proces putin cunoscut, datorita dificultatilor de modelare experimentala si se produce in trepte. La reovirusuri, decapsidarea se initiaza inainte de contactul cu celula gazda, sub actiunea proteazelor intestinale si este incompleta, pentru ca replicarea genomului este catalizata de o enzima asociata virionului. La picornavirusuri, capsida se dezagrega partial la suprafata celulei, dupa legarea de receptorul celular. Cel mai adesea, decapsidarea are loc in vezicula endosomala, sub actiunea proteazelor lizosomale si a pH acid.
Capsida virusurilor herpetice si adeno se dezagrega la contactul cu porul nuclear.
Dezvelirea virusurilor din grupul pox se face in doua etape: invelisul extern este degradat sub actiunea enzimelor citoplasmatice, iar dezagregarea invelisului intern si eliberarea ADN este catalizata de produsele de sinteza a unor gene virale timpurii.
In vitro, dezvelirea virusurilor cu peplos este modelata sub actiunea detergentilor neionici (polieteri si esteri poliglicerici, de exemplu, Tween 80). Acestia interactioneaza cu componentele hidrofobe ale membranei si astfel peplosul este rupt si solubilizat.
Deplasarea intracelulara pana la locul replicarii este necesara numai pentru virusurile care au sedii caracteristice ale replicarii. Cele care se multiplica in citoplasma ajung usor la sediul desfasurarii procesului, imediat dupa ce au strabatut membrana citoplasmatica.
Virusurile care se multiplica in nucleu, necesita transferul de la locul patrunderii in celula, pana in nucleu. Deplasarea lor pare a fi "orientata" de un tropism molecular ale carui mecanisme nu se cunosc. Reorganizarea unor componente ale citoscheletului* are un rol important in mecanismul transportului citoplasmatic.
Nu se cunoaste nici un acid nucleic viral transportat in nucleu ca molecula libera.
Citoscheletul este format din 3 elemente structurale: microfilamente, microtubuli si filamente intermediare. Microfilamentele sunt alcatuite din subunitati de actina, iar microtubulii sunt formati din tubulina. Aceste elemente sunt comune marii majoritati a tipurilor celulare. Ele au rol structural, de transport si de mobilizare a organitelor. Filamentele intermediare sunt formate din subunitati de citocheratina si sunt specifice pentru starea de diferentiere celulara.
Adeno- si herpesvirusurile sunt transportate prin citoplasma sub forma nucleocapsidelor, in vacuola membranara de endocitoza, pana la contactul cu un por nuclear, prin care acidul nucleic este transferat in nucleu, iar capsida ramane la nivelul membranei nucleare.
Proteinele virale asociate cu acidul nucleic au rol esential in procesul de transport si indeplinesc doua functii:
furnizeaza semnale specifice si orienteaza transportul complexului spre nucleul celulei;
confera complexului o configuratie stabila, compatibila cu transferul prin porii membranei nucleare.
Acizii nucleici monocatenari sunt transportati cu o eficienta mai mare deoarece moleculele monocatenare sunt polare, mai flexibile si sunt tapetate cu proteina SSB (single strand binding). De exemplu, ARN de influenza este transportat in nucleu sub forma ribonucleoproteinei. Proteinele complexului mediaza transferul nuclear.
Dezoxiribovirusurile si retravirusurile intra in nucleul celulei, fie ca particule intregi (nucleocapside) fie sub forma complexelor nucleoproteice(ADN si proteinele asociate). Nu se cunoaste mecanismul prin care nucleocapsida interactioneaza cu membranele nucleare. Transferul complexului nucleoproteic in nucleu se realizeaza probabil prin fuziunea nucleocapsidei cu membrana nucleara.
Virusurile nude din grupul Papova patrund in nucleu ca virioni intregi, prin fuziunea nespecifica a veziculei de endocitoza, cu membrana nucleara externa, dupa care, virionul sau numai complexul nucleoproteic trece in nucleoplasma, prin fuziunea vacuolei cu membrana interna.
Tranzitul acestor virusuri in nucleu este rapid (virionii de SV40 se gasesc in nucleu la l5 min. dupa infectie) si se explica prin tropismul nuclear al proteinelor.
Sinteza ARNm viral
Existenta mesagerilor specific virali este o conditie esentiala si o restrictie majora pentru initierea procesului de multiplicare. Virusul ofera aparatului de sinteza al celulei, un ARNm pe care celula trebuie sa-l recunoasca si sa-l traduca in proteine. Generarea mesagerilor virali semnifica inceputul subordonarii aparatului de sinteza proteica si trecerea de la sinteza proteinelor celulare, la sinteza celor specific virale. Transcrierea este prima treapta a expresiei genelor virale si urmeaza patrunderii nucleocapsidei in celula. Unele virusuri au enzime de transcriere asociate genomului si activitatea lor incepe foarte curand dupa dezagregarea partiala a capsidei. Alteori, chiar molecula genomica de ARN functioneaza ca ARNm.
In citoplasma nu s-a detectat activitate ARN-polimerazica, astfel incat genomul virusurilor care nu au transcriptaze proprii, nu poate fi transcris. Datorita acestui fapt, genomul ADN (adeno, herpes, papova) poate fi transcris in ARNm numai dupa ce ajunge in nucleu. Poxvirusurile sunt o exceptie. Ele au propria enzima de transcriere (ARN-polimeraza) pentru sinteza ARNm si se multiplica in citoplasma.
Ribovirusurile se multiplica in citoplasma. Genomul viral ARN este transcris in ARNm de o enzima proprie de transcriere, ori ARN genomic functioneaza si ca ARNm.
Sinteza ARNm viral este catalizata de doua categorii de polimeraze:
ARN-polimeraza II celulara, pentru virusurile a caror informatie genetica este transcrisa in nucleu (dezoxiribovirusuri);
ARN-polimeraza virala, pentru cele care se multiplica in citoplasma (poxvirusuri si ribovirusri). Cele doua tipuri de polimeraze au omologii extinse ale secventei de aminoacizi, inclusiv ale secventei Gly-Asp-Asp. Acest tripeptid se gaseste chiar si in ARN-polimeraza fagica si in reverstranscriptaza. De aceea se considera ca are rol in recunoasterea matritei de acid nucleic.
Cele mai multe molecule de ARNm viral sunt monocistronice, adica sunt traduse intr-o singura molecula proteica.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 9113
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2026 . All rights reserved