| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
Din relatia (4.187) reiese ca la T = 0 K, G = H.
Studiind procesele ce au loc in sisteme solide si lichide, Nernst, in 1906, a constatat ca la temperaturi coborate, dar deasupra punctului de zero absolut, entalpia de reactie este practic egala cu variatia de entalpie libera. Rezultatul duce la concluzia ca nu numai aceste marimi termodinamice, dar si coeficientii lor de temperatura tind spre aceeasi limita in apropierea temperaturii de zero absolut, adica:
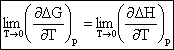 (4.207)
(4.207)
Ecuatia (4.207) este formularea matematica a teoremei lui Nernst si inseamna ca cele doua curbe G - T si H - T au tangenta comuna orizontala, conform fig. 4.5.
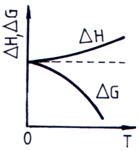
Fig. 4.5. Variatia G si H in functie de T
Se poate enunta teorema lui Nernst: in vecinatatea temperaturii de zero absolut, H si G sunt egale, iar derivatele lor partiale cu temperatura sunt nule
Din teorema lui Nernst rezulta o serie de consecinte importante.
Din legea lui Kirchhoff (4.97) prin care coeficientul de temperatura al efectului termic este dat de diferenta caldurilor molare ale produsilor de reactie si ale reactantilor si pe baza teoremei lui Nernst formulata in raport cu entalpia (4.207) rezulta:
![]() (4.208)
(4.208)
Relatia (4.208) este un alt enunt al principiului II si inseamna ca: in cazul proceselor ce au loc in apropierea temperaturii de zero absolut, diferenta dintre caldurile molare izobare devine nula.
Pe baza teoremei lui Nernst (4.207) formulata in raport cu entalpia libera si tinand cont de relatia (4.163) rezulta un alt enunt al principiului III:
![]() (4.209)
(4.209)
adica: variatia de entropie care insoteste orice transformare fizica sau chimica este nula cand temperatura tinde la zero.
Rezulta ca suma entropiilor reactantilor este egala cu suma entropiilor produsilor de reactie la zero absolut.
Nernst a aratat ca teorema sa enunta imposibilitatea de a atinge temperatura de zero absolut.
Principiul III al termodinamicii poate fi considerat principiul imposibilitatii existentei unui perpetuum mobile de speta a III-a, adica nu se poate construi o masina termica care sa functioneze pe seama racirii unui corp pana la 0 K.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 2931
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2026 . All rights reserved