| CATEGORII DOCUMENTE |
| Alimentatie nutritie | Asistenta sociala | Cosmetica frumusete | Logopedie | Retete culinare | Sport |
PENICILINA V
1.1 Prezentarea produsului.Variante tehnologice
Antibioticele formeaza o grupa importanta de medicamente cu toxicitate selectiva ,inhiband in concentratii foarte mici unele procese metabolice din celula microbiana sau producand adevarate ruperi ale acesteia ,fara a fi nocive pentru celulele gazda. Se cunosc antibiotice produse de microorganisme si plante superioare dar importanta terapeutica au capatat numai unele din antibioticele produse de microorganisme.
Dupa descoperirea microbilor de catre Pasteur s-a observat ca microorganismele inferioare se apara de alte microorganisme prin utilizarea intensiva a substantelor nutritive prin modificarea pH-ului, a tensiunii superficiale etc. , sau elaborand anumite substante chimice nocive.Acest fenomen este numit antibioza iar substantele rezultate din metabolismul organismelor autogoniste poarta numele de antibiotice.Primul care a sugerat ideea ca prin autogonism se produc substante chimice cu actiune inhibanta asupra microorganismelor a fost savantul roman Victor Babes in anul 1885.El a remarcat si faptul ca aceste substante pot fi folosite in terapeutica pentru distrugerea agentilor patogeni purtatori ai bolilor infectioase.
Introducerea in practica medicala a antibioticelor cu un spectru larg de actiune si cu potenta neantalnita constitue cea de-a doua etapa extrem de importanta dupa introducerea sulfamidelor (1935) , in dezvoltarea chimioterapiei.Antibioticele se aplica in medicina umana si veterinara ca metode antiinfectioase , bacteriene ,in combaterea bolilor virale si canceroase precum si in unele afectiuni de natura neinfectioasa.
Productia mondiala de antibiotice a inceput in anul 1943 cu fabricarea pe cale biochimica a penicilinei si a continuat sa se extinda ajungand astfel la peste 12000 tone annual.In tara noastra fabricarea industriala a antibioticelor a inceput in anul 1955, iar in prezent se fabrica o gama destul de larga de antibiotice a caror productie se cifreaza la aproximativ 100 tone anual.
1.2 Clasificarea antibioticelor
Numarul foarte mare de antibiotice cunoscute pana in prezent a pus problema clasificarii acestor produse. S-au propus mai multe criterii de clasificare in functie de originea microorganismului producator , structura chimica a antibioticului si actiunea antibacteriana.Cu toate ca fiecare metoda folosita la clasificare este nesceptibila la anumite critici, clasificarea antibioticelor se va face in functie de originea microorganismelor producatoare, structura chimica a antibioticelor, biogeneza si actiunea lor farmacologica.
Dupa originea microorganismului producator antibioticele se clasifica in urmatoarele grupe:
antibiotice produse de bacterii: gramicidina, gramidina S,bacitracina, polimixinele, etc.
antibiotice produse de actinomicete ; streptomicina, tetraciclina, neomicina, nistatina, etc.
antibiotice produse de fungi : penicilina
Clasificarea in functie de originea microorganismului producator nu este concludenta deoarece este cunoscut faptul ca acelasi microorganism poate produce mai multe antibiotice diferite ca structura si proprietati fiziologice.
Dupa constitutia chimica antibioticele se clasifica in urmatoarele grupe:
antibiotice cu structura alifatica: alicina
antibiotice cu structura aromatica: acidul gladiolic, cloramfenicolul
antibiotice cu structura chimonica: fumigatina,fticolul
antibiotice cu cicluri de furan si piran: acidul penicilic
peniciline antibiotice heterociclice cu azot in molecula: acidul aspergilic,acidul hidroaspergilic
antibiotice heterociclice cu azot si sulf in molecula: penicilinele
antibiotice cu structura polipeptidica: gramicidina
antibiotice cu structura complexa: macrolidele
antibiotice cu structura nedeterminata; viomicina;
antibiotice cu structura complexa: macrolidele
antibiotice cu structura nedeterminata; viomicina
Dupa biogeneza antibioticele se clasifica in urmatoarele grupe:
antibiotice derivate din aminoacizi sau din unitati asemanatoare: oxamicina, azoserina, cloramfenicolul, penicilinele, etc
antibitice derivate partial sau din acetat; grizeofulvina, tetraciclinele, grupul macrolidelor;
antibiotice derivate din glucide simple: streptomicina, kanamicina, neomicina
antibiotice diverse: novobiocina, vancomicina
Clasificarea dupa structura chimica ofera posibilitatea formarii unor grupe ce elucideaza legatura dintre constitutia chimica si proprietatile antibacteriene
Dupa actiunea farmacologica antibioticele se clasifica in urmatoarele grupe:
antibiotice cu actiune antibacteriana
antibiotice cu actiune antituberculoasa
antibiotice cu actiune antivirolica
antibiotice cu actiune anticanceroasa
antibiotice cu actiune antifungica
antibiotice cu actiune antiprotozoare
Antibioticele nu exercita aceeasi actiune antimicrobiana asupra tuturor germenilor patogeni;ele au un spectru antibacterian caracteristic determinat de rezistenta specifica a microorganismelor patogene.Penicilinele constitue un grup de antibiotice, obtinute prin biosinteza sau semisinteza caracterizate printr-un larg spectru bacteriostati si bactericid in faza de multiplicare logaritmica a germenilor patogeni.Actiunea penicilinelor este complexa , ele impiedica incorporarea unor factori in membrana bacteriana , ducand la multiple tulburari de nutritie si metabolism bacterian.Deoarece majoritatea penicilinelor mai ales cele naturale sunt inactivate de penicilinaza si acilaza se impune gasirea unor peniciline de rezistenta si actiune ridicata.
Penicilinele "ideale" ar trebui sa posede un larg spectru antibacterian,stabilitate in mediu acid,rezistenta la penicilinaza, stabilitate in solutie , absorbtie rapida si sa nu produca hipersensibilitate la administrare.
Penicilinele de biosinteza
sunt substante chimice produse de diferite specii de microorganisme din clasa
Penicilliumsi Aspergillius printre care: Penicillium crysogenum,P. notatum, A.
In terapeutica se folosesc numai penicilinele G si V sub forma de saruri de sodiu, potasiu,calciu,trietilamina si novocaina.Fenoximetil penicilina(penicilina V) se utilizeaza si sub forma de acid liber.
Formula chimica a penicilinei V este:
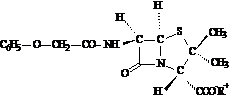
Formula bruta
Masa moleculara
Compozitia procentuala
Denumirea stiintifica: fenoximetilpenicilina, acid (2S,5R,6R)-3,3-dimetil-7-oxo-6-fenoxiacetamida-4-tio-1-aza-biciclo[3.2.0]heptan-2-carboxilic
Denumirea comerciala:
penicilina V, Osacilin, Ospen, Oratren
Penicilina V este antibiotic antibacterian ce contine in structura lui un
sistem biciclic tiazolidin-b-lactomic.Dupa originea microorganismului producator este un antibiotic
produs de fungi cu structura heterociclica derivat din doi aminoacizi si anume
L cisteina si D-valina [1,180]
Clasificarea farmacologica apenicilinelor
Pe langa clasificarea structurala a penicilinelor, o importanta foarte mare pentru practica clinica o reprezinta clasificarea lor farmacologica. Fiecare element structural specific peniclinelor contribuie atat la raspunsul terapeutic, cat si la stabilitatea chimica si/sau enzimatica a moleculei, absorbtie etc. (figura 6).
![]()

![]()
Figura 6. Rolul elementelor structurale in actiunea farmacologica a penicilinelor
Din punct de vedere farmacologic, pencilinele se clasifica in trei mari grupe. Clasele farmacologice, impreuna cu exemple caracteristice si speciile microbiene principale pe care acestea sunt active si folosite clinic, se regasesc in tabelul 2.
Tabel 2. Grupele farmacologice de peniciline
|
Grupa |
Caracteristici farmacologice |
Exemple |
Spectrul pentru care sunt utilizate clinic |
|
I (tip G) |
Spectru ingust Sensibile la penicilinaze |
Penicilinele naturale G si V Feneticilina |
Specii de Streptococcus, Neisseria, anaerobe, spirochete etc. |
|
II (tip M) |
Spectru ingust Rezistente la penicilinaze |
Meticilina Oxacilina, Cloxacilina Nafcilina |
Staphyloccocus aureus |
|
III (tip A) |
Spectru larg sau modificat spre Gram - |
Ampicilina Carbenicilina Azlocilina Mecilinam |
Haemophilus influenziae, E. coli, Proteus mirabilis, anterococi, Neisseria, P. aeruginosa, Enterobacter si Proteus sp. |
In prezenta lucrare, tratarea pencilinelor este abordata dupa criteriul grupelor farmacologice din care fac parte, iar pentru fiecare grupa este realizata o subclasificare structurala a acestora.
Deoarece penicilinele G si V sunt precursorii tuturor penicilinelor de semisinteza iar obtinerea acestora comporta elemente biotehnologice specifice, acestea vor fi tratate intr-un subcapitol separat.
1.3Peniciline naturale
Generalitati
Penicilinele de
biosinteza (naturale) sunt substante chimice produse de diferite specii de
microorganisme din clasele Penicillium si Aspergillus printre
care: P. crysogenum, P. notatum, P. crustosum, A.
Dintre numeroasele peniciline naturale (Tabel 3.) care au fost separate din lichidul de cultura a microorganismelor producatoare de peniciline, doar doua au fost si raman in continuare utilizate in terapeutica: penicilina G si penicilina V.
Tabel 3. Principalele peniciline naturale
|
|
||
|
Denumirea penicilinei |
Structura radicalului R |
Denumirea radicalului R |
|
Penicilina F |
|
2-pentenil |
|
Penicilina dihidro F |
|
2-pentil |
|
Penicilina G |
|
benzil |
|
Penicilina K |
|
n-heptil |
|
Penicilina N |
|
6-aminoadipoil |
|
Penicilina O |
|
alilmercaptometil |
|
Penicilina S |
|
3-clor-2-butenil-tiometil |
|
Penicilina V |
|
fenoximetil |
|
Penicilina X |
|
p-hidroxibenzil |
Structura si nomencalatura penicilinelor naturale
Penicilinele naturale, ca si cele de semisinteza, au structura generala (17), in care, pe ciclul tiazolidin β-lactamic se observa trei centre de chiralitate (*), a caror configuratie absoluta trebuie sa fie obligatoriu: C2 - (S), C5 - (R), C6 - (R), pentru ca acestea sa posede activitate antibiotica. In plus, ansamblul biciclic are o structura "de carte deschisa" (18), pusa in evidenta prin difractie cu raze X. Ciclul pentagonal de tiazolidina tinde spre planeitate, iar citeva unghiuri caracteristice sunt, dupa cum urmeaza: C5S4C3 - 95,2; C2N1C7 - 125; S4 C5C6 - 119,7.
Conform sistemului international IUPAC, penicilinele sunt considerate ca derivati de biciclo [3.2.0]heptan, in care atomii de carbon din pozitiile 1 si 4 sunt inlocuiti prin azot (azo) si respectiv sulf (tia). Astfel, penicilinele sunt amide ale acidului (3S, 5R, 6R)-6-amino-3,3-dimetil-7-oxo-4-tia-1-aza-biciclo[3.2.0]heptan-2-carboxilic. Pentru fiecare dintre peniciline, prefixul 6-amino este inlocuit cu numele restului corespunzator. Spre exemlu, pentru penicilina G (R= C6H5-CH2-) se va utiliza termenul 6-fenilacetamido.
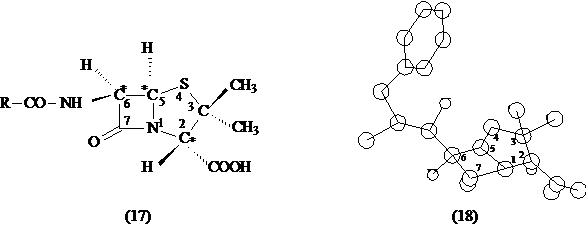
In scopul simplificarii nomenclaturii penicilinelor, acestea au fost denumite ca amide ale acidului 6-amino penicilanic pentru care, in literatuta in limba romana, se utilizeaza cel mai frecvent abrevierea acid 6-AP (in unele cazuri prescurtarea folosita este 6-APA, care provine din denumirea in limba engleza: 6-aminopenicillanic acid). Penicilina G se poate denumi astfel, acidul 6-fenilacetamido penicilanic.
Denumirea Comuna Internationala (D.C.I.) a penicilinelor are ca element de baza acidul 6-AP, continand particola "cilina", plasata la sfarsitul denumirii, care este acompaniata de un prefix care sugereaza structura chimica.
Structura penicilinelor naturale a fost determinata prin reactii de desinteza si confirmata prin sinteza. Din reactiile de degradare a peniclinelor in prezenta agentilor nucleofili si electrofili (vezi subcapitolul Instabilitatea ciclului beta-lactamic) s-a constatat ca drept produse finale de degradare sunt penicilamina si penilaldehida, fapt ce a dus la concluzia ca acestea sunt parti componente ale tuturor penicilinelor. Confirmarea acestei concluzii s-a facut prin sinteze partiale precum si prin realizarea integrala a sintezei Penicilinelor G si V.
Drept exemplificare a obtinerii pe cale sintetica a penicilinei V, sta sinteza realizata de Sheenan si Henry-Logan, in anul 1950 (figura 7.). Conform acestui procedeu, care astazi are doar interes academic, derivatul formilat al glicinei (19), este protejat la functiunea acida printr-un ester tertbutilic iar functiunea aminica este angajata intr-o ftalida. Sub actiunea penicilaminei (20), are loc formarea ciclului tiazolidinic, urmata de separarea diasteroizomerului util. Sub actiunea hidrazinei, are loc eliberarea functiunii aminice din ftalida, care ulterior se acileaza cu clorura acidului fenoxiacetic; gruparea COOH este eliberata la randu-i cu ajutorul HCl anhidru. Acidul fenoxiacetil peniciloic (21) obtinut se trateaza cu un echivalent de NaOH care blocheaza gruparea carboxilica cea mai disociata si permite ciclizarea la lactama (22, Penicilina V), etapa realizata prin deshidratare, in prezenta diciclohexilcarbodiimidei (DCC).

Figura 7. Principiul sintezei Penicilinei V
1.4 Mecanismul de actiune al antibioticelor β lactamice
Antibioticele cu structura β-lactamica actioneaza la nivelul peretelui celular microbian, prin inhibarea biosintezei acestuia, producand astfel un efect bacteriostatic sau bactericid. In compozitia peretelui celular microbian intra macromolecule complexe, formate din fibre de peptidoglican, care se leaga prin punti peptidice, formand o structura tridimensionala complexa.
Actiunea antibioticelor se manifesta cu conditia ca acestea sa-si atinga tinta, anume, peptidoglicanul.
Daca peptidoglicanul este expus direct agentilor externi in cazul germenilor Gram +, nu acelasi lucru se intampla in cazul germenilor Gram -, la care, o membrana lipidica suplimentara impiedica actiunea directa a antibioticelor asupra peptidoglicanului (figura 1):

Figura 1. Reprezentarea schematica a membranei germenilor Gram + si Gram -
Structura peptidoglicanului are la baza lanturi lungi de glicani, formate din alternanta N-acetil-glucozaminei (simbolizata prin G) si acidului N-acetil-muramic (simbolizat prin M), legate prin punti oxidice:
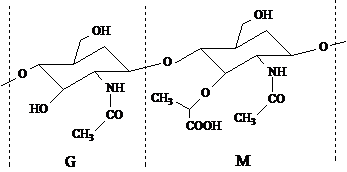
De aceste lanturi glicanice sunt atasate, la nivelul functiunii carboxilice libere din acidul muramic, tetrapeptide constituite din patru aminoacizi a caror secventa este urmatoarea:
L-alanina-acid-D-glutamic-L-lisina-D-alanina
Unirea lanturilor tetrapeptidoglicanice prin punti peptidice constituite din cinci resturi de glicina (numite peptide de legatura) conduce la peptidoglican, care este un ansamblu tridimensional rigid (figura 2).

Figura 2 Reprezentarea schematica a peptidoglicanului
La ultima etapa a biosintezei peretelui celular (reticularea totala a peptidoglicanului) participa peste 30 de enzime, iar cateva dintre acestea prezinta afinitate ridicata pentru antibioticele β-lactamice, de care se leaga prin legaturi covalente. Este vorba de proteinele enzimatice denumite proteine fixatoare de peniciline: PFP (in engleza, penicillin binding proteins: PBP). Aceste PFP (transpeptidaze si/sau carboxipeptidaze) sunt localizate in membrana citoplasmatica si au rolul de a finaliza biosinteaza peretelui celular prin crearea de punti intre lanturile de peptidoglican.
Aceasta ultima etapa constituie tinta preferentiala a β-lactamicelor, antibiotice care joaca rol de inhibitori enzimatici competitvi. La randul lor, PFP-urile joaca rol de receptori pentru aceste medicamente.
Capacitatea antibioticelor de a perturba sinteza peptidoglicanului prin fixarea covalenta a moleculei de anumite PFP, confera acestora proprietatea bacteriostatica.
Pentru a ajunge la PFP tinta, beta-lactamice trebuie sa:
-traverseze bariara membranara lipidica in cazul germenilor Gram - si, respectiv, peptidoglicanul, in cazul germenilor Gram + ;
-sa reziste la actiunea hidrolizanta a beta-lactamazelor secretate de anumiti germeni, in special Gram -.
In cazul germenilor Gram +, unde peptidoglicanul singur constituie peretele extern, penetrarea este usor realizabila datorita structurii sale reticulate in schimb, la bacteriile Gram-, pasajul antibioticului prin membrana externa este adesea dificil pe cale pasiva deoarece beta-lactamicele, puternic ionizate la pH fiziologic, prezinta un caracter hidrofil pronuntat. Bariera membranara lipofila este traversata de antibiotic la nivelul lipopolizaharidelor, prin intermediul ionilor Mg2+ si Ca2+ (figura 3).
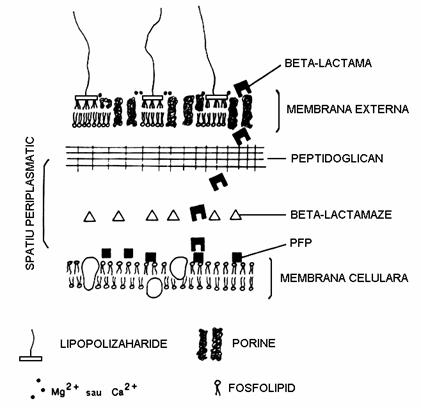
Figura 3. Pasajul unei beta-lactame prin peretele celular al unei bacterii Gram -
Pentru a actiona, beta-lactamele trebuie sa traverseze canale proteice fine, denumite porine. Penetrarea acestora este cu atat mai dificila cu cat molecula medicamenroasa este mai voluminoasa, hidrofila si purtatoare de sarcini negative.
Acest tip de penetrare prin porine explica diferentele de activitate observate atunci cand lipofilicitatea moleculei este diminuata de exemplu, prin inlocuirea atomului de sulf din cefalosporine cu un atom de oxigen.
Capacitatea unei beta-lactame (si in special a unei cefalosporine) de a traversa membrana externa este apreciata prin-un factor de cripticitate (factor de permeabilitate) care poate fi masurat:
-fie prin raportul intre concentratia minima inhibitorie (CMI) si concentratia unei solutii de transpeptidaza izolata si purificata ce produce inhibarea efectului antibiotic;
-fie, atunci cand exista o beta-lactamaza in spatiul periplasmatic, prin raportul intre numarul de moli de antibiotic hidrolizat si numarul de moli de antibiotic intact.
Spre exemplificare sunt redate valorile factorului de cripticitate (penetrare) a catorva cafalosporine pentru Escherichia coli:
|
Cefalosporina |
Cefaloridina |
Cefamandol |
Cefuroxima |
Cefoxitina |
|
Cripticitate: C |
Pe langa efectul bacteriostatic, antibioticele manifesta un efect bactericid indirect, prin activarea unor enzime hidrolitice. Se cunoaste ca, sub actiunea autolitica a murein-hidolazei, in peptoglican se produce scindarea legaturii dintre acidul N-acetil muramic si L-alanina. In prezenta antibioticului, enzimele hidrolitice sunt activate, ceea ce are drept efect o dezorganizare a peptidoglicanului, cu consecinte letale pentru microorganism.
Plecand de la acestea, s-a introdus notiunea de toleranta la antibiotice care se exprima prin concentratia minima inhibitorie (CMI) si concentratia minima bactericida (CMB). Un antibiotic are numai efect bacteriostatic cind CMI este mic si CBI este ridicat. Aceasta se poate traduce fie prin faptul ca peretele celular este insensibil la enzimele hidrolitice, fie ca medicamentul nu induce sau nu amplifica actiunea enzimelor hidrolitice.
Cele doua moduri de actiune a β-lactamicelor sunt reprezentate schematic in figura 4.

Figura 4 Reprezentarea schematica a celor doua moduri de actiune a antibioticelor β-lactamice
1.5 Fenomenul de rezistenta bacteriana
S-a constatat ca, mai devreme sau mai tarziu, microorganismele dezvolta fenomenul de rezistenta la antibiotic, ceea ce duce la scaderea drastica sau chiar anularea activitatii medicamentului. "Imunizarea" microorganismelor la actiunea antibioticelor se poate datora urmatorilor factori:
producerea de catre microorganisme a unor enzime capabile sa incativeze antibioticul: in mod special beta-lactamaze (penicilinaze si cefalosporinaze);
reducerea permeabilitatii membranei celulare a microorganismului;
absenta sau modificarea proteinelor tinta: PFP;
modificarea activitatii enzimelor autolitice, cu efect de suprimare a efectului bactericid.
Rezistenta bacteriana poate fi intrinseca (naturala) sau dobandita. Rezistenta naturala se refera la specii care nu au fost si nu vor fi niciodata sensibile la un numit antibiotic. Rezistenta dobandita se refera la tulpini sau specii care initial au fost sensibile la un anumit antibiotic dar care, in timp, au dezvoltat tulpini rezistente. Acest fenomen este urmarea unor mutatii sau dobandirea unui nou ADN.
Mutatia este un fenomen care apare spontan, indiferent de prezenta sau absenta vreunui antibiotic. O bacterie capabila de mutatii este avantajata de faptul ca antibioticul distruge rapid celulele sensibile, lasand loc, in schimb, unei populatii rezistente.
Se cunosc mai multe mecanisme de baza la care apeleaza bacteriile in scopul autoapararii la actiunea unui antibiotic. Mecanismul cel mai cunoscut consta in modificarea antibioticului, asa cum se intampla in cazul beta-lactamazelor. Aceste enzime scindeaza nucleul beta-lactamic, producand inactivarea antibioticului. Beta-lactamazele sunt raspandite in multe specii microbiene, atat Gram-pozitive cat si Gram-negative si sunt inhibate in grade diferite de inhibitorii de beta-lactamaza precum acidul clavulanic si sulbactama.
Unul din cele mai fascinante mecanisme de rezistenta, descoperit in cazul multor bacterii, consta in efluxul antibioticului. Conform acestui mecanism, antibioticul este pompat in spatiul extracelular cu aceeasi viteza cu care patrunde in celula. Este in curs de cercetare rolul pe care il pot juca inhibitorii pompei de eflux, in calitate de adjuvanti ai agentilor antimicrobieni.
In bacteriile Gram-negative, antibioticele beta-lactamice isi asigura transportul in celula tinta prin intermediul unei proteine membranare denumita porina. In cazul bacteriei Pseudomonas aeruginosa, imuna la cefalosporine, rezistenta este datorata absentei porinei specifice, ceea ce face ca antibioticul sa nu poata patrunde in celula.
Transformarile survenite la nivelul primului situs de actiune pot fi datorate faptului ca antibioticul patrunde in celula si ajunge la situsul tintei, dar este incapabil sa inhibe activitatea tintei din cauza modificarilor structurale ale moleculei. Se considera ca enterococii au o rezistenta innascuta la cefalosporine din cauza ca enzimele implicate in sinteza peretelui celular (producerea peptidoglicanului polimeric) au o afinitate scazuta pentru cefalosporine si deci, nu sunt inhibate de acestea.
Un alt mecanism prin care bacteriile se apara de actiunea antibioticelor este reprezentat de producerea unei tinte alternative (de obicei o enzima) care rezista la actiunea inhibitorie a antibioticului, concomitent cu producerea in continuare a tintei primare, sensibile. Aceasta permite bacteriei sa supravietuieasca, adica enzima ocoleste efectul antibioticului. Acest mecanism biochimic poarta denumirea de mecanism by pass.
Interactiunile antibioticelor beta-lactamice cu bacteriile Gram-pozitive si Gram-negative pot fi schematizate precum in figura 5.:
Bacterii Gram-pozitive

Bacterii Gram-negative

Figura 5. Interactiunea beta-lactamicelor cu microorganisme Gram + si Gram -
Unele bacterii sunt capabile sa utilizeze ca strategie de aparare mai mult decat unul dintre aceste mecansime.
Producerea de catre bacterii a beta-lactamazelor este considerat a fi cel mai important mecanism de rezistenta bacteriana la antibioticele beta-lactamice. Enzimele reactioneaza cu centrul activ al antibioticului, producand scindarea ciclului beta-lactamic.
O clasificare functionala simplificata a principalelor grupe de beta-lactamaze, este redata in tabelul 1. Informatii mai ample asupra beta-lactamazelor sunt furnizate in capitolul Inhibitori de beta-lactamaza.
Tabel 1. Clasificarea functionala a beta-lactamazelor
|
Clasa |
Substratul preferat |
Enzima reprezentativa (bacteria) |
|
Cefalosporine |
Amp. C (Enterobacter spp.) |
|
|
2a |
Peniciline |
Penicilinaza (S. aureus) |
|
2b |
Peniciline, Cefalosporine |
TEM 1 (E. coli); SHV 1 (Klebsiella) |
|
2be/r |
Peniciline, Cefalosporine |
TEM 364; SHV 212 (Enterobacter spp.) |
|
2c |
Peniciline |
PSE 1 (Pseudomonas spp.) |
|
2d |
Peniciline |
OXA 111 (Pseudomonas/ Enterobacter) |
|
2e |
Cefalosporine |
Enzime induse la nivelul cromozomilor din Proteus |
|
2f |
Peniciline, Cefalosporine, Carbapeneme |
SME 1 (Seratia) |
|
Peniciline |
IMP 1 (Pseudomonas) |
|
|
Peniciline, Cefalosporine |
Penicilinaza (Pseudomonas cepacia) |
Rezistenta la antibioticele β-lactamice este inscrisa in codul genetic al bacteriei.
Existenta rezistentei dobandite prin transfer genetic a fost recunoscuta in 1959, cand genele de rezistenta descoperite in Shigella au fost transferate in E. coli, prin intermediul plasmidelor.
In functie de localizare, gena ce codifica rezistenta poate fi cromozomiala, daca este situata la nivelul cromozomilor bacterieni sau plasmidica, caz in care gena este situata la nivelul unor structuri inelare de ADN, autoreplicante, de dimensiuni mai mici decat genomul bacterian, numite plasmide.
In evolutia lor, bacteriile au ajuns la mijloace foarte sofisticate in privinta schimburilor informationale continute in moleculele de ADN, atat in cadrul propriilor genuri si specii, cat si intre ele. Plasmidele realizeaza transportul si transferul genelor multirezistente pe o portiune de ADN cunoscuta sub denumirea de transpozon, care poate fi transferata de la o plasmida la alta sau de la o plasmida la un genom. Raspandirea prin plasmide a genelor rezistente se limiteaza la un numar restrans de specii bacteriene, dar cu ajutorul transpozonilor, aceste limite pot fi depasite. Astfel, rezistenta plasmidica se poate transmite intre bacterii apartinand unor tulpini si uneori unor generatii sau chiar specii diferite, avand in consecinta o foarte mare posibilitate de raspandire.
Introducerea in anii 1980 a celei de a III-a generatii de cefalosporine si a fluorochinolonelor nu a avut ca efect scaderea rezistentei bacteriene ci, dimpotriva, cercetatorii apreciaza ca aceasta s-a extins. In ultimii 10 ani s-a constatat un proces progresiv de propagare intercontinentala a S. aureus, rezistent la meticilina si Streptococcus pneumoniae, rezistent la penicilina.
Se apreciaza ca cefalosporinele din generatia a III-a pot fi inactivate de peste 40 de beta-lactamaze cu spectru larg, la care se adauga o penetrare mai dificila prin peretele bacteriilor Gram-negative. Acestea sunt principalele cai prin care se produce fenomenul de rezistenta la cefalosporinele din generatia a III-a.
Intr-un studiu efectuat in 30 de spitale americane pe 1525 de tulpini de Streptococcus pneumoniae, 25% dintre tulpini erau rezistente la penicilina si 9% la cefotaxima.
Numeroase tulpini de E. coli si Klebsiella pneumoniae au in plasmide material genetic care determina sinteza beta-lactamazei TEM 10, care inactiveaza ceftazidima. Cu toate acestea, bacteriile producatoare de TEM 10 sunt in proportie de 96 % sensibile la doze mari de ceftriaxona. Klebsiella pneumoniae producatoare de beta-lactamaza SHV-5 este rezistenta la multe cefalosporine (cefotaxima, ceftazidima) si este implicata in numeroase infectii nosocomiale. In aceste infectii, cefalosporinele de generatia a IV-a, precum cefepima si cefpiroma, s-au dovedit a fi unul din raspunsurile terapeutice cele mai importante.
Fenomenul de rezistenta bacteriana a devenit promotorul unui intens efort de cercetare in vederea obtinerii de noi compusi cu spectru antibacterian foarte larg sau deosebit de specific, care sa pastreze increderea clinicienilor in eficienta terapeutica a antibioticelor beta-lactamice.
1.6 Proprietati fizice
Fenoximetilpenicilina este o sbstanta alba utilizata sub forma de acid liber , avand punct de topire 118-120 grade celsius ,solubila in apa, solubila in solventi. Sub forma acida este o substanta incolora ,cristalizata in diferite forme [1.86].Penicilina V este o pulbere cristalina alba sau alb-galbuie fara miros sau practic cu gust amar.este usor solubila in alcool ,foarte greu solubila in apa,insolubila in parafina lichida si uleiuri grase.Cloroformul este un bun solvent pentru penicilina V.
Aspectul solutiei: 10 ml solutie 1% in alcool trebuie sa fie limpede si incolora.O eventuala coloratie trebuie sa fie mai intensa decat coloratia unei solutii etalon preparate din 0,05 ml cobalt, 0,20 ml fier si apa pana la 10 ml.
Penicilina V se comporta ca un acid tare pKa=2,76 , ca acid liber in stare cristalina nu este stabila decat cateva ore la temperatura camerei dar sarurile alcaline cu cat sunt mai pure cu atat sunt mai stabile, iar atunci cand sunt foarte pure sunt stabile timp indelungat [4,86]
FENOXIMETILPENICILINA [Penicilina V, Fenacilin, Orocilin, Stabicilina] acid liber are p.t. 118-120C si [α]D20 + 193C. Solubilitatea in apa la pH 1 (acidulare cu HCl) = 25 mg/100 ml. Este solubila in solventi organici polari. Penicilina V are acelasi spectru farmacologic ca si Penicilina G, dar este mai activa in infectiile stafilococice.
Dozarea formelor farmaceutice ale penicilinelor sunt, cel mai adesea, exprimate in unitati internationale (U.I.) definite dupa cum urmeaza:
1 U.I.= 0,6 mg benzilpenicilina sodica, adica 1 mg = 1667 U.I.
1 U.I.= 0,627 mg benzilpenicilina potasica, adica 1 mg = 1585 U.I.
1 U.I.= 0,6 mg fenoximetilpenicilina, adica 1 mg = 1695 U.I.
1.7 Date spectrale
Spectre in ultra-violet
Datorita, in special, prezentei in structura lor a unui nucleu aromatic, aceste peniciline dau absorbtii in lumina ultravioleta. Tabelul 4. contine maximele de absorbtie a penicilinelor G si V.
Tabe. Maximele de absorbtie in UV ale penicilinelor G si V (solutii apoase)
|
Penicilina |
Solvent |
λ m | |
|
Benzilpenicilina sodica |
apa | ||
|
Fenoximetilpenicilina sodica |
apa |
Spectre in infrarosu
In spectrele in infrarosu ale penicilinelor, regiunea 1600-1800 cm-1 este cea mai interesanta, furnizand informatii asupra principalelor functiuni prezente in peniciline. Astfel, gruparea lactamica, a carei frecventa de absorbtie se situeaza in domeniul 1760-1730 cm-1 atunci cand este izolata, prezinta o vibratie caracteristica intre 1780 si 1770 cm-1 (in stare solida: suspensie in ulei de parafina sau pastile de KBr) atunci cand aceasta este integrata sistemului biciclic tiazolidin-β-lactamic. Aceasta valoare denota diminuarea rezonantei, provocata de plierea moleculei, ceea ce impiedica conjugarea totala a gruparii amidice. Banda νCO lacatamic reprezinta un test important pentru verificarea calitatii produselor deoarece deschiderea ciclului tiazolidin-β-lactamic (degradarea penicilinei), conduce la disparitia din spectru IR a acestei benzi caracteristice.
Functiunea amidica extraciclica prezinta o banda, νCO extraciclic , situata intre 1700 si 1650 cm-1 (banda amida I), iar functiunea carboxilica, reperata printr-o banda νCOO- , (fie din carboxil, fie din carboxilat) prezinta o absorbtie specifica centrata spre 1600 cm-1. Celelalte benzi ale spectrului se refera la ciclul aromatic din radicalul R, la banda amida II extracicilica, la apa de hidratare etc. Spectrele in IR ale penicilinelor constituie un test de identificare foarte sigur, utilizat de cea mai mare parte a Farmacopeelor, prin comparatie cu substante de referinta.
Tabel . Cateva frecvente IR (KB 1%), in cm-1, caracteristice penicilinelor G si V
|
|
||||||
|
Penicilina |
R |
R' |
νCO lacatamic |
νCO extraciclic |
νCOO- |
νNH |
|
Benzilpenicilina |
|
Na | ||||
|
Fenoximetilpenicilina potasica |
|
K | ||||
Spectre de rezonanta magnetica nucleara
Spectrele de rezonanta magnetica nucleara (RMN) ofera informatii importante in special pentru dispozitia spatiala a celor doua grupari metil,
neechivalente, atasate la C3 (endo-, mai dezecranat si exo) si a dispozitiei reciproce a ciclurilor azetidin-2-onic si tiazolidinc, pentru care constanta de cuplaj intre protoni H-5 si H-6 (care se constituie intr-un sistem de tip AB), de aproximativ 4 Hz, pledeaza pentru dispozitia cis a celor doua cicluri. In tabelul 6 sunt redate valorile medii ale deplasarilor chimice ale protonilor situati in pozitia alfa fata de gruparea amidica exociclica, in sarurile solubile ale penicilinelor G si V.
Tabel 6. Deplasarile chimice ale protonilor benzilici in penicilinele G si V (100 MHz, D2O)
|
Penicilina |
Structura schematizata |
δ (ppm) |
|
Benzilpenicilina |
| |
|
Fenoximetilpenicilina |
|
1.9 Proprietati chimice
Aciditatea
Prezenta in pozitia 2 din ciclul tiazolidin β-lactamic a gruparii COOH, confera penicilinei V aciditate iar pKa-ul are valoarea 2,76.
Prezenta gruparii COOH, confera peniclinelor:
-posibilitatea de a forma saruri de Na sau K foarte solubile in apa. In schimb, sarurile cu metalele grele (ex. sarurile de Cu2+);
sunt insolubile sau provoaca degradarea ciclului b-lactamic
-proprietatea de a forma saruri cu aminele. Aceasta particularitate a fost exploatata pentru obtinerea unor forme retard a penicilinelor.
-aptitudinea de a forma esteri
In tabelul de mai jos sunt prezentate principalele saruri ale penicilinei V
Tabel Sarurile penicilinei V
|
|
||
|
R+ |
D.C.I. |
Denumire inregistrata |
|
K+ |
Fenoximetil penicilina potasica |
Antibiocin, Vepen |
|
|
Benzatinfenoximetilpenicilina |
Ospen, Bicilina |
Instabilitatea ciclului β-lactamic
Toate penicilinele sunt foarte sensibile la atacul agentilor nucleofili, electrofili, oxidanti, sau a unor enzime, suferind reactii de degradare care conduc la pierderea actiunii biologice.
Degradarea in mediu alcalin
La valori ale pH-ului egale sau mai mari de 8, are loc atacul nucleofil al anionului HO- asupra carbonilului din gruparea lactamica, cu deschiderea ciclului si formarea, in general, in etapa finala, a acidului peniciloic (23).
In conditii mai drastice, are loc decarboxilarea acestuia, cu formarea acidului peniloic .
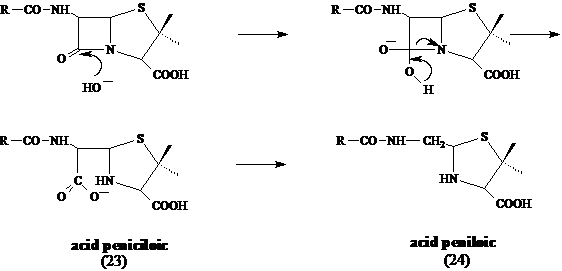
Figura 1 Degradarea penicilinelor in mediu alcalin
Prezenta in mediu a sarurilor metalice (Zn2+, Cd2+, Pb2+) sau a HgCl2, favorizeaza degradarea acidului peniciloic la o carbinolamina instabila (25) care se descompune in D-penicilamina (26) si acid penaldic (27), acesta din urma decarboxilandu-se la penicilaldehida (aldehida penilica), (28).
 Figura 2 Degradarea acidului peniclioic sub influenta sarurilor mercurice
Figura 2 Degradarea acidului peniclioic sub influenta sarurilor mercurice
La pH cuprins intre 9 si 10, viteza de inactivare a penicilinei V este de 2,2 ori mai mare decit viteza de inactivare a penicilinei G.
De remarcat este
faptul ca unul din produsii de degradare: D-penicilamina (Mercaptil, Trolovol)
este utilizata in terapeutica drept tratament de fond in afectiunile
reumatismale cronice precum poliartritele reumatoide. Totodata, este folosit ca agent de chelatizare a cuprului in maladia
Alcooliza si aminoliza penicilinelor
Inafara anionului HO-, ciclul β-lactamic este susceptibil la atacul a numerosi alti nucleofili, (alcooli, amine, hidroxilamine), atac catalizat adesea de ionii metalelor grele: Cu2+, Zn2+, Sn2+ etc.
Atunci cand nucleofilul este anionul alcoxid, se formeaza esteri peniciloici (penicilinoici) (29) iar cind nucleofilii sunt amine sau hidroxilamina, se formeaza amide peniciloice (penicilinoice) (30), respectiv acizi hidroxamici (31).
Acesti produsi de degradare, ca de asemenea si cei intalniti in cadrul degradarii in mediu acid, sunt responsabili pentru alergiile produse la utilizarea penicilinelor.
![]()
![]()
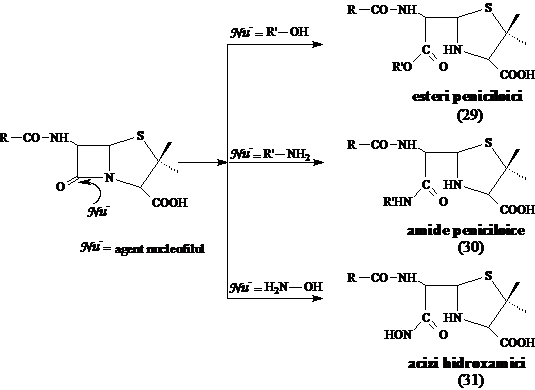
Figura 3 Alcooliza si aminoliza penicilinelor
Degradarea in mediu acid
Sub actiunea electrofila a cationului H+ asupra atomului de sulf din ciclul tiazolidin beta-lactamic, are loc deschiderea ciclurilor tiazolidinc si lactamic, printr-un mecanism concertat. Prin rearanjari ulterioare se obtine acidul penicilenic (32) iar daca mediul este puternic acid se poate
forma sistemul biciclic (33), numit acid penilic (figura 11).
Sub actiunea clorurii mercurice, acidul penilic trece in penicilamina (26) si penicilaldehida (28).
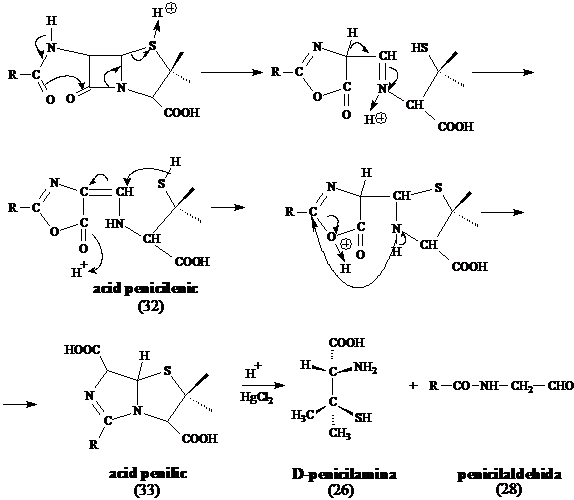
Figura Degradarea penicilinelor in mediu acid
Degradarea penicilinelor in mediu acid este cu atat mai facila cu cat radicalul R are un caracter mai puternic donor de electroni. In schimb, produsii in care R este acceptor de electroni, sunt mai stabili si pot fi administrati pe cale orala, fiind mai rezistenti la aciditatea gastrica.
Urmarindu-se procesul de inactivare a penicilinelor in mediu acid, se constata ca valorile constantelor de viteza difera foarte mult pentru cele doua antibiotice (tabelul 9), in timp ce valorile energiilor de activare sunt foarte apropiate (tabel 10).
Tabel Constantele de viteza la inactivarea penicilinelor G si V in mediu acid
|
Penicilina |
pH=2 |
pH=2,5 |
||
|
T [C] |
k x 103 |
T [C] |
k x 103 |
|
|
Penicilina G | ||||
|
Penicilina V | ||||
Tabel Valorile energiilor de activare la hidroliza penicilinelor G si V in mediu acid
|
pH |
Ea [J/mol] |
|
|
Penicilina G |
Penicilina V |
|
Aceste valori sugereaza faptul ca viteza de inactivare in mediu acid mai scazuta a penicilinei V, comparativ cu a penicilinei G nu este determinata de valoarea energiei de activare ci de scaderea factorului pre-exponential din ecuatia Arrhenius. Totodata, radicalul R=C6H5OCH2, din penicilina V, fiind mai atragator de electroni decat radicalul R=C6H5CH2, din penicilina G, confera penicilinei V o mai buna stabilitate in mediu acid.
Degradarea sub actiunea penicilinazelor
Deschiderea ciclului b-lactamic are loc si la atacului b-lactamazelor, enzime ce se gasesc in spatiul periplasmatic si care sunt capabile de a hidroliza penicilinele (penicilinaze) si cefalosporinele (cefalosporinaze). Aceste enzime sunt strategic plasate, in pasajul urmat obligatoriu de moleculele de antibiotic si reprezinta principalul mecanism de rezistenta a bacteriilor fata de antibiotic.
1.10 Proprietati biologice si farmacologice
Actiune terapeutica
Bactericid in faza de multiplicare ca urmare a inhibarii peretelui bacterian, spectrul de actiune cuprinde coci Gram-pozitivi(streptococi, euterococi, pneumococi, stafilococi) si Gram-negativi(Neisseria);Gram-pozitivi (bacilul antraxului); spirochete, trponeme.Preparatu este inactiv fata de bacilii Gram-negativi(colibacili, bacilul tific, paratific, dizenteric, hemofil, virusuri mari si fungi.
Rezistenta se instaleaza relative lent si este diferita ca importanta, in functie de tipul de bacterie( frecventa fata de stafilococ si foarte rara fata de stafilococ β-hemolic sau trponeme ).Absorbtia este buna dupa administrarea parentala, difuziunea este buna (cu exceptia sistemului nervos ,globului ocular, pleurei).Eliminarea se face in forma activa, nu este metabolizata prin urina.Concentratiile urinare sunt superioare celor plasmatice.
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 6876
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2026 . All rights reserved