| CATEGORII DOCUMENTE |
| Aeronautica | Comunicatii | Electronica electricitate | Merceologie | Tehnica mecanica |
FENOMENE BIOELECTRICE
Prezenta, atat in citoplasma oricarei celule, cat si in fluidele extracelulare, a numeroase tipuri de atomi si molecule ionizate, deci incarcate electric, si faptul ca activitatea metabolica mentine diferente de concentratii ale acestor ioni, fac ca fenomenele electrice sa fie proprii tuturor celulelor.
O caracteristica de baza a unei celule vii este existenta unei diferente de potential electric intre fata externa si cea interna a membranei celulare. In interiorul celulei, respectiv in mediul interstitial, potentialul este acelasi. Deci diferenta de potential se stabileste intre aceste medii. Aceasta diferenta de potential se numeste potential de repaus celular (PR)(spre deosebire de cel din timpul activitatii). Are valori cuprinse intre - 50) - (-100) mV. Pentru a explica modul in care apare PR se vor analiza cateva sisteme bicompartimentale simple dintre care ultimul este apropiat de sistemul citoplasma - lichid interstitial.
Cazul 1.
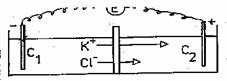
Se considera ca, in cele doua compartimente ale sistemului
(fig.) se gaseste KCl in concentratii diferite (c1 >
c2) si ca acestea sunt separate printr-o membrana
inegal permeabila (coeficientii de permeabilitate pentru K+
si Cl- sunt diferiti).
Conform legilor difuziei va aparea un flux de substanta dinspre compartimentul 1 inspre compartimentul 2. Dar PK+ >PCl- si in acest caz: JK+ > JCl-. Concentratia ionilor de K va creste in compartimentul 2 si acesta devine incarcat pozitiv in raport cu compartimentul 1. Apare o diferenta de potential intre cele doua compartimente, numita potential de difuzie. Potentialul de difuzie va accelera difuzia ionilor de Cl si o va frana pe aceea a ionilor de K. Se ajunge in final la o stare stationara. Potentialul de difuzie are, conform ecuatiei Planck-Henderson, expresia:
![]()
Potentialul de difuzie scade in timp, pe masura ce concentratiile se egalizeaza. In cazul in care PK+ = PCl- potentialul de difuzie este nul (DE = 0).
Cazul 2.
Se considera un montaj similar celui anterior, dar in care compartimentele sunt separate printr-o membrana selectiv permeabila, de exemplu impermeabila pentru Cl (PCl- = 0). In acest caz nu pot sa difuzeze decat ionii de K. La echilibru se stabileste intre cele doua compartimente o diferenta de potential data de relatia lui Nernst:
![]()
Compartimentul 2 devine incarcat pozitiv in raport cu compartimentul 1. Spre deosebire de primul caz, unde dupa un timp se ajunge la anularea diferentei de potential, in acest caz diferenta de potential ramane constanta dupa instalarea echilibrului pentru K+. Datorita diferentei de concentratie a celor doua specii ionice apare si un dezechilibru osmotic care duce la aparitia unui flux de apa inspre compartimentul 1.
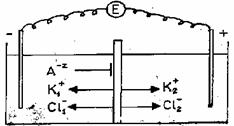
Cazul 3. Echilibrul Donnan. Se considera un
sistem bicompartimental (fig.) in care, la momentul initial, in primul
compartiment (1) se gaseste KCl, iar in al doilea se
gaseste apa distilata. In plus, in primul compartiment se gasesc
anioni proteici nedifuzibili, A-Z. Compartimentele sunt separate
printr-o membrana care este selectiv permeabila numai pentru anionii
proteici.
Intre cele doua compartimente se stabileste un echilibru Donnan:
![]()
cu consecintele:
1)![]()
![]()
![]()
![]()
r > 1
p > p
Cazul 4. Se considera un montaj analog cu cel din cazul 2, dar care contine in compartimentul al doilea un ion nedifuzibil prin membrana, de exemplu Na+. De exemplu, in fibra musculara exista urmatoarea distributie a ionilor (fig.):
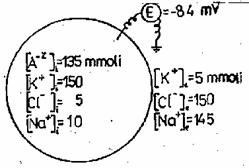
Deoarece numarul de particule in unitatea de volum este acelasi, presiunea osmotica este aceeasi in ambele compartimente (izotonicitate).
![]()
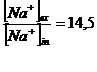
DE va fi dat de relatia lui Nernst pentru K+:
![]()
Asimilarea PR cu potentialul de echilibru al K+ se bazeaza pe ipoteza ca membrana celulara ar fi impermeabila pentru Na+. Aceasta ipoteza a provenit din observatia ca Na+ ramane mult mai abundent in spatiul extracelular fata de citoplasma, desi atat gradientul de concentratie cat si cel de potential tind sa-l introduca in celula. S-a aratat ca Na+ intra pasiv in celula, dar concentratia ramane constanta datorita scoaterii lui active prin pompe. Se creeaza astfel o stare stationara. La blocarea transportului activ cu toxine sau dupa moarte Na+ intra in celula.
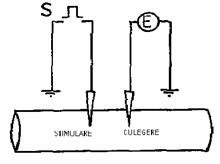
Masurarea PR.
PR poate fi masurat direct, cu ajutorul microelectrozilor de sticla, sau indirect, prin utilizarea unor sunstante fluorescente ionizate (de exemplu tiocianatul).
Microelectrodul de sticla este o pipeta obtinuta prin tragere la cald, avand varful mai mic de 0,5 mm. Strapungerea membranei cu acest microelectrod nu lezeaza considerabil membrana, iar contactul de scurtcircuitare intre citoplasma si fluidul extracelular nu are loc deoarece membrana se strange in jurul varfului de sticla (din cauza tensiunii superficiale). Microelectrodul este umplut cu o solutie de electrolit (de obicei KCl, 3M). Se masoara diferenta de potential intre microelectrodul introdus in celula si un electrod de referinta, nepolarizabil (de calomel).
Relatia Goldman-Hodgkin-Katz.
Teoretic, potentialul de repaus al celulei se calculeaza cu relatia Goldman-Hodgkin-Katz:
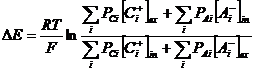
C+, A- - specii de cationi, respectiv anioni, difuzibili
P - permeabilitatea membranei pentru specia respectiva.
Se poate aplica formula Goldman-Hodgkin-Katz in cazul datelor numerice din figura ..pentru celula musculara, Tinand seama de faptul ca PK = PCl = 1 si PNa = 0,02:
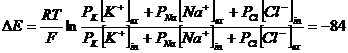 mV
mV
In cazul axonului gigant de calmar permeabilitatile sunt: PK = 1, PCl = 0,45 si PNa = 0,04.
In repaus celula se afla in stare stationara, fluxurile pasive sunt echilibrate de cele active. Ceilalti ioni (Ca++, Mg++) au pondere mai mica. Ca++, de exemplu, joaca un rol important in celula musculara cardiaca.
Circuitul electric echivalent pentru descrierea potentialului de repaus celular (fig.).
Bistratul lipidic se comporta din punct de vedere electric ca un izolator. Deoarece suprafata bistratului este de 200 de ori mai mare decat suprafata canalelor ionice, se poate vorbi despre o capacitate electrica a membranei celulare. Capacitatea electrica reflecta proprietatea membranei de a mentine o incarcare electrica de semne contrare pe cele doua fete ale ei. Capacitatea electrica a membranei, CM are valori in jur de 1 mF/cm2. Daca se noteaza cu EK, ENa, ECl, potentialele de echilibru electrochimic ale diferitilor ioni si cu RK, RNa, RCl, rezistentele canalelor specifice in serie cu E, se obtine o baterie de trei elemente legate in paralel a carei tensiune electromotoare echivalenta va fi:
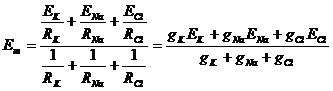
unde se noteaza cu g
conductanta care este inversul rezistentei: ![]() .
.
Aceasta relatie reda mai corect decat ecuatia Nernst valorile experimentale ale potentialului celular de repaus. Em tinde sa devina egal cu Ei al acelui ion pentru care conductanta este mult mai mare decat a celorlalti ioni (de exemplu K+). Valorile gi si Ei se calculeaza pe baza dependentei de Pi si ci.
Potentialul de actiune celular
La toate metazoarele sistemul nervos periferic si central constituie o vasta retea de comunicatie in cadrul organismului, retea in care pentru transmiterea semnalelor este utilizat un fenomen de natura bioelectrica, influxul sau impulsul nervos.
Impulsul nervos reprezinta variatia tranzitorie si propagabila a potentialului de membrana al fibrelor nervoase, numita potential de actiune (PA), produsa de un stimul (uneori exista si o activitate celulara spontana).
Potentialul de actiune este o depolarizare trecatoare a membranei celulare prin care interiorul celulei devine mai putin negativ decat in stare de repaus si diferenta de potential de-o parte si de alta a membranei celulare scade. Exista si potentiale de actiune hiperpolarizante, de exemplu in celulele receptoare retiniene.
Declansarea potentialului de actiune se realizeaza prin deschiderea portilor unor canale cationice sau anionice (uneori prin inchiderea portilor cationice, in cazul PA hiperpolarizante). Apar fluxuri de ioni care determina producerea unui semnal electric. Ionii implicati sunt in special ionii de Na+ (in faza ascendenta a PA) si de K+ (in faza descendenta). In celula musculara, in faza ascendenta sunt implicati ionii de Ca++.
Potentialele de actiune sunt de doua feluri:
1- potentiale locale (de exemplu in dendrite sau in soma neuronala);
2- potentiale de actiune tot sau nimic (de exemplu in axon).
Aceste potentiale se pot masura pe baza experientelor cu microelectrozi.
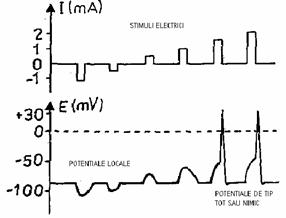
1. Potentialele de actiune locale
(PA-l)(fig.) se obtin la stimuli depolarizanti de intensitate
mica, avand valoarea sub cea a unei valori numita valoare prag.
Acesti stimuli sunt numiti stimuli
subliminari (sub prag).
Ei produc o depolarizare redusa a membranei, care se propaga decremental sau electrotonic. La axonul gigant, de exemplu, o depolarizare de 15 mV determina un potential local. Amplitudinea unui asemenea potential scade exponential cu distanta. Deci potentialele locale se caracterizeaza printr-o amplitudine proportionala cu intensitatea stimulului si printr-o propagare cu pierderi (decrementala).
2. Potentialele de actiune tot-sau-nimic (PA-tn)(fig.) se declanseaza atunci cand intensitatea stimulului atinge o valoare critica "de prag" sau "prag de detonare", deci cand aceasta are valori liminare sau supraliminare. Se produce potentialul de varf (spike) al fibrei nervoase - variatie ampla a potentialului celular in urma careia interiorul celulei devine pozitiv (+ 30 mV). Amplitudinea acestuia este de 120 mV. Odata declansat, indiferent de amplitudinea stimulului, amplitudinea PA-tn ramane constanta. Deci PA-tn este caracterizat de urmatoarele:
- amplitudine constanta (nu depinde de intensitatea excitantului atunci cand stimulii sunt liminari sau supraliminari);
- se propaga pe distante mari, cu viteze mari si fara pierderi (nedecremental);
- amplitudinea potentialului de varf, pragul si viteza de propagare sunt caracteristici ale fibrei (sau celulei).
Toate celulele vii poseda reactivitate, raspunzand la actiunea unui stimul. Capacitatea de a raspunde prin potentiale de actiune locale, pe care o au toate celulele vii, se numeste iritabilitate. Proprietatea de a raspunde prin potentiale de actiune tot sau nimic se numeste excitabilitate si se intalneste la trei tipuri de celule: celulele nervoase, musculare si glandulare.
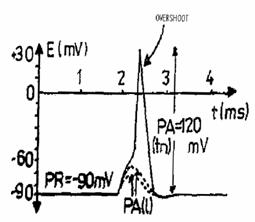
Fazele potentialului de actiune (fig.).
Intre momentul actiunii excitantului si raspunsul celulei exista un interval de timp, caracteristic fiecarui tip de celule, numit perioada de latenta. Prima faza a potentialului de actiune este reprezentata de un potential local si se numeste prepotential. Faza urmatoare este potentialul de varf, cu fazele ascendenta si descendenta. Faza a treia este alcatuita din postpotentialele pozitiv si negativ. Din punct de vedere functional se disting doua perioade refractare, perioada refractara absoluta, in care celula nu poate fi excitata, in faza ascendenta si partial in faza descendenta, si perioada refractara relativa, in care excitabilitatea este redusa, in celelalte faze ale PA.
Atunci cand asupra fibrelor nervoase actioneaza un stimul de durata are loc o acomodare manifestata prin cresterea pragului de excitabilitate. Acomodarea poate fi rapida (fibrele din nervii motori) sau lenta (unele fibre senzitive).
Atunci cand depolarizarea locala este superioara pragului de excitabilitate, dupa perioada refractara absoluta a unui spike se produce un al doilea s.a.m.d., fibra prezinta un raspuns repetitiv (oscilatoriu). Prin aceasta se realizeaza codificarea in frecventa a amplitudinii stimulilor.
Evenimentele in PA (la nivel molecular)
La intrarea in canalul ionic se gasesc grupari polare sensibile la modificarile de potential. Canalele de Na au atat porti externe cat si porti interne, cu sensibilitati diferite la modificarile de potential. In stare de repaus, portile externe sunt inchise, iar cele interne deschise. Ionii de Na, aflati in concentratie mare in mediul extracelular, sunt atrasi de interiorul electronegativ al celulei. Stimulii de intensitate mica determina deschiderea unui numar redus de canale de Na. Prin intrarea Na in celula scade electronegativitatea citoplasmei si atunci cand se ajunge la cca. - 60 mV se deschid portile canalelor de K sensibile la voltaj. Ionii de K ies din celula, se restabileste valoarea potentialului de repaus. Concentratiile ionice caracteristice starii de repaus se refac prin actiunea pompelor ionice (Na,K-ATP-aza). Acesta este mecanismul de producere a unui potential de actiune local (PA-l).
La cresterea intensitatii stimulului se vor deschide mai multe canale de Na, iar la depasirea pragului de detonare are loc procesul de patrundere in avalansa a ionilor de Na. Cu cat patrund mai multi ioni in celula, cu atat se accentueaza depolarizarea membranei si prin aceasta se deschid mai multe porti externe ale canalului de Na (feed-back pozitiv). Valoarea potentialului celular atinge zero si apoi interiorul se pozitiveaza pana la + 30 mV. Acesta este potentialul de actiune tot-sau-nimic - PA-tn. Se tinde astfel spre valoarea potentialului de echilibru al Na, dat de relatia Nernst, care este de + 50 mV. Aceasta ar duce la distrugerea celulei, proces impiedicat de doua evenimente.
1) La o anumita valoare a potentialului celular se inchid portile interne ale canalelor de Na (care erau deschise) si inceteaza patrunderea in avalansa a ionilor de Na. Se produce inactivarea canalului de Na.
2) Al doilea eveniment consta in deschiderea portilor canalelor de K, proces mai lent, de asemenea dependent de valoarea potentialului celular. Ionii de K, in concentratie mai mare in interior decat in exterior vor parasi celula atat sub influenta gradientului de concentratie cat si sub aceea a gradientului de potential electric. In termeni de conductante se poate spune ca procesul de crestere a conductantei pentru Na (gNa) este scurt si este urmat de cresterea conductantei pentru K (gK). In acest mod, se revine la valoarea potentialului de repaus PR (-80 , -90 mV). Intregul proces dureaza cca. 1 ms.
Revenirea la situatia caracteristica starii de repaus se face prin actiunea pompelor ionice si prin transport pasiv.
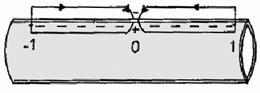
La producerea PA are loc o modificare locala a
distributiei de sarcini electrice - aceasta modificare de polaritate
duce la aparitia unor curenti electrici locali intre zona activa
si zonele invecinate: curentii locali Hermann.
Pentru aparitia unui nou PA trebuie ca intensitatea acestor curenti in zonele din margine sa depaseasca pragul de detonare. Datorita rezistentelor intalnite, intensitatea curentului local scade cu distanta. Se demonstreaza ca distanta la care amplitudinea PA se reduce la jumatate prin caderile de tensiune pe rezistente este:
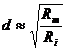
cu Rm - rezistenta electrica transmembranara pe unitate de lungime a membranei
Ri - rezistenta pe unitatea de lungime a lichidului intracelular. Se considera ca rezistenta lichidului extracelular este neglijabila.
Ri creste cu scaderea diametrului fibrei. Cu cat distanta maxima la care se atinge pragul de detonare este mai mare, cu atat creste viteza de propagare. Propagarea se face in mod diferit, in functie de tipul de fibre.
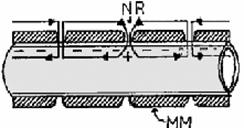
1) Fibre nemielinizate: propagare recurenta (din aproape in aproape) prin curenti
locali ce traverseaza intreaga suprafata a membranei axonale
si se inchid prin axoplasma si lichid interstitial (spre
centru in exterior si invers in interior).
2) Fibre mielinizate: prin conducere saltatorie. Teaca de mielina (izolator) este intrerupta la nodurile Ranvier si acolo se poate face contactul electric intra-extracelular. Curentii locali nu traverseaza toata suprafata membranei, ci sar de la un nod la celalalt, inchizandu-se prin axoplasma si lichidul extracelular. O dovada a acestui lucru este faptul ca narcotizarea nodului blocheaza propagarea impulsului, in timp ce narcotizarea internodului nu o blocheaza.
1) Micsorarea rezistentei lichidului intracelular.
2) Marirea rezistentei transmembranare.
1) Se realizeaza in fibrele nervoase si musculare gigante (1,5 mmm diametru: calmar - axon gigant, molusca barnaclu - fibra musculara giganta).
2) Se realizeaza prin mielinizare - tecile de mielina sunt electric izolatoare si astfel creste rezistenta transmembranara.
Unidirectionalitatea propagarii se realizeaza prin sinapse.
Sinapsa - structura prin care se realizeaza contactul intre doi neuroni sau dintre un neuron si o celula musculara sau glandulara.
Tipuri de sinapse: a) chimice; b) electrice
Elemente: regiune presinaptica cu membrana presinaptica (ramificatii axonale - butoni terminali, vezicule sinaptice), spatiu sinaptic (20-50 nm), regiune postsinaptica cu membrana postsinaptica (in care se afla receptori si canale ionice).
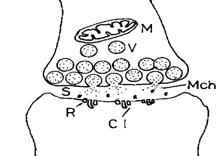
Functionare, etape. Sinteza mediator, eliberare mediator, difuzie prin spatiul sinaptic, legare de receptori, depolarizare, inactivare, revenire. In apropierea membranei presinaptice exista un mare numar de vezicule cu mediator chimic. La sosirea unui PA local (depolarizare), membranele unor vezicule (cca 40 nm) fuzioneaza cu membrana presinaptica si continutul este expulzat prin exocitoza in spatiul sinaptic (semnalul electric PA este tradus in semnal chimic). Moleculele de mediator (mesager prim) se combina cu moleculele receptoare din membrana postsinaptica, activandu-le. Acestea vor comanda deschiderea portilor canalelor ionice. In celula postsinaptica vor intra ioni si in acest fel este generat un PA local. Semnalul chimic este transformat in semnal electric. Conform teoriei cuantice a transmisiei sinaptice, eliberarea mediatorului se face sub forma de cuante. O cuanta (continutul unei vezicule) - cca. 104 molecule de Ach. Prin spargerea unei vezicule se produce un PA-l miniatural. Prin insumarea mai multor PA-l miniaturale apare un PA-l postsinaptic ce se deplaseaza decremental spre axon. PA locale aparute simultan in mai multe puncte sau in acelasi punct la intervale mici de timp pot da nastere unui potential mai amplu prin sumatie spatiala si/sau temporala. Ulterior, mediatorul este descompus enzimatic si resintetizat tot enzimatic, dupa revenirea prin membrana presinaptica in terminatiile nervoase. Ex. in sinapsele colinergice acetilcolinesteraza descompune si colinacetilaza reface Ach.
Sinapsele electrice - functioneaza fara mediatori chimici. Sinapsele electrice nu sunt atat de raspandite ca sinapsele chimice. Se gasesc, de exemplu, in anumite parti ale creierului sau intre celulele receptoare si cele orizontale in retina.
Structura: membrana sinaptica, spatiu sinaptic (mult mai mic - 2 nm).
Functionare: intre canalele membranei presinaptice si postsinaptice exista o contiguitate, ceea ce face ca o variatie de potential la nivelul membranei presinaptice sa induca o variatie similara in membrana postsinaptica. Transmiterea fiind directa este foarte rapida. In timp ce in sinapsa chimica intarzierea este de 0,5 - 5 ms, in cea electrica transmiterea este practic instantanee. Spre deosebire de sinapsa chimica, in sinapsa electrica nu se poate face o gradare in intensitate. Este importanta in cazul sincronizarii unui numar mare de celule efectoare. In sinapsele electrice transmiterea poate fi bidirectionala, spre deosebire de cele chimice in care este unidirectionala. Exista si sinapse in care depolarizarea si hiperpolarizarea se propaga in sensuri opuse - functi e de redresare cu conduce unidirectionala.
Din punct de vedere al efectului pe care il produc, sinapsele pot fi 1) excitatorii si 2) inhibitorii. Sinapsele excitatorii determina depolarizarea celulei, producand in membrana postsinaptica un potential excitator postsinaptic (EPSP)(ex. jonctiunea neuromusculara, mediator acetilcolina; prin legarea Ach de receptorii sai, se deschid canalele de sodiu operate de ligand si aceasta determina depolarizarea membranei). Sinapsele inhibitorii determina hiperpolarizarea celulei, producand un potential inhibitor postsinaptic (IPSP)(ex. anumite sinapse din creier: legarea GABA de receptorii GABAA duce la deschiderea canalelor de clor operate de ligand si celula se hiperpolarizeaza).
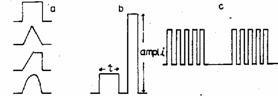
Excitant - variatie suficient de intensa,
indelungata si brusca a proprietatilor mediului, care
poate sa produca excitarea sistemului biologic. Parametrii unui
stimul (excitant) sunt urmatorii: forma, amplitudine, durata,
frecventa de repetitie.
Excitare - fenomenul prin care excitantul modifica permeabilitatea membranei celulare pentru ioni (inchiderea sau deschiderea canalelor ionice). Un factor fizic sau chimic este excitant daca este capabil sa determine intr-un fel sau altul deschiderea portilor canalelor ionice (ex. canale operate electric sau canale operate de ligand).
Excitatia celulara - totalitatea fenomenelor care au loc in celula ca urmare a excitarii acesteia de catre factorii excitanti.
Excitatia are aspecte: electrice (PA), optice (modificari ale transparentei, refringentei si activitatii optice a celulei), radiante (emisie de IR, vizibil, UV), chimice (hidroliza ATP, producere de NH3 etc.), calorice (producere si absorbtie de caldura).
Excitabilitate - proprietatea unui sistem biologic de a raspunde prin excitatie la actiunea excitantilor (stimulilor).
Reobaza si cronaxia.
Cantitativ, excitabilitatea se evalueaza cu ajutorul marimilor numite reobaza si cronaxie.
Reobaza - intensitatea minima a unui excitant (stimul) cu durata de actiune foarte mare (teoretic infinita) care poate sa declanseze excitatia in sistemul biologic.
Cronaxia - durata minima a unui excitant de intensitate egala cu dublul reobazei pentru care acesta poate produce excitarea.
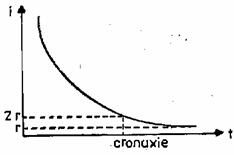
Relatia lui Weiss este o relatie intre valorile intensitatii si duratei unui stimul care poate produce excitarea unui sistem biologic:
i = a/t + b
unde a, b - constante ce depind de sistem.
Pentru t , i = b (reobaza)
Pentru i = 2b, t = a/b (cronaxia)
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 3742
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved