| CATEGORII DOCUMENTE |
| Astronomie | Biofizica | Biologie | Botanica | Carti | Chimie | Copii |
| Educatie civica | Fabule ghicitori | Fizica | Gramatica | Joc | Literatura romana | Logica |
| Matematica | Poezii | Psihologie psihiatrie | Sociologie |
POTENTIAL DE OXIDO-REDUCERE
Se ia o solutie apoasa care contine sare de fier (II) si sare de fier (III) in amestec. In solutie se introduce un electrod inert de platina (inatacabil de catre solutie). Ionii Fe2+ au tendinta de a trece in Fe3+ prin cedarea unui electron electrodului, iar ionii Fe3+ au tendinta de a capta un electron pentru a trece in Fe2+:
![]() Fe2+ Fe3+ + e
Fe2+ Fe3+ + e
La stabilirea echilibrului intre solutie si electrod, se stabileste o diferenta de potential a carui valoare, exprimata in volti, este data de relatia lui Nernst:
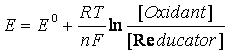
unde R este
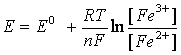
Inlocuind valorile R, F si T pentru t = 20oC si trecand de la logaritmul natural la cel zecimal (inmultind cu 2,303), ecuatia (9.18) devine:
![]()
Potentialul E0 se numeste potential normal al sistemului redox sau potential standard. El corespunde starii in care concentratiile oxidantului si reducatorului sunt egale (raportul lor este egal cu 1, lg1 = 0, deci E = E0). Potentialul standard al unui sistem red-ox, nu are valoare absoluta ci se determina in raport cu un electrod de referinta, electrodul normal de hidrogen. Potentialul normal al electrodului de hidrogen, in raport cu o solutie normala de acid tare (H2SO4) este considerat in mod conventional egal cu 0.
Potentialul redox standard poate fi utilizat la caracterizarea capacitatii de oxidare sau reducere a sistemelor chimice. Atunci cand intr-un sistem chimic se afla doi componenti care ar putea functiona fiecare atat ca oxidant cat si ca reducator, sistemul cu potential red-ox mai mare va oxida pe cel cu potential red-ox mai mic. Se poate sti in acest fel, care este oxidantul si care reducatorul in reactia respectiva, consultand tabelele cu potentiale standard ale sistemelor chimice redox. Asa de exemplu, daca in sistem se afla acid azotos si permanganat de potasiu, ambii fiind oxidanti, permanganatul oxideaza acidul azotos conform reactiei:
5HNO2 + 2KMnO4 + 3H2SO4 = 5HNO3 + 2MnSO4 + K2SO4 + 3H2O
deoarece are potetialul redox standard E0 mai mare (+1,51 V):
![]()
De aici concluzia ca substantele sunt cu atat mai oxidante cu cat au valoarea potentialului redox mai mare, iar capacitatea lor de a reduce este cu atat mai puternica cu cat valoarea potentialului redox este mai negativa. Sirul valorilor potentialelor standard ale diverselor sisteme chimice asezate in ordinea lor crescatoare, de la valorile negative spre valorile pozitive trecand prin zero, constituie seria tensiunilor. Potentialul standard zero corespunde electrodului normal de hidrogen, iar potentialele standard negative caracterizeaza sistemele reducatoare (elementele situate inaintea hidrogenului in seria tensiunilor), in timp ce potentialele pozitive caracterizeaza sistemele oxidante fata de hidrogen (sunt asezate dupa H in seria tensiunilor). Deoarece sistemele cu potentiale mai negative dislocuiesc pe cele cu potentiale mai pozitive, rezulta ca proprietatea de oxidant sau reducator are caracter relativ, aceeasi substanta comportandu-se ca oxidant fata de una mai reducatoare decat ea si ca reducator fata de una mai oxidanta decat ea.
In majoritatea cazurilor reactiile de oxido-reducere nu pot fi separate sau localizate. in procesele electrolizei si ale surselor electrochimice de energie, aceste reactii insa, pot sa se desfasoare si separat, cind oxidarea are loc la anod (oxidare anodica) iar reducerea, la catod (reducere catodica).
Portiunea din sistemul de reactie la care are loc unul sau altul din procesele redox, se numeste electrod. Electrodul este un conductor de ordinul intii (metal, conductor electronic) introdus intr-un electrolit (conductor ionic, ' solutie sau topi tura).
|
Politica de confidentialitate | Termeni si conditii de utilizare |

Vizualizari: 4256
Importanta: ![]()
Termeni si conditii de utilizare | Contact
© SCRIGROUP 2025 . All rights reserved